铁死亡在乳腺癌预后和靶向治疗中的研究进展
2023-05-19郑博文
郑博文, 房 林
(1. 同济大学医学院,上海 200092; 2. 同济大学附属第十人民医院甲状腺乳腺外科,上海 200072)
最近的研究数据表明,乳腺癌超越肺癌成为世界范围内发病率最高的恶性肿瘤,其发生发展严重威胁了女性的生命健康[1]。放化疗和靶向治疗诱导的肿瘤细胞死亡成为了失去手术机会患者的主要治疗手段,然而在一些临床实验中发现,肿瘤耐药的发生时常导致了不良预后[2-3]。铁死亡作为一种近几年被发现的细胞死亡方式,不同于既往发现的细胞凋亡、细胞焦亡及坏死性细胞程序性死亡,铁死亡发生时细胞的主要特征为铁离子稳态破坏和脂质过氧化物(lipid reactive oxygen species, LipROS)累积。近些年,铁死亡的不同机制逐渐被研究者发现,也出现了小分子的铁死亡诱导剂,成为了耐药肿瘤治疗的新方向。
1 铁死亡概述
1.1 铁死亡的发现
2008年,Stockwell等[4]发现小分子化合物RSL3和RSL5可以诱导一种非凋亡的细胞死亡方式,且铁离子螯合剂(DFO)和抗氧化剂(vitamin E)可以抑制这一过程,2012年他们将这一细胞死亡方式正式命名为铁死亡(ferroptosis)[5]。
1.2 铁死亡的特征
铁死亡发生时,电镜下细胞主要表现出线粒体嵴减少(消失);线粒体外膜破裂、皱缩;线粒体颜色深染;细胞膜破裂等现象,与细胞程序性死亡不同的是,细胞较少发生核损坏(如核膜破裂、核固缩)[6]。此外,发生铁死亡的细胞表现出Fe2+、谷胱甘肽(gluta-thione, GSH)、谷胱甘肽过氧化物酶4(glutathione peroxidase 4, GPX4)和还原性辅酶NADPH的下调,Fe3+、LipROS和环加氧酶2的上调[7]。
1.3 铁死亡的机制
正常细胞中,在氧化还原酶细胞色素P450的作用下,还原性辅酶NAD(P)H将电子传递给氧分子(O2)后生成过氧化氢(H2O2),H2O2与Fe2+发生芬顿反应生成Fe3+、氢氧根(OH-)和羟基自由基(OH·)。生成的羟基自由基在细胞内有较高的氧化活性,会导致脂质体膜上多不饱和脂肪酸长链双键间的氢原子被剥夺进而形成LipROS,LipROS在多不饱和脂肪酸存在时易被转运至细胞膜,当过多的LipROS被堆积在细胞膜而无法清除时,细胞膜发生不可以的破裂进而导致细胞死亡[8]。铁离子在这一过程中发挥了催化作用,因此这一死亡方式被成为铁死亡。然而,正常细胞有多套抗氧化系统,用于清除过量的LipROS,从而抑制铁死亡,这些抗氧化系统也是多个癌症相关信号通路调控的下游靶点,抗氧化系统的失衡是影响细胞铁死亡进程的关键因素。我们将简述现阶段普遍认可的3个抗氧化系统,见图1。
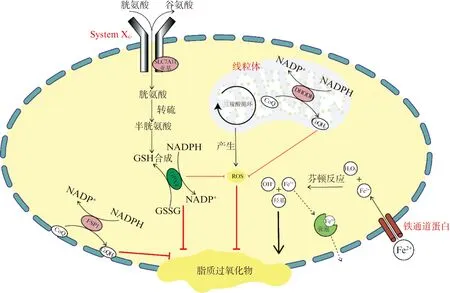
图1 铁死亡机制中的芬顿反应及3种抗氧化系统Fig.1 Fenton reaction and three antioxidant systems in the mechanism of ferroptosisGSH: 谷胱甘肽;CoQ: 泛醌;CoQH2: 泛醇;GSSG: 氧化型谷胱甘肽;ROS: 活性氧类;DHODH: 二氧乳清酸脱氢酶
1.3.1 System Xc-胱氨酸/谷氨酸转运系统 System Xc-胱氨酸/谷氨酸转运系统作为较早被发现的抗氧化系统,研究较为深入。System Xc-又称胱氨酸谷氨酸反向转运体(cystine/glutamate antiport),能够以1∶1的比例将胱氨酸转入胞内同时将谷氨酸转出胞外,胱氨酸在胞质被分解为半胱氨酸,参与还原型GSH的合成[9]。GSH能帮助还原胞膜上的LipROS,其自身变为为氧化型谷胱甘肽[glutathione(oxidized), GSSG],谷胱甘肽过氧化物酶4(gluta-thion peroxidase 4, GPX4)通过促进NAD(P)H中的氢原子转移促进GSH再生。在这套抗氧化系统中,System Xc-转运蛋白的轻链亚基溶质载体家族7成员11蛋白被发现具有主要的转运活性,其编码基因转录也受多个癌基因和抑癌基因调控,如TP53、YAP/TAZ,成为研究者关注的重点[10]。GPX4作为关键酶加速GSH/GSSH循环,帮助及时清除过量的LipROS。研究发现,小分子化合物丁硫氨酸亚砜亚胺可以抑制GSH的合成,从而抑制GPX4活性,破坏抗氧化系统进而介导氧化损伤的细胞铁死亡[11]。Stockwell等发现小分子化合物RSL3是通过直接共价结合并抑制GPX4促进了铁死亡发生[12]。此外,由于GSH和GSSG含量检测较为容易,GSH/GSSG值成为了判断铁死亡发生的一个重要指标。
1.3.2 胞质FSP1-CoQH2系统 铁死亡抑制蛋白1(ferroptosis suppressor protein 1, FSP1)既往被命名为线粒体相关凋亡诱导因子2(apoptosis-inducing factor mitochondria-associated 2, AIFM2),是一种黄素蛋白,其编码基因被认为是P53响应基因[13],但其真正作用机制长时间来未被发掘。Doll等[14]发现FSP1能介导一种区别于System Xc-系统的独特的抗氧化防御系统,并将其正式命名。机制上,在胞质中,FSP1将NAD(P)H上的还原氢转移到泛醌上,形成其还原形式泛醇[coenzyme Q10(reduced), CoQH2],泛醇能够还原LipROS从而抑制铁死亡的发生,这一过程是谷胱甘肽非依赖的。FSP1的抑制和GPX4的抑制能够发挥很好的协同作用,促进铁死亡的发生。进一步研究发现,FSP1的敲低和泛醌的缺陷均会导致细胞铁死亡抑制的消失。
1.3.3 线粒体DHODH-CoQH2系统 由于发生在线粒体中的三羧酸循环伴随了广泛的电子传递和氧化磷酸化,线粒体成为细胞活性氧产生的主要场所,而铁死亡的发生伴随着LipROS的沉积,线粒体在铁死亡过程发挥了重要作用。最近的研究中,Gan等[15]发现了线粒体内由二氢乳清酸脱氢酶(dihydr-oorotate dehydrogenase, DHODH)介导的抗氧化机制。DHODH的作用与FSP1类似,促进了泛醌的还原从而清除LipROS,只是其在线粒体内发挥作用。他们发现在GPX4低表达的肿瘤细胞中,铁死亡水平上升并不显著,作为代偿,细胞内的DHODH含量显著上升。此外,使用DHODH抑制剂(brequinar)能选择性促进GPX4低表达肿瘤细胞的死亡。Gan等认为线粒体内DHODH和GPX4介导的抗氧化系统是平行关系的,可以发生互补,但线粒体抗氧化系统与胞质抗氧化系统则是互不干扰的[15]。
2 铁死亡与乳腺癌的相关性
铁死亡与多个肿瘤进展及耐药相关,铁死亡基因被发现是多个肿瘤信号通路的下游靶点,例如在耐药性肝细胞癌中,Hippo信号通路中的关键蛋白YAP/TAZ入核后以TEAD和ATF4依赖的方式促进了SLC7A11的表达,从而克服了索拉非尼诱导的铁死亡[16]。抑癌因子P53能通过抑制SLC7A11或者增加亚精/精胺n1-乙酰转移酶1和谷氨酰胺酶2的表达来促进肿瘤细胞铁死亡,有趣的是,P53也能直接抑制二肽基肽酶4活性或诱导细胞周期蛋白依赖性激酶抑制剂1A的表达来抑制铁死亡发生[17]。我们综述了铁死亡和乳腺癌进展、预后预测、靶向治疗的研究进展。
2.1 铁死亡和乳腺癌进展
铁死亡作为许多基因调控模式的下游共同环节,与乳腺癌进展关系密切。Chen等[18]的研究中发现筋素肌动蛋白捆绑蛋白1可以与SLC7A11相互作用,促进其发生泛素介导的蛋白酶体降解进而诱导乳腺癌细胞对他莫昔芬耐药。Lin等[19]的研究发现上皮-间充质转化介导的复发性乳腺肿瘤的盘状结构域受体酪氨酸激酶2上调,在维持肿瘤细胞生长优势的同时激活了YAP/TAZ介导的铁死亡敏感,解释了复发肿瘤细胞具有更高铁死亡敏感性的原因。此外,在三阴性乳腺癌细胞系BT549中发现,酰基辅酶a合成酶长链亚型1能介导的α-桐木酸(αESA,一种代表性多不饱和酸)合成诱导BT549细胞发生铁死亡,且这类铁死亡不能被GPX4干扰所抑制[20],α-桐木酸合成抑制为GPX4抑制剂耐药的乳腺癌治疗提供了新的方向。
乳腺癌细胞铁死亡也被许多非编码RNA调控。环状RNA circGFRA1可以竞争性结合miR-1228,调控靶基因FSP1的表达进而介导恶性肿瘤表型[21]。长链非编码RNA PGM5P3-AS1通过与RNA结合蛋白NOP58结合稳定靶基因微管相关蛋白轻链C的表达,促进铁死亡的发生进而抑制三阴性乳腺癌的恶性进展[22]。Yadav等[23]发现SLC7A11作为miR-5096的下游靶点,SLC7A11挽救能够减少miR-5096介导的铁死亡和促癌作用。还有许多其他非编码RNA和乳腺癌铁死亡相关性的研究,但是目前这方面研究主要聚焦于分子关系的阐述和非编码RNA在预测铁死亡发生和肿瘤预后的潜能,我们期待靶向铁死亡相关非编码RNA的小分子化合物合成,为乳腺癌治疗提供更多方法。
肿瘤微环境(tumor microenvironment, TME)是一个复杂的整体,探究乳腺癌中肿瘤细胞和微环境内其他成分的相互作用是更为重要的,铁死亡在其中也发挥了作用。Xie等[24]在脂肪细胞和乳腺癌细胞的共培养体系中发现了脂肪细胞对铁死亡的保护作用,进一步的研究发现,脂肪细胞分泌的油酸可以在酰基辅酶a合成酶长链亚型3存在时抑制乳腺癌铁死亡。Liu等[25]发现急性暴露在高27-羟基胆固醇下的乳腺癌细胞由于固醇调节元件结合蛋白信号干扰出现了脂质代谢紊乱,进而抑制了肿瘤细胞生长。而慢性暴露在高27-羟基胆固醇的乳腺癌细胞则表现出更高的致瘤和转移能力,究其原因,这些细胞上调了GPX4轴活性并减少System Xc-抗氧化系统的依赖以适应脂质代谢异常的应激。这一研究也一定程度上解释了肥胖和高胆固醇作为肿瘤不良预后因素的原因。有趣的是,研究者还发现TME中的细胞交互与铁死亡相关,三阴性乳腺癌肿瘤细胞产生的白介素-6可以激活肿瘤相关巨噬细胞中JAK2/STAT3轴,诱导其分泌TGF-β1,又反向激活肿瘤细胞中的TGF-β1通路并调控肝白血病因子(HLF,一种新的癌蛋白)表达,HLF反转录激活γ-谷氨酰基转移酶1抑制铁死亡,促进乳腺癌生长和化疗耐药[26]。尽管上述研究发现了TME通过铁死亡途径对肿瘤进展的影响,但铁死亡环节大都局限于肿瘤细胞内。肿瘤免疫逃逸作为肿瘤进展的重要因素和免疫治疗的理论基础,主要特征是肿瘤细胞诱导的效应T细胞耗竭,目前普遍认为这是程序性细胞死亡介导的,铁死亡和免疫细胞耗竭关系的研究仍存在较大空白,尽管检测上可能较为困难,但我们认为这对更好地认识TME是有意义的。
2.2 铁死亡和乳腺癌预后预测
生物信息学的发展帮助研究者从肿瘤数据库中挖掘铁死亡相关基因,并构建预后预测模型完善乳腺癌预后评价体系。万坤铭等[27]从TCGA数据库中筛选出11个铁死亡相关差异表达基因并构建乳腺癌预后预测模型,多因素COX回归结果提示,该模型高风险评分是乳腺癌不良预后的独立危险因子。也有分别针对Luminal型乳腺癌[28]和新辅助治疗的乳腺癌[29]患者的类似研究。此外一项临床研究中,Sha等[30]对紫杉醇-顺铂新辅助化疗的乳腺癌患者穿刺样本进行免疫组化检测,探究已知铁死亡相关基因ACSL4和GPX4作为病理完全缓解预测标志的潜能,发现ACSL4高表达、GPX4低表达及其联合状态是无病生存的独立预后因素。铁死亡和乳腺癌预后间有紧密联系,许多差异表达基因被发现是铁死亡环节中的关键基因并影响患者的临床结局。但也有很多基因的功能仍未知,对他们进行更深入的分子机制研究能够帮助研究者克服生物信息学预测准确性的限制,同时寻找更多乳腺癌药物治疗靶点。
2.3 铁死亡和乳腺癌治疗
2.3.1 小分子化合物诱导铁死亡 研究发现表皮生长因子酪氨酸激酶抑制剂吉非替尼耐药的三阴性乳腺癌细胞普遍存在GPX4表达升高[31],铁死亡诱导剂(erastin)对耐药细胞有很好的杀伤作用[5],然而鉴于erastin肾毒性仍未用于人体。FDA目前已经批准部分能诱导细胞铁死亡的小分子化合物用于临床肿瘤治疗,同时也有许多药物被开发出来。Ding和他的团队[32]开创性地合成了DMOCPLT(天然菊内酯的衍生物)的前体化合物,通过促进GPX4的泛素化降解诱导铁死亡,小鼠实验没有观察到明显的药物毒性同时显著延长了乳腺癌模型小鼠的生存时间。一些临床常见药物也与乳腺癌铁死亡发生相关,例如Li等[33]发现氨氯酮通过靶向KAT5/GPX4轴抑制乳腺癌细胞增殖。此外,二甲双胍通过诱导SLC7A11的UFMylation修饰促进乳腺癌细胞铁死亡,且这一过程不被AMPK信号通路调控,揭示了二甲双胍抗癌新机制[34]。中草药人参中的活性成分红参多糖被发现能够抑制GPX4的表达,与铁死亡诱导剂(erastin)联用能发挥更好的抗乳腺癌生长作用[35]。目前开发或发现的小分子化合物主要靶向肿瘤细胞铁死亡的经典System Xc抗氧化系统,针对其他非经典系统如FSP1-CoQH2以及TME中免疫细胞的死亡调控是未来药物开发的方向。
2.3.2 针对铁死亡的靶向递药 铁死亡诱导剂的副作用是其应用的主要障碍,研究者试图通过纳米颗粒靶向给药解决这一问题。Pan等[36]构建了铁(Fe)-四(4-羧基苯基)卟啉的聚乙烯吡咯烷酮分散纳米金属有机框架,并被乳腺癌细胞膜包覆,形成纳米颗粒和癌细胞膜的复合体。由于包装了癌细胞膜,使复合体不易被免疫清除进而聚集于癌灶。随后颗粒内的Fe3+通过芬顿反应促进GSH的耗竭和LipROS的累积诱发铁死亡。Zhou等[37]构建了血红蛋白、全氟碳、铁死亡激动剂、声敏剂verteporfin组成的红细胞膜杂交伪装的纳米复合物,超声刺激下SAFE大量供养并诱导乳腺癌细胞发生铁死亡。体外实验证明SAFE表现出肿瘤组织选择性且在轻度超声刺激下抑癌效果更好。此外,还有对pH敏感[37]和光敏感[38]的纳米颗粒诱发铁死亡的研究,这类纳米颗粒设计的主要思路有以下四点: (1) 使用自体细胞膜包装克服免疫清除;(2) 通过Fe3+和LipROS的被动累积和(或)抗氧化系统破坏诱发铁死亡;(3) 联合化疗药物发挥协同作用;(4) 设计外部启动方式如超声提高靶向性。
2.3.3 铁死亡增加治疗敏感性 放疗和药物耐受是乳腺癌治疗效果不佳的主要原因。Zhang等[39]发现铁饱和的MDA-MB-231细胞对放射治疗更为敏感,机制上除了铁死亡外,铁饱和细胞下调HIF-1α表达,改善肿瘤缺氧微环境,促进辐射诱导的缺氧DNA损伤,他们的研究为放疗联合铁负荷治疗提供依据。对于化疗耐药细胞,联合铁死亡激动剂发挥了效果[5],今后的方向是提升临床应用安全性。此外Zou等[40]发现曲妥珠单抗治疗耐药相关基因FGFR4,通过FGFR4-βcatenin/TCF4-SLC7A11轴抑制铁死亡并促进HER2阳性乳腺癌耐药,联合铁死亡激动剂同样发挥了显著治疗效果。以上研究均提示激活铁死亡和传统治疗方法的联合应用能发挥协同作用。
3 总 结
铁死亡作为近年来被发现的新的细胞死亡方式,在乳腺癌治疗中发挥重要作用。与其他细胞死亡方式不同,铁死亡发生时有独特的细胞特征。越来越多研究发现铁死亡与乳腺癌的发展及预后有密切关系。随着铁死亡的机制被不断发现,更多针对铁死亡机制的药物及治疗手段被开发并用于乳腺癌治疗。今后铁死亡药物开发的方向是TME的整体调控以及对非经典抗氧化系统的发掘,期待副作用更小且靶向性更强治疗手段。
