PRMT7抑制前列腺癌细胞体外迁移和侵袭的研究
2023-05-19何燕燕孙馨悦王建军
胡 平, 何燕燕, 孙馨悦, 王建军, 陈 平*
(1.同济大学生命科学与技术学院,上海 200092; 2.同济大学附属第十人民医院病理科,上海 200072;3.同济大学附属东方医院妇产科,上海 200123)
前列腺癌是全球男性生殖系统最常见的肿瘤。在2020年,全世界报道有1 414 259例新诊断的病例,占到所有新诊断癌症病例的7.3%;375 304例死亡病例,占所有癌症死亡病例的3.8%[1]。当前列腺癌发生淋巴结转移及其他远端转移时,其死亡率会极大增加。因此,理解前列腺癌转移的机制对于制定治疗策略具有重要意义。
蛋白质精氨酸甲基转移酶7(protein arginine methyltransferase 7, PRMT7),作为唯一进化保守的Ⅲ型酶,只催化产生单甲基精氨酸残基[2]。PRMT7参与了不同的生物学过程,包括DNA损伤修复[3]、早期胚胎发育[4]、脂肪形成[5]、成肌细胞分化[6]、神经元兴奋性调节[7]。PRMT7在肿瘤组织中也有表达。在肾癌患者中,PRMT7在癌组织中的表达高于非癌组织[8]。在肺癌细胞中,PRMT7的表达与侵袭性呈正相关[9]。在高侵袭性乳腺癌细胞中PRMT7表现为高表达[10]。PRMT7在肝癌癌旁组织的表达率高于癌组织,在肝癌细胞系低表达,且PRMT7降低癌细胞的增殖、侵袭和迁移能力[11]。本研究旨在分析PRMT7在前列腺癌组织和前列腺癌细胞中的表达水平、过表达PRMT7对前列腺癌细胞表型的影响,通过对过表达细胞株进行转录和蛋白测序初步探索其机制,进一步明确PRMT7在前列腺发生发展的作用。
1 实验与方法
1.1 数据采集
GTEx数据库(https:∥gtexportal.org/home/)中检索得到100例正常前列腺组织RNAseq数据,TCGA(The Cancer Genome Atlas)数据库(https:∥www.cancer.gov/)中检索得到52例正常前列腺组织RNAseq数据以及496例前列腺癌组织RNAseq数据,最终分析的样本数目: 正常前列腺组织为152,前列腺癌组织为496。将TPM格式的RNAseq数据进行log2转化后进行样本间的表达比较。使用R软件进行统计分析和可视化。
1.2 细胞培养
实验所用细胞均购自中国科学院细胞库;胎牛血清、0.25%胰酶、1640培养基、F-12培养基、MEM培养基、Defined Kerntinocyte-SPF培养基购自美国Gibco公司。双抗(青霉素、链霉素)购自上海碧云天生物技术有限公司。所有细胞培养在10%胎牛血清、1%双抗的培养基中,并在5%CO2、37 ℃细胞培养箱中培养。
1.3 Western印迹法
所有细胞使用RIPA裂解液裂解制备成蛋白悬液,加入上样缓冲液后制备上样悬液。一抗、二抗稀释比为1∶1 000。PRMT7抗体购自美国Abcam公司,β-actin抗体、GAPDH抗体、MAP2抗体和S100A4抗体购自上海碧云天生物技术有限公司,KISS1R抗体购自美国Affinity公司。
1.4 PRMT7过表达稳转细胞株的构建
将状态良好的前列腺癌细胞传代至六孔板中,至第2天汇合度达到40%50%。将病毒浓缩液从-80 ℃拿出放冰上融化,取200 μL病毒浓缩液加入六孔板中,轻轻混匀,放回细胞培养箱中孵育。48 h后,在显微镜下观察细胞状态,在显微镜下观察感染病毒后细胞的绿色荧光的比率,加入嘌呤霉素进行筛选,每2天更换1次培养基,培养1周左右后,在荧光显微镜下观察荧光达到90%时即构建稳转株成功,后续降低嘌呤霉素浓度维持培养得到过表达PRMT7的LNCaP细胞株PRMT7-L和过表达PRMT7的PC3细胞株PRMT7-P。
1.5 细胞划痕
细胞在六孔板中生长汇合度达到80%后,用20 μL移液管尖端借助直尺于六孔板每个孔划4条平行线。使用PBS轻柔的洗涤3次,加入无血清培养基在显微镜下观察确认无悬浮细胞后,定点在4倍物镜下拍照。24 h后,再在定点进行拍照。
1.6 Transwell迁移
每个Transwell小室种植50 000细胞,培养48 h后,使用乙醇固定,结晶紫染色,使用棉签擦去未穿过小室的细胞后在光学显微镜下拍照计数。
1.7 Transwell侵袭
基底膜基质(美国BD公司)用1∶5的培养基稀释,每个Transwell小室加入稀释后的基质胶50 μL。每个Transwell小室种植50 000个细胞,培养48 h后,使用乙醇固定,结晶紫染色,使用棉签擦去未穿过小室的细胞后在光学显微镜下拍照计数。
1.8 转录测序和蛋白组分析
在3个不同时间点收取状态良好的细胞沉淀送至公司进行转录组测序和Label-free蛋白组分析。P<0.05,|log2FoldChange|>0作为筛选差异基因的标准。P<0.05,FoldChange>1.5筛选出表达上调的蛋白;P<0.05,FoldChange<0.67,筛选出表达下调的蛋白。
1.9 siRNA转染
将状态良好的细胞传代至六孔板中使第2天细胞汇合度达到70%,每孔换上2 mL新鲜培养基;每个孔准备1个洁净无菌的离心管,加入125 μL Opti-MEM培养基(美国Gibco公司),再加入100 pmoL siRNA轻轻吹打混匀后再加入4 μL Lipo8000转染试剂(上海碧云天生物技术有限公司),轻轻吹打混匀。配制完成后,室温存放6 h内稳定,取125 μL混合物,均匀滴加到整个孔内,随后轻轻混匀,继续培养约23 d后,收取细胞用Western印迹法检测siRNA对于靶基因的下调效果。
1.10 统计学处理
2 结 果
2.1 PRMT7在前列腺组织和细胞中的表达水平
通过检索GTEx和TCGA数据库得到PRMT 7在正常前列腺组织和前列腺癌组织的表达水平。PRMT7在正常152例前列腺组织中的转录水平高于496例前列腺癌组织,差异具有统计学意义(P<0.01),见图1A。本次又检测了PRMT7在正常前列腺上皮细胞RWPE-1和4种前列腺癌细胞LNCaP、PC3、22RV1、DU145的表达水平,发现PRMT7在正常前列腺上皮细胞的表达高于前列腺癌组织,表达差异具有统计学意义(P<0.001),见图1B。
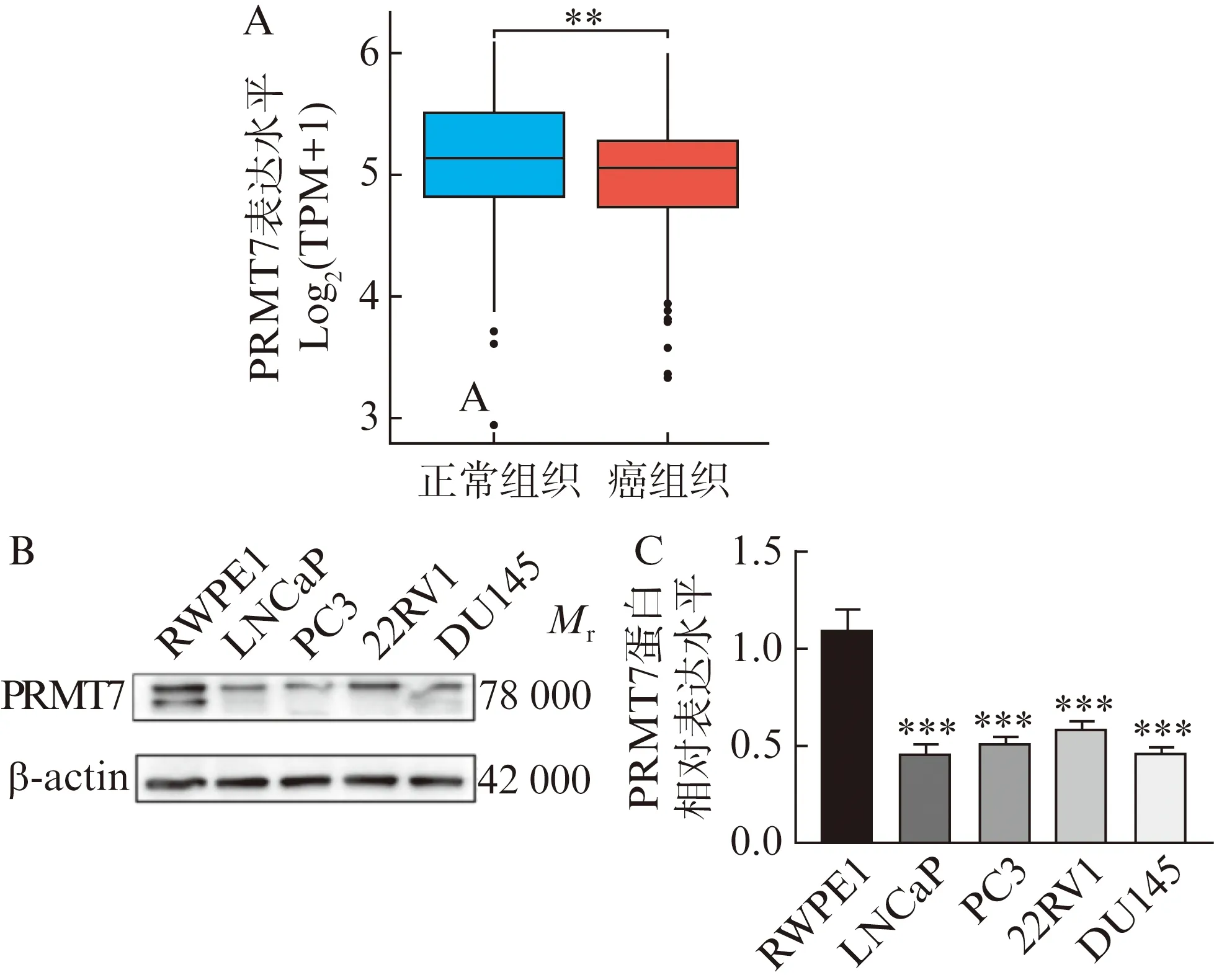
图1 PRMT7在前列腺癌组织和细胞系下调表达Fig.1 PRMT7 is down-regulated in prostate tissues and cell linesA: 数据库分析正常前列腺组织和前列腺癌组织中PRMT7的表达,**P<0.01;B: Western印迹法检测PRMT7在正常前列腺上皮细胞和4种前列腺癌细胞的蛋白表达水平;C: PRMT7在不同细胞中表达相对柱状图,***P<0.001
2.2 PRMT7抑制前列腺癌细胞迁移和侵袭
通过慢病毒感染构建了雄激素依赖型前列腺癌细胞LNCaP、雄激素非依赖型前列腺癌细胞PC3稳定过表达PRMT7细胞株。通过细胞划痕实验、Transwell迁移实验,检测PRMT7过表达对前列腺癌细胞的迁移能力的影响,结果显示PRMT7抑制前列腺癌细胞的体外迁移能力(P<0.000 1),见图2A、B。通过Transwell侵袭实验,检测PRMT7过表达对前列腺癌细胞的侵袭能力的影响,结果显示PRMT7抑制前列腺癌细胞的体外侵袭能力(P<0.000 1),见图2C。
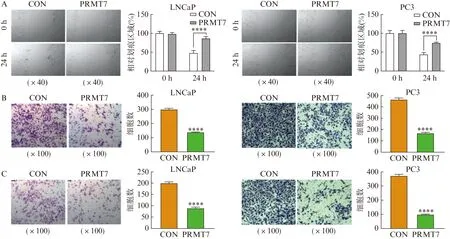
图2 PRMT7抑制前列腺癌细胞LNCaP和PC3迁移和侵袭Fig.2 PRMT7 inhibits the migration and invasion of prostate cancer LNCaP and PC3 cellsA: 细胞划痕实验检测过表达PRMT7对前列腺癌细胞LNCaP、PC3迁移的影响(n=3),****P<0.000 1;B: 细胞Transwell迁移实验检测过表达PRMT7对前列腺癌细胞LNCaP、PC3迁移的影响(n=3),****P<0.000 1;C: 细胞Transwell侵袭实验检测过表达PRMT7对前列腺癌细胞LNCaP、PC3侵袭的影响(n=3),****P<0.000 1
2.3 PRMT7影响前列腺癌细胞的转录水平
通过对PRMT7过表达稳转细胞株LNCaP及其对照组细胞进行RNA-seq,PRMT7上调545个基因转录,下调612个基因转录(P<0.05)。GO分析显示,差异表达基因富集的信号通路包括细胞外基质,见图3A。KEGG分析显示,差异表达基因富集的信号通路包括细胞黏附分子(CAMs),见图3B。在肿瘤转移相关基因中,PRMT7显著上调KISS1R的转录水平,见图3C。
2.4 PRMT7影响前列腺癌细胞的翻译水平
通过对PRMT7过表达稳转细胞株LNCaP及其对照组细胞进行蛋白测序,PRMT7上调17个蛋白,下调22个蛋白的表达(P<0.05),见图3D。上调最显著的蛋白是MAP2,它与肿瘤转移相关,见图3E。Western印迹法结果显示,LNCaP和PC3细胞中MAP2表达上调。本研究发现PRMT7通过RNA测序在LNCaP细胞中下调S100A4的表达(P<0.01);通过Western印迹法检测LNCaP细胞中S100A4的水平;在PC3中,观察到同样的趋势,S100A4表达下调,见图3F。
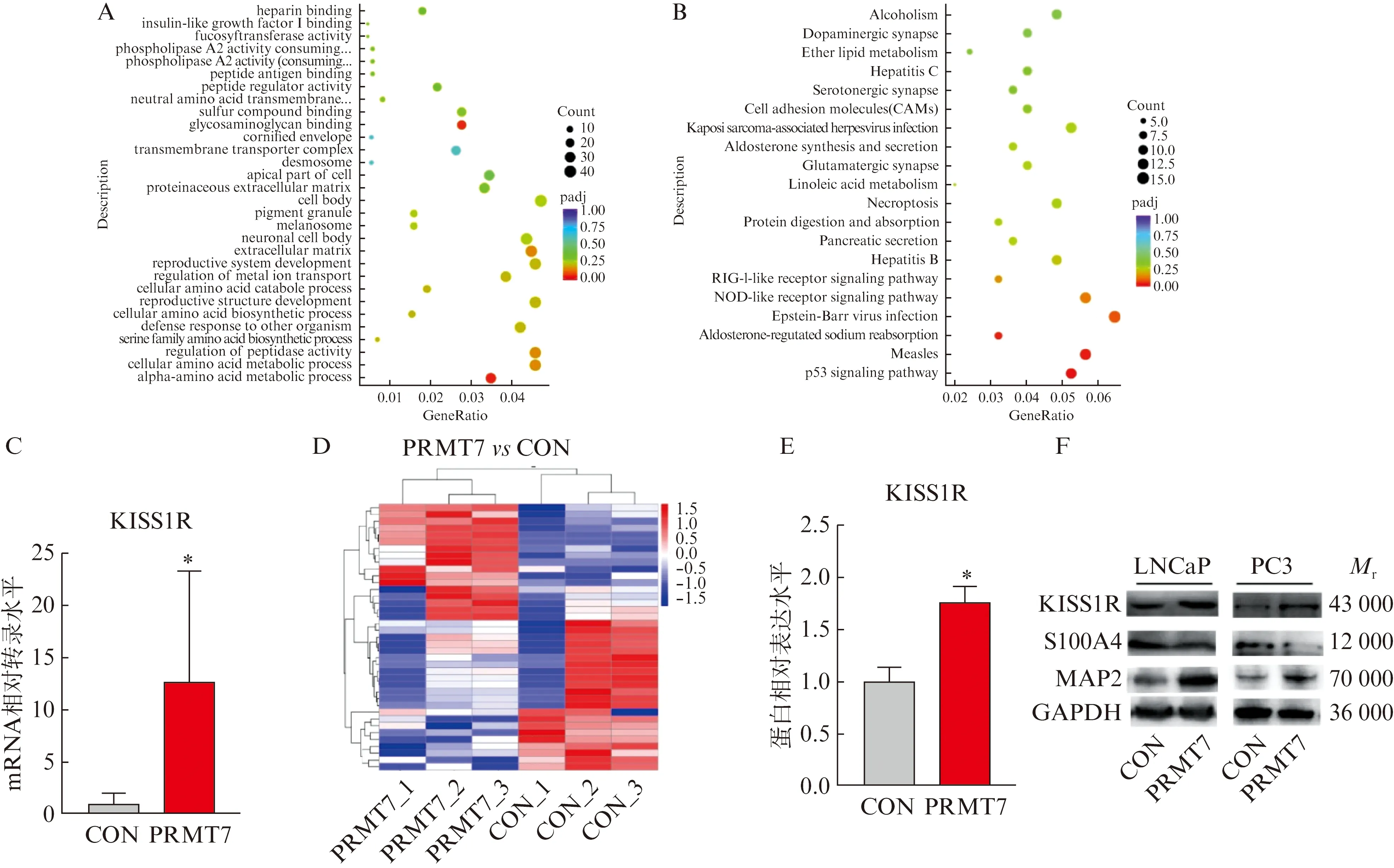
图3 PRMT7影响前列腺癌细胞的转录和蛋白水平Fig.3 PRMT7 affectes transcription and protein levels in prostate cancer cellsA: 差异基因GO功能分析 ;B: 差异基因KEGG功能分析;C: 转录测序检测KISS1R基因转录水平,*P<0.05;D: 蛋白测序差异蛋白热图;E: 蛋白组分析检测MAP2蛋白表达水平,*P<0.05;F: Western印迹法检测在过表达PRMT7稳转株中与前列腺癌细胞转移相关蛋白的表达水平
2.5 PRMT7调控下游蛋白KISS1R的表达
为了研究KISS1R是否能挽救PRMT7对前列腺癌细胞迁移和侵袭的抑制作用,在PRMT7-L和PRMT7-P中敲低KISS1R蛋白。通过细胞划痕实验、Transwell迁移实验,检测在PRMT7-L和PRMT7-P细胞株中敲低KISS1R对前列腺癌细胞的迁移能力的影响,结果显示siKISS1R能够逆转PRMT7抑制前列腺癌细胞的体外迁移能力(P<0.000 1),见图4A、B。通过Transwell侵袭实验,检测在PRMT7-L和PRMT7-P细胞株中敲低KISS1R对前列腺癌细胞的侵袭能力的影响,结果显示siKISS1R能够逆转PRMT7抑制前列腺癌细胞的体外侵袭能力(P<0.000 1),见图4C。Western印迹法显示,在PRMT7-L和PRMT7-P中,siKISS1R还逆转了与前列腺癌转移相关蛋白的表达,MAP2表达下调,S100A4表达上调,见图4D。PRMT7通过上调KISS1R的表达抑制前列腺癌细胞的迁移和侵袭并且改变了前列腺癌转移相关蛋白S100A4、MAP2的表达。

图4 PRMT7调控下游蛋白KISS1R的表达Fig.4 PRMT7 regulates downstream protein KISS1R expressionA: 细胞划痕实验检测敲低KISS1R对PRMT7-L和PRMT7-P迁移的影响(n=3),****P<0.000 1;B: 细胞Transwell迁移实验检测敲低KISS1R对PRMT7-L和PRMT7-P迁移的影响(n=3),****P<0.000 1;C: 细胞Transwell侵袭实验检测敲低KISS1R对PRMT7-L和PRMT7-P侵袭的影响(n=3),****P<0.000 1;D: Western印迹法检测KISS1R敲降后PRMT7-L和PRMT7-P中KISS1R、S100A4、MAP2的表达水平
3 讨 论
前列腺癌转移机制的表观遗传学研究是当前研究的热点。有报道称,Ⅰ型和Ⅱ型PRMTs的过表达参与了前列腺癌的发生、发展、侵袭和转移。通过生物信息学数据挖掘,本研究发现PRMT7表达与前列腺癌分期呈负相关[12]。前列腺是男性特有的器官;PRMT7在雄性生殖细胞中大量表达,PRMT7敲除小鼠在胚胎发育过程中生殖细胞数量和睾丸大小显著减少[13]。PRMT7在雄性生殖细胞系H19印迹基因甲基化过程中起关键作用[14]。因此,PRMT7是研究前列腺癌发生发展的一个有前景的上游靶点。本研究选取了雄激素依赖型和雄激素非依赖型前列腺癌细胞,结果显示,PRMT7在前列腺癌中与雄激素敏感无关。
KiSS-1转移抑制受体(KISS1R),又称G蛋白偶联受体54(GPR54),最初被归类为黑色素瘤转移抑制因子。在许多不同的癌症中,KISS1/KISS1R系统发挥着抑制肿瘤转移的作用。在一项66例患者研究中,KISS1R高表达的结直肠肝转移患者(67.9%)的5年生存率是KISS1R低表达患者(39.3%)的1.7倍。在另一项研究中,66例患者中较高的KISS1R表达与长期总生存期呈正相关[15]。在子宫内膜癌中,KISS1R已被确定为抑制转移的靶点[16]。在食管鳞状细胞癌中,KISS1R的丢失容易导致淋巴转移[17]。一项研究基于186例手术前列腺组织标本,免疫组化显示KISS1R在正常前列腺组织中表达较高[18]。另一项研究也发现,KISS1R在原发性和转移性前列腺癌中的表达水平较低,且与临床分期密切相关。在细胞水平上,高转移细胞系PC-3M的KISS1R表达低于PC3、DU-145和MDA-PC-2b[19]。KISS1R参与前列腺癌细胞的迁移和侵袭。
前列腺癌转移相关蛋白S100A4、MAP2的表达变化调控前列腺癌细胞侵袭和迁移的表型。S100A4是钙结合蛋白,是S100蛋白家族的成员,参与细胞骨架与细胞膜的相互作用。它与多种恶性肿瘤的转移有关,可在前列腺癌中发挥作用。在73例患者的组织中,S100A4的表达随着恶性程度的增加而增加。在前列腺增生中,染色较弱或无染色是常见的,然而在癌症中可观察到强染色[20]。骨转移性前列腺癌细胞在mRNA和蛋白水平上可存在S100A4高表达[21]。在前列腺癌细胞中,S100A4敲低可以抑制PC3[22]和LNCAP-LA[23]的迁移和侵袭能力。在裸鼠皮下注射S100A4的siRNA,可通过减少肿瘤血管抑制肿瘤生长[24]。前列腺根除手术后S100A4蛋白表达水平显著降低,在良性前列腺增生男性血清中表达水平较低[25]。微管相关蛋白2是MAP家族成员之一,通过附着在微管上增加蛋白的稳定性。Fisetin通过上调MAP2的表达抑制前列腺癌细胞的增殖、迁移和侵袭[26]。
综上所述,PRMT7对前列腺癌的转移具有保护作用。PRMT7在前列腺癌组织和细胞系中下调表达。PRMT7通过上调KISS1R抑制体外前列腺癌细胞的迁移和侵袭。这些发现表明了PRMT7在前列腺癌远处转移中的潜在重要作用。
