以皮下结节首诊的转移性透明细胞性肾细胞癌一例
2023-05-15张晓莹
赵 晶 张晓莹 李 晶
1山东省立第三医院皮肤科,山东济南, 250000;2山东省立第三医院病理科,山东济南, 250000
内脏系统恶性肿瘤可通过血管、淋巴管或直接扩散等转移至皮肤,出现皮肤转移癌。皮肤转移癌比较少见,临床表现多样,无特异性,常常误诊,且一旦出现往往提示预后不佳。近日我科接诊一例患者,主诉右侧季肋部皮下结节,经组织病理检查联合免疫组化最后确诊为透明细胞性肾细胞癌皮肤转移,现报道如下。
临床资料患者,男,63岁,右侧季肋区皮下结节4个月余,无特殊感觉。自诉曾于当地诊所就诊,考虑“粉瘤”,给予“针刺、挤压”等处理,无明显变化。后结节渐增大,遂于2022年3月1日来我科就诊。皮肤科情况:右侧季肋区可见一皮下结节,约3 cm×2 cm,表面大致呈肤色,中央可见抠抓后浅褐色痂,质软,无触痛(图1)。拟诊:脂肪瘤?建议进一步手术切除并行组织病理检查。
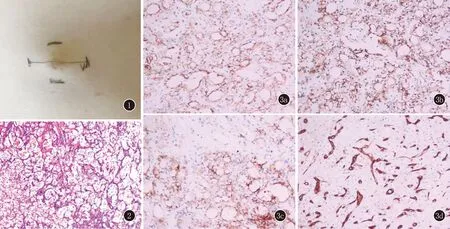
图1 右侧季肋区皮下结节,约3 cm×2 cm,表面呈肤色,中央可见抠抓后浅褐色痂 图2 皮下组织内查见大量透明细胞聚集的癌巢(HE,×200) 图3 免疫组化 3a:CK阳性(×200);3b:CAIX阳性(×200);3c:CD10局灶阳性(×200);3d:CD34血管阳性(×200)
术前皮下结节超声检查示:皮下脂肪层内大小约2.8 cm×0.7 cm低回声团,边界清,形态欠规则,回声欠均匀,周边及内部可见血流信号,表皮样囊肿?纤维瘤?皮下结节全切后组织病理示:皮下组织内查见大量透明细胞聚集(图2),怀疑肾脏来源肿瘤;进一步免疫组化检查示(图3):CK(+),CAIX(+),PAX-8(弱+),CD10(局灶+),TFE3(弱+),CD34(血管+),CD68(组织细胞+),CD163(组织细胞+),Fli-1(血管+),S100(-),ERG(-),CK7(-),HMB45(-)MelanA(-),KI67(10%~20%+)。组织病理检查结合免疫组化,符合转移性透明细胞性肾细胞癌。完善相关检查,肾脏超声示:右肾实性占位。PET-CT示:右肾肿瘤诊断明确,左肺上叶、左侧肾上腺不除外转移。诊断:透明细胞性肾细胞癌多发转移。
治疗:2022年3月17日于全麻下行腹腔镜下右肾根治性切除术+右肾周粘连松解术。术后组织病理示:透明细胞性肾细胞癌,II级,免疫组化:PAX8(+),CD10(+),CA9(+),Vimentin(弱+),CK7(-)。术后规律服用培唑帕尼,现密切随访中。
讨论皮肤转移癌50~70岁发病率最高[1],来源于内脏,在男性中,皮肤转移癌主要来源于肺癌、大肠癌、口腔,而女性的原发肿瘤多为乳腺癌、卵巢癌、口腔。肾脏来源的皮肤转移癌比较罕见,且主要见于男性患者,约有4.7%[2]。皮肤转移癌较少见,10%内脏肿瘤可出现皮肤转移,而这其中有22%的病例通过皮肤表现作为首发症状进而确诊内脏肿瘤[3]。内脏肿瘤出现皮肤转移往往预后不良,在诊断出皮肤转移的情况下,患者的平均生存期约为7.5个月,而且,内脏肿瘤出现皮肤转移时,往往提示肿瘤细胞已经广泛扩散,有76.6%的患者在诊断时已广泛转移到淋巴结和其他器官[2]。故了解皮肤转移的临床表现和正确诊断对及时治疗原发性恶性肿瘤是至关重要的。
透明细胞性肾细胞癌作为肾细胞癌中最常见的类型,具有较强的侵袭转移性,文献报道,30%患者在根治性肾切除术或部分肾切除术后发生转移,20%~30%患者在局部症状和体征出现之前就已经发生了转移。累及肺、肝、骨、肾上腺和脑,皮肤转移罕见,而以皮肤转移为首发症状就诊者则更少[4,5]。
透明细胞性肾细胞癌发生皮肤转移后临床表现不典型,最常见表现为无痛、质硬的结节,由于缺乏特异性,常被误诊为脂肪瘤、皮样囊肿、纤维瘤等。最终确诊需行组织病理检查,表现为大量透明细胞聚集,应与以下原发性皮肤透明细胞肿瘤鉴别:透明细胞基底细胞癌、透明细胞棘皮瘤、透明细胞鳞状细胞癌、汗管瘤透明细胞亚型、良性及恶行的透明细胞汗腺瘤、皮脂腺癌等[6]。除了组织病理检查,有报道通过彩超诊断肾癌皮肤转移的病例,皮肤转移性肿瘤声像图像上呈圆形或椭圆形,欠规则,内部多为低回声或等回声,强弱分布不均匀,与周围组织分界较清楚,彩超可探及丰富的血流信号[7]。与本例患者声像图一致,但患者初诊时超声检查未明确诊断,需进一步整理总结皮肤转移肿瘤的声像特点。
透明细胞性肾细胞癌发生皮肤转移后预后不佳,且常合并有其他器官或者淋巴结多发转移,中位生存期约为12个月,5年生存率不足10%[4]。治疗多为手术切除联合放疗或分子靶向药物治疗。本例患者行右肾根治性切除术后规律服用靶向药物培唑帕尼治疗,现术后7个月密切随访中。
