基于Q-Orbitrap MS/MS的山银花标准汤剂多指标成分定量及指纹图谱研究*
2023-05-13孙冬梅刘晓霞陶晨璐刘艳梅李振雨朱德全陈向东
孙冬梅,丁 青,刘晓霞,陶晨璐,刘艳梅,李振雨,朱德全,陈向东
(广东一方制药有限公司/广东省中药配方颗粒企业重点实验室,广东 佛山 528244)
中药饮片标准汤剂是以中医理论为指导、临床应用为基础,参考现代提取方法,经标准化工艺制备而成的单味中药饮片水煎剂。中药饮片标准汤剂可用于标化临床用药,保障用药的准确性和剂量的一致性,规范目前临床广泛使用的包括配方颗粒在内的新型饮片形式[1]。
山银花,主产于湖南南部及西部、广西东北部、贵州东部和西北部[2],为忍冬科植物灰毡毛忍冬Lonicera macranthoidesHand.-Mazz.、红腺忍冬Lonicera hypoglaucaMiq.、华南忍冬Lonicera confusaDC.或黄褐毛忍冬Lonicera fulvotomentosaHsu et S.C.Cheng的干燥花蕾或带初开的花[3]。山银花味甘,性寒,归肝、心、肺经,有清热解毒、疏风散热之功。其主要用于治疗痈肿疔疮、喉痹、丹毒、热毒血痢、风热感冒、温病发热。目前,从山银花中已分离鉴定出200多种化合物,主要包括有机酸类、黄酮类、三萜皂苷类、生物碱类、环烯醚萜类等[4]。山银花中的酚酸类成分对多种致病菌和病毒具有较强的抑制和杀灭作用,皂苷类成分具有保肝作用[5]。山银花的相关文献报道多集中于药材、饮片等原料的质量研究[6-8],而关于山银花标准汤剂质量研究内容颇少。本研究收集了15批来自广西壮族自治区桂林市、湖南省邵阳市、湖南省怀化市、贵州省遵义市的山银花药材,并按照标准汤剂制备方法制备成山银花标准汤剂,建立了山银花标准汤剂指纹图谱结合多成分定量测定的检测方法,以及对共有指纹峰采用Q-Orbitrap MS/MS技术进行鉴定,对山银花标准汤剂进行全面的质量评价,旨在为以标准汤剂为基础的其他山银花制剂质量评价提供参考依据。
1 仪器与材料
1.1 仪器 VanquishTM超高效液相色谱仪(赛默飞世尔科技有限公司);Q-Exactive-Orbitrap型Thermo Vanquish Flex超高效液相-Thermo Fisher 高分辨质谱联用仪,配备光电二级管阵列检测器(DAD)(赛默飞世尔科技有限公司);Waters ACQUITY HSS T3色谱柱(100 mm×2.1 mm,1.8 μm);ME204E型万分之一天平(METTLER TOLEDO公司);XP26型百万分之一天平(METTLER TOLEDO 公司);HWS-28型电热恒温水浴锅(上海一恒科技有限公司);KQ-500DE型超声清洗仪(昆山市超声仪器有限公司)。
1.2 试剂 绿原酸对照品(批号:110753-201817,含量:96.80%)、灰毡毛忍冬皂苷乙对照品(批号:111814-201604,含量:94.40%)、川续断皂苷乙对照品(批号:111813-201804,含量:96.80%)均购于中国食品药品检定研究院;新绿原酸(批号:wkq18030107,含量:98.0%)、异绿原酸A(批号:wkq18041207,含量:98.0%)、异绿原酸C(批号:wkq18050905,含量:98.0%)、异绿原酸B(批号:wkq21022206,含量:98.0%)均购于四川维克奇生物技术有限公司;乙腈为色谱纯,购自默克股份有限公司;甲酸为色谱纯,购自上海安谱实验科技股份有限公司;甲醇为分析纯,购自西陇科学股份有限公司;磷酸为色谱纯,购自天津市科密欧化学试剂有限公司;Milli-Q超纯水实验室自制。
1.3 材料 试验用15批山银花于2020年6—7月采摘,采摘后的药材以蒸汽杀青,置50~55 ℃电热恒温鼓风干燥箱中烘干,即得。样品依次编号为S1~S15,样品信息见表1,经广东一方制药有限公司魏梅主任中药师鉴定,为忍冬科植物灰毡毛忍冬Lonicera macranthoidesHand.-Mazz.。15批样品按照2020年版《中华人民共和国药典》山银花项下规定进行检验,符合规定。

表1 山银花样品信息
2 方法与结果
2.1 山银花标准汤剂的制备 取山银花饮片100 g,置电热陶瓷壶中,加水煎煮2次,第1次煎煮加12倍量水,浸泡30 min,武火(500 W)加热煮沸后文火(200 W)保持微沸30 min,用350目筛趁热过滤,滤液迅速用冷水冷却;第2次煎煮加10倍量水,武火(500 W)加热煮沸后文火(200 W)保持微沸25 min,用350目筛趁热过滤,滤液迅速用冷水冷却;合并2次滤液,减压浓缩至清膏体积约为150 mL,分装至10 mL西林瓶中,每瓶分装2 mL,真空冷冻干燥,取出,轧铝盖,即得。
2.2 指纹图谱方法
2.2.1 对照品溶液的制备 取绿原酸对照品2.801 mg、新绿原酸对照品2.297 mg、异绿原酸A对照品2.328 mg、异绿原酸C对照品2.130 mg、灰毡毛忍冬皂苷乙对照品2.067 mg、川续断皂苷乙对照品2.146 mg、异绿原酸B对照品2.129 mg,置于5 mL容量瓶中,加甲醇溶解制成质量浓度分别为542.274、450.212、456.288、417.480、390.250、415.466、417.284 μg/mL 的混合对照品溶液a。取隐绿原酸对照品2.122 mg,置于5 mL溶量瓶中,加甲醇溶解制成质量浓度415.912 μg/mL的对照品溶液b。
2.2.2 供试品溶液的制备 取山银花标准汤剂冻干粉约0.2 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇50 mL,密塞,称定质量,超声处理30 min,放冷,再称定质量,用70%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.2.3 色谱条件 色谱柱:Waters ACQUITY HSS T3(100 mm×2.1 mm,1.8 μm),流动相为乙腈(A)-0.05%磷酸溶液(B),梯度洗脱,0~1 min,7%A~10%A,1~9 min,10%A~21%A,9~24 min,21%A~42%A;流速:0.3 mL/min;柱温:30 ℃;进样量:1 μL;检测波长:210 nm。
2.3 指纹图谱方法学验证
2.3.1 精密度试验 取山银花标准汤剂S1供试品溶液,按“2.2.3”项下色谱条件进样,连续进样测定6次,以16号峰(异绿原酸A)为参照峰,计算21个指纹峰的相对保留时间RSD值在0.03%~0.24%范围内,相对峰面积RSD值在0.26%~0.86%范围内,表明仪器精密度良好。
2.3.2 稳定性试验 取山银花标准汤剂S1供试品溶液,于室温下放置,分别在制备后的2、5、8、13、16 h,按“2.2.3”项下色谱条件进样测定,以16号峰(异绿原酸A)为参照峰,计算21个指纹峰的相对保留时间RSD值在0.17%~0.89%范围内,相对峰面积RSD值在1.05%~2.13%范围内,表明供试品溶液在16 h内稳定。
2.3.3 重复性试验 取同一批山银花标准汤剂6份,按“2.2.2”项下制备6份供试品溶液,按“2.2.3”项下色谱条件进样测定,以16号峰(异绿原酸A)为参照峰,计算21个指纹峰的相对保留时间RSD值在0.14%~0.49%范围内,相对峰面积RSD值在0.97%~2.43%范围内,表明该方法重复性良好。
2.4 指纹图谱测定与分析 取15批不同产地的山银花标准汤剂,按“2.2.2”项下制备供试品溶液,按“2.2.3”项下色谱条件进样测定,记录15批山银花标准汤剂色谱图,并将所有的色谱图导入《中药色谱指纹图谱相似度评价系统》2012版进行分析。以S1为参照图谱,对15批山银花标准汤剂指纹图谱共有峰进行匹配,选择分离度较好,峰型对称,峰纯度高的色谱峰为指纹峰,共标定21个指纹峰,共有峰模式见图1,山银花标准汤剂S1和对照品色谱图见图2。采用平均数法生成对照指纹图谱,进行相似度计算,15批不同产地的山银花标准汤剂样品相似度在0.90以上,表明不同产地的山银花标准汤剂相似度较高。由于16号峰峰面积较大,成分已知,出峰位置居中,因此选择16号峰(异绿原酸A)为参照峰,计算15批山银花标准汤剂共有峰的相对保留时间RSD值在0.04%~0.64%范围内,相对峰面积RSD值在18.80%~123.73%范围内。

图1 15 批山银花标准汤剂指纹图谱叠加图及对照指纹图谱

图2 HPLC 色谱图
2.4.1 聚类分析 采用SPSS 20.0软件,对15批山银花标准汤剂指纹图谱共有峰峰面积进行标准化处理,采用Ward法,以平方欧氏距离为测度,全矩从0到1标准化转化,进行聚类分析,结果见图3。当分类间距离在15时,山银花标准汤剂被分为4类,其中S1、S4~S12、S14~S15聚为一类,S2、S3、S13各自聚为一类;而S2、S3、S13都来自于广西壮族自治区桂林市;分类结果表明当前方法不可区分不同产地的山银花标准汤剂,相同产地或不同产地的山银花标准汤剂既具有相似性又具有差异性。

图3 15 批山银花标准汤剂聚类分析树状图
2.4.2 主成分分析 采用SPSS 20.0软件,将15批山银花标准汤剂指纹图谱共有峰峰面积进行标准化处理,计算主成分特征值、累积贡献率及主成分得分。以特征值大于1为标准,提取出的主成分有5个,累积方差贡献率为87.340%,表明提取出的5个主成分反映了15批山银花标准汤剂指纹图谱的主要信息,碎石图进一步说明了5个主成分可以表征山银花标准汤剂的整体特征。(见图4)根据载荷矩阵分析结果,可知,主成分1与10个指纹峰有关,主成分2与11个指纹峰有关,主成分3与10个指纹峰有关,主成分4与16个指纹峰有关,主成分5与12个指纹峰有关,表明山银花的质量差异是由多个成分共同作用引起。(见表2)

表2 15 批山银花标准汤剂载荷矩阵图

图4 15 批山银花标准汤剂主成分分析碎石图
2.4.3 正交偏最小二乘法判别分析 为了进一步研究不同批次间山银花标准汤剂的质量差异,将15批山银花标准汤剂指纹图谱共有峰峰面积同时导入SIMCA14.1软件,采用正交偏最小二乘法判别分析(OPLS-DA),以21个指纹峰峰面积为变量建立OPLS-DA。根据结果可知,R2x为0.993,R2y为0.826,Q2为0.787,表明模型可靠,预测程度较好。根据变量权重VIP值筛选引起不同批次之间质量差异的特征性成分,选取VIP值>1的变量指标为质量标志物。结果表明,在21个指纹峰中峰3、峰5(新绿原酸)、峰6、峰7、峰11(隐绿原酸)、峰12、峰15(异绿原酸B)、峰16(异绿原酸A)、峰18(异绿原酸C)、峰21(川续断皂苷乙)的VIP值均大于1。(见图5)这些成分是15批山银花标准汤剂之间产生差异的主要原因,为了更加全面、有效评价山银花标准汤剂质量,应重点关注上述成分的质量变化。

图5 15 批山银花标准汤剂各成分VIP 值图

图6 山银花标准汤剂负离子模式(A)和正离子模式(B)下一级离子流图
2.5 共有峰的鉴定
2.5.1 色谱条件 色谱柱:Waters ACQUITY HSS T3(100 mm×2.1 mm,1.8 μm),流动相为乙腈(A)-0.1%甲酸溶液(B),梯度洗脱,0~1 min,7%A~10%A,1~9 min,10%A~21%A,9~24 min,21%A~42%A;24~48 min,42%A~100%A;流速:0.3 mL/min;柱温:30 ℃;进样量:1 μL;检测波长:210 nm。
2.5.2 质谱条件 采用电喷雾离子源(ESI),喷雾电压为3.2 kV(+/-),S-lens电压为50 V;鞘气流速为35 arb;辅助气流速为10 arb;毛细管温度为350 ℃;质荷比范围为100~1 500;数据采集模式:正负离子同时扫描(Full ms dd-MS2 Discovery);分辨率为17 500,碰撞能(NCE)为20 V。
取“2.2.2”项下制备供试品溶液,按照“2.5”项下的色谱与质谱条件进行分析,得到山银花标准汤剂正、负离子模式下的一级离子流及二级离子流图。(见图3)根据实际测得的相对分子质量与理论相对分子质量二者偏差小于5 ppm,同位素丰度比及一级、二级质谱碎片信息以及文献报道等,结合Xcalibur数据处理平台、Thermo m/z Vault数据库,对21个共有指纹峰进行化合物推断鉴别,鉴定结果见表3。其中8种成分采用对照品对比确认,分别为峰5(新绿原酸)、峰9(绿原酸)、峰11(隐绿原酸)、峰15(异绿原酸B)、峰16(异绿原酸A)、峰18(异绿原酸C)、峰19(灰毡毛忍冬皂苷乙)、峰21(川续断皂苷乙);其余13个成分根据产生的二级质谱碎片离子与文献报道进行比对推导;例如保留时间为1.20 min的峰1,正离子扫描模式下准分子离子峰为(m/z)268.103 7,二级裂解碎片可见(m/z)136.061 6、(m/z)137.066 0,通过Xcalibur数据处理平台、Thermo m/z Vault数据库鉴定该化合物为腺苷;保留时间为3.68 min的峰5,负离子扫描模式下准分子离子峰为(m/z)353.087 7,二级裂解碎片可见(m/z)179.034 1、(m/z)191.055 4、(m/z)192.058 7,通过Xcalibur数据处理平台、Thermo m/z Vault数据库以及对照品比对确定该化合物为新绿原酸;保留时间为4.93 min的峰8,负离子扫描模式下准分子离子峰为(m/z)389.108 8,二级裂解碎片可见(m/z)345.119 3、(m/z)209.048 8,通过Xcalibur数据处理平台以及文献报道鉴定该化合物为断马钱子苷半缩醛内酯。

表3 山银花标准汤剂共有指纹峰化学成分鉴定结果
2.6 多成分含量测定 山银花标准汤剂指纹图谱化学剂量分析结果表明峰3、峰5(新绿原酸)、峰6、峰7、峰11(隐绿原酸)、峰12、峰15(异绿原酸B)、峰16(异绿原酸A)、峰18(异绿原酸C)、峰21(川续断皂苷乙)为质量标志物,而峰9(绿原酸)、峰19(灰毡毛忍冬皂苷乙)既为共有峰,且成分已知,因此本试验在指纹图谱的基础上,对上述已采用对照品确定的8种成分进行含量测定。
2.6.1 线性关系考察 精密吸取混合对照品溶液a 1 mL,分别置于2、5、10、20 mL容量瓶中,加甲醇稀释至刻度,进样分析。精密吸取对照品溶液b 1 mL,分别置于2、5、10、20 mL容量瓶中,加甲醇稀释至刻度,进样分析。记录8种成分的峰面积,以进样的质量浓度为横坐标(x),以峰面积为纵坐标(y),绘制标准曲线,线性结果见表4。
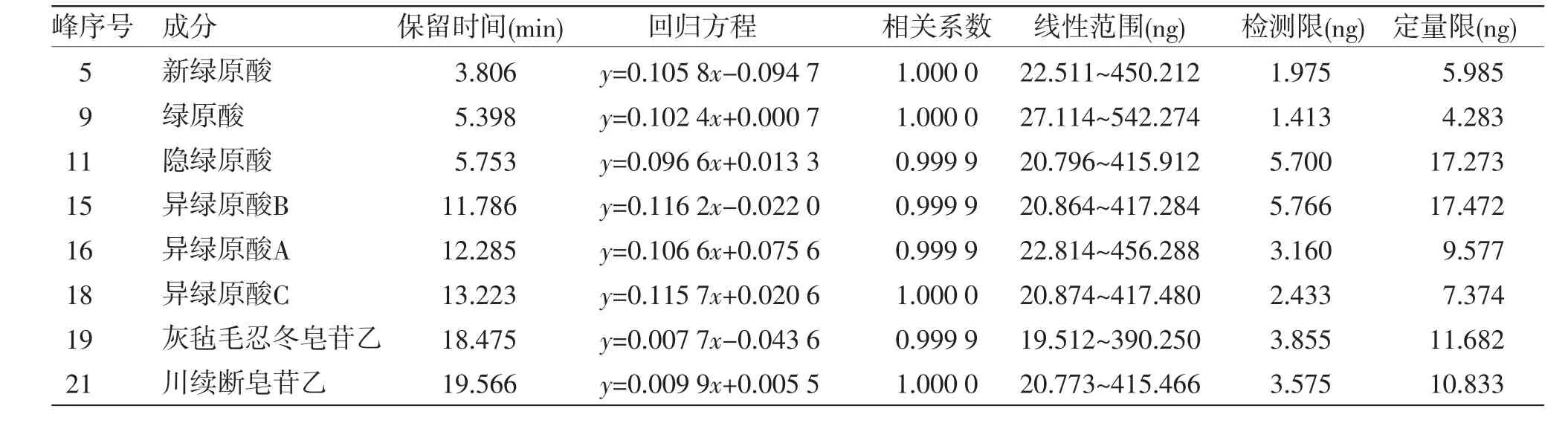
表4 8 种成分的保留时间、线性回归方程、相关系数、线性范围、检测限和定量限
2.6.2 精密度试验 取“2.2.1”项下对照品溶液,按“2.2.3”项下色谱条件进样,连续进样测定6次,记录8种成分的峰面积,计算RSD值。结果显示新绿原酸、绿原酸、隐绿原酸、异绿原酸B、异绿原酸A、异绿原酸C、灰毡毛忍冬皂苷乙、川续断皂苷乙的峰面积RSD值在0.23%~0.96%范围内,表明仪器的精密度良好。
2.6.3 稳定性试验 取山银花标准汤剂冻干粉(S1)供试品溶液,分别在制备后的0、2、8、12、16、24 h进样测定,记录8种成分的峰面积,计算峰面积的RSD值,结果显示在24 h内新绿原酸、绿原酸、隐绿原酸、异绿原酸B、异绿原酸A、异绿原酸C、灰毡毛忍冬皂苷乙、川续断皂苷乙的峰面积RSD值在0.23%~0.99%范围内,表明供试品溶液在24 h内稳定性良好。
2.6.4 重复性试验 取同一批山银花标准汤剂冻干粉(S1)样品,按“2.2.2”项下供试品制备方法平行制备6份供试品溶液,按“2.2.3”项下色谱条件进样测定。记录8种成分的峰面积,并计算含量的RSD值。结果表明8种成分含量的RSD值在0.23%~2.13%范围内,表明本试验方法重复性良好。
2.6.5 加样回收率试验 取已知含量的山银花标准汤剂冻干粉(S1)样品,按对照品加入量与供试品中待测成分含量之比分别为0.5∶1、1∶1、1.5∶1设计3组,每组平行3份,分别加入8种待测成分对照品适量,按“2.2.2”项下制备6份供试品溶液,按“2.2.3”项下色谱条件进样测定,记录8种成分的峰面积,计算各成分含量及加样回收率。结果显示新绿原酸、绿原酸、隐绿原酸、异绿原酸B、异绿原酸A、异绿原酸C、灰毡毛忍冬皂苷乙、川续断皂苷乙的平均加样回收率分别为100.45%、96.38%、98.47%、103.11%、100.27%、98.59%、99.13%、99.46%,表明该方法的准确性良好
2.6.6 样品测定 对15批山银花标准汤剂冻干粉中的8种成分进行含量测定,结果见表5。

表5 15 批山银花标准汤剂中8 种成分含量测定结果(mg/g)
3 讨论
3.1 检测波长的选择 由于山银花中有机酸类、黄酮类和环烯醚萜类成分较多,因此山银花指纹图谱检测波长多集中在230~240 nm[11-12]或330~360 nm[13]。本试验采用二极管阵列检测器对山银花标准汤剂指纹图谱进行全波长扫描,发现在210 nm下指纹峰数量最多,峰容量更大;由于山银花中的专属性成分灰毡毛忍冬皂苷乙和川续断皂苷乙共轭系统少,在其他检测波长下无法检出,因此在指纹图谱和含量测定中以210 nm为检测波长以全面表征山银花标准汤剂的物质信息。
3.2 指纹图谱分析 本研究采用了聚类分析、主成分分析、正交偏最小二乘法判别分析3种模式识别方法,筛选到10种差异性质量标志物,分别为峰3、峰5(新绿原酸)、峰6、峰7、峰11(隐绿原酸)、峰12、峰15(异绿原酸B)、峰16(异绿原酸A)、峰18(异绿原酸C)、峰21(川续断皂苷乙)。朱香梅等[14]通过对山银花种植资源、化学成分进行成分归纳总结后,预测山银花中的质量标志物为绿原酸、咖啡酸、异绿原酸A、灰毡毛忍冬皂苷乙、川续断皂苷乙、木犀草苷等,部分预测指标与本研究结果相同。后续研究应重点关注这10种成分的变化,并对未定量成分建立定量分析方法,以便科学评价山银花标准汤剂的质量。
本研究发现,15批山银花标准汤剂指纹图谱的相对峰面积RSD值在18.80%~123.73%范围内,表明不同批次的山银花标准汤剂中指纹峰对应的化学成分组成比例差异较大,尤其峰2的相对峰面积RSD值最大,可能是由于该色谱峰峰面积较小,易受周围杂质峰的影响,从而导致不同批次间峰面积积分差异较大。
3.3 Q-Orbitrap MS/MS分析 本试验采用Q-Orbitrap MS/MS技术对山银花标准汤剂中的共有指纹峰对应的化学成分进行鉴定。由于山银花标准汤剂中的化合物主要为酚酸类,具有较多的羟基,可形成稳定的氧负离子,因此多数化合物在负离子模式下色谱峰的响应更好。21个共有指纹峰鉴定了18种化合物,有8种化合物已采用对照品进行确认,但是还有峰4、峰7、峰13在现有文献和数据库中尚未匹配到相对应的化合物,有待进一步研究。根据文献报道,山银花药材中还含有黄酮类成分,如紫云英苷[15]、木犀草素-7-O-β-D-半乳糖苷[16]、山奈酚-3-O-芸香糖苷[17]、木犀草素[18]等;环烯醚萜类成分,如开联番木鳖苷[19]、裂环马钱酸等;皂苷类成分,如α-常春藤皂苷元[20]、灰毡毛忍冬皂苷丙[20]、灰毡毛忍冬皂苷甲[21]等。上述成分在山银花标准汤剂中尚未检测到,可能是由于此类成分在山银花药材中含量和极性较低,在标准汤剂中转移率低,因此标准汤剂中基本无响应。
3.4 含量测定分析 本研究基于山银花标准汤剂指纹图谱,对其中6种质量标志物及2种采用对照品确认的共有成分进行定量测定。8个含量测定指标中包括酚酸类成分6个,皂苷类成分2个。研究结果显示不同批次的山银花标准汤剂中各成分含量差异较大,尤其是酚酸类成分。文献报道花蕾型灰毡毛忍冬黄白期灰毡毛忍冬皂苷乙显著降低[22],三青期的绿原酸含量最高,其次为大白、二白期,银花、金花期绿原酸含量最低[23],不同产地的山银花花蕾中绿原酸、灰毡毛忍冬皂苷乙、川续断皂苷乙的含量也存在较大差异[24],因此不同批次的山银花标准汤剂中各成分含量可能与地域因素、采收时间等有关。此外,根据文献报道[25],山银花药材中灰毡毛忍冬皂苷的含量最高,其次为绿原酸和异绿原酸A。而本研究结果也显示山银花标准汤剂中灰毡毛忍冬皂苷的含量最高,为(155.99±22.57)mg/g;其次为绿原酸(88.51±11.77)mg/g和异绿原酸A(35.99±12.69)mg/g,与文献报道结果一致,表明这些极性较大的成分从药材到标准汤剂转移率良好,可以用于标化、表征水提物的一致性。
