泻白糖浆中杏仁水的质量研究
2023-05-11王静,周军
王 静,周 军
(天津市药品检验研究院,天津 300070)
泻白糖浆为儿童中药制剂,由石膏、桑白皮、瓜蒌子、葶苈子、麻黄、甘草、前胡、紫菀、款冬花、川贝母、苦杏仁、紫苏叶油、薄荷脑共十三味药组成。该品种具有宣肺解热,化痰止咳的功效。用于伤风咳嗽,痰多胸满,口渴舌干,鼻塞不通。该制剂收载于《中华人民共和国卫生部药品标准》中药成方制剂第十五册,现行标准的【制法】项下要求“苦杏仁提取杏仁水备用”。但目前国家标准中没有统一制备杏仁水的方法,各厂家提取方法各有不同。该制剂中也未对杏仁水制定相关质量标准,经查阅相关文献发现,苦杏仁中主要有效成分为苦杏仁苷[1-3],因苦杏仁苷属芳香族氰苷,其化学名为苯羟基乙氰-β-D-葡萄糖-6-O-β-D-葡萄糖苷,该成分性质不稳定,在β-葡萄糖苷酶或加热作用下生成葡萄糖和杏仁腈,而杏仁腈可以自发或经羟基腈裂解酶作用产生氢氰酸和苯甲醛[4]。故杏仁水的主要有效成分为苯甲醛和氢氰酸。小剂量氢氰酸对呼吸中枢有镇静作用,可以麻痹咳嗽中枢,体现苦杏仁的止咳平喘等效果;而大剂量的氢氰酸进入人体后则发生中毒,氢氰酸系剧毒物质,人体内氰化物急性中毒剂量为0.5~3.5 mg/kg[5]。为了保证儿童用药的安全有效,本试验分别建立了苦杏仁苷的检查方法、氢氰酸和苯甲醛的含量测定方法,以期为完善该制剂的质量标准提供参考。
1 仪器与试药
1.1 仪器 岛津LC-20AD 高效液相色谱仪;DAD 检测器;LC Solution 工作站。Agilent 6890N 气相色谱仪;NPD 检测器;安捷伦7697A 顶空进样器。XS205 电子分析天平(瑞士梅特勒公司)。Milli-QA10 型超纯水仪(美国Millipore 公司)。
1.2 试药 苦杏仁苷(中国食品药品检定研究院,批号110820-201808,供含量测定用,含量以88.2%计);苯甲醛(北京曼哈格生物科技有限公司,批号B0002957,供含量测定用,含量以99.8%计);水中氰标准溶液(中国计量科学研究院,批号21044,供含量测定用,浓度:50.0 μg/ml);甲醇、乙腈(色谱纯,默克股份有限公司);磷酸(色谱纯,天津市赢达稀贵化学试剂厂);水为Milli-Q 超纯水;样品分别购自A、B、C 3 个厂家共计18 批次。
2 方法与结果
2.1 苦杏仁苷的检查(HPLC 法)
2.1.1 色谱条件与系统适用性试验 色谱柱:SHISEIDO CAPCELL PAK C18(250 mm×4.6 mm,5 μm);流动相:以甲醇为流动相A,水为流动相B,按照表1进行梯度洗脱;检测波长为210 nm,流速:1.0 ml/min;柱温:40 ℃,进样量:10 μl。

表1 梯度洗脱程序
2.1.2 溶液的制备
2.1.2.1 对照品溶液的制备 精密称取苦杏仁苷对照品适量,加甲醇制成每1 ml 含40 μg 的溶液,即得。
2.1.2.2 供试品溶液的制备 精密量取样品5 ml,置50 ml 量瓶中,加50%甲醇稀释至刻度,摇匀,用0.45 μm 微孔滤膜滤过,取续滤液,即得。
2.1.2.3 阴性样品溶液的制备 按处方配比,取除苦杏仁外其他药材,按【制法】项下的工艺制成制剂,再按“2.1.2.2”项下制备方法制得阴性样品溶液。
2.1.3 测定方法 分别取上述对照品溶液、供试品溶液和阴性样品溶液各10 μl,注入液相色谱仪,记录色谱图。结果详见图1。
2.1.4 样品测定 对本次抽验的3 家生产企业共计18 批样品按照“2.1.2.2”项下供试品溶液制备操作,按“2.1.1”项下色谱条件分析,结果均未检出苦杏仁苷。
2.2 氢氰酸的含量测定(GC 法)
2.2.1 色谱条件与系统适用性试验 色谱柱:Agilent HP-PLOT/Q(30 m×0.53 mm,40.0 μm)色谱柱;程序升温:初始温度100 ℃,保持2 min,以10 ℃/min 的速率升温至200 ℃,保持2 min。进样口温度:220 ℃;检测器温度:250 ℃;分流比:1∶1;顶空瓶平衡温度:85 ℃;平衡时间:30 min。

图1 对照品(A)A 厂家供试品(B)B 厂家供试品(C)C 厂家供试品(D)阴性样品(E)HPLC 色谱图
2.2.2 溶液的制备
2.2.2.1 对照品溶液的制备 精密吸取对照品溶液1 ml,加水制成每1 ml 中含1 μg 的对照品溶液。
2.2.2.2 供试品溶液的制备 精密量取本品5 ml,置10 ml 量瓶中,加50%磷酸溶液稀释至刻度,摇匀,即得。
2.2.2.3 阴性样品的制备 按处方配比,取除苦杏仁外其他药材,按【制法】项下的工艺制成制剂,再按“2.2.2.2”项下方法制得阴性样品溶液
2.2.2.4 测定方法 精密量取上述对照品溶液2 ml置于顶空瓶中,快速加入50%磷酸溶液2 ml,密封,摇匀;分别精密量取上述供试品溶液、阴性样品溶液各4 ml 置于顶空瓶中密封,将上述对照品溶液、供试品溶液及阴性样品溶液顶空进样,记录色谱图。结果见图2。

图2 对照品(A)供试品(B)阴性样品(C)空白溶剂(D)HPLC 色谱图
2.2.3 标准曲线的制备 精密量取水中氰标准溶液,加水分别制成0.005、0.20、0.50、1.00、1.70、2.50 和3.20μg/ml 的对照品溶液,按“2.2.2.4”项下方法进样测定,以峰面积为纵坐标(Y),浓度为横坐标(X)绘制标准曲线,回归方程为Y=89.497 0X-33.239 2(r=0.999 8)。结果表明,氢氰酸在0.005~3.20 μg/ml 浓度范围内,线性关系良好。
2.2.4 检出限与定量限 精密量取水中氰标准溶液加水制成0.005 μg/ml 的对照品溶液,并进行测定,按信噪比3∶1 确定检出限。精密量取水中氰标准溶液加水制成0.015 μg/ml 的对照品溶液,并进行测定,按信噪比10 ∶1 确定定量限。
2.2.5 重复性试验 取同一批样品(A 厂家,批号300099)6 份,按照“2.2.2.2”项下方法操作,按“2.2.2.4”项下测定方法进样测定,样品中氢氰酸平均值为0.950 5 μg/ml,RSD 为1.9%,符合要求。
2.2.6 精密度试验 取同一批样品(A 厂家,批号300099),按照“2.2.2.2”项下方法操作,按“2.2.2.4”项下测定方法进样测定,连续进样6 次,测定样品中氢氰酸峰面积值的RSD 为1.9%,精密度符合要求。
2.2.7 稳定性试验 取同一批样品(A 厂家,批号300099),按照“2.2.2.2”项下方法操作,按“2.2.2.4”项下测定方法进样测定,分别于0、2、4、8、12 和24 h 进样,测得氢氰酸峰面积的RSD 为1.7%,结果表明,供试品溶液在24 h 内测定稳定。
2.2.8 加样回收率试验 取同一批样品(A 厂家,批号300099)6 份,每份精密量取2.5 ml,加入与供试品中各组分浓度相当的对照品溶液,按“2.2.2.2”项下方法制备供试品溶液,按“2.2.2.4”项下测定方法进样测定,计算回收率,结果氢氰酸平均回收率为84.06%,RSD 为3.4%。结果见表2。
2.2.9 样品测定 对本次抽验的3 家生产企业共计18 批样品按照“2.2.2.2”项下方法操作,按“2.2.2.4”项下测定方法进样测定,测定氢氰酸含量。结果见表3。
2.3 苯甲醛含量测定(HPLC 法)
2.3.1 色谱条件与系统适用性试验 色谱柱:OSAKA SODA CAPCELL PAK C18(250 mm×4.6 mm,5 μm);流动相:以乙腈为流动相A,以0.1%磷酸溶液为流动相B,按表4 进行梯度洗脱;流速:1.0 ml/min;柱温:35 ℃;检测波长:250 nm;进样量:10 μl。理论板数按苯甲醛峰计算应不低于5 000。
2.3.2 溶液的制备
2.3.2.1 对照品溶液的制备 取苯甲醛对照品适量,精密称定,置棕色量瓶中,加甲醇制成每1 ml 含20 μg的溶液,即得。
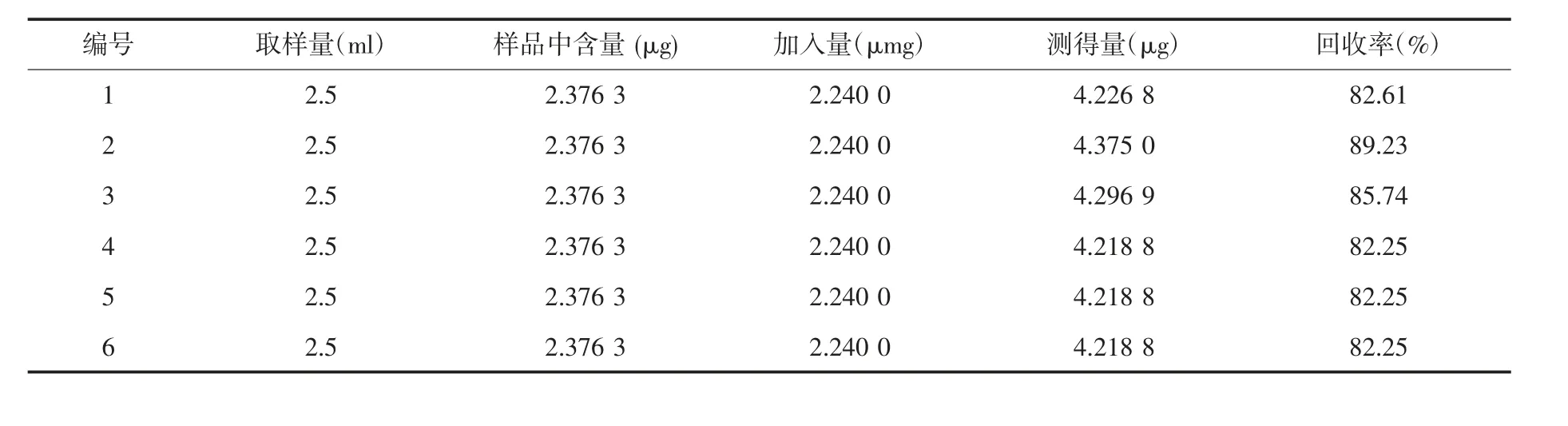
表2 氢氰酸加样回收率试验结果(n=6)

表3 样品测定结果

表4 梯度洗脱程序
2.3.2.2 供试品溶液的制备 取本品原液滤过,取续滤液,即得。
2.3.2.3 阴性样品溶液的制备 按处方配比,取除苦杏仁外其他药材,按【制法】项下的工艺制成制剂,再按“2.3.2.2”项下方法制得阴性样品溶液。
2.3.2.4 测定方法 分别取上述对照品溶液、供试品溶液各10 μl,注入液相色谱仪,记录色谱图。结果见图3。
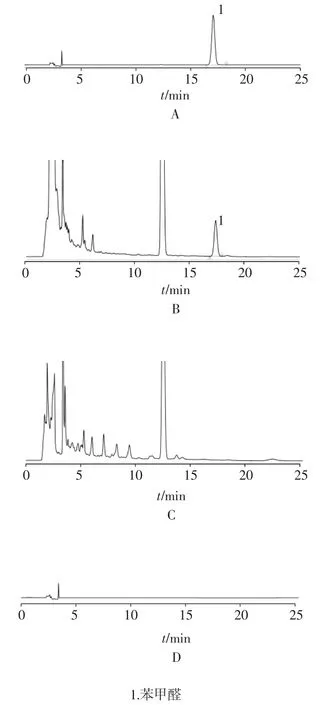
图3 对照品(A)供试品(B)阴性样品溶液(C)空白溶剂(D)HPLC 色谱图
2.3.3 标准曲线的制备 取苯甲醛对照品适量,精密称定,加甲醇分别制成每1 ml 含苯甲醛0.391 2、0.978 0、1.956 0、3.912 0、9.780 0、19.560 0、29.340 0、39.120 0、48.90 0 和78.244 0 μg 的系列溶液,分别精密吸取10 μl,注入液相色谱仪,按“2.3.1”项下色谱条件测定峰面积,以进样量(μg)为横坐标,峰面积值为纵坐标,绘制标准曲线并计算回归方程:Y=6 536 181.351 2X+6 224.320 5(r=1.000 0)。结果表明苯甲醛进样量在0.003 91~0.782 44 μg 之间,线性关系良好。
2.3.4 重复性试验 取同一批号样品(批号300069)6 份,按照“2.3.2.2”项下方法操作,按“2.3.1”项下色谱条件分析,测定,样品中苯甲醛平均值为12.799 μg/ml,RSD 为0.4%,符合要求。
2.3.5 精密度试验 取“2.3.4”项下供试品溶液1 份,按“2.3.1”项下色谱条件分析,精密吸取供试品溶液10 μl,连续进样6 次,测得苯甲醛峰面积值的RSD 为0.6%,精密度符合要求。
2.3.6 稳定性试验 取“2.3.4”项下供试品溶液1 份,分别于0、2、4、8、12、16、20 和24 h 进样,按“2.3.1”项下色谱条件分析,测得苯甲醛峰面积的RSD 为1.2%,结果表明,供试品溶液在24 h 内测定稳定。
2.3.7 加样回收率试验 取同一批号(300069)样品6 份,精密量取5 ml,置10 ml 量瓶中,分别精密加入每1 ml 中含苯甲醛对照品31.536 8 μg 的甲醇溶液2 ml,加水稀释至刻度,摇匀,制得供回收率用的供试品溶液,按“2.3.1”项下色谱条件分析,计算回收率,结果苯甲醛平均回收率为100.77%,RSD 为0.4%。结果见表5。
2.3.8 样品测定 对本次抽验的3 家生产企业共计18 批样品按照“2.3.2.2”项下方法操作,按“2.3.1”项下色谱条件分析,测定苯甲醛含量。结果见表6。

表5 苯甲醛加样回收率试验结果(n=6)

表6 样品测定结果
3 讨论
3.1 泻白糖浆中的苦杏仁以蒸馏芳香水入药,理论上不应该含有苦杏仁苷,经查阅并参考相关文献,本试验采用高效液相色谱法,采用50%甲醇为提取溶剂[6],以甲醇-水为流动相[7],采用梯度洗脱方式进行测定,检查该制剂中是否存在苦杏仁苷成分,目的是考查3家生产企业的制备工艺是否存在不按【制法】严格制备情况。经试验发现,3 家生产企业均未检出苦杏仁苷成分,证明不存在苦杏仁直接投料现象。
3.2 苦杏仁苷的最终分解产物为氢氰酸和苯甲醛,理论上两者含量成正比(摩尔比为1∶1)。氢氰酸的沸点低,极易挥发,且无紫外吸收,含量测定非常困难。经查阅文献发现,氢氰酸的测定一般多用于食品和司法鉴定方面,有的采用顶空进样器注入气相色谱仪进行分离,电子捕获检测器进行检测食品中氰化物含量[8];有的同样采用气相色谱电子捕获检测器,利用制品中氰化物在酸性条件下用氯胺T 将其衍生为氯化氢进行测定[9];有文献报道采用离子色谱法,电导检测器测定饮用水中的氰根等阴离子[10]。但本文经过查阅司法相关文献[11]发现,采用气相色谱,氮磷检测器方法,应用磷酸酸化样品,使氢氰酸释放出来再进行检测,该方法相对于气相色谱-电子捕获器检测方法更简便。经试验发现,A 厂家均检出氢氰酸;B 厂家4 批次样品检出氢氰酸,2 批次样品未检出;C 厂家均未检出氢氰酸。含量测定结果显示,氢氰酸的检出量均很低。
3.3 苯甲醛作为另一个指标成分,从侧面能反映氢氰酸的含量,故本试验对制剂中苯甲醛含量进行测定,结果显示:3 家生产企业均检出苯甲醛,但含量差异悬殊,C 企业苯甲醛均检出,但含量极低,B 企业苯甲醛含量最高。结合氢氰酸含量比较,并未呈现出正比例关系。且根据《中国药典》一部苦杏仁中苦杏仁苷限度理论推算,与苦杏仁苷分解理论值也相差很大。分析原因可能为:①企业投料苦杏仁质量较差,苦杏仁苷含量极低;②企业制备苦杏仁水未提取完全;③企业制备的杏仁水储存不当,造成氢氰酸和苯甲醛的挥发。
综上所述,泻白糖浆存在一定的质量问题,分析原因可能主要与各企业的杏仁水制备工艺和投料质量控制不严有关。建议相关部门加强监管并提升法定标准。本研究建立了苦杏仁苷的检查方法,氢氰酸和苯甲醛的含量测定方法,可为该制剂的质量标准升级提供参考依据。
