某新冠肺炎三级定点医院医护感染的风险评估
2023-05-07王兆睿刘娜郑阳张云帆郭琳琳宋银森
王兆睿,刘娜,郑阳,张云帆,郭琳琳,宋银森
(1.河南中医药大学第五临床医学院/郑州人民医院 a.转化医学研究中心;b.检验科,河南 郑州 450000;2.郑州大学第一附属医院 放疗二科,河南 郑州 450000)
新型冠状病毒自首次出现以来,在全球范围内广泛传播,并不断演变出现新的变异株以逃避免疫监视。新型冠状病毒变异株包括Alpha(B.1.1.7)、Beta(B.1.351)、Gamma(P.1)、Delta(B.1.617.2)和Omicron(BA.1、BA.2 和BA.3亚型)。目前Omicron已经取代Delta变异株成为主要流行株[1]。资料表明,Omicron变异株病毒载量大,突变位点多,具有更快的传播速度和更高的传染性,一时间医疗卫生系统的压力骤然增加,同时也导致大量一线医护人员的感染[2]。2020年2月对武汉同济医院2 009例新型冠状病毒感染患者调查发现,110例为医务人员[3],其中17例(15.45%)在发热门诊或病房工作;同年2月7日,美国医学会杂志在线发表Wang等[4]的研究,结果显示武汉大学中南医院首批138例感染者中医护人员有40例。世界卫生组织新型冠状病毒全球监测的不完全数据统计,新型冠状病毒病例中约有14%为医护人员[5],医务人员感染问题不容忽视。在新冠防控政策的不断优化下,医护人员是参与儿童和危重症患者救治的主力军,大量医护人员感染不仅会导致卫生系统瘫痪从而救治病人难度升级,同时医护之间快速传播也会进一步扩大传染范围。基于以上情况,为了解医护人员感染的途径,本研究对在定点医院隔离病区工作的医护人员的防护装备及体表等采样进行新型冠状病毒的核酸检测,旨在为医院感染防控提供科学的建议。
1 材料与方法
1.1 材料样本来源:采集2022年11月14日至12月11日在郑州人民医院(新型冠状病毒感染定点救治医院)隔离病区工作的8名医护人员每日进入一脱区未消杀前的物表及脱掉防护服后裸露空气中的体表核酸标本,具体采样内容参照《新型冠状病毒肺炎防控方案(第七版)》[6]、《国家卫生健康委办公厅关于印发消毒剂使用指南的通知》[7]及GB 19193―2015《疫源地消毒总则》[8]相关规定,分别采集防护服、N95口罩、防护面屏、外科手套、靴套、内穿洗手衣、内穿手术鞋7个部位的物表及脱掉防护服后裸露空气中的体表(即手、脸、脖颈、头发、胳膊)样本。8名医护人员采取轮岗制,每日进入隔离病区工作6 h,其间与病人有接触。样本采集:采样人员的防护按照进入隔离病区医护人员的防护标准,在一脱区对医护人员未消杀前的物表及脱掉防护服后裸露空气中的体表进行采样。(1)物表:每个位置对应取5根病毒拭子,按照《关于印发医疗机构内新型冠状病毒感染预防与控制技术指南(第三版)的通知》采样[9],使用病毒拭子沾湿病毒采样液体,在面积较大的区域内,呈S形来回连续涂抹大约60 cm×60 cm的面积(防护服、内穿洗手衣);在面积小于60 cm×60 cm的表面擦拭对应物体表面(N95口罩外侧、防护面屏内外侧、外科手套内外侧、靴套、内穿手术鞋)。(2)体表采样按照面积小于60 cm×60 cm的标准。采集完成后将5根病毒拭子放入一个3 mL病毒采样管中,即为一个合格样本,并登记上对应编号。每日采集8名职工共计56份物表核酸标本及8份体表核酸标本,持续28 d,共计1 792份。
1.2 试剂病毒样本采集保存液(江苏默乐生物科技股份有限公司,灭活型,批号20221102);新冠提取试剂盒(西安天隆科技有限公司,批号221116A0T183);新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法)(武汉明德生物科技股份有限公司,批号20203400212)。总体系25 μL,即5 μL待测样本RNA+20 μL反应液,靶基因位点为N基因和ORF1ab基因,最低检测限200拷贝·mL-1。
1.3 仪器天隆GeneRotex96核酸提取仪;全自动医用PCR分析系统(Lepgen-96)
1.4 实验方法
1.4.1样本处理以及核酸检测 将采集样本放置于56 ℃恒温培养箱30 min灭活处理,使用实时荧光定量RT-PCR方法进行新型冠状病毒核酸检测。
1.4.2结果判定 若1ab或N基因CT值≤40,且有典型扩增曲线,判定为阳性;若1ab和N基因CT值均>40,或者没有典型扩增曲线,判定为阴性[10]。
1.4.3质量控制 每批次核酸检测中均加有3孔阴性对照,1孔阳性对照(为试剂盒中提供),当阴性对照符合结果判读,阳性对照3种基因(N基因、ORF1ab基因和内参基因)通道曲线均呈指数型增长且CT值<35,两者同时符合即为结果有效,否则实验无效,需重新进行实验。
1.5 统计学方法使用SPSS 26.0软件进行统计学分析。计数资料用例数和率(%)表示,阳性检出率的比较采用χ2检验,检验水准α=0.05。
2 结果
2.1 基本情况共采集核酸标本1 792份,每个部位均采集224份,共收集1 568份物表样本和224份体表样本。1 792份样本中阳性物表共计308份,占总物表数的19.64%;阳性体表共计8份,占总体表数的3.57%。308份阳性物表标本中,其中最小CT值出现在外科手套物表(N基因29.36,ORF1ab基因29.13)。
2.2 不同部位核酸检测结果分析共计308份阳性物表核酸标本,7个部位均有阳性物表检出。阳性物表检出率较高部位为靴套(66.10%)、外科手套(28.57%)、手术鞋(16.96%),最低部位为内穿洗手衣(1.78%)。见表1。7个不同物表部位的阳性检出率比较,差异有统计学意义(χ2=501.804,P<0.001)。

表1 不同部位物表核酸结果
2.3 物表不同部位核酸CT值1 568份物表样本中有308份阳性物表标本,CT值<35的阳性标本有38份,占总物表数的2.42%;35≤CT值≤40的阳性标本有270份,占总物表数的17.22%。见表2。
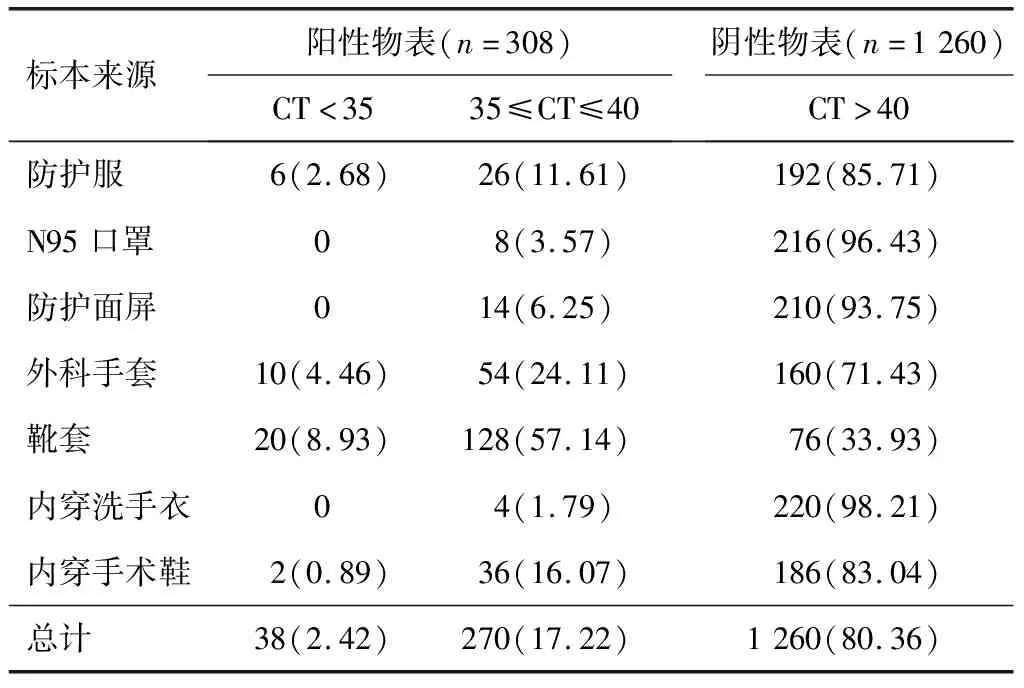
表2 不同部位核酸物表CT值[n(%)]
2.4 体表核酸结果及CT值224份体表核酸结果中,阳性样本共计8份,其CT值结果均在35~40内。见表3。

表3 体表核酸CT值[n(%)]
3 讨论
随着新型变异株Omicron的出现,其更高的传播力和传播速度已经明确,在同一时间感染的人数是Delta变异株的3到6倍,且极大增加了重复感染的风险[11-14]。对于医院来说,面临政策优化后医院就诊人数增加和医护人员不足的双重压力。因此,医护人员应更加注意防护,降低感染率。有研究表明,冠状病毒等传染性较强的病毒除通过飞沫直接传播感染外,还可以通过直接接触传播、接触被污染环境的方式间接接触传播[15-16]。因此,本研究通过对负压隔离病房医护人员的防护用品物表及体表核酸检测,来进行医务人员感染风险的评估,为定点医院感染防控提供科学依据。
本研究显示,在1 568份物表核酸标本中,阳性物表有308份,总阳性检出率17.22%。对阳性物表标本进行CT值划分,其中35≤CT值≤40的标本有270份,占阳性物表的87.66%(270/308);CT值<35的标本有38份,占12.34%(38/308)。由此数据可知,医护人员物表的CT值普遍偏高,即病毒载量普遍偏低,这或许与隔离病房的环境消杀和对患者的防护管理相关。在CT值<35和35≤CT值≤40 2个范围内,均以靴套和外科口罩的阳性检出率位居前两位。其中靴套物表的阳性检出率为66.10%,外科手套的阳性检出率为28.57%,这与吴洪敏等[17]报道的物表阳性检出率一致,提示靴套和外科手套是最容易被污染的部位,因此医护在进入一脱区进行脱防护服前,应先对靴套底部和外科手套进行消杀,以降低污染概率。
在224份体表核酸结果中,有8份阳性样本,总阳性检出率3.57%,其CT值结果均在35~40内。由于是对脱掉防护服后裸露空气中的体表采样,且同时在内穿手术鞋和洗手衣也有阳性检出,本研究认为可能与穿脱防护服不规范造成的污染相关。有研究表明病毒附着在干燥的各类材料可以持续24 h,通过实验者的手传播到其他的物表或体表,表明医护人员在摘脱防护装备过程中面临被病毒污染体表的风险[18-19]。相关报道也显示,在204例医务人员感染病例中,有25.5%为医院获得性感染,原因主要与手卫生不合格、接触患者前后手卫生欠佳、个人防护用品使用不规范、脱摘区消杀不到位相关[20],提示医护应加强防污染意识,以降低感染风险。
本研究发现,采集的7个部位的物表和体表均有阳性出现,或许与气溶胶沉积、一脱区的污染和消杀不到位相关。气溶胶的形成主要是飞沫和表面病毒在空气中沉积,通过气流的形式被广泛散布[21]。相关研究显示,防护用品脱卸区的环境气溶胶确实有新型冠状病毒核酸存在,且检出率较高[17]。气溶胶在空气中散布和沉积到地面,造成靴套底部污染的可能性较大。此外,根据湖南大巴、广州某餐厅等密闭空间聚集性案例以及定点医院和方舱医院被感染医护调查结果[21],提示气溶胶感染可能是新型冠状病毒传播的一种方式。发表在柳叶刀的一篇评论文章也提出,空气传播应该是新型冠状病毒传播的主要途径[22]。因此,对于脱摘区地面以及环境气溶胶的消杀要极为重视,这也是降低医护感染风险的关键环节。此外,清华大学江亿院士[23]提出新风量是造成脱摘区医护感染的重要因素,因此,建议在脱摘区安装CO2浓度、PM2.5浓度和相对湿度监测和排风系统,减少院感的发生。
综上所述,本次研究利用对隔离病区医护人员防护装备的物表及体表核酸检测,证实在医护进行脱摘防护用品时,是有一定的感染风险的。要求医护不仅要规范穿脱防护用品,更要注意消杀环节,注意对靴套、外科手套处的消杀,提高防护意识。其次对于院感来说要制定更精细的消杀计划,尤其注重脱摘区的地面以及环境气溶胶的消杀和净化,尽可能降低医护感染风险。
