宏基因组二代测序技术确诊儿童巨细胞病毒脑炎1例
2023-05-07成利张妮李元枭李强杨强
成利,张妮,李元枭,李强,杨强
(兰州大学第二医院 a.小儿消化科;b.神经外科,甘肃 兰州 730030)
儿童巨细胞病毒脑炎是儿童感染人巨细胞病毒引起的中枢神经系统疾病,在免疫正常的儿童中少见,临床表现多样,易漏诊、误诊。宏基因组二代测序(metagenomic next-generation sequencing,mNGS)是一种新型的、有效的病原体检测技术,近年来在临床中的应用逐渐增多。本文回顾了1例经mNGS技术确诊的儿童巨细胞病毒脑炎的诊治经过,并进行文献复习。
1 病例资料
1.1 病史患儿,女,2月龄,因“间断发热10 d”于2021年4月14日收住兰州大学第二医院。患儿于4月4日无明显诱因出现间断发热,热峰38.0 ℃,伴呻吟、腹泻,大便呈黄色稀水样,每日3~4次。无寒战、抽搐、恶心呕吐、咳嗽、呼吸困难等不适,无皮疹及皮下出血点。遂就诊于当地医院,4月5日查血常规:白细胞计数2.3×109L-1,淋巴细胞比率55.9%,单核细胞比率17%,血红蛋白84 g·L-1,血小板计数391×109L-1,C反应蛋白6.50 mg·L-1,降钙素原16.68 μg·L-1,红细胞沉降率65 mm·h-1。见表1。大便常规未见异常,血培养见大肠埃希菌。腰穿脑脊液检查:白细胞计数110×106L-1,多核细胞比率40%,单核细胞比率60%,葡萄糖1.6 mmol·L-1。见表2。头颅核磁共振示双侧硬膜下积液,当地医院诊断患儿为化脓性脑膜炎(大肠埃希菌);双侧硬膜下积液。给予患儿静脉输液治疗:美罗培南40 mg·kg-1,每日3次,利奈唑胺10 mg·kg-1,每日3次,静注人免疫球蛋白每日500 mg·kg-1,共计4 d,地塞米松0.15 mg·kg-1,每日4次, 4 d后患儿发热腹泻均好转,热峰下降至37.1 ℃,大便每日3次,呈黄色糊样。4月 9日复查腰穿脑脊液检查提示较前明显好转:白细胞计数8×106L-1,葡萄糖2.6 mmol·L-1。但4月12日患儿再次出现发热,热峰38.1 ℃,无腹泻,复查头颅核磁示双侧硬膜下积液较前增多。4月13日复查血常规:白细胞计数7.3×109L-1,中性粒细胞比率40%,淋巴细胞比率45%,单核细胞比率13%;血沉25 mm·h-1,降钙素原0.07 μg·L-1。当地医院继续给予患儿美罗培南联合利奈唑胺抗感染治疗,患儿无好转,仍反复发热,家长遂于2021年4月14日至兰州大学第二医院门诊就诊,门诊以“化脓性脑膜炎”收住院。患儿为顺产足月儿,既往体健,否认过敏史及家族史。
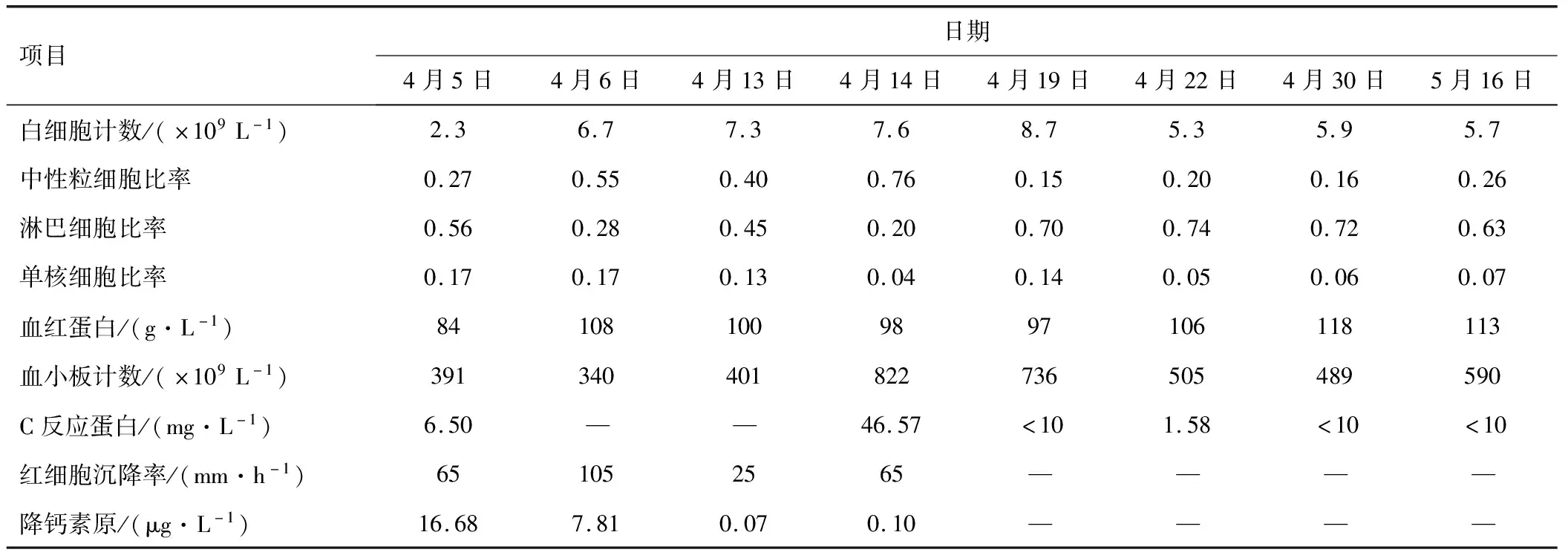
表1 患儿病程中血常规及炎性指标的动态变化

表2 患儿病程中腰穿脑脊液指标的动态变化
1.2 入院体格检查体温36.8 ℃,脉搏每分158次,呼吸每分42次,血压74/49 mmHg(1 mmHg=0.133 kPa),体重4.5 kg,发育正常,营养中等,神清,精神差。全身皮肤黏膜无黄染,浅表淋巴结未扪及肿大。头颅五官无畸形,前囟未闭,约2 cm×2 cm,张力平软,瞳孔等大等圆,直径3 mm,对光反射灵敏。咽无充血,颈软,无抵抗。心、肺、腹体检未见明显异常。脊柱四肢无畸形,双下肢不肿。生理反射存在,双侧巴宾斯基征阳性。
1.3 入院后诊疗4月14日收住医院后完善相关检查:白细胞计数7.6×109L-1,中性粒细胞比率76%,血红蛋白98 g·L-1,血小板计数822×109L-1,C反应蛋白46.57 mg·L-1,降钙素原0.10 μg·L-1,红细胞沉降率65 mm·h-1,肝功、肾功、电解质、凝血功能、免疫球蛋白、淋巴细胞亚群未见异常。给予患儿万古霉素15 mg·kg-1,每日4次,联合美罗培南40 mg·kg-1,每日3次,地塞米松0.15 mg·kg-1,每日4次。4月19日患儿C反应蛋白下降至<10 mg·L-1,但复查腰穿脑脊液检查显示白细胞计数142×106L-1,中性粒细胞比率9%,淋巴细胞比率91%,葡萄糖1.0 mmol·L-1,蛋白1.43 g·L-1;患儿仍间断有发热,热峰38.0 ℃,无寒战、咳嗽、腹泻,精神稍差。4月22日复查腰穿脑脊液检查:白细胞计数114×106L-1,中性粒细胞比率4%,淋巴细胞比率96%,葡萄糖1.9 mmol·L-1,蛋白0.99 g·L-1。患儿仍有发热情况,且脑脊液检查无明显好转。因此,4月22日的腰穿检查同时送检了患儿脑脊液行mNGS检查,4月24日结果回报:检出巨细胞病毒(cytomegalovirus,CMV),序列数4 158,相对丰度99.88%,关注度高。当日完善患儿尿液标本CMV聚合酶链式反应(polymerase chain reaction,PCR):6.28×105L-1,血液标本CMV PCR:1.20×103L-1,患儿母亲乳汁CMV PCR提示阴性,血液标本CMV PCR阴性,CMV IgM、IgG抗体阴性。4月25日完善头颅CT检查,双侧额顶颞部硬膜下积液。见图1。至此患儿诊断明确:巨细胞病毒脑炎,双侧硬膜下积液。当天即停用万古霉素,继续给予美罗培南抗感染、地塞米松抗炎治疗,给予患儿更昔洛韦静滴5 mg·kg-1,每12 h 1次(4月24日至5月7日共计14 d)抗巨细胞病毒治疗,5月5日复查腰穿脑脊液检查较前有所好转,白细胞计数30×106L-1,中性粒细胞比率10%,淋巴细胞比率90%,葡萄糖2.2 mmol·L-1,蛋白0.98 g·L-1,5月6日复查头颅CT,检查示双侧额顶颞部硬膜下积液,与4月25日相比变化不大。见图2。5月 8日起更昔洛韦减量至5 mg·kg-1,每日1次,静滴共计10 d,5月16日复查腰穿脑脊液检查较前好转,白细胞计数14×106L-1,中性粒细胞比率12%,淋巴细胞比率88%,葡萄糖1.9 mmol·L-1,蛋白0.63 g·L-1。

图1 患儿2021年4月25日头颅CT示双侧额顶颞部硬膜下积液
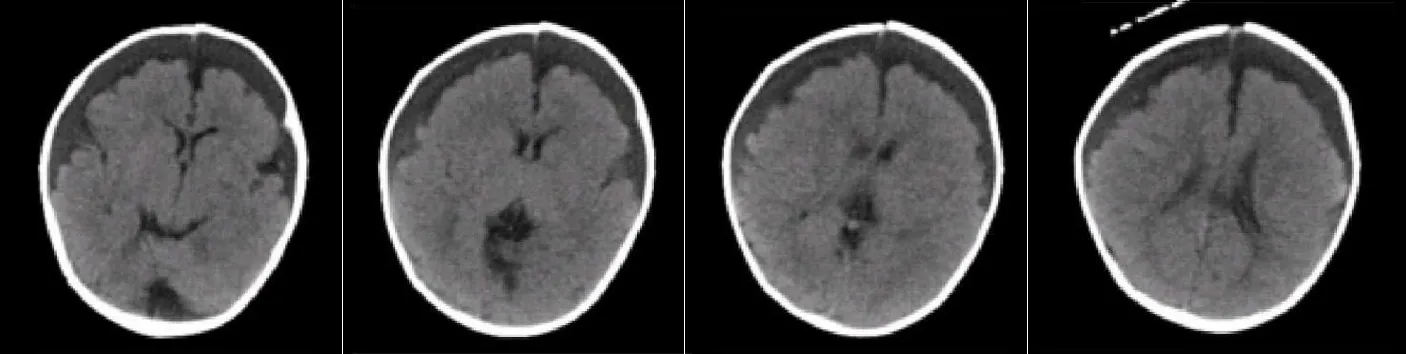
图2 患儿2021年5月6日复查头颅CT示双侧额顶颞部硬膜下积液
1.4 随访5月18日患儿出院,出院后继续口服缬更昔洛韦16 mg·kg-1,每12 h 1次,共3个月,至2021年8月20日,至医院门诊复诊,患儿生长发育正常,营养良好,一般情况良好,复查血常规、肝肾功能、血沉无异常,CMV PCR阴性。继续口服缬更昔洛韦3个月,复查各项指标正常。继续随访1 a,患儿生长发育正常,营养良好。
2 讨论
1957年Craig等[1]分离出了CMV。CMV又名人类疱疹病毒5型,是一种双链DNA病毒,与人类疱疹病毒6A、6B和7型同属于乙型疱疹病毒亚科。CMV为一直径150~200 nm的二十面体,包括4个基本的结构元素:包膜、被膜、核衣壳和含基因组的内部核蛋白。病毒包膜包含脂质蛋白和至少33种结构蛋白,包括参与病毒进入细胞的蛋白质。被膜由结构蛋白组成,包括pp65抗原,是CMV常规检测方法的主要靶点[2]。基因组是一个64 nm的线性双链DNA分子,包含165~252个不重叠的开放阅读框[3],其中一种蛋白是DNA聚合酶,它在病毒复制中起着不可或缺的作用,是目前抗CMV药物的主要靶点[4]。
CMV在世界大多数地区流行。其血清阳性率在不同地区存在差异,美国的一项调查报告指出,CMV的总体血清阳性率为50.4%,并随着年龄的增长而增加,在1~5岁的儿童中低至20.7%,但在发展中国家的老年人中,其接近100%[5-6]。我国CMV血清阳性率在新生儿中为0.6%~8.5%,在婴儿中为58%~84%,在生育妇女中为95.6%~98.7%[7]。CMV最常在儿童时期到成年早期感染。
1965年,已有研究报道CMV与健康个体类似传染性单核细胞增多症的一种疾病相关[8]。直至今日,大量研究表明,CMV引起的临床表现多种多样,程度轻重不一,从免疫功能良好宿主的无症状感染,到免疫功能缺陷个体例如器官移植受者的严重感染甚至致命。CMV感染可引起多种组织器官损伤,先天性CMV感染引起肺炎最常见,其次为肝炎,围生期及生后CMV感染最常引起CMV肝炎,其次是肺炎、肾炎等,而中枢神经系统感染少见[9-10]。CMV感染中枢神经系统临床类型多样,包括全脑炎、脑室膜炎、局灶性脑炎、脊髓炎等。有关CMV脑炎报道主要集中于艾滋病患者、骨髓及器官移植术后患者、系统性红斑狼疮治疗过程中出现免疫功能低下的患者,在免疫大致正常的人群中少有[11]。CMV脑炎可表现为多种症状,包括发热寒战、恶心呕吐、纳差乏力、意识障碍、感觉异常、定向障碍、视力障碍、尿潴留、便秘等。CMV脑炎的影像学表现具有多样性,先天感染的患儿头颅CT可见严重的脑积水及环侧脑室壁的钙化,而获得性感染的典型影像学表现为侧脑室内室管膜下强化[12],本例患儿的影像学表现并不典型。
我国2012年《儿童巨细胞病毒性疾病诊断和防治的建议》[13]中指出:我国儿童CMV感染的诊断标准:具有CMV活动性感染的证据、同时具备CMV疾病的相关临床表现,并排除现症疾病的其他常见病因,可做出临床诊断;将从活检病变组织或特殊体液如脑脊液内分离到CMV病毒或检出病毒复制标志物(病毒抗原和基因转录产物)作为CMV感染的确诊依据。特殊部位CMV DNA检测有临床诊断意义:如艾滋病患儿脑脊液内检出CMV DNA可诊断中枢神经系统感染。CMV感染根据原发感染时间分为先天感染、围生期感染和出生后感染:出生后2周内的CMV感染为先天感染;生后第3~12周内为围生期感染;出生12周后经水平传播途径获得,为生后感染,又称获得性感染。本例患儿以发热、精神反应差为主要症状,虽然病程早期患儿降钙素原增高,且血培养提示大肠埃希菌感染,但回顾病程初始时,患儿脑脊液检测结果已经提示脑脊液中增高的白细胞以单核细胞为主,而不是化脓性脑炎常见的多核细胞为主,且给予患儿针对大肠埃希菌引起的化脓性脑膜炎的标准治疗后,患儿的C反应蛋白、降钙素原快速降至正常,但再次出现发热、精神差、红细胞沉降率增高表现,脑脊液检查仍无明显好转,此时需考虑初始的诊断及治疗是否正确,患儿的病因是否另有原因。此时完善脑脊液mNGS检测提示存在高置信度的CMV感染,给予抗生素治疗无效,给予抗巨细胞病毒治疗后患儿明显好转,故该患儿巨细胞病毒性脑炎诊断成立。
巨细胞病毒脑炎在免疫功能良好的患者中报道较少,在免疫功能低下的宿主中感染较多[14]。婴幼儿由于生长发育不完全,属于免疫功能低下的人群,因此是CMV的主要感染人群之一,婴幼儿感染CMV后虽不立即引起病情的迅速恶化,但若不能得到及时有效的治疗,则可能继发肝损伤、肺损伤、中枢神经系统损伤等严重的功能损伤[15]。因此,及时明确诊断及治疗,对于婴幼儿巨细胞病毒脑炎至关重要。
在临床诊疗中,一些感染性疾病患者由于不能明确感染的病原体,导致延误治疗或治疗不充分,住院时间延长,再入院率、致残率及死亡率增加等[16]。通常,这些患者感染的病原体包括常见和不常见的病毒、细菌、寄生虫、真菌等。由于早期广谱或预防性抗菌药物的使用以及微生物生长缓慢、生长环境要求苛刻,常规培养基中培养微生物的阳性率有限[17]。mNGS技术是一种允许数千至数十亿个DNA或RNA片段同时独立测序的技术,可以无偏倚地检测一份样本中的多种病原微生物。几乎所有的病原微生物都包含DNA或RNA基因组,这使得mNGS成为一种有效的病原体检测方法[18]。自2004年出现以来,mNGS的成本已经大幅降低,成为检测临床样本微生物的一项新技术,有望提高我们诊断和跟踪传染病的能力。但与任何新技术一样,mNGS检测的临床广泛应用和推广普及需要时间,因为医疗机构需要熟悉它并制定新的指南[19]。2021年2月,《宏基因组高通量测序技术应用于感染性疾病病原检测中国专家共识》[20]对mNGS技术的临床适应证、实验流程、质量管理、性能验证和报告解读等方面给出了推荐意见和处理方法。指南提出,当患者出现不明原因发热、考虑感染所致或尚不排外感染,并已经规范给予经验性抗感染治疗,仍然无明显疗效时,应当完善病原体的常规技术检测,并同时开展mNGS;各种原因导致患者出现急危重症表现,不除外感染所致,或考虑继发或并发危及生命的严重感染时,建议常规检测的同时开展mNGS。因此,此例病例中mNGS的应用,在患儿反复发热,常规经验性抗感染治疗无明显好转,且患儿临床表现、影像学表现均无CMV脑炎的特异性或典型表现的情况下,为患儿的诊断提供了决定性的证据,最终针对CMV脑炎的诊断,取得了良好的治疗效果。
综上所述,免疫功能正常的儿童CMV脑炎因其发病率低、临床少见、临床表现缺乏特异性,易误诊、漏诊。mNGS技术在感染性疾病的病因诊断中,能够提供有力的依据。本例患儿的远期预后尚待观察,应继续随访。
