2-(溴代吡咯腈-1-基)乙酸衍生物的设计、合成及生物活性
2023-04-18张列雄马俊豪郭倩男昌勤哲徐志红
周 蒲, 张列雄, 马俊豪, 郭倩男,游 江, 昌勤哲, 徐志红*,,2
(1.长江大学 农学院,湖北 荆州 434025;2.长江大学 农药研究所,湖北 荆州 434025)
溴代吡咯腈(tralopyril,图式1)是经天然抗生素dioxapyrrolomycin改造合成的2-芳基吡咯类化合物,具有优异的杀虫、杀螨活性,其作用机理是阻断昆虫线粒体内的氧化磷酸化作用,破坏线粒体内二磷酸腺苷(ADP)到三磷酸腺苷(ATP)的转化,使昆虫无法正常产生能量,最终导致昆虫死亡[1-2]。然而,溴代吡咯腈会对作物产生严重药害[3]。为了改善溴代吡咯腈的生物活性,降低其对作物的药害,研究人员对溴代吡咯腈及其类似物进行了大量的结构修饰[4-13],例如:图式1 中化合物a(虫螨腈),其进入虫体后会代谢为溴代吡咯腈,在发挥杀虫、杀螨作用的同时也降低了对作物的药害[7];化合物b在10 mg/L 下对南方黏虫成虫及幼虫、烟芽叶蛾的致死率可达100%[8];化合物c对豆蚜、南方黏虫和秀丽隐杆线虫均表现出优异的杀虫及杀线虫活性[9];化合物d对烟芽夜蛾、南方黏虫、西部马铃薯叶蝉及叶螨具有优异的杀虫、杀螨活性[10];化合物e对水稻稻瘟病菌表现出优异杀菌活性,对黏虫、棉红蜘蛛等也表现出优异的杀虫、杀螨活性[11]。
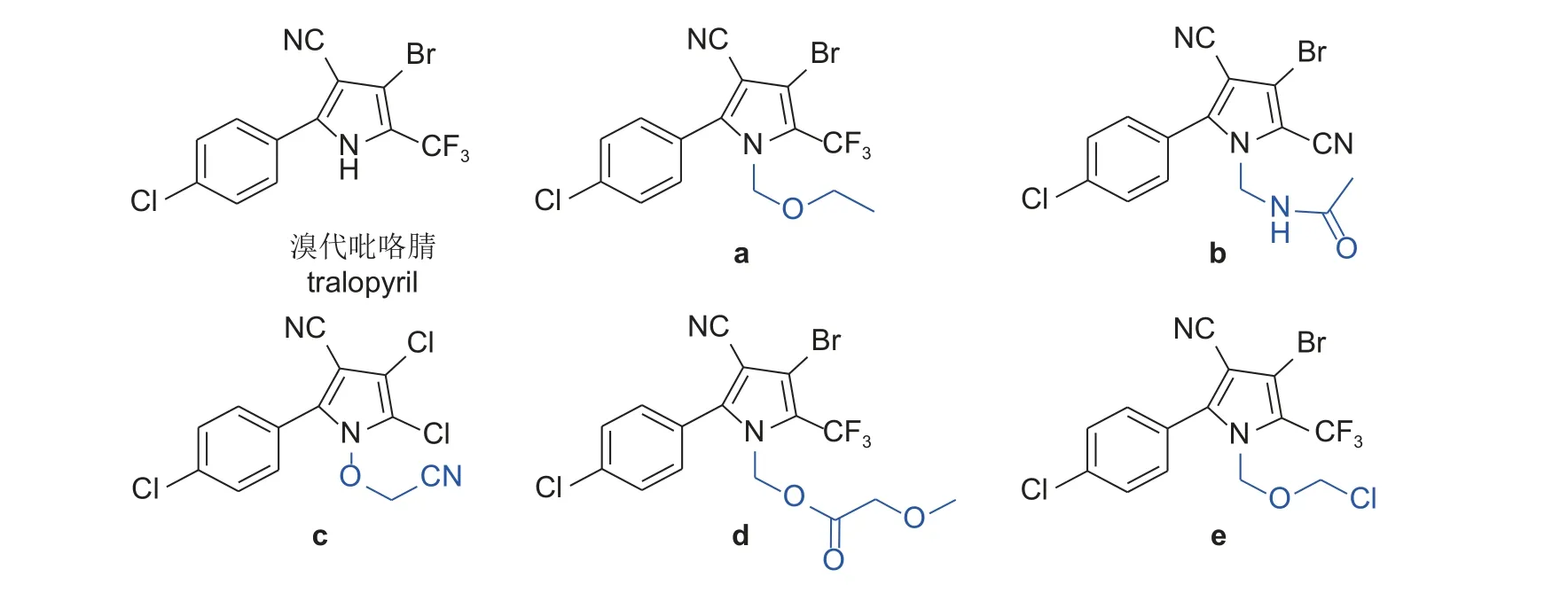
图式 1 溴代吡咯腈衍生物结构式Scheme 1 Structural formulas of tralopyril derivatives
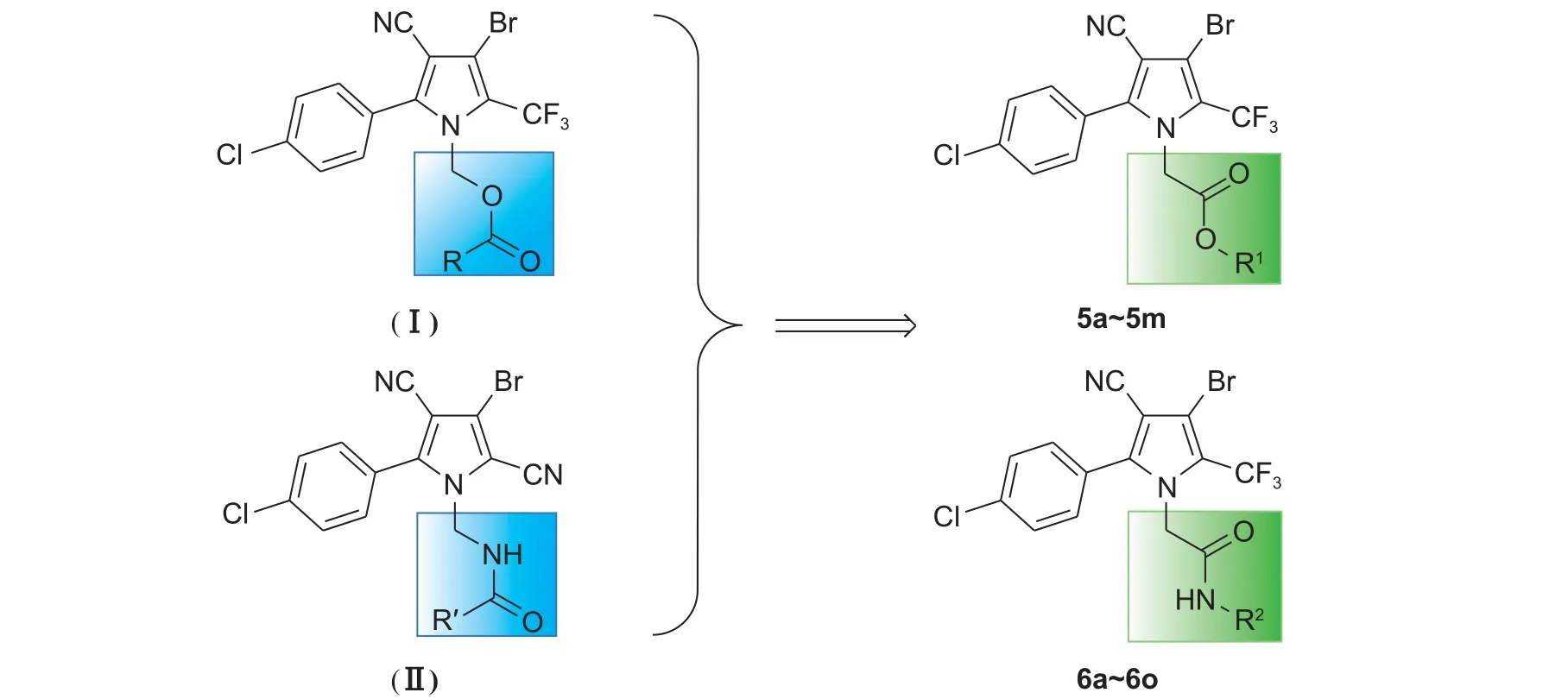
图式 2 溴代吡咯腈羧酸酯 (Ⅰ) 及酰胺 (Ⅱ) 衍生物设计思路Scheme 2 Design strategy of tralopyril carboxylic acid esters (Ⅰ) and amides derivatives (Ⅱ)
含有羧酸酯结构或酰胺结构的化合物具有广泛的生物活性,包括杀菌、杀虫、杀螨、杀线虫等[14-18]。前人在溴代吡咯腈及其类似物的吡咯环N位引入羟基或胺基作为桥链,合成了一系列溴代吡咯腈羧酸酯与酰胺类化合物,发现其具有优异杀虫、杀螨活性[8,10]。受此启发,本研究采用官能团翻转策略,尝试在溴代吡咯腈的吡咯环N位引入乙酸作为桥链,拟设计合成溴代吡咯腈羧酸酯及酰胺两类衍生物,测定其生物活性并开展作物安全性研究,期望得到具有高活性且对作物安全的溴代吡咯腈衍生物。
目标化合物的设计思路见图式2,合成路线见图式3。

图式 3 目标化合物的合成路线Scheme 3 Synthesis routes of target compounds
1 材料与方法
1.1 仪器与药剂
Bruker Avance DPX400 型核磁共振仪(以TMS 作内标物,CDCl3或DMSO-d6作溶剂,德国-瑞士布鲁克光谱公司);WRR 熔点测定仪(上海精密科学仪器有限公司);Themo Scientific Q-Exactive型高分辨质谱仪(ESI-MS,赛默飞世尔科技 (中国)有限公司)。
所有化学药品均为市售国产分析纯试剂。98%溴代吡咯腈(tralopyril)原药,天津希恩思生化科技有限公司提供;97%咯菌腈(fludioxonil)原药、98%虫螨腈(chlorfenapyr)原药和90%嘧菌酯(azoxystrobin) 原药,长江大学农药研究所提供;97%噻唑膦(fosthiazate)原药,由75%噻唑膦乳油(河北三农农用化工有限公司)纯化得到。
1.2 供试材料
水稻纹枯病菌Rhizoctonia solani、小麦根腐病菌Bipolaris sorokiniana、柑橘褐腐病菌Phytophthora citrophthora和水稻稻瘟病菌Magnaporthe oryzae,由长江大学农学院植物病理实验室提供;斜纹夜蛾Spodoptera litura与朱砂叶螨Tetranychus cinnabarinus,由长江大学农学院昆虫实验室提供;秀丽隐杆线虫Caenorhabditis elegans,由长江大学医学院提供;水稻Oryza sativaL.与油菜Brassica campestrisL.种子,由长江大学农药研究所提供。
1.3 目标化合物的合成
1.3.1 化合物3 的合成 参照文献[19]方法得化合物2。参照文献[20]方法合成化合物3:称取化合物2 29.41 g (67.51 mmol)和单水氢氧化锂4.25 g(101.27 mmol)于500 mL 圆底烧瓶中,加入四氢呋喃300 mL,常温反应4 h,薄层色谱 (TLC,(V(石油醚) :V(乙酸乙酯) = 6 : 1) 监测至反应完毕。减压浓缩至干。将反应液倒入水中,在冰浴条件下,滴加稀盐酸调节pH 值至2,出现白色沉淀,抽滤,烘干得化合物3 26.14 g。
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸(3):纯白色固体,收率95%,m.p.148.5~149.7 ℃.1H NMR (400 MHz, CDCl3),δ: 7.61~7.47 (m, 2H), 7.41~7.31(m, 2H), 4.71 (s, 2H).13C NMR (101 MHz, DMSO-d6),δ:168.80, 144.84, 136.41, 132.04, 129.98, 125.65, 120.41(q,JC-F= 271.7 Hz), 119.69(q,J= 37.4 Hz), 113.95, 102.74, 97.99,49.41.HRMS, 计算值 C14H7BrClF3N2O2( [M + NH4]+):423.967, 实测值 423.9673.
1.3.2 化合物4 的合成 参照文献[21]方法合成得淡黄色固体4,无需纯化直接投入下一步反应。
1.3.3 目标化合物(5a~5m,6a~6o)的合成 参照文献[21]的方法并略有改进。以化合物5a 的合成为例:称取甲醇0.24 g (8.10 mol)于250 mL 圆底烧瓶中,加入三乙胺3.28 g (32.4 mmol)和二氯甲烷100 mL,常温反应0.5 h。化合物4 (7.36 mmol)用二氯甲烷溶解,在冰浴条件下滴加于反应体系中,室温反应3 h,TLC [V(石油醚) :V(乙酸乙酯) =2 : 1]监测至反应完毕。用饱和食盐水洗涤3 次,有机相用无水硫酸钠干燥,减压浓缩至干。用柱层析[V(石油醚) :V(乙酸乙酯) = 6 : 1]分离纯化,烘干后得产物5a。采用相同方法合成目标化合物(5b~5m,6a~6o)。
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸甲酯(5a):纯白色固体,收率94%,m.p.120.2~121.5 ℃.1H NMR (400 MHz, CDCl3),δ: 7.55~7.49 (m, 2H),7.39~7.33 (m, 2H), 4.65 (s, 2H), 3.78 (s, 3H).13C NMR (101 MHz, CDCl3),δ: 167.05, 144.33, 137.57, 131.06, 129.90,124.87, 120.30(q,J= 38.4 Hz), 120.00(q,JC-F= 270.7 Hz),113.17, 103.22, 99.41, 53.30, 48.09.HRMS, 计算值C15H9BrClF3N2O2( [M + H]+): 420.956, 实测值 420.9557.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸丙酯(5b):纯白色固体,收率92%,m.p.114.8~116.4 ℃.1H NMR (400 MHz, CDCl3),δ: 7.55~7.48 (m, 2H),7.40~7.34 (m, 2H), 4.64 (s, 2H), 4.14 (t,J= 6.8 Hz, 2H), 1.64(q,J= 7.2 Hz, 2H), 0.90 (t,J= 7.2 Hz, 3H).13C NMR (101 MHz, CDCl3),δ: 166.67, 144.35, 137.52, 131.07, 129.86,124.93, 120.32 (q,J= 37.4 Hz), 120.01 (q,JC-F= 271.7 Hz),113.22, 103.12, 99.30, 68.18, 48.27, 21.79, 10.08.HRMS, 计算值 C17H13BrClF3N2O2([M + H]+): 448.987, 实测值 448.9872.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸异丙酯(5c):纯白色固体,收率90%,m.p.129.5~131.3 ℃.1H NMR (400 MHz, CDCl3),δ: 7.54~7.48 (m, 2H),7.41~7.34 (m, 2H), 5.08 (m, 1H), 4.59 (s, 2H), 1.24 (d,J= 6.4 Hz, 6H).13C NMR (101 MHz, CDCl3),δ: 166.10, 144.31,137.50, 131.08, 129.82, 124.99, 120.32 (q,J= 38.4 Hz),120.02 (q,JC-F= 271.7 Hz), 113.26,103.06, 99.24, 70.92,48.52, 21.50.HRMS, 计算值 C17H13BrClF3N2O2([M + H]+):448.987, 实测值 448.9871.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸丁酯(5d):纯白色固体,收率89%,m.p.80.2~82.0 ℃.1H NMR (400 MHz, CDCl3),δ: 7.54~7.47 (m, 2H),7.40~7.33 (m, 2H), 4.63 (s, 2H), 4.18 (t,J= 6.8 Hz, 2H),1.63~1.58 (m, 2H), 1.36~1.27 (m, 2H), 0.92 (t,J= 7.2 Hz,3H).13C NMR (101 MHz, CDCl3),δ: 166.65, 144.34, 137.52,131.08, 129.85, 124.94,120.32 (q,J= 37.4 Hz), 120.01 (q,JC-F= 270.7 Hz), 113.22, 103.11, 99.31, 66.48, 48.27, 30.35,18.84, 13.53.HRMS, 计算值 C18H15BrClF3N2O2([M + H]+):463.003, 实测值 463.0027.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸异丁酯(5e):纯白色固体,收率85%,m.p.120.6~122.6 ℃.1H NMR (400 MHz, CDCl3),δ: 7.54~7.47 (m, 2H),7.40~7.33 (m, 2H), 4.65 (s, 2H), 3.96 (d,J= 6.8 Hz, 2H),1.96~1.86 (m, 1H), 0.89 (d,J= 6.8 Hz, 6H).13C NMR (101 MHz, CDCl3),δ: 166.64, 144.36, 137.53, 131.07, 129.86,124.92, 120.34 (q,J= 38.4 Hz), 120.02 (q,JC-F= 270.7 Hz),113.22, 103.13, 99.31, 72.54, 48.24, 27.62, 18.77.HRMS, 计算值 C18H15BrClF3N2O2( [M + H]+): 463.003, 实测值 463.0035.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸叔丁酯(5f):纯白色固体,收率88%,m.p.136.5~138.2 ℃.1H NMR (400 MHz, CDCl3),δ: 7.54~7.48 (m, 2H),7.40~7.34 (m, 2H), 4.52 (s, 2H), 1.44 (s, 9H).13C NMR (101 MHz, CDCl3),δ: 165.61, 144.24, 137.43, 131.06, 129.75,125.11, 120.32 (q,J= 37.4 Hz), 120.04 (q,JC-F= 270.7 Hz),113.30, 102.87, 99.10, 84.22, 48.98, 27.77.HRMS, 计算值 C18H15BrClF3N2O2([M + H]+): 463.003, 实测值 463.0029.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸正辛酯(5g):纯白色固体,收率84%,m.p.52.6~53.7 ℃.1H NMR (400 MHz, CDCl3),δ: 7.53~7.48 (m, 2H),7.39~7.34 (m, 2H), 4.64 (s, 2H), 4.16 (t,J= 6.8 Hz, 2H),1.66~1.56 (m, 2H), 1.28 (s, 10H), 0.89 (t,J= 6.8 Hz, 3H).13C NMR (101 MHz, CDCl3),δ: 166.64, 144.34,137.51,131.07, 129.85, 124.94, 120.32 (q,J= 37.4 Hz), 120.01 (q,JC-F= 271.7 Hz), 113.22, 103.10, 99.30, 66.78, 48.28, 31.73,29.13, 29.06, 28.38, 25.62, 22.62, 14.08.HRMS, 计算值C22H23BrClF3N2O2([M + H]+): 519.066, 实测值 519.0654.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸对甲基苯酯(5h):纯白色固体,收率82%,m.p.174.8~175.5 ℃.1H NMR (400 MHz, CDCl3),δ: 7.59~7.49 (m, 2H),7.47~7.37 (m, 2H), 7.19 (d,J= 8.4 Hz, 2H), 6.94~6.84 (m,2H), 4.87 (s, 2H), 2.35 (s, 3H).13C NMR (101 MHz, CDCl3),δ: 165.51, 147.53, 144.46, 137.73, 136.66, 131.14, 130.25,129.98, 124.82, 120.48, 120.1 (q,JC-F= 270.7 Hz), 119.96 (q,J= 37.4 Hz),113.11, 103.38, 99.57, 48.29, 20.91.HRMS, 计算值 C21H13BrClF3N2O2([M + H]+): 496.987, 实测值 496.9876.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸对甲氧基苯酯(5i):纯白色固体,收率83%,m.p.141.8~143.5 ℃.1H NMR (400 MHz, CDCl3),δ: 7.59~7.50 (m,2H), 7.46~7.37 (m, 2H), 6.97~6.91 (m, 2H), 6.91~6.87 (m,2H), 4.86 (s, 2H), 3.80 (s, 3H).13C NMR (101 MHz, CDCl3),δ: 165.69, 157.90,144.46, 143.19, 137.73, 131.14, 129.98,124.82, 121.64,120.31 (q,J= 37.4Hz),120.09 (q,JC-F= 271.7 Hz), 114.70, 113.10, 103.40, 99.58, 55.66,48.26.HRMS, 计算值 C21H13BrClF3N2O3([M + H]+): 512.982, 实测值 512.9823.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸对氟苯酯(5j):纯白色固体,收率79%,m.p.153.9~155.2 ℃.1H NMR (400 MHz, CDCl3),δ: 7.62~7.48 (m, 2H),7.46~7.35 (m, 2H), 7.14~7.05 (m, 2H), 7.03~6.92 (m, 2H),4.88 (s, 2H).13C NMR (101 MHz, CDCl3),δ: 165.42,160.68(d,JC-F= 246.4 Hz), 145.49, 144.47, 137.80, 131.11,130.03, 124.74, 122.41, 122.33, 120.27 (q,J= 38.4 Hz),120.01 (q,JC-F= 270.7 Hz), 116.65, 116.41, 113.03, 103.52,99.70, 48.18.HRMS, 计算值 C20H10BrClF4N2O2([M + H]+):500.962, 实测值 500.9625.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸对氯苯酯(5k):纯白色固体,收率82%,m.p.159.5~161.3 ℃.1H NMR (400 MHz, CDCl3),δ: 7.63~7.49 (m, 2H),7.45~7.39 (m, 2H), 7.39~7.32 (m, 2H), 7.05~6.90 (m, 2H),4.88 (s, 2H).13C NMR (101 MHz, CDCl3),δ: 165.19, 148.12,144.46, 137.82, 132.36, 131.10, 130.04, 129.87, 124.72, 122.23,120.28 (q,J= 37.4 Hz), 120.11 (q,JC-F= 270.7 Hz), 113.01,103.57, 99.73, 48.18.HRMS, 计算值 C20H10BrCl2F3N2O2([M + H]+): 516.932, 实测值 516.9321.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸对溴苯酯(5l):纯白色固体,收率80%,m.p.161.3~163.1 ℃.1H NMR (400 MHz, CDCl3),δ: 7.58~7.53 (m, 2H),7.53~7.48 (m, 2H), 7.43~7.36 (m, 2H), 6.96~6.87 (m, 2H),4.88 (s, 2H).13C NMR (101 MHz, CDCl3),δ: 165.12, 148.69,144.47, 137.81, 132.86, 131.10, 130.04, 124.71, 122.64, 120.27(q,J= 37.4 Hz), 120.05, 120.09 (q,JC-F= 270.7 Hz), 113.02, 103.54,99.71, 48.20.HRMS, 计算值 C20H10Br2ClF3N2O2([M + H]+):560.882, 实测值 560.8817.
2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酸对硝基苯酯(5m):纯白色固体,收率68%,m.p.159.8~161.2 ℃.1H NMR (400 MHz, CDCl3),δ: 8.30 (d,J=9.0 Hz, 2H), 7.56 (d,J= 8.4 Hz, 2H), 7.41 (d,J= 8.4 Hz, 2H),7.24 (d,J= 9.0 Hz, 2H), 4.95 (s, 2H).13C NMR (101 MHz,CDCl3),δ: 164.66, 154.03, 146.01, 144.50, 137.95, 131.07,130.12, 125.55, 124.59, 121.94,120.26 (q,J= 36.4 Hz), 120.10(q,JC-F= 270.7 Hz), 112.89, 103.76, 99.92, 48.12.HRMS,计算值 C20H10BrClF3N3O4([M + H]+): 527.957, 实测值527.9594.
N-乙基-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6a):纯白色固体,收率92%,m.p.220.0~220.9 ℃.1H NMR (400 MHz, CDCl3),δ: 7.49 (d,J= 8.8 Hz,2H), 7.44 (d,J= 8.8 Hz, 2H), 5.71 (t,J= 6.0 Hz, 1H), 4.50 (s,2H), 3.30 (p,J= 7.2 Hz, 2H), 1.12 (t,J= 7.2 Hz, 3H).13C NMR (101 MHz, CDCl3),δ: 164.91, 144.75, 137.42,131.25, 129.71, 125.06, 120.12 (q,J= 37.4 Hz), 120.05 (q,JC-F= 270.7 Hz), 113.44, 103.20, 98.97, 49.60, 34.97, 14.56.HRMS, 计算值 C16H12BrClF3N3O ([M + H]+): 433.988, 实测值 433.9874.
N-丙基-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6b):纯白色固体,收率89%,m.p.209.7~210.5 ℃.1H NMR (400 MHz, CDCl3),δ: 7.51~7.46 (m, 2H),7.46~7.41 (m, 2H), 5.60 (t,J= 6.0 Hz, 1H), 4.52 (s, 2H),3.26~3.21 (m, 2H), 1.53~1.46 (m, 2H), 0.90 (t,J= 7.2 Hz,3H).13C NMR (101 MHz, CDCl3),δ: 164.97, 144.71, 137.43,131.25, 129.71, 125.08, 120.14 (q,J= 38.38 Hz), 120.07 (q,JC-F= 271.7 Hz), 113.34, 103.24, 99.13, 49.62, 41.74, 22.65,11.13.HRMS, 计算值 C17H14BrClF3N3O ([M + H]+): 448.003,实测值 448.0029.
N-异丙基-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6c):纯白色固体,收率86%,m.p.263.1~265.1 ℃.1H NMR (400 MHz, CDCl3),δ: 7.50 (d,J=8.8 Hz, 2H), 7.45 (d,J= 8.8 Hz, 2H), 5.28 (d,J= 8.0 Hz, 1H),4.48 (s, 2H), 4.13~4.04 (m, 1H), 1.15 (d,J= 6.4 Hz, 6H).13C NMR (101 MHz, CDCl3),δ: 164.04, 144.72, 137.41, 131.28,129.70, 125.12, 120.08 (q,JC-F= 270.7 Hz), 120.07 (q,J=37.4 Hz), 113.36, 103.25, 99.13, 49.69, 42.41, 22.39.HRMS,计算值 C17H14BrClF3N3O ([M + H]+): 448.003, 实测值448.0030.
N-丁基-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6d):纯白色固体,收率84%,m.p.210.5~211.3 ℃.1H NMR (400 MHz, CDCl3),δ: 7.51~7.46 (m, 2H),7.46~7.41 (m, 2H), 5.58 (t,J= 6.0 Hz, 1H), 4.51 (s, 2H),3.29~3.24 (m, 2H), 1.50~1.42 (m, 2H), 1.33~1.28 (m, 2H),0.92 (t,J= 7.2 Hz, 3H).13C NMR (101 MHz, CDCl3),δ:164.93, 144.72, 137.42, 131.26, 129.70, 125.08, 120.14 (q,J=38.4 Hz), 120.07 (q,JC-F= 270.7 Hz), 113.36, 103.23, 99.11,49.62, 39.76, 31.39, 19.85, 13.60.HRMS, 计算值C18H16BrClF3N3O ([M + H]+): 462.019, 实测值 462.0187.
N-异丁基-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6e):纯白色固体,收率84%,m.p.212.9~214.2 ℃.1H NMR (400 MHz, CDCl3),δ: 7.49 (d,J=8.4 Hz, 2H), 7.44 (d,J= 8.4 Hz, 2H), 5.58 (s, 1H), 4.53 (s,2H), 3.10 (t,J= 6.4 Hz, 2H), 1.78~1.70 (m, 1H), 0.88 (d,J=6.8 Hz, 6H).13C NMR (101 MHz, CDCl3),δ: 165.03, 144.72,137.42, 131.26, 129.70, 125.10, 120.16 (q,J= 38.4 Hz),120.08 (q,JC-F= 271.7 Hz), 113.36, 103.22, 99.12, 49.59,47.34, 28.46, 19.87.HRMS, 计算值 C18H16BrClF3N3O ([M +H]+): 462.019, 实测值 462.0192.
N-叔丁基-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6f):纯白色固体,收率80%,m.p.207.2~208.2 ℃.1H NMR (400 MHz, CDCl3),δ: 7.48 (d,J=8.8 Hz, 2H), 7.44 (d,J= 8.8 Hz, 2H), 5.41 (s, 1H), 4.43 (s,2H), 1.32 (s, 9H).13C NMR (101 MHz, CDCl3),δ: 164.02,144.69, 137.32, 131.28, 129.61, 125.23, 120.14 (q,J= 37.4 Hz), 120.07 (q,JC-F= 270.7 Hz), 113.56, 102.92, 98.76, 52.37,49.93, 28.48.HRMS, 计算值 C18H16BrClF3N3O ([M + H]+):462.019, 实测值 462.0187.
N-苯基-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6g):纯白色固体,收率85%,m.p.230.1~231.8 ℃.1H NMR (400 MHz, CDCl3),δ: 7.48 (d,J= 8.8 Hz,2H), 7.45 (d,J= 8.8 Hz, 2H), 7.41 (d,J= 8.0 Hz, 2H),7.37~7.29 (m, 3H), 7.17 (t,J= 7.2 Hz, 1H), 4.68 (s, 2H).13C NMR (101 MHz, DMSO-d6),δ: 164.57, 145.47, 138.45,136.33, 132.20, 129.88, 129.38, 125.89, 124.45, 120.48 (q,JC-F= 271.7 Hz), 119.78, 119.68 (q,J= 37.4 Hz), 114.10, 102.64,97.81, 50.62.HRMS, 计算值 C20H12BrClF3N3O ([M + H]+):481.998, 实测值 481.9874.
N-(2-异丙基苯基)-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6h):纯白色固体,收率76%,m.p.221.4~223.0 ℃.1H NMR (400 MHz, CDCl3),δ:7.53~7.43 (m, 6H), 7.31 (d,J= 8.0 Hz, 1H), 7.24~7.18 (m,2H), 4.76 (s, 2H), 2.87~2.80 (m, 1H), 1.20 (d,J= 6.8 Hz, 6H).13C NMR (101 MHz, CDCl3),δ: 164.17, 144.78, 142.00,137.56, 132.25, 131.25, 129.76, 127.51, 126.59, 126.05,125.53, 124.97, 120.18 (q,J= 37.4 Hz), 120.01 (q,JC-F=270.7 Hz), 113.35, 103.35, 99.18, 49.84, 28.00, 23.26, 23.10.HRMS, 计算值 C23H18BrClF3N3O ([M + H]+): 524.035, 实测值 524.0342.
N-(4-甲基苯基)-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6i):纯白色固体,收率79%,m.p.247.8~249.3 ℃.1H NMR (400 MHz, CDCl3),δ: 7.49 (d,J= 8.8 Hz, 2H), 7.46 (d,J= 8.8 Hz, 2H), 7.30 (d,J= 8.4 Hz,2H), 7.15 (d,J= 8.4 Hz, 2H), 7.11 (s, 1H), 4.68 (s, 2H), 2.33(s, 3H).13C NMR (101 MHz, CDCl3),δ: 163.22, 144.89,137.53, 135.43, 133.68, 131.27, 129.81, 129.75, 124.99,120.41, 120.11 (q,JC-F= 270.7 Hz), 119.50(q,J= 34.3 Hz),113.41, 103.49, 99.15, 49.59, 20.93.HRMS, 计算值C21H14BrClF3N3O ([M + H]+): 496.003, 实测值 496.0038.
N-(4-三氟甲基苯基)-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6j):纯白色固体,收率78%,m.p.219.8~221.0 ℃.1H NMR (400 MHz, CDCl3),δ: 7.61 (d,J= 8.4 Hz, 2H), 7.57 (d,J= 8.8 Hz, 2H), 7.49 (d,J= 8.2 Hz,2H), 7.44 (d,J= 8.4 Hz, 2H), 4.72 (s, 2H).13C NMR (101 MHz, DMSO-d6),δ: 165.34, 145.51, 141.99, 136.37, 132.21,129.91, 126.73, 124.67 (q,JC-F= 271.7 Hz), 124.49 (q,J=32.3 Hz), 125.82, 121.14 (q,JC-F= 268.7 Hz), 119.74(q,J=37.4 Hz), 119.76, 114.05, 102.72, 97.90, 50.71.HRMS, 计算值 C21H11BrClF6N3O ([M + H]+): 549.975, 实测值 549.9754.
N-(4-氟苯基)-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6k):纯白色固体,收率82%,m.p.238.5~240.3 ℃.1H NMR (400 MHz, CDCl3),δ: 7.50 (d,J= 8.8 Hz, 2H), 7.45 (d,J= 8.8 Hz, 2H), 7.42~7.36 (m, 2H),7.05 (t,J= 8.8 Hz, 2H), 4.69 (s, 2H).13C NMR (101 MHz,DMSO-d6),δ: 164.55, 158.83 (d,JC-F= 241.4 Hz), 145.47,136.35, 134.81, 132.22, 129.90, 125.87, 121.71, 121.62,120.48 (q,JC-F= 270.7 Hz), 119.70 (q,J= 37.4 Hz), 116.13,115.91, 114.09, 102.68, 97.83, 50.12.HRMS, 计算值C20H11BrClF4N3O ([M + H]+): 499.978, 实测值 499.9782.
N-(4-氯苯基)-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6l):纯白色固体,收率84%,m.p.234.6~236.4 ℃.1H NMR (400 MHz, DMSO-d6),δ: 10.46(s, 1H), 7.72~7.65 (m, 2H), 7.62~7.55 (m, 2H), 7.54~7.47 (m,2H), 7.41~7.35 (m, 2H), 4.88 (s, 2H).13C NMR (101 MHz,DMSO-d6),δ: 164.80, 145.50, 137.39, 136.35, 132.22, 129.91,129.33, 128.06, 125.86, 121.37, 120.46(q,JC-F= 270.7 Hz),119.66 (q,J= 37.4 Hz), 114.09, 102.69, 97.84, 50.61.HRMS,计算值 C20H11BrCl2F3N3O ([M + H]+): 515.949, 实测值515.9490.
N-(4-溴苯基)-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6m):纯白色固体,收率82%,m.p.240.1~242.0 ℃.1H NMR (400 MHz, CDCl3),δ: 7.49 (d,J= 8.4 Hz, 2H), 7.47~7.42 (m, 4H), 7.33 (d,J= 8.4 Hz, 2H),4.68 (s, 2H).13C NMR (101 MHz, CDCl3),δ: 163.11, 144.89,137.53, 135.43, 133.68, 131.27, 129.83, 129.76, 124.99,120.68 (q,J= 38.4 Hz), 120.41, 120.11 (q,JC-F= 270.7 Hz),1 1 3.4 2, 1 0 3.3 5, 9 9.1 2, 5 0.4 4.H R M S, 计算值C20H11Br2ClF3N3O ([M + Na]+): 581.880, 实测值 581.8806.
N-(4-氰基苯基)-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6n):纯白色固体,收率72%,m.p.216.4~218.0 ℃.1H NMR (400 MHz, CDCl3),δ: 7.64 (d,J= 8.8 Hz, 2H), 7.60 (d,J= 8.8 Hz, 2H), 7.53~7.47 (m, 2H),7.46~7.39 (m, 2H), 4.74 (s, 2H).13C NMR (101 MHz, CDCl3),δ: 163.70, 145.06, 140.70, 137.71, 133.49, 131.19, 129.91,124.84, 120.24 (q,J= 37.4 Hz), 120.06 (q,JC-F= 270.7 Hz),119.94, 118.52, 113.46, 108.16, 103.46, 99.17, 49.94.HRMS,计算值 C21H11BrClF3N4O ([M + H]+): 506.983, 实测值506.9827.
N-(4-硝基苯基)-2-(3-溴-5-(4-氯苯基)-4-氰基-2-(三氟甲基)-1H-吡咯-1-基) 乙酰胺(6o):纯白色固体,收率65%,m.p.176.5~178.4 ℃.1H NMR (400 MHz, CDCl3),δ: 8.24 (d,J= 9.2 Hz, 2H), 7.66 (d,J= 9.2 Hz, 2H), 7.51 (d,J= 8.4 Hz,2H), 7.44 (d,J= 8.4 Hz, 2H), 4.76 (s, 2H).13C NMR (101 MHz, DMSO-d6),δ: 165.73, 145.51, 144.46, 143.24, 136.38,132.22, 129.93, 125.78, 125.58, 120.25 (q,JC-F= 270.7 Hz),119.63, 119.69 (q,J= 36.4 Hz), 114.03, 102.78, 97.94, 50.80.HRMS, 计算值 C20H11BrClF3N4O3([M + H]+): 526.973, 实测值 526.9723.
1.4 生物活性测定
1.4.1 离体杀菌活性测定 参考文献[19]中的菌丝生长速率法测定。药剂初筛浓度为0.2 mmol/L,以97% 咯菌腈原药和90% 嘧菌酯原药为对照药剂。
1.4.2 杀虫活性测定 参考浸叶法[19]测定。药剂浓度为0.2 mmol/L,以98% 虫螨腈原药为对照药剂。
1.4.3 杀螨活性测定 参考琼脂保湿浸叶法[19]测定。药剂浓度为0.2 mmol/L,以98%虫螨腈原药为对照药剂。
1.4.4 杀线虫活性测定 参照直接触杀法[19]测定。药剂浓度为0.2 mmol/L,以97%噻唑膦原药为对照药剂。
1.5 作物安全性初步测定
参照文献方法[22-23]对作物安全性进行初步测定。选取高活性目标化合物,采用培养皿法初步测定其对水稻和油菜的安全性。药剂浓度设定为0.2、0.4、0.8 mmol/L,以98%溴代吡咯腈原药为对照药剂。
2 结果与讨论
2.1 目标化合物的合成
在化合物4 的合成过程中,采用TLC 监测反应进程,取样点板时应事先向样品管中加入甲醇,以便使化合物4 转变为对应的甲酯后再进行TLC 监测。如果直接取样监测,则化合物4 与空气中的水分反应又会转变为化合物3。在目标化合物(5a~5m,6a~6o)合成过程中,化合物4 用二氯甲烷溶解后,需在冰浴条件下进行恒压滴定。
2.2 目标化合物的生物活性
2.2.1 离体杀菌活性 杀菌活性测定结果(表1)显示:在0.2 mmol/L 浓度下,大部分化合物对供试病原菌表现出良好的杀菌活性。其中,化合物2、3、5b、5h、5l 和5m 对水稻稻瘟病菌的抑制率分别为81.72%、97.33%、63.39%、59.06%、58.27%和100.00%,优于对照药剂咯菌腈(57.63%);化合物5m 对水稻纹枯病菌和小麦根腐病菌的抑制率达100.00%,与对照药剂咯菌腈相当。

表1 目标化合物下在0.2 mmol/L 下对4 种植物病原菌菌丝生长的抑制作用Table 1 Inhibition of target compounds against four pathogenic fungi in vitro at 0.2 mmol/L
选取杀菌活性初筛时抑制率大于80%的化合物进行杀菌EC50测试,结果(表2)显示,化合物5m 对水稻纹枯病菌、小麦根腐病菌的EC50值分别为0.0218 和0.0420 mmol/L,不及对照药剂咯菌腈(0.0002、0.0010 mmol/L);化合物2、3、5m 对水稻稻瘟病菌的EC50值分别为0.0532、0.0470 和0.0174 mmol/L,优于咯菌腈(0.0914 mmol/L),但不及嘧菌酯(0.0001 mmol/L)。
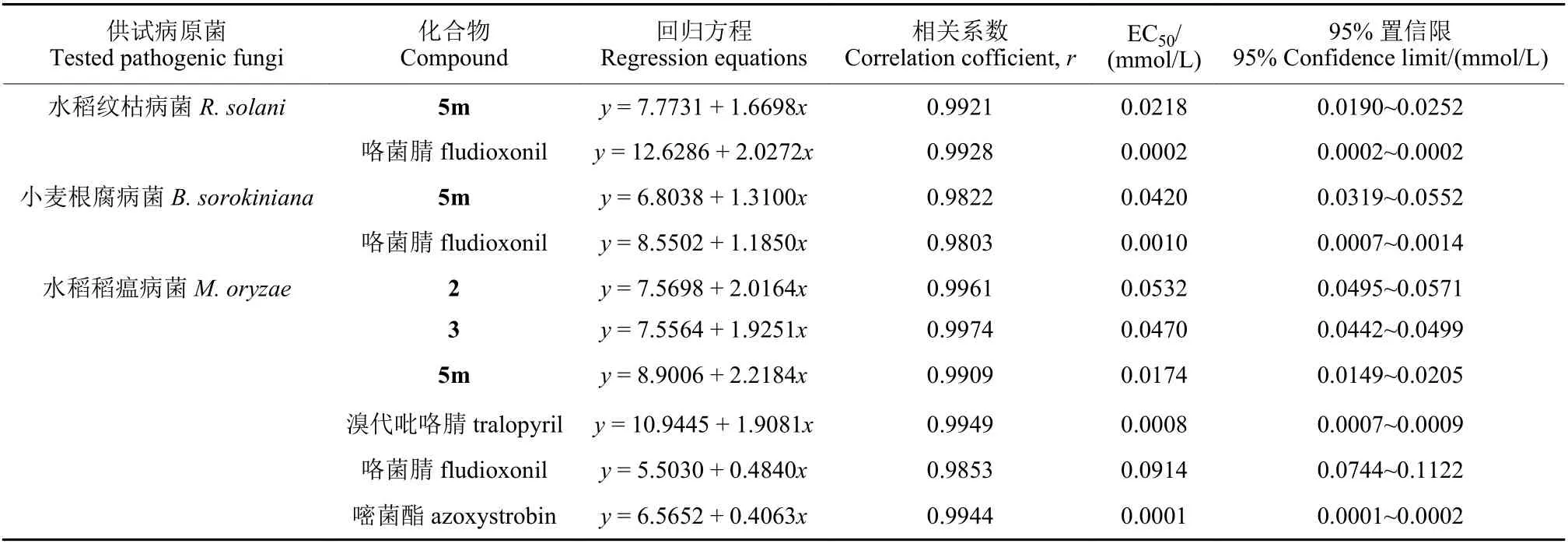
表2 部分目标化合物对供试植物病原真菌的EC50 值Table 2 The EC50 values of some target compounds against tested pathogenic fungi
初步构效关系分析发现,溴代吡咯腈羧酸酯类衍生物(5a~5m)的杀菌活性普遍优于酰胺类衍生物(6a~6o)。当R1为直链烷烃时,随着碳链的增长,化合物的杀菌活性呈现先增高后降低的趋势,其中以化合物2 (R1= Et) 的活性最优;当R1为丙基或丁基时,含直链烷基化合物的杀菌活性优于含支链烷基化合物,比如化合物5b (R1=Pr)的活性优于化合物5c (R1=i-Pr),化合物5d(R1= Bu) 的杀菌活性优于化合物5e (R1=i-Bu)与5f (R1=t-Bu);当R1为苯基时,苯基对位被吸电子基取代时,随着吸电子基能力增强,目标化合物杀菌活性也随之增强,其中化合物5m (R1=4-NO2-phenyl)杀菌活性最佳,具有一定的广谱性。
2.2.2 杀虫活性 杀虫测试结果(表3)显示,在0.2 mmol/L 下,大部分目标化合物在药后48 h 对斜纹夜蛾具有一定的杀虫活性,但均低于对照药剂虫螨腈 (校正死亡率100%)。
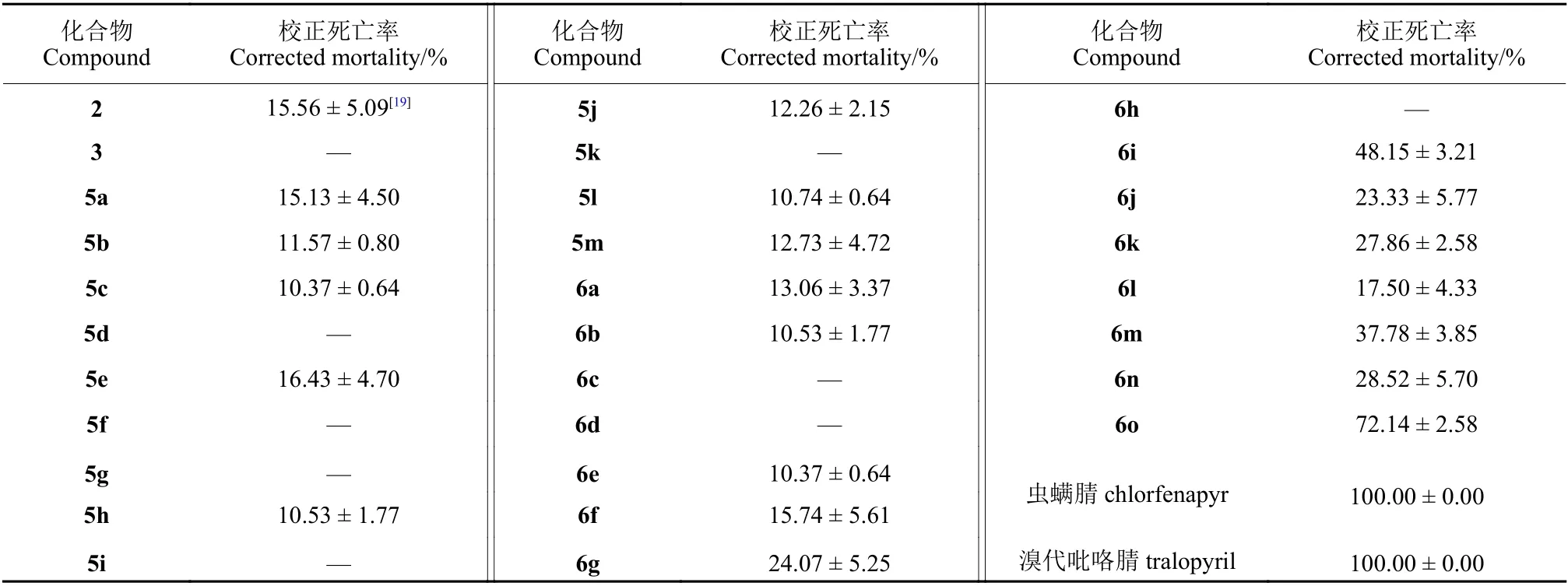
表3 目标化合物在0.2 mmol/L 时对斜纹夜蛾杀虫活性Table 3 Insecticidal activity of target compounds against Spodoptera litura at 0.2 mmol/L
初步构效关系分析发现,当R1与R2取代基为烷烃时,目标化合物对斜纹夜蛾基本无杀虫活性;当R1与R2取代基为苯基时,酰胺类衍生物的杀虫活性优于同类型羧酸酯类衍生物;当R2为苯基,且苯基对位被吸电子基取代时,化合物均有一定的杀虫活性,其中化合物6o (R2= 4-NO2-phenyl)活性最佳。
2.2.3 杀螨活性 测定结果(表4)显示,在0.2 mmol/L 时,大部分目标化合物在药后48 h 对朱砂叶螨雌成螨具有一定的杀螨活性,但均低于对照药剂虫螨腈(校正死亡率100%)。
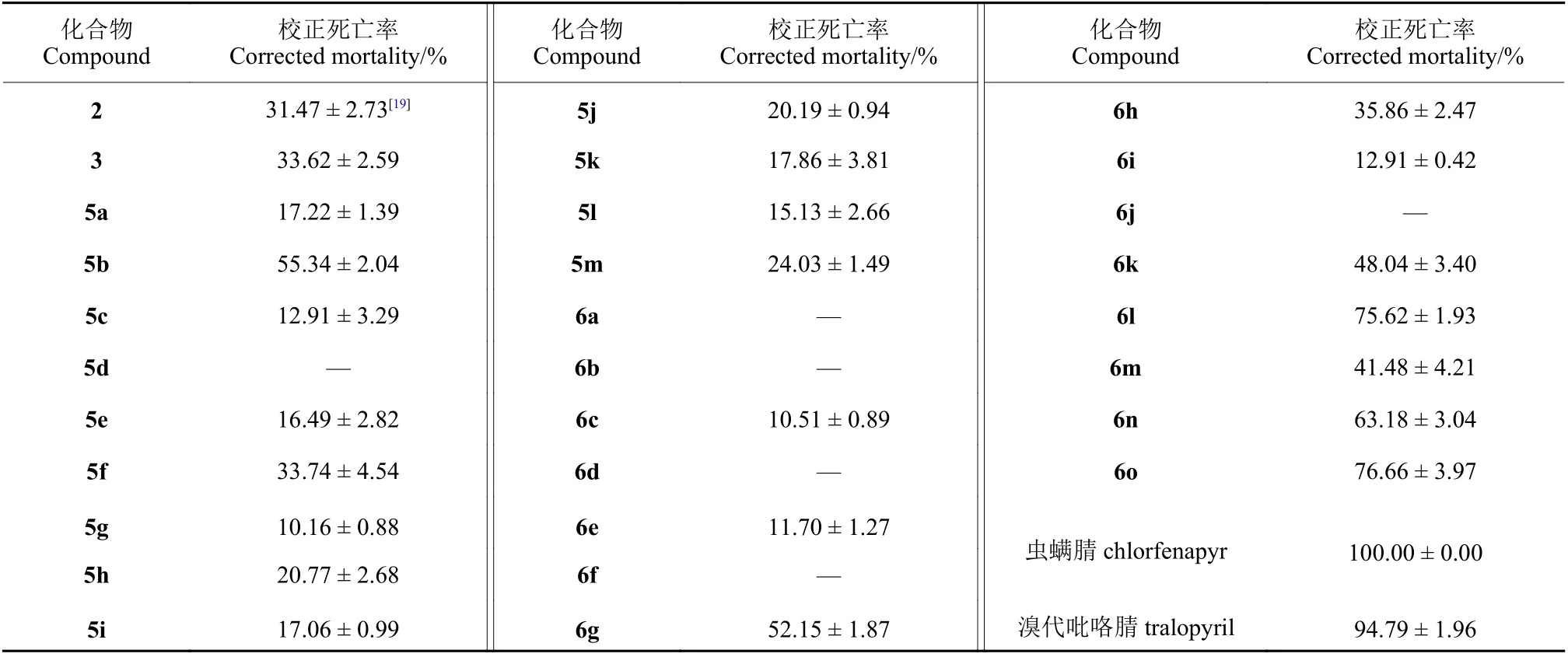
表4 目标化合物在0.2 mmol/L 时对朱砂叶螨雌成螨的杀螨活性Table 4 Insecticidal activity of some target compounds against adult mite of T.cinnabarinu at 0.2 mmol/L
初步构效关系分析发现,当取代基R1与R2为直链烷基时,羧酸酯类衍生物的杀螨活性优于酰胺类衍生物,且随着碳链增长,目标化合物的杀螨活性呈现先增高后降低的趋势,其中化合物5b (R1= Pr) 活性最好;当R1与R2取代基为苯基,且苯基对位被吸电子基取代时,酰胺类衍生物的杀螨活性优于羧酸酯类衍生物,其中化合物6l (R2= 4-Cl-phenyl)与6o (R2= 4-NO2-phenyl)的活性最佳。
2.2.4 杀线虫活性 测定结果(表5) 显示,在0.2 mmol/L 时,大部分化合物对秀丽隐杆线虫表现出优异的杀线虫活性,其中化合物2、3、5b和5g 在处理48 h 后对秀丽隐杆线虫的校正死亡率达到90%以上,优于对照药剂噻唑膦 (43.89%)。
根据初筛结果,测定了对秀丽隐杆线虫具有较高杀线虫活性化合物的LC50值。结果(表6)显示,所测试的目标化合物对秀丽隐杆线虫的LC50值均优于对照药剂噻唑膦(0.2798 mmol/L),但均不及母体溴代吡咯腈(0.0004 mmol/L)。

表6 部分目标化合物对秀丽隐杆线虫的 LC50 值Table 6 The LC50 values of some target compounds against C.elegans
初步构效关系分析发现,当取代基R1与R2为直链烷基时,随着碳链的增长,酰胺类衍生物的杀线虫活性呈现先增高后降低的趋势,以化合物6b (R2= Et) 的活性最好。当碳链长度在1~3个碳原子时,羧酸酯类衍生物与酰胺类衍生物均具有优异的杀线虫活性,但羧酸酯类衍生物均优于酰胺类衍生物;当R1与R2为苯基,且当苯基对位被强吸电子基取代时,目标化合物均具有优异的杀线虫活性,如化合物5m (R1= 4-NO2-phenyl)、6n (R2= 4-CN-phenyl)、6o (R2= 4-NO2-phenyl)的杀线虫活性分别为73.26%、80.86%和83.47%,均优于对照药剂噻唑膦(43.89%)。
2.3 作物安全性
根据目标化合物的生物活性测定结果,选取高活性化合物测定其对水稻与油菜作物安全性。初步结果(表7)显示:在0.2、0.4、0.8 mmol/L浓度下,溴代吡咯腈对水稻根部、油菜根部与茎部的生长均具有明显抑制作用,对作物产生明显药害;而在同等浓度下,高活性目标化合物相比母体溴代吡咯腈,对水稻根部、油菜根部与茎部的生长抑制作用明显减弱(图1),其中部分化合物甚至对作物生长产生促进作用。

图1 目标化合物在0.8 mmol/L 下对水稻 (A) 和油菜 (B) 的生长抑制作用Fig.1 Growth inhibition of target compounds against O.sativa and B.campestris at the concentration of 0.8 mmol/L
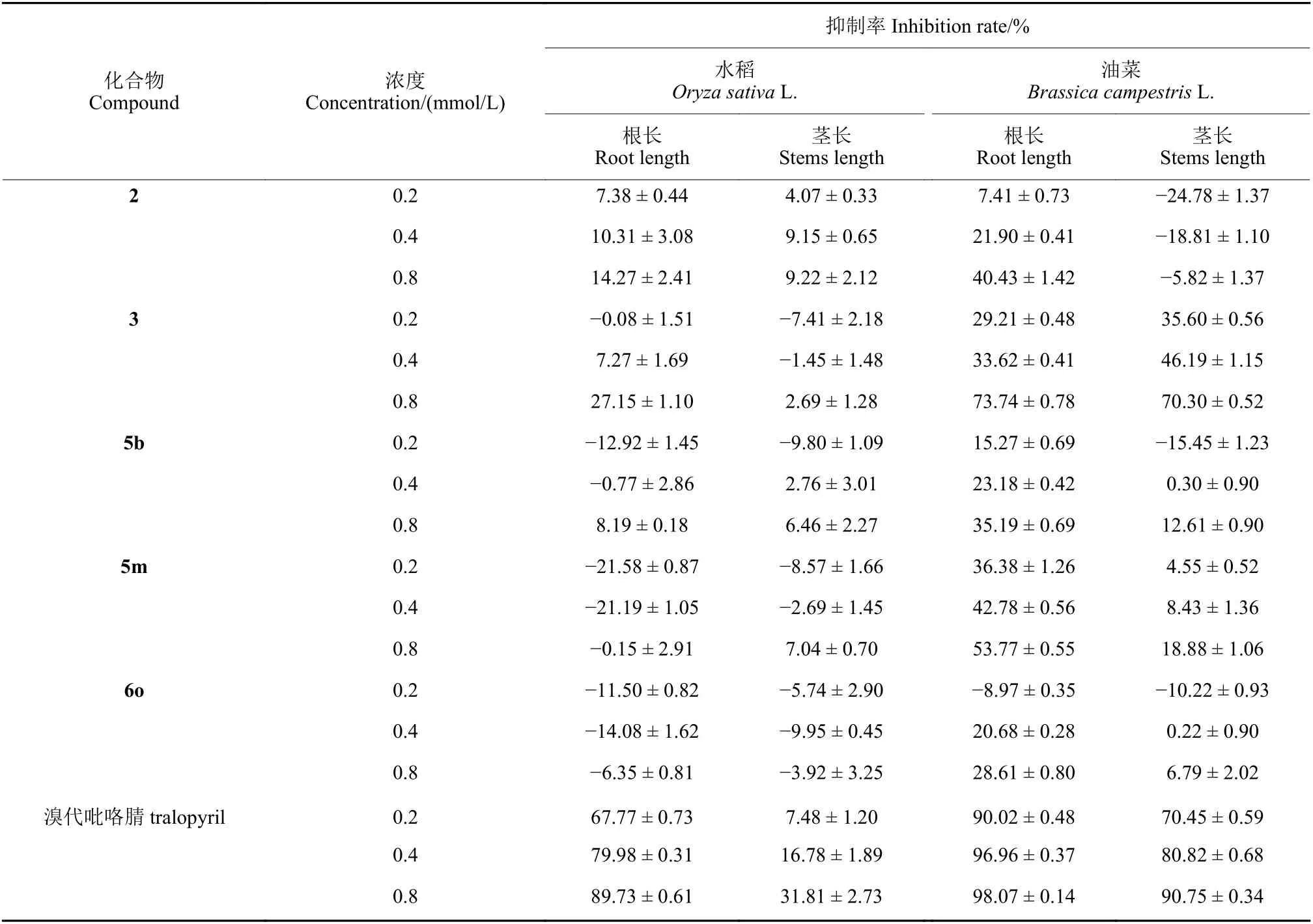
表7 目标化合物对水稻和油菜生长的抑制作用Table 7 Growth inhibition of target compounds on rice and rape
3 结论
本研究通过对溴代吡咯腈进行亲核取代等反应设计合成了28 个新型的2-(溴代吡咯腈-1-基)乙酸衍生物,其结构均经过1H NMR、13C NMR 和HRMS 确证。生物测定结果表明,目标化合物具有一定的杀菌、杀虫、杀螨与杀线虫活性。其中化合物2、3和5m表现出良好的杀菌与杀线虫活性,化合物6o表现出良好的杀虫杀螨活性,可作为先导化合物进行后续优化。目标化合物杀虫杀螨活性较母体溴代吡咯腈显著下降,推测主要为两方面原因导致:一方面,目标化合物自身不具备足够的亲脂性,不能完全穿透昆虫表皮层,或在穿透昆虫表皮层后不能完全穿透线粒体膜,进而导致杀虫杀螨活性下降;另一方面,目标化合物遮蔽了溴代吡咯腈吡咯环N位的H,且目标化合物在昆虫体内不能被相应的酶分解为溴代吡咯腈,导致其无法破坏线粒体内二磷酸腺苷(ADP)到三磷酸腺苷(ATP)转化过程中涉及的质子梯度,进而导致杀虫杀螨活性下降。作物安全性初步试验结果表明,相比母体溴代吡咯腈,目标化合物减轻了对作物产生的药害,对作物更安全。本研究为溴代吡咯腈衍生物的设计与改造提供了思路,对探究溴代吡咯腈衍生物的生物活性多样性具有参考意义。
