材料科学基础课程中原子结构术语标准化探讨
2023-04-02曾盛渠夏益青伦英慧林修洲
曾盛渠 夏益青 伦英慧 林修洲

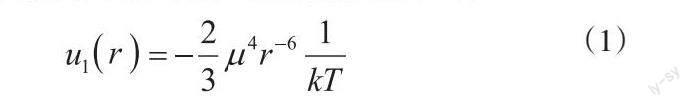
摘 要:目前在材料科学基础课程中,原子尺度教学的一些术语和基础数据前、后学习的课程缺少统一性。本文针对材料科学基础教学中关于原子尺度结构的几个概念,以及不同教材中表述不同的术语进行了讨论,建议依据全国科学技术名词审定委员会公布的术语进行统一。教学中除了课本已有的知识外,更要培养学生的怀疑精神和创新能力。对材料原子尺度的结构提出几个探索性的讨论问题,通过问题引导学生对材料的结构与性能进行深层次的思考,培养其探索与创新精神。
关键词:教学,材料科学基础,结构,原子尺度,术语
DOI编码:10.3969/j.issn.1002-5944.2023.18.008
0 引 言
材料科学是建立在化学、物理、冶金、晶体学等学科基础上的一个交叉学科。材料类专业人才的培养,通常会先学习化学、物理等基础课程再进入《材料科学基础》的学习。而《材料科学基础》又是后续专业课程以及进行材料相关科学研究非常重要的基础教材。因此,《材料科学基础》的教学需要做好承上启下的作用。高中化学选择性必修课、无机化学等课程都已经学习了原子结构的基本知识。然而之前的学习中,并未从材料的角度深入讨论。原子结构对材料的性质、使用性能都有非常重要的影响,可以说是根本所在。因此,《《材料科学基础》》教学很有必要从原子尺度的结构与材料性质和使用性能关系的角度来进行深入学习,弄清原子尺度的结构对材料性能和使用表现的影响。
原子尺度的电子、离子,其相互作用和运动规律都遵循量子力学,与宏观物质有根本性的不同。要准确理解原子尺度的结构,需要一定的量子力学基础知识,这对于普通学习者来说有一定的困难。但是,在《材料科学基础》的教学中,应该引导同学们建立和材料原子尺度结构相关的量子力学、固体物理/化学基础概念,为后续的深入学习和研究打下基础。目前《材料科学基础》的教材很多,其中很多优秀教材为我国材料相关的人才培养奠定了坚实的基础。然而不同的教材中原子尺度结构相关的概念和术语缺少标准化和统一性。相关的术语应该在前面和后面的课程当中保持一脉相承的连贯和自洽性,避免表述不一和矛盾。
在具体的课程教学中,应该激发同学们深入思考和探索的兴趣,而不只是给出教材上现有的知识点。教学中适当提出一些问题,引导学生进行更深入的思考,对培养同学们的创新意识和能力有重要的意义。
在目前《材料科学基础》的相关教材、著作、研究文献中,与原子结构相关的一些术语较为多样,一些用语和学生前面的化学类课程及后续学习的《结构化学》《固体物理》等教材不同。除此以外,一些课本现有的结论仍然值得深入讨论。本文以《材料科学基础》中关于原子尺度的结构相关的概念与术语标准化问题和教学方式为例进行探讨。
1 固体中键的结合强度
关于化学键的强度习惯于使用“键能”进行表征。《材料科学技术名词》中对“键能(b o n denergy)”定义为:表征结合键牢固程度的物理量。对于双原子分子,在数值上等于把一个分子的结合键断开拆成单个原子所需要的能量[1]。《化学名词》对键能定义:在给定的温度和压力下断开气态化合物中的1个化学键生成气态产物所需的平均能量[2]。由上可见,“键能”主要针对的是单个化学键。
对于金属材料和共价键形成的原子晶体,在《材料科学技术名词》中给出的术语“晶体结合能(cohesive energy of crystal)”更适用于描述原子间的键合强度。晶体结合能定义为“将粒子从自由状态结合为晶体所放出的能量,或将晶体拆散为自由粒子所需的能量”,它和固体物理中的内聚能定义类似,用公式可以表示为:
式中的孤立粒子,根据其形成晶体前的状态,可以是离子、原子或分子,在不同场合意义不同。在英文科技文献中也常用binding energy表示晶体结合能,注意与bond energy不同。
对于固态的离子型晶体材料而言,大量离子组合在一起形成固态整体,因为键的不饱和性和库仑力的长程作用,一个离子受到周围各方向不同距离的多个键合作用力,牵一发而动全身。因此离子型晶体常用晶格能(lattice energy)来描述键的强度[3]。晶格能的定义为:标准状况下,拆开单位物质量的离子晶体使其变为气态组分离子所需吸收的能量。以NaCl为例,是在常压、0K温度下将1 mol离子晶体拆散为1 mol气态Na+阳离子和1 mol气态Cl-阴离子所需要的能量。不难发现,对于双元离子晶体,例如NaCl,其晶格能的数值是晶體结合能即内聚能的2倍。对于单个原子为晶体格点的单质材料,晶格能和晶体结合能数值相同。
关于离子晶体中键的强度术语,在无机化学的教材中有所阐述[3]“离子化合物的化学结合力不是简单的两个阴阳离子之间的结合,而是整块晶体内的整个结合力,因此用晶格能描述离子键的强度,经常比离子键的键能更好”。任何材料必定是大量微观粒子形成的,因此对于材料来说,更应该考虑整体的结合能。
由此,建议《材料科学基础》的教学中,金属、共价晶体及范德瓦耳斯键形成的分子晶体使用“晶体结合能”或“内聚能”来表征原子间结合的强度;离子晶体根据结构化学和固体物理的习惯,使用“晶格能”描述键的强度。在教学中应该向学生介绍键能、晶体结合能、晶格能三个术语的区别和适用场合,保持在前后的课程中知识的自洽和连贯性。
2 原子键的含义
在英文原版教材中,关于原子间的键合作用或作用力,与键合的状态是分别用“bonds”“bonding”两个词来表示的。例如A s k e l a n d编写的“ T h escience and engineering of materials”英文版[4]关于共价键的描述、“Materials with covalent bondingare characterized by bonds that are formed by sharingof valence electrons among two or more atoms”中,“covalent bonding”是指材料中的原子键合状态。下一段“Covalent bonds are very strong.”中“covalentb o n d s”则是指原子间的相互作用力。而不管是“covalent bonding”还是“covalent bonds”,中文都习惯用“共价键”这一个词来表达。
我国《材料科学基础》教学中关于原子键的具体意义表述不一。以金属键的定义为例,上海交大胡赓祥[5]定义为“这种由金属中的自由电子与金属正离子相互作用所构成的键合称为金属键。”西北工大刘智恩[6]定义为“键是一种力。通过正离子与电子之间相互吸引,这些正离子与电子结合起来。这种结合力就是金属键。”可见,部分教材中将原子键定义为一种键合状态,另一部分教材定义为作用力。
实际的应用中,原子键可能会表示相互作用力,也可能表示原子的结合状态。例如,当提到键的方向性,主要是原子间的相互作用力;而提到键的饱和性则可能是指键合的状态有饱和性。考虑以上两方面的术语应用场合,建议在《材料科学》的教学中按如下方式对原子键进行表述:
原子键(金属键、离子键、共价键)一方面,是指原子之间的相互作用,特别是相互作用力(bonds),另一方面,习惯上原子键也表示原子之间结合的方式或状态(bonding)。
3 主价键中的排斥力
国内《材料科学基础》教材对原子键常见的表述“正负离子相互吸引,使原子结合在一起,这就是离子键”;“金属键正是依靠正离子与自由电子之间的相互吸引而结合起来”[7]。“因为金属正离子之间和电子云之间存在排斥力,所以不能靠得太近”[8]。可以看到,关于原子键往往只介绍了原子或离子之间的引力,对其排斥力没有介绍或是不够完整。
实际上,离子或离子实之间距离太近时,排斥力来源于两个方面。一方面是离子实之间的静电排斥力,其遵循库仑定律。更主要的另一方面是因为离子实靠近导致全充满的原子轨道发生重叠产生的电子简并压。根据泡利不相容原理,一个原子轨道不允许超过2个电子,重叠区域的部分电子就会跃迁到更高能级轨道,导致系统能量上升,产生强烈的排斥力。这称为电子简并压或费米简并压[9]。可见,电子简并压是排斥力的主要原因,其与服从库仑定律的静电排斥力是不同的。
原子键合状态必定是吸引力和排斥力的平衡状态,因此不可忽视对排斥力的介绍。原子之间的相互作用本身既有吸引力,又有排斥力,两者平衡才形成了稳定的结合。例如《近代晶体学》[10]对金属键的定义“吸引力和排斥力达到平衡时能量最低,这样形成的键合方式称为金属键。”从问题的正反两方面分析,更符合唯物主义辩证观。
4 取向力、诱导力、色散力与分子间距离的关系
关于三种范德瓦耳斯力,即取向力、诱导力、色散力,部分教学资料给出了如下观点:“取向力与分子间距离r 的6次方成反比”。而某些资料又介绍“取向力与分子间距离的3次方成反比”。这个规律的来源何处,表述是否足够准确呢。
《结构化学基础》给出结论是6次方反比[11];另外《结构化学基础》中称取向力为静电力不妥,依据全国科学技术名词审定委员会公布的术语,取向力、葛生力更合适。因为产生取向力的极性偶极子为不断运动而非静态,正是其相对运动改变了作用力与分子间距离r的数学关系。《固体物理》给出了推导过程,静态的取向排列偶极子势能与r是3次方反比关系,耦合分子的振动后降低到6次方反比[12];《现代晶体学-2晶体的结构》“热运动搅乱偶极位向使之降低”,这一互作用能表示为:
式中:u 1为结合能,μ为极性分子的偶极矩,k为玻尔兹曼常数,T 为热力学温度。可见,取向力形成的分子间结合能与r的6次方反比。
综上,热运动不可忽视的情况下,取向力形成的范德瓦耳斯键能是与分子间距离r的6次方反比,注意这里是结合能。力是键能的导数,常常比结合能的指数大1。根据相互作用力和键合能的求导关系,取向力与r应该是7次方反比关系。
《无机化学》《物理化学》中都直接给出“取向力与分子间距离的7次方成反比”[13-14]。
由于材料类专业的同学通常已经学习了《无机化学》和《物理化学》,但基础课程教学内容多,关注点不同。在《材料科学基础》中有必要再从材料的结构与性能关系角度阐述分子间的作用力,并且在前后学习的不同课程教学中,应该保持相洽的阐述。
5 离子实
在固体的金属材料或合金中,价电子摆脱单个原子核的束缚在整个晶体内所有原子间自由运动,故称为离域电子或自由电子。失去价电子的金属原子可称为“离子实”,它包括原子核以及原来的内层全充满轨道电子,带正电[10]。这里用离子实这个术语,目的是与原子核中“核”的意义进行区分。因为如果用离子核,可能理解为离子中的核,也就是离子里面的质子和中子形成的核,与原子核中的核有相同的意义。原子或离子核的尺度是10-15 m,而离子实为10-10 m。知网查閱相关文献,也支持上述的表达。个别的教学资料中使用“离子核”,建议修改为“离子实”更恰当。
6 键能或晶格能数据
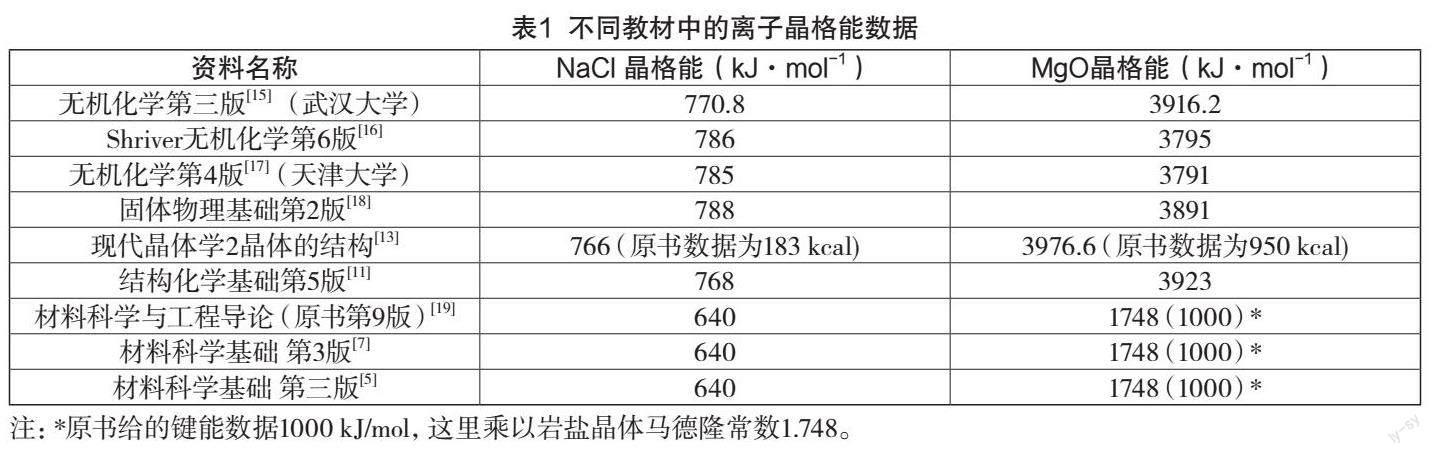
关于离子的键能或晶格能的数据,不同的教材有较大的差别。严格地讲,晶格能是指在0K和101.32 KPa条件测量的能量变化。如果是在298 K和101.32 KPa条件下进行时,则释放的能量为该化合物的晶格焓[11]。例如,NaCl的晶格能、晶格焓分别为786 kJ·mol-1、788 kJ·mol-1。晶格能和晶格焓通常只差几kJ·mol,所以在作近似计算时,可忽略不计。
但习惯上通常使用晶格能这一概念。这里罗列了几本教材中的NaCl和MgO的晶格能数据,可以发现数据相差较大(见表1)。因为晶格能需要用Born-Harber(波恩-哈勃)循环的实验间接测定,涉及原子的电子亲和能、离解能数据误差,因此不同作者给出的晶格能数据略有差异。正常的差异值小于10 kJ/mol。但材料科学书籍中的数据和无机化学、固体物理、晶体学等教材都有较大差异,建议参考《结构化学基础》、《无机化学》数据进行修改,保持不同课程中数据的自洽性。
7 键的方向性讨论
金属键、离子键中的吸引力本质都是电场力,必然与电子的空间分布相关。而p/d/f轨道都有方向性,也就是p/d/f轨道内电子的空间分布有方向性,就必然导致金属键、离子键也有一定的方向性。只是其电子的空间不对称性不明显,所以键表现为方向性不明显,通常近似为没有方向性。在教学中应该说明没有方向性只是一种理论上的近似模型,并引导同学们深入探索和思考,避免同学们形成了思维定势,偏离事实真相。例如,教学中请同学们思考,离子晶体也有特定的外形;铁等金属的配位数为8,低于完全等直径球堆积的配位数12,这些如何解释,是否是无方向性的反例?实际的离子键和金属键中都可能含有一定的共价键成分[11],这是否是其有一定方向性的一种解释。
通过对固有知识点的反面提问,让同学们认识到一些已有的知识也只是为了方便认识微观结构的理论模型,有一定的适用限度。这样的问题引导,有利于培养学生的怀疑精神和创新能力。
8 结 论
针对《材料科学基础》教学中关于原子尺度结构的概念和术语标准化等问题进行了探讨,结论如下。
(1)不同课程以及同一课程不同的教材等教学资料中,个别科学技术术语呈现多样化的特征,建议依据全国科学技术名词审定委员会公布的术语进行统一。
(2)原子尺度结构相关的一些术语和概念在不同教材中的含义有分歧,本文提出了与其他课程相洽的解释。
(3)对原子尺度的材料结构提出探索性的讨论问题。在课堂教学中,不固守课本资料,大胆怀疑提出问题,有利于对学生探索与创新精神进行培养。
参考文献
全国科学技术名词审定委员会审定.材料科学技术名词(2010)[M].北京:科学出版社,2011.
化学名词审定委员会编.化学名词[M].北京:科学出版社,1991.
宋天佑,程鹏,王杏乔.无机化学(上册)[M].北京:高等教育出版社,2004.
ASKELAND, FULAY D R, WRIGHT P P, et al. Thescience and engineering of materials[M]. 北京:清华大学出版社,2005.
胡赓祥,蔡珣,戎咏华.材料科学基础(第3版)[M].上海:上海交通大学出版社,2010.
刘智恩.材料科学基础(第5版)[M].西安:西北工业大学出版社,2019.
石德珂,王红洁.材料科学基础(第3版)[M].北京:机械工业出版社,2021.
赵长生,顾宜.材料科學与工程基础(第3版)[M].北京:化学工业出版社,2020.
阎守胜.固体物理基础[M].北京:北京大学出版社,2011.
张克从.近代晶体学[M].北京:科学出版社,2011.
周公度,段连运.结构化学基础(第5版)[M].北京:北京大学出版社, 2017.
C.基泰尔,固体物理导论(原著第8版)[M].项金钟,等,译.北京:化学工业出版社,2012:43-44.
B·K·伐因斯坦, V·M·弗里特金, V·L·英丹博姆.现代晶体学2晶体的结构[M].合肥:中国科学技术大学出版社,2011:47.
傅献彩.物理化学(第五版)[ M ] .北京:高等教育出版社,2005.
武汉大学.无机化学上册(第3版)[M].北京:高等教育出版社,1994.
WELLER M T , OVERTON T, ROURKE J, et al.无机化学(原著第6版)[M].李珺,等,译.北京:高等教育出版社,2018.
天津大学无机化学教研室.无机化学(第4版)[M].北京:高等教育出版社,2010.曹全喜.固体物理基础(第2版)[M].西安:西安电子科技大学出版社,2017.
WILLIAN D C, 材料科学与工程导论[M].陈大钦,译.北京:科学出版社,2020.
作者简介
曾盛渠,博士,副教授,研究方向为高分子复合材料。
(责任编辑:张瑞洋)
