LC-MS/MS法测定人血浆中比阿培南浓度
2023-04-01钱亚芳杨旭萍蒋艳胡楠常州市第一人民医院药学部江苏常州213003
钱亚芳,杨旭萍,蒋艳,胡楠(常州市第一人民医院药学部,江苏 常州 213003)
碳青霉烯类药物在重症感染治疗中有举足轻重的地位,是革兰氏阴性杆菌治疗的最后一道防线[1]。比阿培南属于碳青霉烯类抗菌药物,相较于其他品种,具有稳定性更好、耐药性更小的优势[2],其抗菌活性和美罗培南相当,神经毒性和肾毒性小,更加安全有效[3],临床上常作为治疗重症感染的杀手锏[2]。比阿培南的血药浓度及维持时间是保证其临床效果的关键[2]。比阿培南血药浓度测定已报道的方法多为HPLC法[4-9],分析效率较低,易受干扰。本研究使用LC-MS/MS技术,建立一种快速、准确地测定比阿培南血药浓度的方法,为其临床合理便用提供依据。
1 材料
1.1 仪器
Jasper HPLC液相色谱仪、Triple Quad 4500MD三重四极杆串联质谱仪(美国AB SCIEX),Direct-Q纯水仪(美国Millipore),BT25S电子分析天平(德国Sartorius),5417R低温高速离心机(德国Eppendorf),Vortex-Genie 2涡旋混合器(美国Scientific industries)。
1.2 待测药品
对照品比阿培南(批号:130578-201602,纯度:99.0%)、法罗培南(内标,批号:130532-201301,纯度:80.3%)(中国食品药品检定研究院)。乙腈(色谱纯,Merck公司),水由Milli-Q超纯水系统制得。
2 方法与结果
2.1 色谱条件
色谱柱:Kinetex HILIC柱(2.1 mm×50 mm,2.6 μm,Phenomenex,USA);柱温:40℃;流动相:0.1%甲酸-水(含10 mmol·L-1乙酸铵)(A)和95%乙腈-水(含10 mmol·L-1乙酸铵)(B),梯度洗脱(0.01~0.70 min:95%B,0.70~1.00 min:95%~40%B,1.00~2.50 min:40%B,2.50~2.70 min:40%~95%B,2.70~5.00 min:95%B);流速:0.4 mL·min-1;进样量:5 μL;分析时间:5 min。
2.2 质谱条件
采用电喷雾离子源(ESI),正离子多反应监测(MRM)模式扫描,毛细管电压(IS)为5500 V,离子源温度(TEM)为550℃,气帘气(CUR)为30 psi,碰撞气(CAD)为8 psi,雾化气(GS1)为50 psi,辅助气(GS2)为50 psi。比阿培南和内标(法罗培南)的MS-scan图见图1,各自的监测离子对、去簇电压(DP)、碰撞电压(CE)等质谱参数见表1。
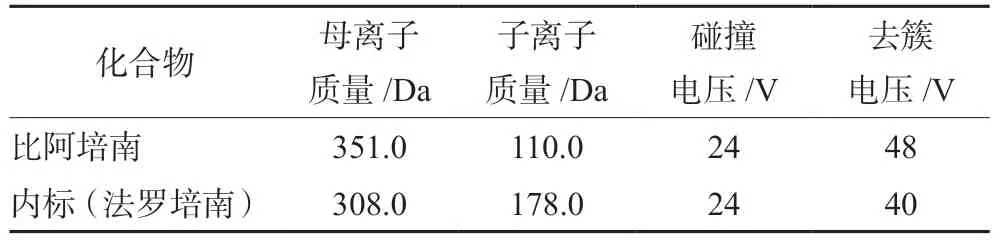
表1 比阿培南和内标LC-MS/MS 测定参数Tab 1 LC-MS/MS measurement parameters of the biapenem and internal standard
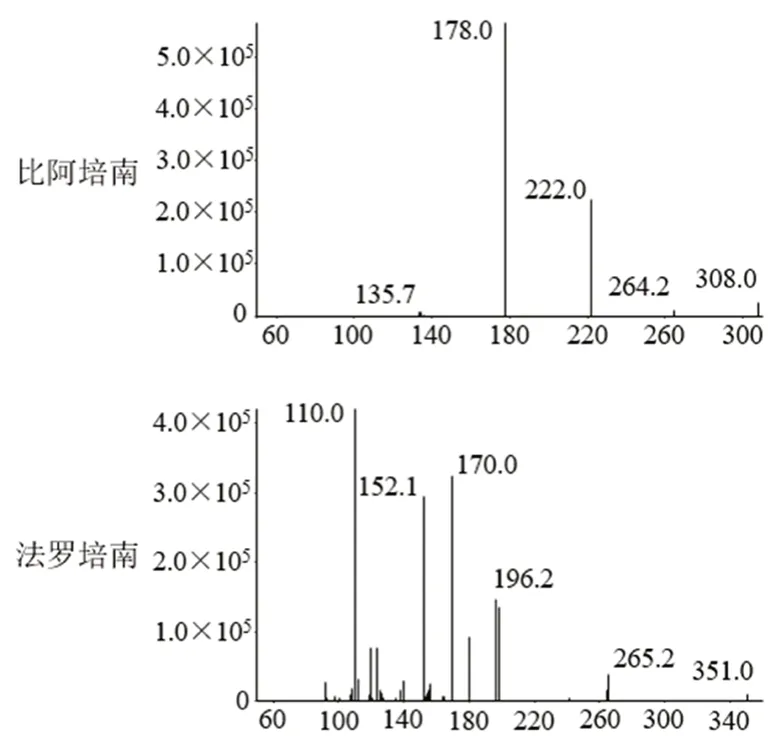
图1 比阿培南和内标(法罗培南)的MS-scan图Fig 1 MS-scan image of biapenem and internal standard(faropenem)
2.3 溶液配制
精密称取比阿培南对照品适量,用甲醇定量配制成15.00 mg·mL-1的对照品储备液,置于-20℃冰箱中保存,使用前用甲醇稀释成2.00、5.00、10.00、20.00、50.00、100.00、200.00、400.00、500.00 μg·mL-1的系列对照品工作液。
精密称取法罗培南对照品适量,用甲醇-水溶液(4∶1)配制成5.00 mg·mL-1的内标储备液,置于-20℃冰箱中保存,临用前用甲醇-水溶液(4∶1)稀释成10.00 μg·mL-1的内标工作液。
2.4 血浆样品的处理
精密移取血浆样品50 μL(含5 μL标准工作液和45 μL空白血浆)于离心管中,加入内标工作液(10.00 μg·mL-1)5 μL,加入乙腈150 μL沉淀蛋白,涡旋3 min,于16 400 r·min-1离心10 min,精密移取上清液20 μL至另一离心管中,加入180 μL乙腈-水溶液(95∶5)稀释,置于进样小瓶中,按“2.1”和“2.2”项下方法进样测定。
2.5 方法学验证
2.5.1 专属性 取6 份不同来源的人空白血浆、加入对照品的血浆样品(质量浓度为0.2 μg·mL-1和2 μg·mL-1)、使用比阿培南的患者血浆样品按“2.4”项下方法处理分析。结果比阿培南和法罗培南的保留时间分别为1.94 min和0.98 min,见图2。

图2 血浆中比阿培南和法罗培南的LC-MS/MS 色谱图Fig 2 LC-MS/MS chromatogram of biapenem and faropenem in the plasma
2.5.2 标准曲线 向空白血浆中分别加入“2.3”项下的系列对照品工作液,配制成0.20、0.50、1.00、2.00、5.00、10.00、20.00、50.00 μg·mL-1的对照品血浆样本,按“2.4”项下方法处理后进样分析。
以比阿培南的浓度(X)为横坐标,比阿培南与内标的峰面积比值(Y)为纵坐标,进行回归分析(W=1/X2),得到标准曲线回归方程:Y=1.460X-0.0177(r=0.9959),r≥0.9950,结果说明在本研究条件下血浆中比阿培南在0.20~50.00 μg·mL-1与峰面积线性关系良好。
2.5.3 精密度与准确度 向空白血浆中分别加入“2.3”项下质量浓度为5.00、50.00、400.00 μg·mL-1的对照品工作液,配制成低、中、高3个浓度水平(0.50、5.00、40.00 μg·mL-1)的质控样本,每6份为1个分析批,按“2.4”项下方法处理后进样分析,根据随行标准曲线,计算质控样本的准确度和批内精密度。在2周内对3个分析批质控样本进行检测分析,计算质控样本的准确度和批间精密度,结果见表2。
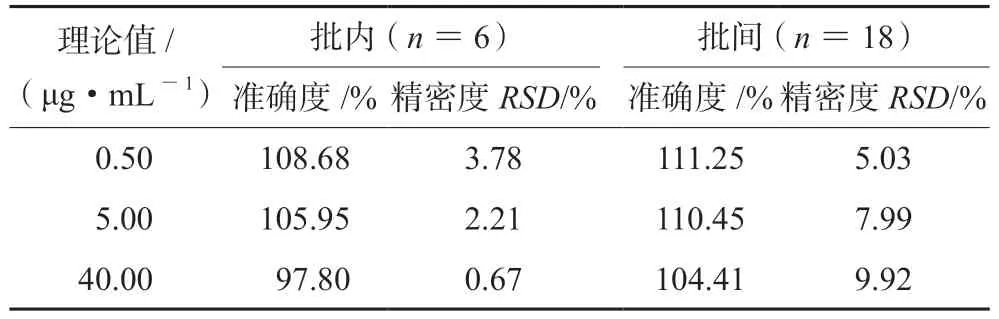
表2 比阿培南血药浓度测定的准确度和精密度结果Tab 2 Accuracy and precision of biapenem
本研究方法下,比阿培南血药浓度测定的准确度为97.80%~111.25%,低、中、高3个浓度水平质控样本的精密度RSD<15%,均符合生物样本定量分析的要求。
2.5.4 提取回收率和基质效应 取“2.5.3”项下低、中、高3个质量浓度水平(0.50、5.00、40.00 μg·mL-1)的质控样本,每个浓度水平6 份,按“2.4”项下方法处理后进行分析,得到比阿培南的峰面积A1;另取人空白血浆,乙腈沉淀蛋白后取得上清液,向上清液中加入分别加入“2.3”项下质量浓度为5.00、50.00、400.00 μg·mL-1的对照品工作液,配制成低、中、高3个质量浓度水平(0.50、5.00、40.00 μg·mL-1)的样本,每个浓度水平6份,分析后得到比阿培南的峰面积A2,峰面积比A1/A2即为比阿培南的提取回收率。结果见表3,本研究方法下,比阿培南的提取回收率为80.25%~84.11%(RSD<15%),说明本样品前处理方法适用于比阿培南的提取分析。
以纯水作为基质,配制低、中、高3个质量浓度水平(0.50、5.00、40.00 μg·mL-1)的样本,每个浓度水平6份,进样分析得到比阿培南的峰面积A3。根据峰面积比A2/A3求算比阿培南的基质效应。结果见表3,比阿培南的基质效应结果为109.19%~117.91%(RSD<15%),表明基质中内源性物质对比阿培南的影响较小。
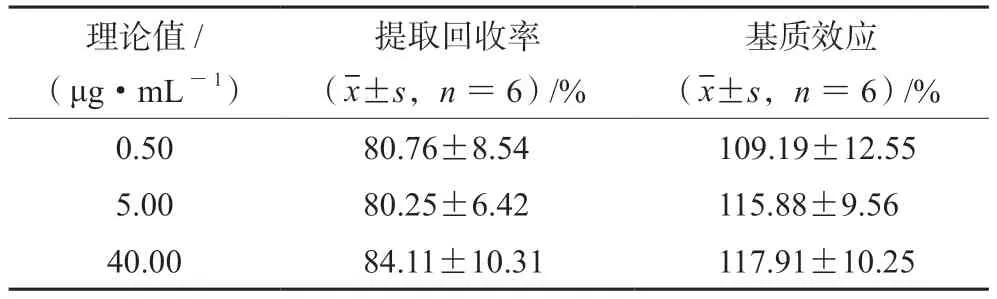
表3 人血浆样本中比阿培南提取回收率和基质效应结果Tab 3 Extraction recovery and matrix effect of biapenem
2.5.5 稳定性考察 取低、中、高3个质量浓度水平(0.50、5.00、40.00 μg·mL-1)的质控样本,分别于室温放置1 h,4℃冰箱放置6 h,-80℃冰箱放置14 d以及经过3次冻融循环后,按“2.4”项下方法处理后进样分析,考察样本在上述4种条件下的稳定性。
另取低、中、高3个质量浓度水平(0.50、5.00、40.00 μg·mL-1)的质控样本,按“2.4”项下方法处理,将处理好的样本于自动进样器(15℃)中放置6 h 后分析,考察处理后样本在自动进样器中的稳定性。
稳定性考察结果见表4,在上述5种不同条件下,低、中、高3个浓度水平的测定值与理论值的平均偏差均在±15%范围内,表明人血浆中比阿培南在本实验条件下稳定。

表4 人血浆样本中比阿培南测定的稳定性结果Tab 4 Stability of biapenem
2.6 临床应用
应用本方法对15例发生感染并使用比阿培南的患者进行血药浓度测定,其中男性11例,女性4例,年龄47~92岁。具体用药方案为比阿培南0.3 g ivgtt q8h或0.3 g ivgtt q6h,连续给药3~4次,于第4次给药前抽取患者静脉血,离心后得到患者血浆,按“2.4”项下方法处理后进样分析得到患者谷浓度,结果见表5,测得比阿培南谷浓度为0.30~11.82 μg·mL-1,可为临床合理化用药提供重要依据。

表5 患者感染灶、用药方案和谷浓度检测结果Tab 5 Infection condition,therapeutic regimen and results of trough concentration determination of patients
3 讨论
在临床实际的抗感染治疗中,使用碳青霉烯类药物的患者病情多较为严重,且联用药物较多。不同品种的碳青霉烯类药物药效学和药动学方面均存在一定差异,不同病理生理状态也会影响其药动学[10]。碳青霉烯类血药谷浓度是否达到目标范围,可用于优化给药方案,提高抗感染治疗的有效性和安全性[10]。比阿培南具有抗菌谱广、抗菌活性强、临床效果好等特点,其对耐药的铜绿假单胞菌及鲍曼不动杆菌有一定优势,且无中枢神经系统毒性,不会诱发癫痫发作[11]。
比阿培南是新一代碳青霉烯类抗菌药物[1],检索现有文献,已报道的比阿培南血药浓度测定方法多为HPLC法[4-9],分析效率低,易受干扰。本研究建立的LC-MS/MS分析方法,相较于已报道的HPLC法[4-9],专属性更强,分析效率得到显著提高,能满足大批量样本分析的要求。本研究考察了C18柱以及HILIC柱,在研究初期尝试使用C18柱对比阿培南进行分离,发现比阿培南在C18柱上保留不佳,与比阿培南极性较大、亲水性较好有关。HILIC 柱采用两性离子修饰的固定相,相较于C18柱,更适用于极性和亲水性化合物的分析[12]。本研究最终使用了HILIC柱对比阿培南和内标(法罗培南)进行了分离和测定,两种物质得到了很好的保留和分离。通过调整流动相比例以及梯度洗脱程序改善峰形,降低了干扰。
比阿培南的国内药品说明书中适应证描述简单,用法用量保守,限制了其临床应用[11]。比阿培南的主要排泄途径为肾脏排泄,患者肾脏功能、血流动力学、液体复苏、CRRT等体外循环支持等因素均会影响比阿培南的血药浓度[10]。重症患者联合用药较多,发生药物相互作用的机会增加,也会对比阿培南的血药浓度产生影响。监测比阿培南的谷浓度可以比较直接地验证是否在目标范围内,实现个体化给药,提高治疗的有效性和安全性[10]。有文献报道,1~5 μg·mL-1为比阿培南的谷浓度目标范围[8]。在本研究中,有4例患者谷浓度低于1 μg·mL-1,将此结果反馈至临床,临床考虑此4例患者抗感染效果不佳,换用亚胺培南西司他丁或美罗培南;1例患者谷浓度高于5 μg·mL-1,将此情况反馈至临床,建议将比阿培南给药剂量调整为0.3 g ivgtt q12 h;10例患者的比阿培南谷浓度在1~5 μg·mL-1,临床治疗有效,病程中患者未出现不良反应。
本研究建立的LC-MS/MS分析方法,专属性强,准确度和重现性好,分析效率高,适用于比阿培南的临床治疗药物监测。