基于建模思想的高中化学工艺流程题解题策略研究
2023-03-18张丽丽
张丽丽
(广东省湛江四中 524000)
“证据推理与模型认知”是《普通高中化学课程标准》(2017版)中化学学科五大核心素养之一,模型认知作为其中一个关键要素被列入核心素养当中.它要求学生通过分析、推理等方法建立认知模型,能够运用模型解释化学现象,揭示现象的本质和规律,并应用到解决化工生产的实际问题当中.
1 化学建模教学
建模是一种科学的思维方法,是一种认识的工具.建模思想是运用模型解决问题的一种思想,就是将复杂的化学问题去掉非本质的东西,抽象出解决问题的思维方式,然后运用这一模型去解决相关问题.建模思想的优点在于把研究对象的一些次要细节及非本质的联系或提取或舍去,从而建立程序化模型有助于判断和推理.化工流程题是高考复习的重难点,在课堂设计中帮助学生建立化学工业流程的解题模型,有助于学生对化学工业流程的各步骤及其作用有更清晰的理解和认识,从而胜任高考中化工流程类题目的考查.
2 化学工艺流程题
2.1 化工流程题的命题分析
试题考查形式主要有物质制备类(如图1所示)和混合物分离提纯类(如图2所示)两大类,其中以物质制备类为主.

图1

图2
命题情境:
(1)生产环保情境:自然资源的综合利用,生产条件的优化,废物回收利用和毒害物质处理.
(2)学术探究情境:最新的生产方法,提取技术的应用等.
命题立意:
(1)以典型无机物、部分过渡元素的性质及其转化为知识载体,以化学实验的基本操作,物质的检验、分离、提纯,实验数据的处理与分析为手段,结合电解质溶液、电化学、热力学、动力学等方面知识,综合考查物质的制备、分离、提纯.
(2)通过理解、辨析基础知识、基本概念、基本理论、基本信息,考查学生的信息提取、整合能力和迁移应用能力.通过对数据、图表、图像等计算、分析,考查学生的思维认知能力.通过实验现象、实验数据、方案设计与评价,考查学生通过实验技能解决生产中的实际问题的能力.
(3)以实际生产中的真实问题为背景,加强对实验探究与创新意识实践基础的考查,培养学生证据推理与模型认知、宏微结合与变化平衡的学科核心思维,渗透绿色、节能、环保等科学精神与社会责任的核心价值立场.
2.2 化工流程题的结构和特点
化工流程题的结构可分为题头、题干和题尾三个部分.题头:主要介绍该工艺生产用到的原材料(包括杂质)、工艺生产的目的、获得的产品、用途等信息,有时根据题头的需要,会提供一系列文字、图表和其他相关注释信息;题干:主要用框图形式将操作或物质转化之间的关系或原料到产品的主要生产工艺流程表示出来;题尾:主要是根据流程中涉及到的化学知识设计成系列问题,构成一道完整的化学试题.
此类试题集综合性、真实性、开放性于一体,包含必要的操作名称、化工术语或文字说明.题型包括选择题和非选择题,选择题主要考查元素化合物知识和工艺流程中的基本操作.非选择题考查知识面广、综合性强、思维容量大.题干的呈现形式多为流程图、表格和图像,设问角度一般为操作措施、物质成分、化学反应、条件控制的原因和产率计算等;能力考查侧重于获取信息的能力、分析问题的能力、语言表达能力和计算能力;涉及的化学知识有基本理论、元素化合物和实验基础知识等.
3 化学工艺流程题解题策略
3.1 题头分析
题头信息一般给出原材料和杂质成分及指定产品,有时还会提及原材料或产品的基本性质.这些基本属性可以在分析流程图后解决问题时使用,在解答问题之前需要先分析原材料、产品的性质和化合价是否发生变化等基本信息,并初步判断原料转化为产品的过程经历了哪些步骤,是否为氧化还原反应,以便于结合后续工艺中添加的物质转化关系和反应条件的控制书写相关反应方程式,并分析滤渣、滤液的成分,推导出除杂顺序、选择分离提纯方法.
3.2 流程图分析
化学工艺流程图主要由原料的预处理、核心化学反应和产品的分离提纯三个部分组成,涉及主产品的制备、副产品的制备和循环过程三条流程线.原料的预处理,包括煅烧、酸溶、碱溶、除杂、过滤等过程;核心化学反应就是生成产品的反应,这个阶段也可能会生成副产品;产品的分离提纯,包括过滤、结晶、蒸馏、萃取分液、醇洗、水洗等过程,通常还要考虑分离条件如调节pH、温度等.三条流程线:从原料到产品的过程称为主线,原料到副产品的过程称为分支线,循环利用的工序组成了回头线.即:“主线一主产品”“分支一副产品”和“回头一为循环”.
3.3 建构化工流程题分析模型
化工流程问题是以元素化合物知识为基础,通过流程图将一个化学工艺生产过程中的主要生产流程表示出来,并根据生产流程中涉及的化学知识设计问题.加强对该类题型结构框架的认识,建构工艺流程题的分析模型,能帮助学生形成化学学科的思维方法,提升学科素养.
工艺流程题的基本框架为:原料→核心化学反应→产品,从元素的角度分析,观察主线中留下哪些元素,除去了哪些元素,通过追踪元素的去向明确各个环节的目的,是除杂还是核心反应?是中间产物还是对于下一步的预处理?若是除杂问题,考虑化学实验过程中的分离、提纯原理和实验操作方法,化工生产的最终目的是为了获得更多更纯净的产品.若是核心反应,考查的一般都是高中化学中常见的几个反应类型,氧化还原反应,复分解反应和电化学反应.其它的问题则从生产条件控制、平衡移动、具体的生产措施、绿色化学、成本控制、工艺步骤、设备腐蚀等这些角度思考,从而找到解题思路.
现以2022年全国甲卷26题为例,分析其结构框架,剖析转化流程,建构化工流程的分析模型.
真题(2022全国甲卷26题)硫酸锌(ZnSO4)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用.硫酸锌可由菱锌矿制备.菱锌矿的主要成分为ZnCO3,杂质为SiO2以及Ca、Mg、Fe、Cu等的化合物.其制备流程如图3所示.

图3
本题中所涉及离子的氢氧化物溶度积常数见表1.

表1
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为____.
(2)为了提高锌的浸取效果,可采取的措施有____、____.
(3)加入物质X调溶液pH=5,最适宜使用的X是____(填标号).
A.NH3·H2O B.Ca(OH)2C.NaOH
滤渣①的主要成分是____、____、____.
(4)向80~90℃的滤液①中分批加入适量KMnO4溶液充分反应后过滤,滤渣②中有MnO2,该步反应的离子方程式为____.
(5)滤液②中加入锌粉的目的是____.
(6)滤渣④与浓H2SO4反应可以释放HF并循环利用,同时得到的副产物是____、____.
解题分析基本框架分析如图4所示:

图4

结合流程图逐一分析:

问题(2)浸取的目的是将矿物中的元素转移进溶液,提高浸取效率可理解为加快化学反应速率,可采用增大压强、将焙烧后的产物碾碎,增大接触面积、增大硫酸的浓度等方式提高锌的浸取率;实际考查的是影响化学反应速率的因素,体现了学生思辨能力的运用.
问题(3)用物质X调节pH的目的是除去溶液中某些杂质离子,X的选择要考虑无污染、低成本、不引入新杂质,NH3·H2O易分解产生NH3污染空气,且成本较高,故A不合适;Ca(OH)2不会引入新的杂质,且成本较低,故B合适;NaOH会引入杂质Na+,且成本较高,C不合适;当沉淀完全时即离子浓度小于10-5mol/L,结合表格Ksp计算各离子完全沉淀时pH<5的只有Fe3+,故滤渣①中有Fe(OH)3,又CaSO4是微溶物,SiO2不溶于酸,故滤渣①的主要成分是Fe(OH)3、CaSO4、SiO2;透过题目分析出背后的考点为pH控制与试剂选择,滤渣成分分析,考查酸碱中和、除杂、沉淀溶解平衡相关知识.判断滤渣成分涉及沉淀溶解平衡相关计算,难度和综合性较强,突出了信息迁移能力和计算能力的考查.
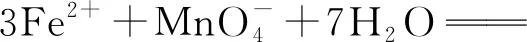

问题(6)滤渣④为CaF2、MgF2,与浓硫酸反应可得到HF,同时得到的副产物为CaSO4、MgSO4.考查知识点为实验室制备氢卤酸原理,利用高沸点酸制低沸点酸,侧重知识迁移运用能力.
试题背景:以菱锌矿制备硫酸锌的工艺为情景素材,通过对菱锌矿焙烧、酸浸预处理,考查化学方程式书写及原料预处理的措施,再通过核心反应条件控制,逐步分离除去杂质,考查步骤中试剂的选择、成分的推断,提供有关金属离子难溶电解质的溶度积,要求学生基于数据综合分析整个工艺流程,引导学生思考不同物质的分离条件,考查学生综合运用化学知识解决实际问题的能力.
