高活性低温甲烷化Ni基催化剂的制备及表征
2023-03-15刘先知孙利民孙锦昌张谦温
刘先知,贺 友,王 斌,孙利民,孙锦昌,张谦温
(1.北京石油化工学院 新材料与化工学院 燃料清洁化及高效催化减排技术北京市重点实验室,北京 102617;2.中国石油 石油化工研究院,甘肃 兰州 730060)
甲烷化反应指CO或CO2加氢生产甲烷的反应,1902年科学家发现了镍催化CO和氢气反应生成甲烷[1],而后CO甲烷化反应得到了广泛的应用[2-4]。工业上甲烷化反应的应用主要有两类:高温甲烷化和低温甲烷化。高温甲烷化主要用于煤制天然气[5-6],要求催化剂在高温下(550 ℃以上)具有良好的稳定性。低温甲烷化主要用于合成氨、燃料电池、炼油与化工等过程中的氢气净化[7-8]。将CO与CO2气体加氢生成惰性的甲烷是最常用和最有效的氢气净化方法。工业上特别是乙烯装置,含有CO的富氢馏分(粗氢)是经过低温分离产生的,需要加热到甲烷化反应需要的温度以脱除CO与CO2,而在CO与CO2加氢生成甲烷的同时会产生水,又需要在较低的温度下将水吸附脱出,因此低温甲烷化反应具有能耗低和操作成本低的优点,在石油化工领域得到了越来越多的应用[9]。
本工作在前期研究[10]的基础上,改变催化剂的制备方法,引入电子型和结构型助剂进一步提高催化剂的甲烷化活性,得到催化活性更高和稳定性好的低温甲烷化催化剂,考察了催化剂的结构及性能。
1 实验部分
1.1 主要试剂
硝酸镍、硝酸镁、硝酸锰、硝酸铝、无水碳酸钠:分析纯,国药集团化学试剂有限公司;硝酸镧:分析纯,北京新华化学试剂厂。
1.2 催化剂的制备
1.2.1 浸渍法
采用多次浸渍(等体积)法制备低镍含量的负载型催化剂。将水溶性的镍及其金属盐溶解在去离子水中,经过干燥的载体Al2O3在室温下浸渍在金属盐水溶液中2 h,然后在烘箱中120 ℃下干燥4 h,最后在马弗炉中480 ℃下焙烧4 h,重复上述操作,制得预定的Ni含量的氧化态催化剂。
1.2.2 共沉淀法
采用共沉淀法制备高含量的镍基甲烷化催化剂。镍的前体为可溶性盐硝酸镍、氧化铝的前体为可溶性盐硝酸铝、氧化硅的前体为硅藻土。将硝酸镍和助剂金属的可溶性盐置于去离子水中溶解,配制成Ni浓度为0.5~2.0 mol/L的待沉淀液;采用碳酸钠(1~3 mol/L)为沉淀剂,控制溶液pH=9~11,沉淀结束后将沉淀浆液在50~90 ℃下老化1~3 h;老化后将浆液进行多次抽滤洗涤,除去Na+;将滤饼取出放置在干燥箱中80~150℃下干燥,然后放入马弗炉中400 ℃下焙烧 4 h,制得氧化态的催化剂。
1.3 表征方法
采用美国Micromeritics公司ASAP-2020型氮气吸附仪测定催化剂的比表面积、孔体积和孔径。采用Quantachrome公司Chembet-3000型化学吸附仪对催化剂的性能进行研究,具体方法:将40~60目的催化剂(约0.1 g)在氩气气氛下(流量为30 mL/min)以20 ℃/min的升温速率升至300 ℃,恒温保持30 min;然后将温度降至室温(25~30 ℃)后,切入还原气(5%(x)H2的氩气,流量为30 mL/min),待检测器稳定后进行程序升温,记录温度和TCD的信号值。采用美国Micromeritics公司ASAP-2020M+C型全自动物化吸附分析仪进行氢气吸附分析,分析条件:将0.6 g催化剂(20~40目)在450 ℃下还原2 h,于真空条件下降温至35 ℃进行氢气吸附分析。采用日本岛津公司XRD-7000型X射线衍射仪进行XRD表征,分析条件:CuKα射线,管电压40 kV,管电流30 mA,扫描速率4(°)/min,步长0.02°,扫描范围10°~80°。
1.4 催化剂的性能评价
采用天津大学北洋化工实验设备公司的固定床微型反应装置对甲烷化催化剂的性能进行评价。装置采用不锈钢管式反应器,由压力、流量及温度控制和在线分析等单元组成,出口尾气经冷凝器后进入在线色谱分析。反应器采用内径8 mm的316不锈钢管,催化剂装填量 1 mL(20~40目),在催化剂的上部和下部装入高度3~5 cm的惰性材料支撑催化剂。
氧化态的Ni基催化剂反应前需要在线还原。催化剂还原过程采用程序升温法,升温速率2 ℃/min,还原气体为5%(φ)H2和95%(φ)N2的混合气,在400 ℃下恒温4 h,还原气体流量为100 mL/min。经还原的催化剂在温度降至100 ℃以下时切换为原料气。原料气由钢瓶经减压阀、稳压阀及流量计进入反应器中,反应压力由背压阀调节控制,出口气经过冷凝器冷凝后进入气相色谱仪自动采集分析,催化剂经1 h反应达到性能稳定后再进行采样分析。
实验所用原料气为含有CO,CO2,H2的混合气,其中,CO含量为5 000×10-6(x),CO2含量为100×10-6(x),其他为氢气。原料气经反应后,出口尾气中含有极少量的CO和CO2。CO的出口含量是评价催化剂性能的主要指标,因此所使用的气相色谱仪需要对CO与CO2气体具有较高的分析灵敏度(检测最低限0.1×10-6),分析方法参照文献[10]。
2 结果与讨论
2.1 Ni含量对催化剂性能的影响
2.1.1 浸渍法制备低Ni含量催化剂
Ni基催化剂中金属分散度的定义为催化剂表面上具有活性的Ni原子数和催化剂中Ni原子总数的比值[11]。金属分散度体现活性组分在载体表面上的分散情况,表1为低Ni含量催化剂的H2化学吸附表征结果。从表1可看出,浸渍法制备的催化剂的金属分散度均小于1.0%,分散度在Ni含量为30%(w)时最大,继续增加活性组分Ni的含量,金属分散度会下降。这表明过多的活性组分Ni不能很好地在载体表面分布。随活性组分Ni含量的增加,Ni的晶粒尺寸也会增加,说明活性组分Ni在催化剂表面发生了聚集,因此Ni含量增加,金属分散度下降。

表1 低Ni含量催化剂的H2化学吸附表征结果Table 1 H2 chemisorption characterization results of catalysts with low Ni content
图1是低Ni含量催化剂的CO出口含量随温度的变化曲线。从图1可看出,随温度上升,CO的出口含量逐渐下降。在相同温度下,甲烷化催化活性会随活性组分Ni含量的增加而逐渐增加,当活性组分Ni负载量为50%(w)时,在反应温度180 ℃的条件下,CO的出口含量小于0.1×10-6(x),CO的转化率达100%。

图1 低Ni含量催化剂的CO出口含量与反应温度的关系曲线Fig.1 Relation curve between outlet CO content of catalysts with low Ni content and reaction temperature.Reaction conditions:2.0 MPa,GHSV=5 000 h-1.
2.1.2 共沉淀法制备高Ni含量催化剂
表2是高Ni含量催化剂的CO出口含量随气时空速的变化关系。从表2可看出,在10 000 h-1气时空速下,Ni含量为50%(w)催化剂的CO出口含量为181×10-6(x),CO的转化率为96.5%,出口CO的含量无法达到工业应用要求。Ni含量为60%(w)催化剂的CO出口含量为0,CO的转化率为100%,可以实现CO完全甲烷化。继续增加活性组分Ni含量,CO出口含量均为0。
图2是高Ni含量催化剂的CO2出口含量随气时空速的变化曲线。从图2可看出,随气时空速的增加,CO2的出口含量增加,这表明催化剂的CO2转化率呈下降的趋势。Ni含量70%(w)的催化剂的CO2甲烷化活性最高,在气时空速10 000 h-1下,CO2出口含量为30×10-6(x),转化率达70%。Ni含量75%(w)的催化剂的CO2出口含量为45×10-6(x),转化率下降到55%。这表明过多的活性组分Ni会降低催化剂的CO2甲烷化催化活性。

图2 高Ni含量催化剂的CO2出口含量与反应气时空速的关系曲线Fig.2 Relation curve between outlet CO2 content of catalyst with high Ni content and GHSV.Reaction conditions:2.0 MPa,160 ℃.
表3为高Ni含量催化剂的织构性质。从表3可看出,随Ni含量的增加,催化剂的比表面积和孔体积下降,平均孔径增加,这说明随活性组分Ni含量的增加,Ni晶粒会在载体表面聚集长大,形成更多NiO与Ni2O3晶体,堵塞催化剂孔道[12],减小催化剂的比表面积与孔体积。Ni含量大于70%(w)时,催化剂的比表面积、孔体积以及孔径的变化不明显。

表3 高Ni含量催化剂的织构性质Table 3 Textural properties of catalysts with high Ni content
表4为高Ni含量催化剂的H2化学吸附表征结果。从表4可看出,随Ni含量的增加,催化剂的金属分散度增加,但活性组分Ni含量大于70%(w)后,金属分散度开始下降,但总体变化较小。这说明当活性组分Ni含量过多时,活性组分开始聚集,使催化剂的比表面积下降,Ni的晶粒尺寸增加,表明过多的活性组分Ni会导致活性组分聚集,形成较大晶粒,降低催化剂比表面积,从而降低催化剂的催化活性。
对比表1和表4可知,不同方法制备的Ni含量为50%(w)的催化剂的金属分散度和晶粒大小有显著区别。共沉淀法制备的催化剂金属分散度高、晶粒小,因此活性高,说明在制备Ni负载量较高的催化剂时应采用共沉淀法。

表4 高Ni含量催化剂的H2化学吸附表征结果Table 4 H2 chemisorption characterization results of catalysts with high Ni content
2.2 氧化铝含量对催化剂性能的影响
表5是不同氧化铝含量催化剂的CO出口含量随反应气时空速的变化关系。从表5可知,在气时空速10 000 h-1下,不含氧化铝的催化剂CO出口含量为1 927×10-6(x)。加入结构助剂氧化铝之后,催化剂的CO加氢活性提升,可以实现CO完全甲烷化。

表5 不同气时空速下CO气体的出口含量Table 5 Outlet CO content at different GHSV
图3是不同氧化铝含量Ni基催化剂的CO2出口含量随气时空速的变化曲线。从图3可发现,氧化铝含量对催化剂的CO2甲烷化催化活性影响较大,增加催化剂中氧化铝的含量,CO2的出口含量下降、转化率升高。氧化铝含量达到10%(w)时,催化剂具有最高的CO2转化率。继续添加氧化铝,反应出口CO2的含量升高。

图3 不同Al含量Ni基催化剂的CO2出口含量与气时空速的关系Fig.3 Relationship between outlet CO2 content of Ni-based catalysts with different Al contents and GHSV.Reaction conditions referred to Table 5.
综上可知,助剂氧化铝对催化剂的CO和CO2甲烷化催化活性影响不同:对催化剂的CO2甲烷化活性提高明显,对催化剂的CO甲烷化性能影响不明显。推测加入结构型助催化剂氧化铝,可以产生更多的孔道结构,增加了催化剂的比表面积,可提供更多的活性位点。
图4为不同Al含量Ni基催化剂还原前的XRD谱图。从图4可看出,2θ=36.2°,42.2°,63.9°,74.2°处的峰为NiO的衍射峰,2θ=14.6°,22.7°处的峰为SiO2的衍射峰,2θ=42.2°处的峰为Al2O3的衍射峰。随着氧化铝含量的增加,NiO衍射峰的弥散度增加,说明添加结构助剂氧化铝可以增加活性组分NiO的分散度,从而提高催化剂的催化活性。
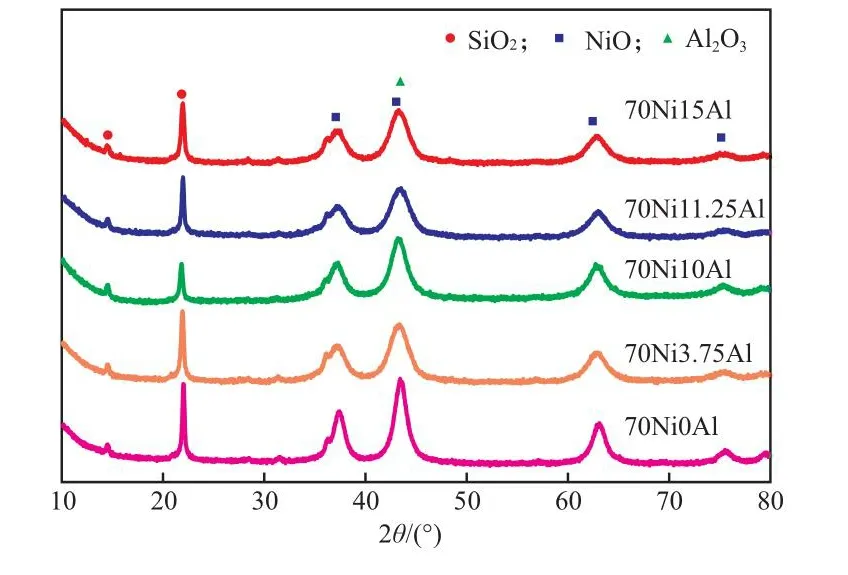
图4 不同氧化铝含量Ni基催化剂还原前的XRD谱图Fig.4 XRD patterns of Ni-based catalysts with different Al content before reduction.
表6为不同氧化铝含量催化剂的织构性质。从表6可看出,氧化铝含量增加,催化剂的比表面积呈先增加后下降的趋势。催化剂比表面积越大,活性位点越多,催化剂的活性提高;少量添加结构助剂氧化铝,会减小催化剂的平均孔径,增加催化剂的比表面积。该表征结果与XRD表征结果一致。结构助剂氧化铝通过改变催化剂的孔结构和比表面积对催化剂的加氢活性产生影响;但氧化铝含量对催化剂孔体积的影响不明显。

表6 不同氧化铝含量催化剂的织构性质Table 6 Textural properties of catalysts with different Al2O3 content
表7为不同氧化铝含量Ni基催化剂的H2化学吸附表征结果。由表7可知,适量增加氧化铝含量可以增加催化剂的金属分散度,促进Ni金属晶粒在载体上的分布、增加活性金属的比表面积,提供更多的活性位点。但氧化铝含量过多会降低催化剂的金属分散度与金属比表面积,降低催化剂的活性。

表7 不同氧化铝含量催化剂的H2化学吸附表征结果Table 7 H2 chemisorption characterization results of catalysts with different Al2O3 content
2.3 助催化剂对催化剂性能的影响
表8为添加不同助剂的Ni基催化剂的CO出口含量随气时空速的变化。由表8可知,添加不同种类助剂对催化剂的CO甲烷化催化活性影响较大。添加助剂La,Mn,Mg不会影响催化剂的CO甲烷化催化活性,而添加Cu助剂会降低催化剂的CO甲烷化催化活性,CO出口含量大于100×10-6(x),不满足工业应用的要求。

表8 不同气时空速下CO的出口含量Table 8 Outlet CO content at different GHSV
图5为添加不同助剂的Ni基催化剂的CO2出口含量随气时空速的变化曲线。从图5可看出,添加不同助剂对催化剂的CO2甲烷化催化性能有较大影响。添加La助剂与Mn助剂可以增强催化剂的CO2甲烷化催化活性。添加Cu助剂与Mg助剂会降低催化剂CO2甲烷化催化活性。

图5 添加不同种类的助剂Ni基催化剂的CO2出口含量Fig.5 Outlet CO2 content of Ni-based catalysts with different additive.Reaction conditions referred to Table 5.
综上可知,添加La助剂与Mn助剂,可以在不影响CO甲烷化催化活性的同时,提高催化剂的CO2甲烷化催化活性。这可能是因为添加La助剂与Mn助剂会影响活性组分Ni与载体之间的结合力,使活性组分Ni更容易被还原,提高了催化剂的催化活性。而添加Cu助剂与Mg助剂可能会使催化剂更容易烧结积碳,导致催化剂的催化活性大幅下降。
图6为添加不同种类助剂的Ni基催化剂的H2-TPR谱图。从图6可看出,催化剂的出峰位置均在380 ℃到630 ℃之间。在高温区域未出现还原峰,说明活性组分与载体之间的相互作用力适中,活性组分比较容易还原。添加助剂La,Mn,Cu使催化剂的还原峰向低温区偏移,说明添加助剂La,Mn,Cu可以降低活性组分Ni与载体之间的相互作用力,使活性组分Ni更容易被还原,其中,助剂La和Mn的偏移较为明显。因此添加助剂La和Mn的催化剂具有较高的CO与CO2甲烷化催化活性。

图6 添加不同种类助剂的Ni基催化剂的H2-TPR谱图Fig.6 H2-TPR profiles of Ni-based catalysts with different additive.
2.4 La改性Ni基催化剂的性能
图7为CO和CO2甲烷化转化率随反应时间的变化曲线。

图7 气体转化率和反应时间的关系Fig.7 Relationship between gas conversion and reaction time.Reaction conditions:2.0 MPa,160 ℃,10 000 h-1.
从图7可看出,CO转化率不会随着反应时间的延长发生变化,一直保持在100%。而CO2的转化率会随着反应时间的延长发生微弱的下降,但CO2转化率均高于97.5%,CO2的出口含量小于5.0×10-6(x)。La改性Ni基催化剂具有较好的催化稳定性。
3 结论
1)采用共沉淀法制备的Ni基催化剂加氢活性高于浸渍法制备的Ni基催化剂,且随着Ni含量的增加,催化剂的活性增加。
2)添加结构助剂氧化铝可以增加催化剂的比表面积、金属分散度。催化剂中含有10%(w)的氧化铝时具有最高的比表面积,可以提供更多的活性位点,具有最佳的甲烷化催化效果。
3)催化剂中加入Mn与La助剂可以降低Ni与载体之间的结合力,降低催化剂的还原温度,抑制NiAl2O4尖晶石的形成,提高CO和CO2加氢活性。
4)通过共沉淀法制备的La改性的氧化铝和氧化硅复合氧化物负载的Ni基催化剂具有较好的催化效果,在160 ℃、2.0 MPa、气时空速10 000 h-1下,CO完全转化、CO2出口含量小于1×10-6(x)。
