NaCl-MgCl2复合除冰盐对混凝土盐冻破坏的影响及其作用机理
2023-03-12汪林萍杨全兵
汪林萍,杨全兵,2,*
(1.同济大学 材料科学与工程学院,上海 201804;2.同济大学 先进土木工程材料教育部重点实验室,上海 201804)
含氯除冰盐(NaCl或CaCl2)因除冰融雪效率高、成本低等优点,目前仍是使用最多的一类除冰盐.然而,由于它会引起混凝土表面起皮、剥落等,还会导致钢筋锈蚀,其所造成的破坏程度远大于普通的冻融破坏[1-3].
盐冻破坏机理是进行混凝土抗盐冻性设计的理论依据,其中静水压理论[4]和渗透压理论[5]是解释混凝土盐冻破坏的经典理论.此外,Fagerlund[6]提出的临界饱水度理论,首次揭示了只有当混凝土的饱水度超过其临界值后,混凝土才会发生冻融破坏.杨全兵[7-8]提出的冻融饱水度-结冰压理论,认为混凝土饱水度的增长速率是决定盐冻破坏程度的最关键参数,增长速率越快,结冰破坏力越大.
防治混凝土盐冻破坏的研究大部分集中在提高混凝土的抗盐冻性[9-12]和表面保护技术[13-14],只有少量研究涉及改善除冰盐配方[15-16].Opara 等[15]研究表明,优化的NaCl 复合除冰盐引起的路面破坏面积降低约30%.吴鹏程等[16]研究发现,在NaCl 中掺入黄原胶能有效降低混凝土的盐冻破坏,但黄原胶浓度高时将在路面形成乳白色黏液,影响路面的使用性能.因此,研究以NaCl 为主,既不影响除冰融雪效率,又不引起混凝土盐冻破坏的复合除冰盐,具有重要的实用意义和科学价值.
MgCl2除冰盐的冰点比NaCl 除冰盐的冰点低,其造成的盐冻破坏程度较小,因此,近几年MgCl2除冰盐的使用量在逐步增加[17-18],但尚未有研究能合理解释其造成混凝土盐冻破坏小于NaCl 除冰盐的原因.基于此,本文着重研究了NaCl-MgCl2复合除冰盐对混凝土盐冻破坏的影响及其作用机理.
1 试验
1.1 原材料
水泥为海螺牌P·Ⅱ 52.5 硅酸盐水泥;细骨料为细度模数2.2 的石英砂;粗骨料为3~10 mm 的水磨石;NaCl 除冰盐(N)和MgCl2除冰盐(M)分别来源于中盐金坛盐化有限责任公司和国药集团化学试剂有限公司,纯度(质量分数)分别为99.9%和99.0%;水为自来水.
1.2 试件及盐溶液制备
1.2.1 试件制备
采用非引气混凝土,其配合比(质量比)为m(水泥)∶m(水)∶m(砂)∶m(石子)=1.00∶0.50∶1.25∶2.50.制备尺寸为40 mm×40 mm×160 mm 的混凝土试件,成型好的混凝土试件在(20±2)℃,相对湿度为(60±5)%的环境中自然养护1 d 后脱模,放入标准养护室((20±2)℃,相对湿度≥95%)的水中养护至28 d 备用.
1.2.2 盐溶液制备
复合除冰盐由NaCl与MgCl2按一定的质量比配制而成,NxMy表示复合除冰盐,其中下标x、y分别表示复合除冰盐中NaCl 和MgCl2的质量比.aN、aM 和aNxMy分别表示质量分数为a%的NaCl除冰盐溶液、MgCl2除冰盐溶液和复合除冰盐溶液.配制盐溶液时,根据盐溶液的质量分数(a%)称取所需质量的溶质(各类盐)和溶剂(水),复合除冰盐则根据NaCl 和MgCl2的质量比称取,然后将其倒入烧杯中进行溶解.将配制好的盐溶液转移至容量瓶中,贴好标签备用.所配制的盐溶液的质量分数为2.4%、4.0%、10.0%、15.0%和20.0%.
1.3 试验方法
1.3.1 混凝土的盐冻破坏
用于测定混凝土盐冻破坏的试件为湿试件和含盐自然干试件.在标准养护室的水中养护28 d的混凝土试件为湿试件.湿试件在100 ℃的烘箱中烘干24 h后冷却至室温的混凝土试件为干试件,将室温下浸泡在盐溶液中7 d 的干试件在0.1 MPa 的真空度下抽真空1 d,然后在大气中静置1 d得到饱盐试件,再将饱盐试件放置在(22±2)℃,相对湿度为(70±5)%的室内养护7 d后得到的混凝土试件为含盐自然干试件.
采用单面浸入盐溶液法进行混凝土的盐冻破坏试验,其试验装置示意图与冻融循环温度如图1 所示,其中盐溶液的质量分数与制备含盐自然干试件所用盐溶液的质量分数相同.按式(1)计算混凝土盐冻破坏后的剥落量.

图1 盐冻破坏试验Fig.1 Salt-frost scaling test
式中:Kn为冻融循环次数为n时的剥落量,kg/m2;Mn为冻融循环次数为n时的剥落物质量,kg;A为试块与溶液的接触面积,0.006 4 m2.
经过30次冻融循环后,当K30≥1.0 kg/m2时,即可判定混凝土的抗盐冻性不合格;K30越小,混凝土的抗盐冻性越高[2].
1.3.2 盐溶液的结冰压
盐溶液结冰压的测试参照文献[15].将盐溶液置于无伸缩变化的钢筒内,其体积占钢筒体积的比例为盐溶液的饱水度(S),改变盐溶液在钢筒内的体积,可测试不同饱水度时的盐溶液结冰压,并按式(2)进行计算.
式中:Pt为t时刻盐溶液的结冰压,MPa;Ft为t时刻盐溶液的结冰膨胀力,N;F0为预加约束荷载,2 000 N;r为钢筒内径,3.1 mm.
当盐溶液刚开始产生结冰压时,其饱水度为临界饱水度.当盐溶液完全结冰时,其结冰压将不再发生明显变化,称之为平衡结冰压(Pe).
1.3.3 盐和盐溶液的吸湿性
将纯净水放入干燥器底部,其水面不超过隔板;将装有固体NaCl、MgCl2及其质量分数分别为4.0%、10.0%、20.0%盐溶液的表面皿放置于隔板上;用凡士林涂抹干燥器口并加盖以密封;放置到预定时间时,测定表面皿中盐和盐溶液的质量变化,按式(3)计算其吸水率,用以表示盐和盐溶液的吸湿性.
式中:Qt为t时刻盐的吸水率,%;M0为盐和盐溶液的初始质量,g;Mt为t时刻盐和盐溶液吸水后的质量,g.
1.3.4 混凝土的饱水度
混凝土内部存在可冻水是导致其产生冻融破坏的根本原因,因此饱水度是分析混凝土盐冻破坏机理的重要参数之一.本文分别测试混凝土的毛细管吸水饱水度、常温饱水度和冻融饱水度.
用于测定不同除冰盐对混凝土饱水度影响的试件为湿试件(见1.3.1)、干试件(见1.3.1)、含盐干试件(将饱盐试件在100 ℃的烘箱中烘干24 h 后得到的混凝土试件)和含盐自然干试件(见1.3.1).
采用单面毛细管吸水法[11]测试含盐干试件的毛细管吸水饱水度,按式(4)进行计算,以评价盐的种类对混凝土毛细管吸水饱水度的影响.
式中:St为吸水t时刻试件的毛细管吸水饱水度,%;M∞为饱盐试件的质量,g;M0为含盐干试件的质量,g;Mt为吸水t时刻试件的质量,g.
当试件的单面毛细管吸水饱水度随时间增长不发生变化时,称之为平衡毛细管吸水饱水度(Se,cp).
将湿试件、干试件和含盐自然干试件分别浸没在(22±2)℃的盐溶液中一定时间后,通过测定试件的质量变化,按式(5)计算试件的常温饱水度.
式中:S't为吸水t时刻试件的常温饱水度,%;M'0为试件的初始质量,g.
将湿试件和干试件分别浸泡于盐溶液中,并放入冰柜中进行30 次冻(f)融(t)循环,每次冻融循环制度为在-(20±2)℃下冻12 h,然后在(20±2)℃下融化12 h.在试件融化约1 h,内部还是冻结状态时刮去表面碎冰,测定其在冻结阶段的质量;试件在室温下融化满12 h 后,测定其在融化阶段的质量,按式(6)分别计算混凝土在冻结阶段的饱水度和融化阶段的饱水度.
式中:Sc为冻融饱水度,%;Mc为某一次冻融循环后试件在冻结阶段或融化阶段的质量,g.
2 结果与讨论
2.1 混凝土的盐冻破坏
图2 为冻融循环次数及复合除冰盐中MgCl2含量对混凝土湿试件盐冻剥落量的影响,其中2.4N、4.0N和4.0M 为盐溶液参比样.由图2(a)可见:无论在何种盐溶液中,试件的盐冻剥落量都随着冻融循环次数的增加而增大;在相同冻融循环次数下,试件的盐冻剥落量随着NaCl 盐溶液质量分数的增加而降低,在相同质量分数的MgCl2盐溶液中比在NaCl 盐溶液中降低幅度更大,在复合除冰盐溶液中的盐冻剥落量介于在相同质量分数的NaCl 盐溶液和MgCl2盐溶液之间.由图2(b)可见:在相同冻融循环次数下,试件的盐冻剥落量随着除冰盐中MgCl2含量的增加而显著降低,表明MgCl2的掺加有利于降低NaCl 对混凝土的盐冻破坏;当除冰盐中MgCl2含量不低于40.0%时,混凝土经过30 次冻融循环后的盐冻剥落量均低于1.0 kg/m2,即其抗盐冻指标从原来的严重不合格变为合格;与相同质量分数的4.0N 溶液相比,当除冰盐中MgCl2含量为20.0%、40.0%和100%时,其K30分别降低约35.7%、66.4%和88.2%.
在实际工程中,除冰盐不可避免会进入到混凝土中,因此采用含盐自然干试件研究进入到混凝土内部的除冰盐对混凝土盐冻破坏的影响.图3 为不同浸泡条件对含盐自然干试件盐冻剥落量的影响,其中4.0N 溶液中的湿试件为参比样.由图3 可见:不论含盐自然干试件表面接触水还是盐溶液,相同冻融循环次数下,随着除冰盐中MgCl2含量的增加,其盐冻剥落量均显著降低,与图2 中湿试件的试验结果一致;尽管除冰盐中掺入MgCl2可显著延缓混凝土的盐冻剥蚀破坏,但当冻融循环次数超过一定值后,混凝土的盐冻剥落量也会迅速增大直至混凝土完全溃散,其中含4.0N、4.0N5M5和4.0M 的含盐自然干试件在水中的盐冻剥落量迅速开始增加的冻融循环次数分别为15~20、20~30、55~60 次,在盐溶液中则分别为0~5、10~15、15~20 次;在冻融循环过程中,含盐自然干试件表面接触水时,仍会产生盐冻剥蚀破坏,且其盐冻剥落量均明显小于参比样,但湿试件在同样条件下不会产生剥蚀破坏,当含盐自然干试件表面接触盐溶液时,其盐冻剥落量均显著大于参比样,表明混凝土内部含盐将加剧其盐冻剥蚀破坏;在冻融循环过程中,表面接触水的含盐自然干试件的盐冻剥落量明显小于表面接触盐溶液的含盐自然干试件,且表面接触盐溶液比内部含盐对混凝土盐冻剥蚀破坏的作用更大,例如,与参比样相比,含4.0N、4.0N5M5和4.0M的含盐自然干试件在水中的K15分别降低约93.8%、100.0%和100.0%,其在4.0N、4.0N5M5和4.0M 盐溶液的K5分别增加约1 104.3%、118.5%和34.1%.

图2 冻融循环次数及复合除冰盐中MgCl2含量对湿试件盐冻剥落量的影响Fig.2 Effect of number of freezing-thawing cycles and content of MgCl2 in the compounded deicing salt on the salt-frost scaling of wet specimens

图3 不同浸泡条件对含盐自然干试件盐冻剥落量的影响Fig.3 Effect of various immersing conditions on the salt-frost scaling of naturally dried specimens containing salts
2.2 盐溶液的结冰压
在100%饱水度下,复合除冰盐中MgCl2含量对盐溶液结冰压的影响如图4所示,其中4.0N和4.0M 为盐溶液参比样.由图4可见:使用复合除冰盐后,盐溶液的结冰过程或结冰曲线并没有发生明显改变,其平衡结冰压仅有小幅降低,表明在100%饱水度下,复合除盐中MgCl2的掺入对盐溶液结冰压的影响较小,与2.1中复合除冰盐改善盐冻剥蚀的情况并不一致,因而还有其它更重要的参数影响混凝土的盐冻剥蚀过程.

图4 复合除冰盐中MgCl2含量对盐溶液结冰压的影响Fig.4 Effect of MgCl2 content in the compounded deicing salt on the ice-formation pressure of salt solutions
图5 为盐溶液的平衡结冰压与饱水度的关系,水(H2O)为参比样.由图5可见:水和盐溶液均存在临界饱水度,只有当饱水度超过临界饱水度时,盐溶液结冰才能产生膨胀压力,且盐溶液的平衡结冰压随饱水度增大迅速增加;盐溶液的临界饱水度均大于水的临界饱水度,且随着除冰盐中MgCl2含量的增大而提高,H2O、4.0N、4.0N5M5和4.0M 的临界饱水度分别约为91.0%、92.5%、93.4%和94.8%;在相同饱水度下,4.0N 产生的平衡结冰压明显高于4.0M;在相同平衡结冰压下,除冰盐中MgCl2含量越大,其盐溶液的饱水度更高,对混凝土产生的盐冻破坏越小.

图5 盐溶液的平衡结冰压与饱水度的关系Fig.5 Relationship between ice-formation pressure and saturation degree of salt solutions
2.3 盐和盐溶液的吸湿性
盐和盐溶液在潮湿空气中的吸水率如图6 所示,其中盐为固体粉状.由图6 可见:固体粉状MgCl2在潮湿空气中放置240 h 时的吸水率为148.8%,远高于固体粉状NaCl 在相同条件下的吸水率(40.5%);当盐溶液的质量分数不高于20.0%时,相同质量分数NaCl 溶液的吸水率均大于MgCl2溶液,这是因为固体粉状MgCl2在潮湿空气中,吸水后先转化为含6个结晶水的MgCl2·6H2O,直至吸水率超过一定值后才全部溶解形成溶液,而粉状固体NaCl 在潮湿空气中可以直接溶解形成溶液.
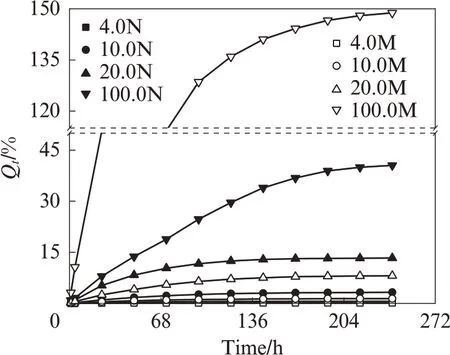
图6 盐和盐溶液在潮湿空气中的吸水率Fig.6 Water absorption ratios of salts and salt solutions in humid air
2.4 饱水度
2.4.1 含盐干试件的毛细管吸水饱水度
含盐干试件的毛细管吸水饱水度如图7 所示,其中不含盐的干试件为参比样.由图7 可见:无论试件含何种盐,其毛细管吸水速率的增长速度均明显比不含盐试件更快,其Se,cp更高;随着含盐试件中MgCl2含量的增大,其Se,cp更高,达到Se,cp所需时间也更短.这主要是因为毛细管吸水饱水度试验采用含盐干试件,试件内部毛细管内含有的固体MgCl2的吸水速率和吸水率均明显大于固体NaCl.

图7 含盐干试件的毛细管吸水饱水度Fig.7 Degrees of saturation of capillary water absorption of dry specimens with salts
2.4.2 湿试件的常温饱水度和冻融饱水度
浸泡在盐溶液中湿试件的常温饱水度和冻融饱水度如图8 所示,水(H2O)为参比样.
由图8(a)可见:在常温条件下,湿试件饱水度由大到小依次为4.0M>4.0N5M5>4.0N;浸入盐溶液的初始阶段,各试件的饱水度均降低,出现失水现象,表明其内部水分向盐溶液迁移,随着盐溶液中MgCl2含量的增大,试件失水持续时间缩短,饱水度降低程度减小;浸入盐溶液200~300 h 之后,各试件的饱水度逐渐增大,直至达到平衡,表明盐溶液向试件内部迁移的质量超过试件的失水量.
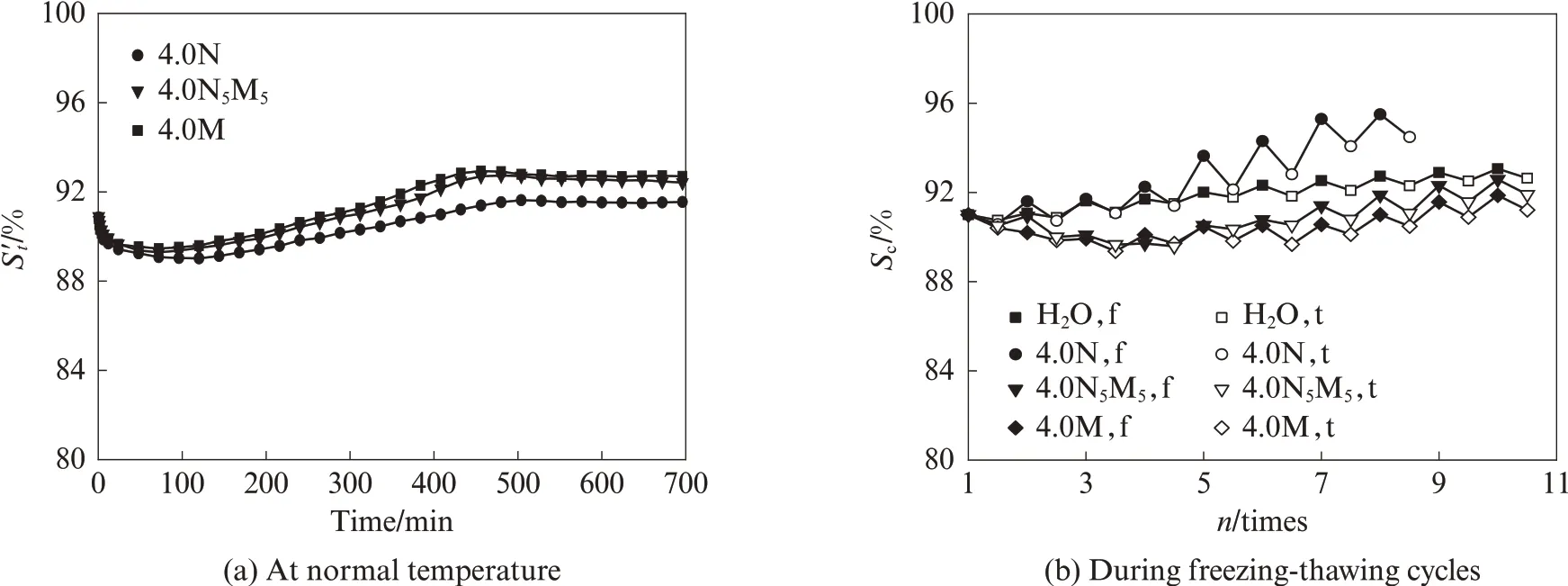
图8 浸泡在盐溶液中湿试件的常温饱水度和冻融饱水度Fig.8 Saturation degree of wet specimens immersed in salt solutions at normal temperature and during freezing-thawing cycles
由图8(b)可见:在冻融循环条件下,浸泡在4.0N盐溶液中的湿试件,其饱水度从2次冻融循环后就开始超过冻融循环前的饱水度和浸泡在水中的饱水度,且随着冻融循环次数的增加,其饱水度增长幅度变大;浸泡在4.0N5M5和4.0M 溶液中的湿试件,在冻融循环次数增加到4次前,其饱水度随着冻融循环次数的增加而降低,随后逐渐增加,8次冻融循环后,其饱水度超过冻融循环前的值,但直到10次冻融循环后,其饱水度仍小于浸泡在水中的饱水度;无论浸泡在何种盐溶液中,试件在冻结阶段的饱水度均明显高于融化阶段的饱水度,表明在冻融循环条件下,试件饱水度的增加主要归因于冻结阶段,而非融化阶段;在4.0N溶液中冻融循环5次以后,试件表面出现较明显的剥蚀破坏,8次冻融循环时,其剥蚀破坏程度非常严重,由此造成的质量损失基本抵消了其吸入溶液量造成的质量增加,若没有剥蚀发生,试件的饱水度将会有更为明显的增加,而浸泡在其他3 种盐溶液中的湿试件,直到10 次冻融循环后才仅有少量的剥蚀破坏.
2.4.3 干试件的常温饱水度和冻融饱水度
浸泡在盐溶液中干试件的常温饱水度和冻融饱水度如图9 所示.
由图9(a)可见:在常温条件下,浸泡在NaCl 溶液中干试件的吸水速率和饱水度远高于浸泡在MgCl2溶液中 的干试 件,且达到Se,cp所需要 时间更少;NaCl 溶液质量分数越高,干试件的吸水速率和Se,cp越 大,浸泡在4.0N、10.0N 和15.0N 中干试件 的Se,cp分别约为87.8%、89.9%和91.9%;MgCl2溶液质量分数越高,干试件的吸水速率和Se,cp越小,浸泡在4.0M、10.0M 和15.0M 中试件 的Se,cp分别约 为30.2%、26.2%和24.6%.
由图9(b)可见:在冻融循环条件下,浸泡在NaCl 溶液中干试件的吸水速率和饱水度远高于浸泡在MgCl2溶液中的干试件;经过4 次冻融循环后,试件开始出现较明显的剥蚀破坏,之后其饱水度增加不明显;经过7 次冻融循环后,试件的剥蚀破坏非常大,此时停止测试;试件的吸水速率和Se,cp随着NaCl 溶液质量分数的增大而增大,与浸泡在4.0M中的试件相比,浸泡在10.0M 和15.0M 中的试件的吸水速率和Se,cp均明显降低.

图9 浸泡在盐溶液中干试件的常温饱水度和冻融饱水度Fig.9 Saturation degree of dry specimens immersed in salt solutions at normal temperature and during freezing-thawing cycles
由图8 和图9 还可以得到以下结论:无论是湿试件还是干试件,在冻融循环条件下,其浸泡在盐溶液中的吸水速率和饱水度均明显大于常温条件下,表明在冻融循环条件下,试件周围的溶液更容易进入混凝土中,并更快地达到和超过临界饱水度;在NaCl中掺入MgCl2制成复合除冰盐,可以有效地改变盐溶液向混凝土内部迁移的特性,显著延缓复合除冰盐溶液进入混凝土中的速率,从而显著降低混凝土内部饱水度的增长速率,其原因可能是盐溶液中的MgCl2与水泥水化产物Ca(OH)2反应,生成难溶的Mg(OH)2沉淀[19],该沉淀物将填充混凝土中的孔隙,从而延缓盐溶液进入混凝土内部的速率.
2.5 NaCl-MaCl2复合除冰盐对混凝土盐冻破坏的作用机理
在常温条件下,当湿试件浸泡入盐溶液时,因NaCl 和MgCl2溶液均具有吸湿性,试件内部水分将向盐溶液迁移;同时由于渗透压作用,盐溶液中的Na+、Mg2+和Cl-将持续向混凝土内部迁移,直至混凝土内、外的物质达到动态平衡.随着盐溶液质量分数的增加,混凝土内、外物质的迁移将更加明显,但无论物质如何迁移,与盐溶液接触的混凝土表层的饱水度始终是最高的.在冻融循环条件下,混凝土内部产生的“泵吸作用”[13,20]远大于盐溶液的吸湿、渗透压和毛细管吸水等作用,因而将驱使试件周围的盐溶液加速进入其内部,导致其饱水度及其随时间的增长速率远大于常温下的值.
根据冻融饱水度-结冰压理论[7],在通常条件下,混凝土试件的冻前饱水度一般均小于其临界饱水度,因此其盐冻破坏速率和破坏程度主要取决于其饱水度的提高速率,以及达到与超过其临界饱水度的速率.混凝土的饱水度超过临界饱水度越多,孔溶液的结冰压越高,产生的盐冻破坏也越严重.由图4和图5 可知,尽管随着除冰盐中MgCl2含量的增加,在100%饱水度下,盐溶液的平衡结冰压变化仅略有降低,但是盐溶液的临界饱水度明显提高,因此可以合理推测出在盐溶液中进行冻融循环时,若除冰盐中MgCl2含量较高,则混凝土试件需要达到更高的饱水度才能产生结冰压,从而更有利于降低混凝土的盐冻剥蚀破坏程度.
随着盐溶液中MgCl2含量的增加,在冻融循环条件下,混凝土试件浸泡在盐溶液中的冻融饱水度提高速率显著降低,因而非常有利于降低混凝土的盐冻破坏程度(见图8 和图9).
结合盐溶液的临界饱水度和试件的冻融饱水度试验结果,可以合理推测,随着盐溶液中MgCl2含量的增加,在冻融循环条件下,混凝土试件达到和超过其临界饱水度所需要的冻融循环次数将显著增加,因此NaCl中掺入MgCl2将大大延缓混凝土的盐冻剥蚀破坏.
尽管向NaCl 中掺入MgCl2可明显提高盐溶液的临界饱水度,但是一旦混凝土试件中盐溶液的饱水度超过临界饱水度,其产生的结冰压将迅速增大,依然会产生巨大的破坏力(见图5).因此在冻融循环条件下,当冻融循环次数足够多或超过混凝土试件的临界饱水度时,浸泡在4.0N5M5和4.0M 溶液中的混凝土试件也将出现严重的盐冻剥蚀破坏(见图3).
3 结论
(1)随着NaCl-MgCl2复合除冰盐中MgCl2含量的增大,其盐溶液造成的混凝土盐冻剥蚀破坏显著减弱;当除冰盐中MgCl2含量达到40.0%时,混凝土的抗盐冻指标由严重不合格变为合格;通过在NaCl中掺入一定量的MgCl2,制备盐冻破坏低且除冰效率高的复合除冰盐是可行的.
(2)浸泡在4.0%盐溶液中的含盐自然干试件的盐冻剥蚀破坏速率远大于浸泡在水中的试件;混凝土的盐冻剥落量随着复合除冰盐中MgCl2含量的增大而减小;当冻融循环次数足够多时,即使在纯MgCl2盐溶液中,混凝土仍然会产生严重的盐冻剥蚀破坏.
(3)在100% 饱水度下,复合除冰盐中掺入MgCl2对4.0%盐溶液的结冰压和结冰过程影响很小,仅使其略有降低,但可以明显提高盐溶液的临界饱水度.
(4)固体粉状MgCl2的吸湿性远高于固体粉状NaCl,但当盐溶液的质量分数不高于20.0%时,相同质量分数NaCl溶液的吸湿性大于MgCl2溶液.
(5)含盐干试件的毛细管吸水速率和平衡饱水度明显大于不含盐干试件;在冻融循环条件下,浸泡在含有MgCl2的4.0%复合除冰盐溶液中试件的饱水度及其提高速率明显小于浸泡在4.0%NaCl溶液中的试件.
(6)在NaCl中掺入MgCl2制备复合除冰盐,可明显降低混凝土盐冻剥蚀破坏,其作用机理主要归因于MgCl2的掺入明显提高了复合除冰盐溶液的临界饱水度,以及显著降低了混凝土内部的饱水度及其增长速率,这可为防治混凝土盐冻破坏及制备低危害除冰盐提供一条新的技术思路.
