冠状动脉异常起源于主动脉的诊疗
2023-03-06王嘉懿张文张海波
王嘉懿 张文 张海波
冠状动脉异常起源于主动脉(AAOCA)指左或右冠状动脉起源位于或高于不相应的主动脉窦,是一种罕见的先天性冠状动脉畸形。文献报道在接受超声心动图、冠状动脉计算机断层血管成像(CTA)、磁共振血管成像(MRA)或冠状动脉造影检查的患者或运动员中AAOCA 检出率为0.01%~2%,然而,在没有临床检查指征的情况下对一般人群进行AAOCA 的筛查很少,其实际发生率未知[1]。AAOCA 被认为与心肌缺血有关,且已成为儿童及青少年心脏骤停或心源性猝死的第二大病因[2]。
1 AAOCA的解剖分型与病理生理
AAOCA 的部分解剖分型被认为是良性变异,不会导致心肌缺血,有研究表明造成心源性猝死潜在风险增加的危险因素是AAOCA 的某些特定解剖特征[3]。AAOCA 按照异常的冠状动脉起源位置,可以分为左冠状动脉异常起源于右冠窦(AAOLCA)和右冠状动脉异常起源于左冠窦(AAORCA)。文献报道,AAORCA 的发生率高于AAOLCA,但后者在心源性猝死的尸检中更为常见,表明AAOLCA 更容易引起心源性猝死[4]。异常的冠状动脉从对侧主动脉窦发出后走行路径可分为5 种:大动脉间型、肺动脉下型(圆锥内或室间隔内)、肺动脉前型、主动脉后型、心脏后型[1]。过去通常认为只有当异常的冠状动脉走行于主肺动脉之间即大动脉间型AAOCA 时,才与心源性猝死风险增加有关,但近年发现室间隔内走行的AAOCA 也可能导致心肌缺血[5]。此外,异常冠状动脉开口和起始段如果具有以下解剖特征则被认为与心源性猝死的风险相关:(1)冠状动脉高开口或缝隙样开口;(2)冠状动脉与主动脉成锐角发出;(3)冠状动脉起始段走行于主动脉壁内;(4)冠状动脉起始段发育不良[4]。AAOCA 引起心源性猝死的病理生理学机制仍不明确,可能与反复发生的有或无症状的心肌缺血所致心肌纤维化和室性心律失常有关。AAOCA 引起心肌缺血通常只发生在剧烈运动中或运动后。运动时心输出量增大,主动脉扩张可能造成异常冠状动脉的缝隙样开口发生活瓣样关闭造成梗阻,或使主动脉壁内走行的起始段管腔进一步狭窄变形,导致异常起源冠状动脉血流障碍,加之运动时患者的心肌耗氧量增加,因此,更易于引起心肌缺血[6]。
2 AAOCA的临床表现
AAOCA 大多是在对心脏杂音、异常心电图等其他原因进行超声心动图或CTA 检查时意外发现[7]。心脏骤停或心源性猝死可以是AAOCA 的首发表现,38%~66%的患者猝死前从未出现过相关症状[1]。也有部分患者是在有症状而接受检查后确诊的,症状包括胸痛、心悸、头晕、晕厥等心肌缺血的表现[8]。先天性心脏病外科医师协会的研究提出,诊断AAOCA 相关的心肌缺血应符合下列任一标准:(1)发生过心源性猝死或心脏骤停;(2)运动中或运动后出现晕厥,无法用脱水或血管迷走反射来解释;(3)胸痛伴有心肌标志物升高,异常冠状动脉供血区域心电图改变,或心肺运动试验阳性;(4)负荷或非负荷状态下的任何影像学检查中异常冠状动脉供血区域出现异常表现[9]。
3 AAOCA的诊断与评估
经胸超声心动图是筛查和评估AAOCA 的最常用技术,其优势在于无创、便捷、经济。对于疑似AAOCA 的患者,经胸超声心动图通常是首先进行的检查,能够显示冠状动脉的起源、是否合并主动脉壁内走行及开口有无狭窄等情况。然而,经胸超声心动图空间分辨率较低,且受患者个体差异及操作者经验影响较大,有6%~10%的漏诊率。冠状动脉CTA 和MRA 是可准确提供AAOCA 解剖特征最重要的检查手段,可以完整显示冠状动脉的开口、走行、角度、狭窄、与大动脉的关系以及周围组织的解剖结构[1]。考虑到大部分AAOCA引起的心源性猝死都发生在剧烈运动时,所有确诊AAOCA 的患者都应接受运动或药物负荷功能检查,特别是无症状的患者,建议结合运动平板试验与负荷超声心动图或核素心肌灌注显像,以识别是否存在可诱导的心肌缺血[7]。冠状动脉造影是有创操作,且其成像为二维图像,不能很好地显示冠状动脉开口和起始段的解剖结构以及与周围组织的关系,一般不作为AAOCA 的首选检查手段。冠状动脉血管内超声及血流储备分数能够提供负荷及非负荷状态下异常冠状动脉的管腔形状及血流动力学改变[10],对评估壁内或室间隔走行的冠状动脉段的血流受限程度有一定价值[11],可作为无创功能检查的补充,进一步识别潜在的心肌缺血[5]。
4 AAOCA的手术指征
美国心脏协会和美国心脏病学会(AHA/ACC)2018 年发布的成人先天性心脏病管理指南对AAOCA 干预措施的建议如下:(1)所有出现心肌缺血症状或异常冠状动脉对应区域存在心肌缺血证据的AAOCA 患者均应进行外科手术治疗(Ⅰ类推荐);(2)所有出现室性心律失常表现的AAOCA 患者进行手术治疗获益大于风险(Ⅱa 类推荐);(3)无症状或心肌缺血证据的AAOLCA患者进行手术治疗获益大于风险(Ⅱa 类推荐);(4)无症状且负荷功能检查无可诱导的心肌缺血或冠状动脉血流受限依据,影像学检查无高危解剖特征的AAORCA 患者可考虑进行外科手术或保守治疗(Ⅱb 类推荐)[4]。
目前暂无指南性文献推荐针对AAOCA 儿童患者进行手术指征。美国胸外科协会(AATS)2017 年发布的AAOCA 专家共识仅对>10 岁的患者就干预措施提出建议:(1)所有出现缺血性胸痛、疑似室性心律失常导致的晕厥以及发生过心源性猝死的AAOCA 患者,应限制活动并进行手术治疗(Ⅰ类推荐);(2)所有大动脉间型AAOLCA 患者应限制竞技体育运动并进行手术治疗(Ⅰ类推荐);(3)AAORCA 患者应接受运动平板试验结合负荷超声心动图或核素心肌灌注显像以评估可诱导的心肌缺血,对于没有缺血症状且运动负荷试验阴性的患者,在与其家庭就心源性猝死的风险进行商议后,可允许参加竞技体育运动(Ⅱa 类推荐)。部分学者主张对10 岁以下无症状的AAOLCA 患者进行保守治疗[10],因为该年龄段儿童运动强度小,发生心源性猝死的风险较低,而手术治疗的风险相对更大[3]。
5 AAOCA的手术方式
AAOCA 的手术方法有冠状动脉去顶术、冠状动脉开窗术、冠状动脉开口成形术、冠状动脉再植术、肺动脉移位术和冠状动脉旁路移植术等。手术的目标在于解决所有引起心肌缺血的高危解剖特征,使冠状动脉尽可能接近正常[12-13]。手术方式的选择主要取决于异常冠状动脉开口和起始段的解剖结构(见图1)。
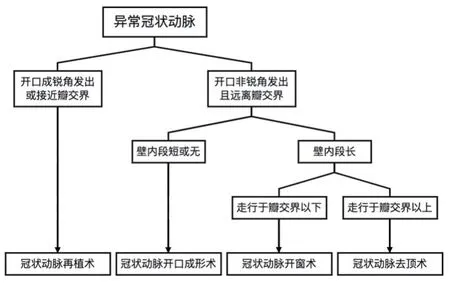
图1 AAOCA的手术方式选择流程图
冠状动脉去顶术是治疗AAOCA 最常用的手术方法,适用于起始段壁内走行的患者。通过从主动脉内切开异常冠状动脉与主动脉之间的共同壁,使其直接与主动脉管腔相通,开口于正确的主动脉窦内并扩大冠状动脉开口。部分AAOCA 的壁内段经主动脉瓣交界后方走行至主动脉瓣水平以下,直接行去顶术可能损伤主动脉瓣交界及主动脉瓣叶,导致术后出现主动脉瓣反流。一种解决方法是先将主动脉瓣交界切下,完成壁内段冠状动脉去顶后,再将其重新悬吊于主动脉壁[14]。然而,有研究表明即使进行主动脉瓣交界再悬吊,仍然会增加主动脉瓣反流的风险[9]。行冠状动脉开窗术可能是更好的选择,即保留原始的异常开口及主动脉瓣交界后方的壁内段,仅将位于正确主动脉窦的壁内段去顶,从而避免与主动脉瓣相关的操作对其造成的损伤。
对于无壁内走行或壁内段相对较短的AAOCA,无法通过去顶术将冠状动脉开口复位到正确的主动脉窦内,则需要行冠状动脉开口成形术或冠状动脉再植术,在主动脉壁上直接创建新的冠状动脉开口。冠状动脉开口成形术纵向切开异常冠状动脉离开主动脉壁后于心外膜走行的起始段,并在对应主动脉窦处做相延续的垂直切口,再使用自体心包补片缝合于两者之间,以连接冠状动脉与主动脉壁形成新的冠状动脉开口[2]。冠状动脉再植术通过对异常冠状动脉的起始段进行充分游离后,将包含其开口的冠状动脉纽片从对侧主动脉窦切下并重新种植在正确的主动脉窦,广泛适用于在主动脉壁有单独开口的AAOCA[14]。也有报道不使用纽片的冠状动脉再植术,在冠状动脉离开主动脉壁后将其切断并进行再植[2],用于异常冠状动脉与主动脉成锐角发出或开口接近主动脉瓣交界的AAOCA 患者[10]。
肺动脉移位术通过在肺动脉分叉近端横断肺动脉干,将肺动脉干吻合至左肺动脉远端,使肺动脉干移向左侧,或在肺动脉分叉处切断右肺动脉,将右肺动脉置于升主动脉前并重新吻合,使肺动脉干向前移动,增加肺动脉干与升主动脉之间的距离,避免对走行于主肺动脉之间的冠状动脉段的挤压。然而,近年的研究表明主肺动脉之间的压迫并不是导致异常冠状动脉缺血的主要原因[3],而肺动脉移位术无法解决任何增加AAOCA 心肌缺血风险的高危解剖特征,因此,一般仅作为上述其他手术方式的补充。
冠状动脉旁路移植术因固有冠状动脉血流竞争,导致移植血管远期通畅性无法令人满意,而极少用于年轻患者[7]。
6 AAOCA的手术疗效及预后
先天性心脏外科医师协会(CHSS)的多中心研究报道AAOCA 手术相关死亡率约为1%,短期疗效满意,80%~95%的患者术后无心肌缺血。有7%~13%的患者发生术后不良事件,包括8%的患者出现轻度以上的主动脉瓣反流,4%的患者发现新的心肌缺血症状或依据,3%的患者因冠状动脉相关原因需要再次手术等治疗。
与总体队列相比,术后不良事件风险增加的危险因素包括术前有缺血、AAOLCA、冠状动脉去顶术以外的手术方式及术中与主动脉瓣交界相关的操作;术后不良事件风险降低的保护因素包括术前无缺血、AAORCA 以及不涉及主动脉瓣交界相关操作的冠状动脉去顶术。AAOCA 术后发生主动脉瓣反流已证实与术中对主动脉瓣交界相关结构的操作有关,最常见于进行冠状动脉去顶术的患者。选择不涉及相关操作的手术方式,可能避免这种情况[9]。有研究分析AAOCA 术后仍有心肌缺血的患者,大多数在手术中仅对较短的冠状动脉壁内段进行去顶,未能将冠状动脉开口复位到正确的主动脉窦内,冠状动脉开口或起始段仍受到主动脉瓣交界相关结构的压迫[15]。冠状动脉开口成形术及冠状动脉再植术能在避免主动脉瓣交界相关操作的同时充分解决其对冠状动脉的压迫,Gaillard等[2]及Bonilla-Ramirez 等[16]的研究报道其短期疗效优于冠状动脉去顶术,长期疗效仍有待进一步随访观察。
7 AAOCA的术后管理与随访
无论是否进行外科手术治疗,AAOCA 患者都应终生随访,包括关注心肌缺血的相关症状,并定期行心电图和超声心动图检查[7]。进行手术治疗的患者在术后随访时,应使用与术前相对应的影像学及功能学检查手段,包括运动或药物负荷试验,以评估心肌缺血的缓解情况[10]。由于AAOCA 患者心源性猝死大部分发生在剧烈运动中或后,有手术指征的患者应自确诊起限制竞技体育运动直至手术治疗3 个月后,如果患者没有出现任何心肌缺血或心律失常的表现,且运动负荷试验阴性,可恢复正常的体育运动。有研究表明,对于术前发生过心脏骤停或心源性猝死的患者,术后一旦恢复体育运动,发生心源性猝死的风险仍然较高,解除体育运动限制应至少1 年没有出现症状且运动负荷试验阴性[7]。
