无机元素的指纹图谱分析在透明质酸钠来源鉴别中的应用
2023-02-26刘航瑞陈玉娟臧洋陆艳丽周希蕊黄思玲李红梅郭学平冯流星
刘航瑞 陈玉娟 臧洋 陆艳丽 周希蕊 黄思玲 李红梅 郭学平* 冯流星*
1(中国计量科学研究院,北京100029)
2(北京化工大学,北京 100029)
3(华熙生物科技股份有限公司,济南 250101)
透明质酸(Hyaluronic acid,HA)是一种高分子材料,具有良好的生物相容性和生物可降解性,广泛应用于生物医学材料[1-2]、美容护肤[3-4]、药物传递[5]和组织工程[6-7]等领域。透明质酸钠(Sodium hyaluronate,SH)是透明质酸的钠盐,具有更好的水溶性和稳定性,更易于加工和应用于化妆品中。HA 的制造方法包括化学合成、酶促反应合成、动物组织提取和生物发酵等。化学合成HA 存在的主要问题是化学交联剂的污染[8],酶促反应的缺点是这些酶缺乏绝对的底物特异性[9],而动物组织提取则存在纯化困难和交叉病毒感染等风险[10]。目前,在HA 产品的生产工艺中,更多采用链球属菌的生物发酵模式,原料选择、发酵和提纯等环节均可能引入不同类型的元素[11],导致不同厂家生产的SH 质量参差不齐,并且不同厂家及不同工艺的HA 产品具有显著的元素指纹特征。
近年来,无机元素指纹图谱分析技术已被广泛应用于食品[12-14]、药品[15-17]和化妆品[18-20]等领域的质量控制,通过对样品中的无机元素含量进行分析,可以为样品建立一个独特的指纹图谱,从而实现对样品的快速鉴别和质量评估。目前,在化妆品的质量控制中侧重于测量少数有害元素(如Pb、Hg 和As 等),以保证产品的安全性,但不能提供足够的信息对产品来源进行分类和鉴别,而无机元素指纹图谱分析技术具有快速、准确、可靠、高灵敏度和高分辨率等特点,能够为样品的质量控制提供重要信息[14,21-23]。
本研究选取市场占有率较高的6 个厂家共计13 个批次的SH 产品,建立了SH 产品无机成分的分析方法。对于含量相对较高的Na 元素,采用电感耦合等离子体发射光谱(ICP-OES)进行外标法测量,Cl 元素采用离子色谱(IC)以外标法测量。对于含量较低的其它无机元素,采用电感耦合等离子体质谱(ICPMS)对样品进行全定量分析。将70 种元素的定量数据进行指纹图谱分析,并选取含量较高的23 种元素绘制SH 指纹图谱;采用主成分分析(PCA)、偏最小二乘判别分析(PLS-DA)和正交偏最小二乘判别分析(OPLS-DA)等统计学方法分析各样品间的相似性和差异性,并通过变量重要性投影(VIP)找出造成差异的关键元素;通过系统聚类分析(HCA)将样品按照其无机成份相似度进行分类,并绘制出聚类树状图。通过元素指纹图谱分析可清楚了解各批次之间的异同,为产品优化和改进提供依据。
1 实验部分
1.1 仪器与试剂
7700x series 电感耦合等离子体质谱仪(美国Agilent 公司);iCAP 7000 series 电感耦合等离子体发射光谱仪和Thermo-ICS-5000+型离子色谱仪(美国ThemoFisher Scientific 公司);KDF S80 马弗炉(日本SANSYO 公司);ETHOS D 消解仪(意大利Milestone 公司)。
浓HNO3和H2O2(BV-Ⅲ级,北京化学试剂所);ICP-MS 调谐液(10 μg/L Ce、Co、Li、Tl 和Y,美国Agilent 公司);钠单元素溶液标准物质(GBW(E)080260)、水中氯根成分分析标准物质(GBW(E)080269)和多元素混合标准溶液(GBW(E)082431、GBW(E)082429 和GBW(E)082430)(中国计量科学研究院)。
13 批SH 样品(编号H1~H13)分别来自6 个生产厂家:公司1(H1~H5),公司2(H6~H8),公司3(H9),公司4(H10~H11),公司5(H12),公司6(H13)。样品均为白色粉末。
1.2 样品前处理方法
1.2.1 微波消解
称取0.1 g 样品于消解罐中,依次加入7 mL 重蒸HNO3和1 mL H2O2,按照表1 中消解程序进行微波消解,消解后的样品呈透明清透的微黄色。将消解后的样品转移至离心管中,加水稀释至33 g,采用ICPMS 测量无机元素,每个样品测量3 次;由于样品中Na 元素含量较高,需再稀释40 倍用于ICP-OES 测量Na 元素,每个样品重复测量3 次。

表1 透明质酸钠(SH)样品的微波消解程序Table 1 Microwave digestion procedure for sodium hyaluronate (SH) samples
1.2.2 马弗炉灰化
将0.1 g 样品置于马弗炉中加热干燥灰化,程序如表2 所示。首先,在加热干燥灰化前,加入适量KOH,尽可能保存Cl–。第一步为干燥样品,第二步和第三步为碳化样品,第四步为灰化样品。灰化后,加入适量稀HNO3以调节pH=7。最后,加入适量超纯水将样品稀释至适当浓度,并称量溶液质量,采用IC测量Cl 元素,每个样品测量3 次。

表2 SH样品使用马弗炉灰化程序Table 2 Muffle furnace ashing procedure for SH samples
1.3 仪器条件和分析方法
1.3.1 ICP-OES仪器条件
射频功率为1150 W,泵速为50 r/min,辅助气流速为0.5 L/min,雾化器气体流速为0.5 L/min,冷却气流速为12 L/min,无辅助气体。将钠单元素溶液标准物质(GBW(E)080260)分别稀释至1.0、2.0、5.0 和10.0 μg/g,采用ICP-OES 测量,绘制标准工作曲线,相关系数应大于0.9999。
1.3.2 IC仪器条件
采用自动抑制外加水模式的抑制器和电导检测器进行检测。色谱柱为Dionex IonPac AS19 阴离子柱,柱箱温度为30 ℃;抑制电流为50 mA;样品进样量为25 μL;流速为1 mL/min。淋洗程序采用24 mmol/L KOH 溶液等度洗脱,运行时长为10 min。采用水中氯根成分分析标准物质(GBW(E)080269)作为样品中Cl‒的定量标准。
1.3.3 ICP-MS仪器条件
使用调谐液(1 μg/L)调谐,使ICP-MS 仪器满足灵敏度、双电荷、氧化物和分辨率等工作指标的要求,再进行样品中70 种元素的全定量分析。射频功率1500 W;等离子体流速15 L/min;载气流速(Ar)1.01 L/min;采样锥深度8.0 mm,积分时间为0.1 s;碰撞模式为NoGas 模式。将多元素混合标准溶液GBW(E)082431、GBW(E)082429 和GBW(E)082430 混合后稀释至合适浓度,建立每种元素的标准曲线,相关系数均需大于0.999。
1.3.4 热图分析处理和指纹图谱绘制
热图分析是一种可视化数据方法,采用不同种类、不同深浅的颜色呈现矩阵数据中每种元素的值,进而发现数据之间的关系。将13 批SH 中70 种元素全定量数据取平均值后导入Origin 程序,使用Z值均一化减少数据差异,提高数据的可比性,然后绘制热图。从70 种元素全定量分析结果中挑选含量较高、有代表性的22 种元素(Li、B、Mg、Al、Si、P、K、Ca、Sc、Ti、Cr、Mn、Fe、Co、Ni、Cu、Zn、Ga、Br、Se、Rb 和Sr)绘制指纹图谱,由于不同元素之间含量相差多个数量级,因此,将Mg、Si、P、K 和Ca 含量缩小100 倍,将Mn 和Sr 含量缩小10 倍。
1.3.5 数据多元统计分析处理
数据处理软件为Microsoft Excel、Origin 2021 和MetaboAnalyst。
PCA 是一种将高维数据降维的方法,高维数据通过线性变换投影到一个新的低维空间中,减少变量,降低维数并同时尽可能地保留数据的信息。PCA 分析不依托数据的分组信息,是一种无监督的分析方法。PLS-DA 是一种有监督的统计方法,结合偏最小二乘回归和判别分析的思想,寻找对分组有显著影响的变量。OPLS-DA 通过正交化进一步放大变量的影响,能更好地解释样本分类,但是OPLS-DA 可能过度拟合数据,导致预测性能下降。
将13 批SH 样品的70 种元素全定量分析的3 次平行数据导入到MetaboAnalyst,使用Z 值均一化后进行PCA 和PLS-DA。PCA 采用协方差矩阵;PLS-DA 依托的分组信息为生产厂家,分为1~6 组;对PLS-DA 分不开的组再单独进行OPLS-DA 分析。
1.3.6 HCA处理和指纹图谱绘制
HCA 是一种无监督的数据分析方法,通过测量样本之间的距离(相似性)将其分为不同的群组,可以直观地从树状图中看出样本之间的相似程度。将上述热图使用的Z值均一化后的数据,采用平均聚类方法和Euclidean 平方距离类型进行HCA 处理。
2 结果与讨论
2.1 SH样品主要元素的测定结果
13 批SH 样品中的Na 元素和Cl 元素检测结果见表3。SH 中Na 元素含量大于400 mg/g,其中,H6~H9 样品中Na 元素含量较低(<450 mg/g),其它样品的Na 元素含量较高;Cl 元素含量在不同厂家样品中的差异较明显,其中,公司4 的H10 的含量超过3000 μg/g,公司6 的H12 的含量超过7000 μg/g,其余样品均超过2000 μg/g,含量最高的H12 与含量最低的H11 相差近68 倍。

表3 SH样品中Na和Cl含量测量结果Table 3 Measurement results of Na and Cl content in SH samples
2.2 统计学分析结果
2.2.1 热图与指纹图谱结果
采用ICP-MS 对样品中70 种元素进行全定量分析,所得数据再进行热图分析,结果见图1A。通过热图可直观地看出所有样品中的无机元素含量,红色代表此样品中该元素的含量相对其它样品偏高,蓝色则代表偏低。由图1A 可见,公司1 的H2 样品中B、P、Ni 和I 等元素含量显著低于其它样品,H3、H4样品中Zn、Ru、Rh、Au 和Pb 含量相似,均高于其它样品。公司2 的H6~H8 样品中Ga、I、La、Tb、Ba~Er 等多种元素含量相似,均高于其它样品。公司6 的H13 样品中多种无机元素含量显著高于其它样品。13 批SH 样品全定量分析结果中22 种含量较高的元素绘制的指纹图谱见图1B,样品的指纹图谱峰型总体走势基本一致,但是Al、Si、P、Ca、Ti 和Cr 等元素含量差异明显。综上所述,通过ICP-MS 全定量分析数据的热图和指纹图谱分析可以快速了解样品中无机元素的相对含量,发现样品之间的差异性和相似性,为质量控制和生产优化提供有力支持。

图1 (A)13 批SH 样品中70 种元素全定量分析结果;(B)13 批SH 样品中22 种元素指纹图谱Fig.1 (A)Semi-quantitative results of 70 kinds of elements in 13 batches of SH samples;(B)Fingerprint map of 22 kinds of elements in 13 batches of SH samples
根据我国《化妆品安全技术规范》(2015 年版)[24]要求,化妆品中相关元素限定标准分别为Pb ≤10 mg/kg,Hg ≤1 mg/kg,As ≤2 mg/kg,Cr ≤5 mg/kg。根据测定结果可知,这6 个生产厂家的13 批SH 样品中相关元素含量均未超过限定标准。但是,有一些分析结果值得注意:公司2 的H6~H8 样品中镧系元素(La~Lu)含量均高于其它样品;公司5 样品中H12 的Cl 元素含量远超其它样品;公司3 的H9样品和公司6 的H13 样品中多种元素含量超过其它样品,并且个别重金属元素也接近我国标准限定水平。这些元素含量过高的产品可能会对人体造成潜在危害,因此,生产厂家应格外重视生产原材料的安全和生产过程的质量控制。
2.2.2 PCA结果
对数据进行PCA 的结果见图2A,主成分贡献率见图2B。此模型中,主成分PC1 和PC2 分别占比26.3%和20.8%,累计贡献率47.1%,占比过小,说明这两种主成分不能完全解释原始数据中的变化,SH样品中多种元素含量具有较大的方差,使得主成分解释力度较弱。由PCA 图可知,公司2 和公司6 的数据点与其它公司距离较远,能明显区分开;但公司1、3、4 和5 的数据点在图中距离较近,不能完全分开,说明PCA 模型构建效果欠佳,需要使用其它方法进一步分析。

图2 (A)来自6 家公司的SH 中70 种元素含量的PCA 图,不同颜色代表来自不同公司(下同);(B)前5 个主成分因子的贡献率(PC1~PC5),横坐标表示主成分顺序Fig.2 (A) Principal component analysis (PCA) score plots of 70 kinds of elements in SH from 6 companies,different colors represent from different companies (the same below);(B) The contribution rate of the first 5 principal component factors (PC1‒PC5),the abscissa represents the principal component order
2.2.3 PLS-DA和OPLS-DA结果
对全定量分析数据进行PLS-DA 的结果见图3A,图3B 为VIP 得分图,公司3~公司6 的样品都得到了较好分离,公司4 和公司5 的样品有少许重叠可以忽略,但是公司1 和公司2 的样品还有较大区域重叠,较难分类,需要进一步进行OPLS-DA 放大两者的差异。由图3B 可见,多种元素(Li、Ca、Nb、P、Mg、Sr、Zr、Al、Pd 和As 等26 种元素)对样品分类非常重要(VIP >1),热图分析也表明这些元素在不同样品之间颜色变化明显(图1A),含量差异较大。PLS-DA 的交叉验证准确率为84.6%,可以较好地评估和鉴别公司3~公司6 生产的SH 的厂家来源。
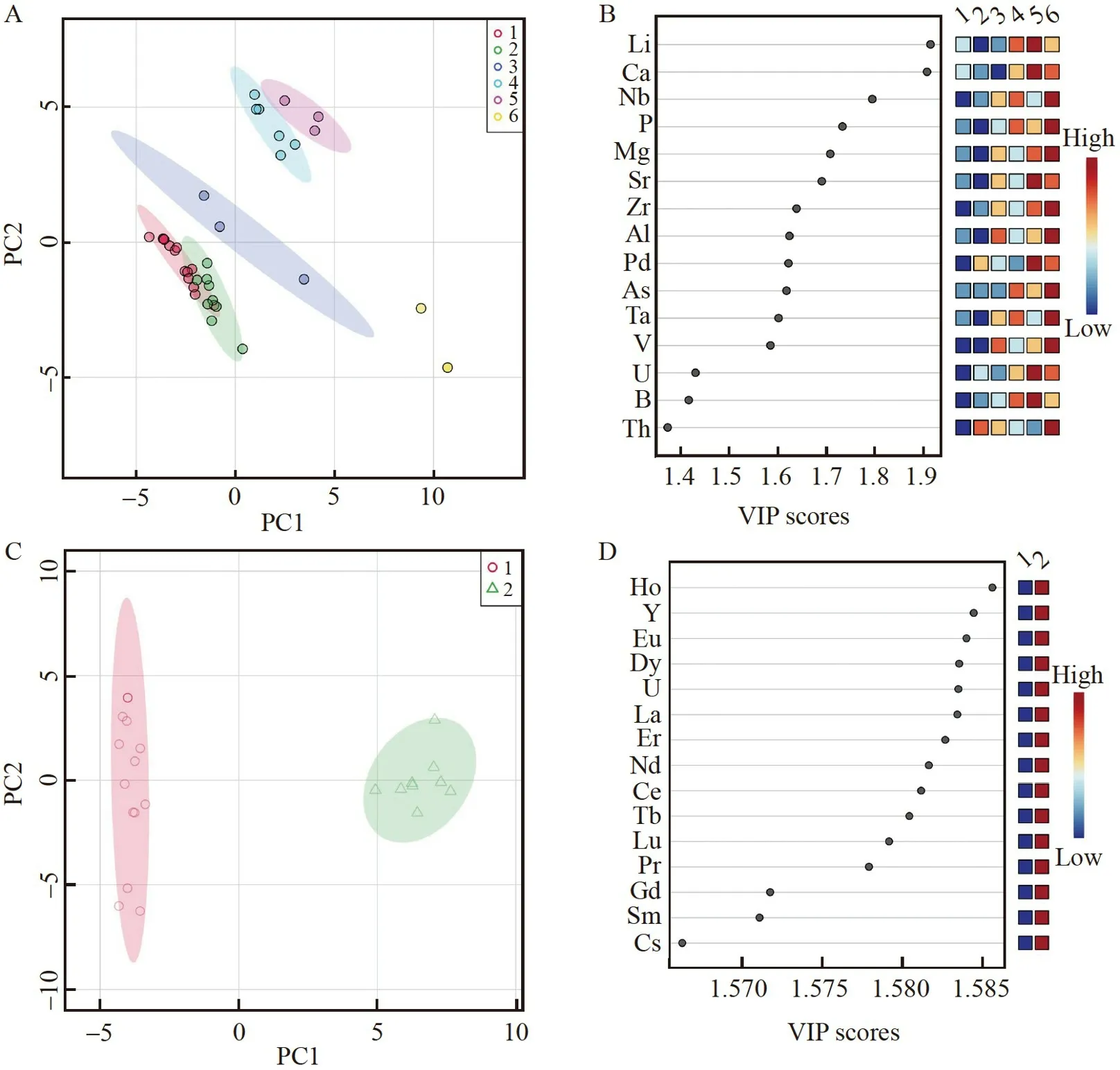
图3 来自6 家公司的SH 中70 种元素含量的(A)PLS-DA 图和(B)PLS-DA 的VIP 得分图;来自公司1和公司2 的SH 中70 种元素含量的(C)OPLS-DA 图和(D)OPLS-DA 的VIP 得分图Fig.3 (A) PLS-DA score plots of 70 kinds of elements of SH from six companies and (B) corresponding VIP plot of PLS-DA;(C) OPLS-DA score plots of 70 kinds of elements in SH from companies 1 and 2,and (D)corresponding VIP plot of OPLS-DA
对公司1 和公司2 的样品使用OPLS-DA 方法进一步分类,以探究对这两组样品分类起重要作用的元素。将公司1 和公司2 的数据单独进行Z值均一化后再进行OPLS-DA 分析,结果如图3C 所示,VIP得分图见图3D。可见公司1 和公司2 的样品得到很好分离,其中,Ho、Y、Eu、Dy、U、La 和Er 等元素对这两个样品分类起到重要作用(VIP >1)。OPLS-DA 的交叉验证准确率为97.8%,表明这些变量包含足够的信息用于区分这两种样品的来源。综上,采用PLS-DA 和OPLS-DA 方法对全定量分析数据进行分析可以鉴别SH 的厂家来源,并确定影响样品分类的重要变量。
2.2.4 HCA结果
HCA 结果如图4 所示,横坐标代表距离,节点越向右代表样品关系越远,在距离100 处,可将13 批样品分为6 组:H1~H5、H10~H11、H12、H9、H6~H8 和H13,恰好对应6 家公司,表明同一公司的SH 产品具有较高的相似程度,不同公司生产的SH 具有较大的差异。在距离150 处,公司1 的H1~H5、公司3的H9、公司4 的H10~H11 和公司5 的H12 可以归为一类;公司2 的H6~H8 为一类;公司6 的H13 为一类,这与PCA 中公司1、3、4、5 的位置相互重叠,而公司2、6 分离较好的结论一致。

图4 聚类分析树状图Fig.4 Cluster analysis dendrogram
3 结论
探讨了无机元素指纹图谱分析技术在SH 鉴别和质量评估中的应用。采用ICP-MS 等方法对13 个不同厂家不同批次的SH 样品中的Na 元素和Cl 元素进行定量分析,对70 种无机元素含量进行了全定量分析,并采用热图、指纹图谱、PCA、PLS-DA、OPLS-DA 和HCA 建立了SH 中的无机元素指纹图谱。结果表明,不同厂家生产的SH 样品中的无机元素含量和种类存在明显差异,通过无机元素指纹图谱可对SH 进行准确鉴别,在SH 的来源鉴别、质量控制、生产管理和监管等方面具有重要意义。本研究涉及的样品数量较少,对市场上销售的SH 产品的代表性不足,未来需要增加样品数量和种类,并考虑更多维度的指纹图谱特征,以提高方法对SH 产品的鉴别和评价能力。
