CoO纳米颗粒/石墨烯纳米纤维复合材料的制备及电化学性能
2023-02-25胡诗颖沈佳艳韩峻山郝婷婷
胡诗颖, 沈佳艳, 韩峻山, 郝婷婷, 李 星
(宁波大学材料科学与化学工程学院, 宁波 315211)
在过去的几十年里, 由于锂离子电池(LIB)具有高工作电压、 无污染、 无“记忆效应”、 高能量密度和高功率密度等优点, 已经被广泛应用在便携式电子设备(如笔记本电脑、 移动电话和照相机)和电气设备(如电动车、 电动自行车和智能电网)[1,2]. 众所周知, 石墨的电极电势低、 循环寿命长和成本低,使其在商业化的LIB负极材料中起着重要作用[3]. 然而, 一方面, 石墨负极的实际容量已达到理论容量的极限(372 mA·h/g); 另一方面, 石墨的离子扩散系数(10-6cm2/s)较低, 限制了其在大倍率快速充放电电池领域的应用[4~7]. 随着对电动汽车续航里程数的要求不断提高, 对高能量密度和高功率密度的LIB的巨大市场需求引起了相当大的关注[8]. 为了克服石墨负极材料的缺点, 急需寻找一种可行的材料来代替石墨[9]. 过渡金属氧化物(TMO)的理论容量为石墨的2~3倍, 如和NiO[15]等都可以替代石墨作为LIB的负极材料. 并且TMO的储量非常丰富, 成本相对较低, 比较符合商用LIB的特性[16,17]. 但TMO材料仍存在以下问题: 导电性和离子扩散较差, 导致倍率性能不好; 在充电/放电过程中体积膨胀较大, 导致电极材料粉碎, 会降低可逆容量[18,19]. 通常, 有两种合理的解决方法: (1) 制备纳米级材料(包括纳米颗粒[20]、 纳米线[21]、 纳米纤维[22]和纳米立方体[23]);(2) 将主体材料与碳基材料(包括石墨烯[24]、 碳质材料[25]和碳基体[26])相结合. 这些策略有以下几个作用: (1) 提供大的电解质/电极表面积, 这意味着有丰富的活性位点, 从而有利于增加主体电极的比容量; (2) 提高电极材料的导电性, 缩短离子扩散路径, 从而提高倍率性能; (3) 缓解电化学反应过程中的体积变化, 从而确保主体材料的结构整体性, 有利于循环稳定性[27,28].
石墨烯是C原子以sp2杂化相连形成的碳六元环, 碳六元环彼此相连形成二维(2D)单层石墨烯结构. 2D石墨烯能够弯曲成零维富勒烯, 卷曲成纳米管, 堆叠成三维(3D)石墨. 石墨烯具有高的理论表面积(2630 m2/g)、 高的导电性(200000 cm2·V-1·S-1)及高的杨氏模量. 这些优异的性能在锂离子电池领域有着巨大的应用前景[29]. 其中, CoO /石墨烯复合材料可以表现出优异的电化学性能. 如Guan等[23]使用牺牲模板法制备了空心分层CoO纳米立方体/氧化石墨烯复合材料. 特定的结构显示出高的锂存储容量, 在150 mA/g的电流密度下容量达到1170 mA·h/g. Cao等[30]将CoO锚定在氧化石墨烯薄片上制成3D网络结构, 在100 mA/g的电流密度下经过100次循环后表现出1309 mA·h/g的可逆容量.Prabakar等[31]将CoO均匀嵌入到石墨烯层制成紧密堆积的复合材料, 在1000 mA/g的大电流密度下, 有800 mA·h/g的可逆容量.
本文采用超声辅助的方法将2D石墨烯自卷曲形成中空纳米纤维结构, 制备得到的CoO纳米颗粒/中空石墨烯纤维, 其作为锂离子电池负极材料在100 mA/g的电流密度下, 循环了160次之后, 可逆容量为800 mA·h/g, 库仑效率保持在99%以上. 中空纤维结构成功实现了内部容纳电解液增加导离子率和表面增强导电子率的目的; 中空纤维相互交叉搭建的3D结构增强了电极材料与集流体之间的连接,提高了材料在深度循环过程中的稳定性.
1 实验部分
1.1 试剂与仪器
石墨、 硝酸钾(KNO3)、 无水乙醇(C2H6O)、 浓硫酸(H2SO4, 质量分数98%)、 高锰酸钾(KMnO4)、 过氧化氢(H2O2, 质量分数30%)和四水合乙酸钴[Co(CH3COO)2·4H2O]均为分析纯, 购自上海麦克林生化科技有限公司; 锂片、 垫片、 隔膜( PE)和电池壳, 购自国药集团化学试剂有限公司; 聚偏二氟乙烯(PVDF)和乙炔黑均为分析纯, 购自科路得股份有限公司; 六氟磷酸锂(LiPF6)、 碳酸乙酯(C5H10O3, 质量分数99%)、 碳酸二甲酯(C3H6O3, 质量分数99%)和N-甲基吡咯烷酮(C5H9NO, 质量分数99%)均为分析纯, 购自阿拉丁试剂有限公司; 去离子水(电阻率1.25 mΩ·cm).
D8 Focus型X射线粉末衍射仪[XRD, Cu靶Kα线(λ=0.154 nm), 扫描范围5°~80°, 扫描速度5°/min, 步宽为0.2°], 德国布鲁克公司; Escalab 250Xi型X射线光电子能谱(XPS), 美国赛默飞世尔科技公司; Hitachi SU-70型扫描电子显微镜(SEM), 日本日立公司; FEI Tecnai F30型透射电子显微镜(TEM), 美国FEI公司; Magna IR 560型傅里叶变换红外吸收光谱仪(FTIR), 美国Nicolet公司;CT3001A型蓝电电池测试系统(LANHE), 武汉蓝和公司; CHI760E型电化学工作站(Electrochemical workstation), 上海辰化公司 .
1.2 实验过程
1.2.1 氧化石墨烯凝胶的制备 采用改性Hummers法[32,33]制备氧化石墨烯. 将1.5 g石墨粉体与1.5 g KNO3混合, 之后加入69 mL浓H2SO4, 并放置在40 ℃水浴条件下进行搅拌; 5 min之后, 缓慢加入4.9 g KMnO4, 持续在40 ℃水浴中搅拌6 h; 之后向上述溶液中加入120 mL去离子水, 调整水浴温度到60 ℃,保温30 min; 之后再加入300 mL去离子水, 搅拌5 min之后加入9 mL 30%H2O2, 分4~5次滴加; 将上述溶液放置在室温下静置, 倒去上层浓H2SO4, 加水, 再静置, 循环3次之后离心, 即得到氧化石墨烯凝胶.
1.2.2 CoO纳米颗粒/中空石墨烯纳米纤维复合材料的制备 将0.5 g Co(CH3COO)2·4H2O溶于40 mL无水乙醇中, 搅拌12 h; 将0.25 g石墨烯凝胶溶于上述溶液中, 再添加40 mL无水乙醇, 搅拌12 h; 之后将混合溶液超声3 h后, 离心分离出样品, 置于60 ℃鼓风干燥箱中干燥3 h; 将干燥后的样品放入瓷舟中, 转移到管式炉中进行煅烧(煅烧温度为450 ℃, 升温速率为3 ℃/min), 保温时间2 h, 自然冷却,即制备出CoO纳米颗粒/中空石墨烯纳米纤维复合材料(CoO/HGOF).
1.2.3 电池的组装和电化学性能测试 将质量比7∶2∶1的CoO/HGOF复合材料、 乙炔黑(导电剂)和聚偏二氟乙烯(PVDF, 黏结剂)进行充分研磨; 将研磨好的混合物分散在适量的N-甲基吡咯烷酮溶剂中,磁力搅拌6 h; 将搅拌均匀的浆料均匀涂布在铜箔上, 转移至110 ℃真空干燥箱中, 12 h后, 取出, 裁成直径为12 mm的极片, 每片负载量为2 mg. 电化学测试使用的电池为CR2032型扣式电池, 该电池的正极是所制备的极片, 负极是纯锂片, 隔膜是PE, 电解液是1.0 mol/L LiPF6+ 碳酸乙酯/碳酸二甲酯(EC/DMC, 体积比1∶1), 在充满氩气的手套箱里组装成型. 使用电池测试系统进行充放电测试, 测试的电压范围为0.01~3 V(vs. Li/Li+), 循环性能的电流密度为100和500 mA/g, 倍率性能的电流密度为100,200, 400, 600, 800和1000 mA/g. 使用电化学工作站测量电池的阻抗谱(频率范围为105~10-2Hz)和循环伏安曲线(电压范围: 3~0.01 V, 扫描速率: 6~10 mV/s).
2 结果与讨论
2.1 XRD表征
图1为CoO/HGOF的XRD谱图, 可见, 主要的衍射峰36.4°, 42.37°, 61.39°, 73.5°和77.4°分别对应(111), (200), (220), (311)和(222) 晶面, 与立方相CoO(JCPDS No.71-1178, space group:Fd-3m)相匹配. 在26.66°和44.3°处出现的衍射峰属于还原石墨烯, 分别对应(002)和(111)晶面, 这表明合成的氧化石墨烯凝胶在煅烧的过程中含氧官能团大部分被去除, 转换成还原石墨烯. 通常, 根据石墨烯合成复合材料的XRD谱图中是否出现26.66°处这个衍射峰来衡量石墨烯是否发生了堆叠[5,8,10]. 本文制备的中空石墨烯纤维是由多层石墨烯片自卷曲形成, 此处, 26.66°处的衍射峰用来表示石墨烯纤维的特征峰. 在对XRD数据分析时发现44.3°处的衍射峰与C的标准卡片(JCPDS No.75-0410)匹配得很好, 而且在很多文献[8,13]中44.3°处的衍射峰都比较微弱, 而在一些纳米石墨管中衍射强度相对较强, 推测所制备的中空石墨烯纤维可能与碳纳米管具有相似的排列方式.
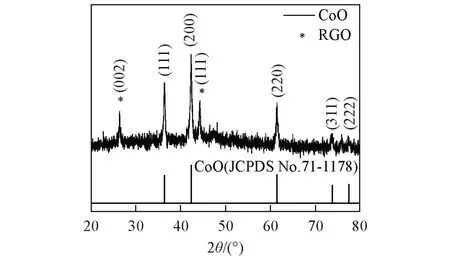
Fig.1 XRD pattern of CoO/HGOF composite
2.2 XPS表征
表1列出了CoO/HGOF各元素的质量百分含量, 可见, CoO/HGOF中Co的含量为7.00%, C的含量为75.33%.

Fig.2 XPS full survey spectrum of CoO/HGOF(A), Co2p(B), C1s(C) and O1s(D) high-resolution XPS spectra of CoO/HGOF
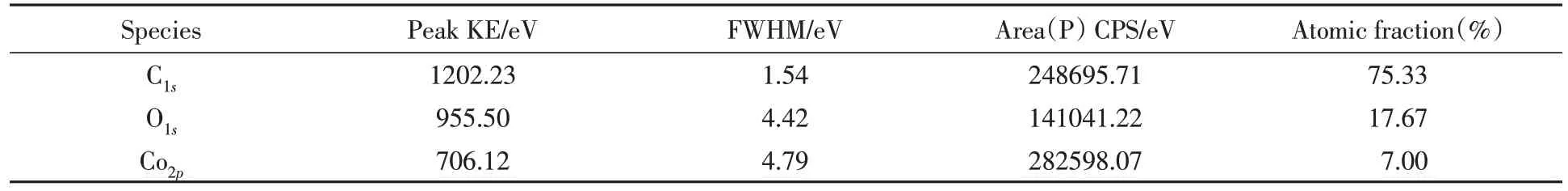
Table 1 Peak KE, FWHM, area(P) CPS and atomic fraction of CoO/HGOF*
2.3 SEM和TEM表征
从图3(A)可以看出, 石墨烯纤维是杂乱分散的, 相互之间交错搭建, CoO纳米颗粒是以抱团的形式搭载在石墨烯纤维上. 2D中空石墨烯纤维相互搭建成3D结构, 是贯穿整个材料体系的桥梁. 该3D结构为CoO提供了电子导电网络, 提高了材料的整体导电性. 从图3(B)也可以看出, 石墨烯构成的框架包裹住了CoO, 这有利于限制其在充放电循环过程中的体积膨胀. 图3(D)~(F)是根据SEM照片[图3(C)]测得的X射线能谱(EDS)元素分布图(mapping), 可见, 碳元素虽然分布均匀, 但是受到钴元素的影响并没有显现出很强的衍射信号. 钴、 氧元素离散地分布在石墨烯纤维间, 这种离散分散是相当重要的, 它能够使大部分晶面用于电化学反应, 提高锂储存.
图4为CoO/HGOF的TEM照片. 从图4(A)可见, 石墨烯纤维内部是中空结构的, 没有明显的CoO颗粒嵌入中空结构内; 黑色颗粒为CoO纳米颗粒. 石墨烯的纤维是自卷曲形成的, 理想状态下卷曲过程中会将纳米颗粒卷入到管内, 但是CoO纳米颗粒体积偏大, 无法卷入内部, 大部分附于纤维的外部. 不过仍然有部分被卷入管内[图4(B)], 嵌入管内的颗粒宽度为7 nm, 即石墨烯的中空结构的中空部分大概宽7 nm, 中空结构的一边宽14 nm, 整个石墨烯纤维大概宽21 nm. 嵌在中空管内的CoO晶格条纹以相同的取向进行生长, 晶格间距为0.14 nm, 在XRD谱图中并没有匹配到准确的晶面与其对应, 比较接近立方CoO结构的(220)晶面. 图4(C)显示石墨烯的晶格间距为0.249 nm, 并且石墨烯的晶格条纹是沿着相同的方向排列. 图4(D)~(F)是CoO纳米颗粒的高分辨率透射电子显微镜(HRTEM)照片, 其粒径大小约为50 nm, 有两种晶格条纹, 对应的晶面间距分别为0.148和0.128 nm, 分别对应立方CoO(220)和(311)晶面.

Fig.3 SEM images(A—C) and EDS elemental mappings C(D), O(E) and Co(F) of CoO/HGOF

Fig.4 TEM image of low-magnification full topography of CoO/HGOF(A), HRTEM images of CoO(B, D, E, F) and HGOF(C) embedded in graphene
2.4 电化学性能
图5(A)给出了CoO/HGOF在100 mA/g电流密度下的循环性能. 初始放电容量为793 mA·h/g, 首次库仑效率为72%, 对于过渡金属氧化物而言已经相当高了. 众所周知, 材料在首次放电过程的初始阶段会生成固态电解质(SEI)膜消耗一部分锂, 其有一定的机械稳定性, 如果材料不发生大的体积变化,产生的应力在SEI膜的承受范围之内, SEI膜完整性就不会被破坏. 低的首次库仑效率一般是由于材料体积不断膨胀, 表面的SEI膜被破坏, SEI膜的再生过程又会消耗大量的锂, 这个过程是不可逆的.CoO/HGOF只在首次充放电阶段容量有衰减, 主要是因为SEI膜的生成, 随后容量有一段上升的过程, 之后基本保持在800 mA·h/g, 经历了160次循环容量几乎没有衰减, 库仑效率保持在99%以上.图5(B)给出了CoO/HGOF的充放电曲线, 可见, 首次放电在0.75 V有一段很长的电压平台, 表示CoO还原生成金属Co纳米颗粒. 0.75~0.01 V电压曲线的倾斜是因为Li+嵌入到石墨烯层间, 该段的部分容量是由石墨烯贡献得到的. 在随后的循环过程中, 0.75 V处的电压平台上升到1.5~1 V, 这是由转换反应过程中CoO的颗粒尺寸发生了变化引起的[24]. 由于CoO纳米颗粒体积较大, 卷入管内的是小部分小颗粒的CoO. 管外的材料反应位点多, 接触电解液面积大, 电化学阻力比管内材料小, 与绝大部分的Li反应, 因此电化学性能大部分由管外材料贡献; 可以通过改变还原时间、 烧结温度等反应条件来调控纳米颗粒的大小.

Fig.5 Cycling performance at a current density of 100 mA/g(A) and voltage-capacity curves(B) of CoO/HGOF electrode material

Fig.6 CoO/HGOF rate performance(A) and cycling performance(B) of CoO/HGOF at a current density of 1000 mA/g

Fig.7 CV curves(A) and EIS spectrum(B) of CoO/HGOF
图6(A)给出了CoO/HGOF在不同电流密度下的倍率性能, 每个电流密度下的第5次循环容量分别为612, 638, 605, 567, 537和497 mA·h/g. 可以看出, 容量在不断增加的电流密度下并没有太大的变化, 表明CoO/HGOF具有优异的倍率性能. 从图6(B)也可见, 在1000 mA/g的电流密度下经历200次的循环, CoO/HGOF仍然保持超过300 mA·h/g的容量.
图7(A)给出了CoO/HGOF在6~10 mV/s不同的扫描速率下, 在0.01~3 V范围内进行的CV测试.可见, 10 mV/s扫描速率下, 既没有氧化峰也没有还原峰, 8~9 mV/s扫描速率下有微弱的氧化峰, 可能是由于石墨烯表面的电容效应[27]. 6 mV/s扫描速率下, 在0.53和1 V处能够发现两个明显的还原峰,对应CoO到金属Co的还原反应, 在2.3 V处的氧化峰对应Co0到CoO的氧化反应[30]. 图7(B)为CoO/HGOF的电化学阻抗谱(EIS), 可见, 有一个很低的溶液电阻(5 Ω), 表明电解液与材料的接触非常好,中空石墨烯内部可以作为电解液的运输管道, 直接输送到CoO颗粒表面, 极大提高了离子的传输速率, 在低频区的斜线进一步证明了材料有良好的扩散速率. 半圆对应的为电荷转移电阻, 只有105 Ω,说明石墨烯的存在提高了材料的导电性.
2.5 红外光谱分析
图8为氧化石墨烯负载CoO前后的红外光谱图, 复合材料在高温制备过程中, 钴原子与石墨烯基团上的碳原子产生新的共价键, 使二者的表面结合得更紧密. 3420 cm-1(曲线a)和3431 cm-1(曲线b)处分别为二氧化碳和水分子中氢键所产生的伸缩振动; 1720, 1620, 1402, 1084 cm-1(曲线a)和1621,1400, 1084 cm-1(曲线b)处分别为C=C, COO—, C=O键伸缩振动峰. 经还原后, 含氧官能团数被还原减少, 说明氧化石墨得到了有效还原.对比Co与石墨烯结合前后的红外谱图,曲线b较曲线a在波长为1620 cm-1处的峰强度变小, 且1720 cm-1处的肩峰消失, 可推测存在极性基团发生蓝移, 存在碳氧双键的伸缩振动, 另一峰的波长从1084 cm-1(曲线a)蓝移到1112 cm-1(曲线b), 为碳氧单键的振动. 由此可推测, 石墨烯与Co之间形成的是—COOM结构, —COO—Co、 氧原子与金属钴原子形成配位键, 紧密结合.

Fig.8 IR spectra of HGOF(a) and CoO/HGOF(b)
2.6 CoO/HGOF与其它材料的对比
由表2[34~36]可见, 将电流密度为100 mA/g的CoO/HGOF与500 mA/g的纳米晶状CoO/GNS复合材料进行对比, 其电容量与循环次数要优于CoO/GNS; 与电流密度为60 mA/g的CoO材料相比, 其循环次数和电容量比较理想; 与电流密度同为100 mA/g的卷曲石墨烯rGO材料相比, 其首次库仑效率、 循环次数和电容量都较为优异. 进一步说明CoO/HGOF有理想的首次库仑效率和循环稳定性能.

Table 2 Comparison of initial Columbic efficiency, cycle number and capacity of four different batteries
3 结 论
利用简单的超声辅助方法合成了CoO纳米颗粒/石墨烯纳米纤维复合材料, 其可作为锂离子电池的负极材料, 能以800 mA·h/g的稳定容量循环160次, 并且库仑效率仍保持在99%以上. 研究发现, 其高的电化学性能可以归功于以下几个方面: (1) 石墨烯纤维能够搭建成3D骨架结构, 提高了材料的整体稳定性; (2) 3D骨架对CoO纳米颗粒的限制有效缓解了反应过程中的体积膨胀; (3) 中空石墨烯纤维的中空结构提供了电解液的流动通道, 大大提高了离子传输速率, 纤维结构传输电子, 提高了材料的电导率. 中空石墨烯纤维有望在其它过渡金属氧化物领域得到普适性的应用.
