2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物在白及质量控制中的应用研究
2023-02-21刘金梅穆开朗刘育辰孙庆文张永萍
刘 刚,刘金梅,穆开朗,刘育辰,孙庆文,张永萍
2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物在白及质量控制中的应用研究
刘 刚,刘金梅#,穆开朗,刘育辰*,孙庆文,张永萍
贵州中医药大学,贵州 贵阳 550025
建立以2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物为对照的白及质量控制方法。采用ZORBAX Eclipse Plus C18(100 mm×2.1 mm,1.8 μm)色谱柱,流动相为0.05%磷酸水溶液(A)- 乙腈(B),梯度洗脱,柱温35 ℃,体积流量0.15 mL/min,进样体积为2 μL,检测波长为220 nm。分别采用对照品法和对照提取物法测定17批白及饮片中1,4-二[4-(葡萄糖氧)苄基]-2-异丁基苹果酸酯-2-葡萄糖苷(2--葡萄糖基白及苷)、1-[4-(葡萄糖氧)苄基]-2-异丁基苹果酸酯(手参苷Ⅰ)、1,4-二[4-(葡萄糖氧)苄基]-2-异丁基苹果酸-2-(6--乙酰基) 葡萄糖苷(手参苷Ⅲ)、1,4-二[4-(葡萄糖氧)苄基]-2-异丁基苹果酸酯(白及苷)4个成分的含量,并进行比较。2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物中2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷线性关系良好(≥0.999 9),进样精密度RSD值在0.001%~0.58%,重复性RSD值在0.27%~0.53%,4种成分的加样回收率在98.42%~101.53%,样品溶液在24 h内各成分稳定性良好。两种方法测定结果进行检验,>0.05,说明两种方法无显著差异,两种检测方法结果具备一致性。验证了2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物可代替单体对照品的可行性,可应用于白及及其制剂的质量控制研究。
白及;2-异丁基苹果酸葡萄糖氧基苄酯类;对照提取物;质量控制;2--葡萄糖基白及苷;手参苷Ⅰ;手参苷Ⅲ;白及苷
白及为兰科植物白及(Thunb.) Reiehb. f.的干燥块茎,具有收敛止血、消肿生肌的功效[1]。白及中主要含有白及多糖、2-异丁基苹果酸葡萄糖氧基苄酯类、联苄类、菲类、黄酮类、苯丙素类、甾体、三萜等成分[2-6]。近年来许多学者对白及质量控制技术方法进行了研究和探索,从单一指标成分定量测定到多指标成分定量测定结合指纹图谱等[7-9]这些研究成果无疑对白及质量评价和控制水平的提高起到了极大的促进作用,但是仍存在的对照品价格贵、不易得、检测成本高,质控指标与药效关联性不强等问题。
《中国药典》2020年版首次以1,4-二[4-(葡萄糖氧)苄基]-2-异丁基苹果酸酯(白及苷)作为单一指标成分进行定量测定,白及苷为2-异丁基苹果酸葡萄糖氧基苄酯类化合物,除白及多糖成分外,此类化合物是白及中主要成分[10-12],除了白及苷,此类成分中其他几个化合物均难以获得。由于中药成分的多样性,仅以单一成分作为检测指标的检测方法,其专属性远低于多指标检测方法,且也无法体现中药整体性概念。而使用对照提取物作为标准物质,相对于难获得、高成本的单体对照品而言,其制备工艺更简便易行。同时,使用对照提取物代替单一对照品可以实现同时测定多个成分的含量,更能反映中药的整体质量[13-15]。
对照提取物系指经特定提取工艺制备的含有多种主要有效成分或指标性成分,用于中药材(饮片)、提取物、中成药等鉴别或含量测定用的国家药品标准物质[16]。同时,规定对照提取物选取应从基原明确的中药材(饮片)或其他动植物中提取获得[17]。对照提取物相比单一对照品制备方法更简单、检测成本更低、适用性更好[18]。
在前期的研究中,本课题组优选了2-异丁基苹果酸葡萄糖氧基苄酯类白及对照提取物的制备工艺,对照提取物中1,4-二[4-(葡萄糖氧)苄基]-2-异丁基苹果酸酯-2-葡萄糖苷(2--葡萄糖基白及苷)、1-[4-(葡萄糖氧)苄基]-2-异丁基苹果酸酯(手参苷Ⅰ)、1,4-二[4-(葡萄糖氧)苄基]-2-异丁基苹果酸-2-(6--乙酰基) 葡萄糖苷(手参苷Ⅲ)、1,4-二[4-(葡萄糖氧)苄基]-2-异丁基苹果酸酯(白及苷)4个成分总含量超过70%,符合对照提取物的要求[19],本研究以2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物为对照,应用于白及药材的质量控制,试图构建高效、易行、科学的白及质量评价新模式。
1 仪器与试药
1.1 仪器
超高效液相色谱仪(Agilent 1290 infinity II,美国Agilent公司);FA2204B型电子天平(上海天美天平仪器有限公司);AG135型电子天平(瑞士Mettler-Toledo公司)。
1.2 试药
乙腈为色谱纯(美国TEDIA公司);其他试剂均为分析纯;纯净水(贵阳娃哈哈食品有限公司);硅胶GF254薄层板(青岛谱科分离材料有限公司,批号20210717);PRP-512B型反相树脂(北京聚福树脂厂)。白及苷(批号CHB180528)购于成都克洛玛生物科技有限公司;手参苷Ⅲ(批号PRF10102503)购于成都普瑞法科技开发有限公司,质量分数均大于98%;手参苷Ⅰ和2--葡萄糖基白及苷由本实验室从白及中分离得到,质量分数均大于98%。17批不同来源的白及饮片经贵州中医药大学孙庆文教授鉴定为兰科植物白及(Thunb.) Reichb. f.,详细信息见表1。
2 方法与结果
2.1 2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物的制备
精密称取白及粉末(过三号筛),按1∶40料液比加入55%乙醇,超声(功率344 W、频率40 kHz)提取56 min,滤过,取上清液减压浓缩,得药材浸膏;按浸膏与PRP-512B型反相树脂1∶150比例称取PRP-512B型反相树脂做好预处理(用95%的乙醇浸泡24 h后装柱,使填料占总柱长约1/2,用95%乙醇冲洗至流分与水1∶5混合不浑浊,再用水洗至流分不含醇,即可),干法上样,以水(3个柱体积)、20%乙醇(2个柱体积)、40%乙醇(3个柱体积)进行梯度洗脱,收集40%乙醇段的流分,减压浓缩,真空干燥得对照提取物。
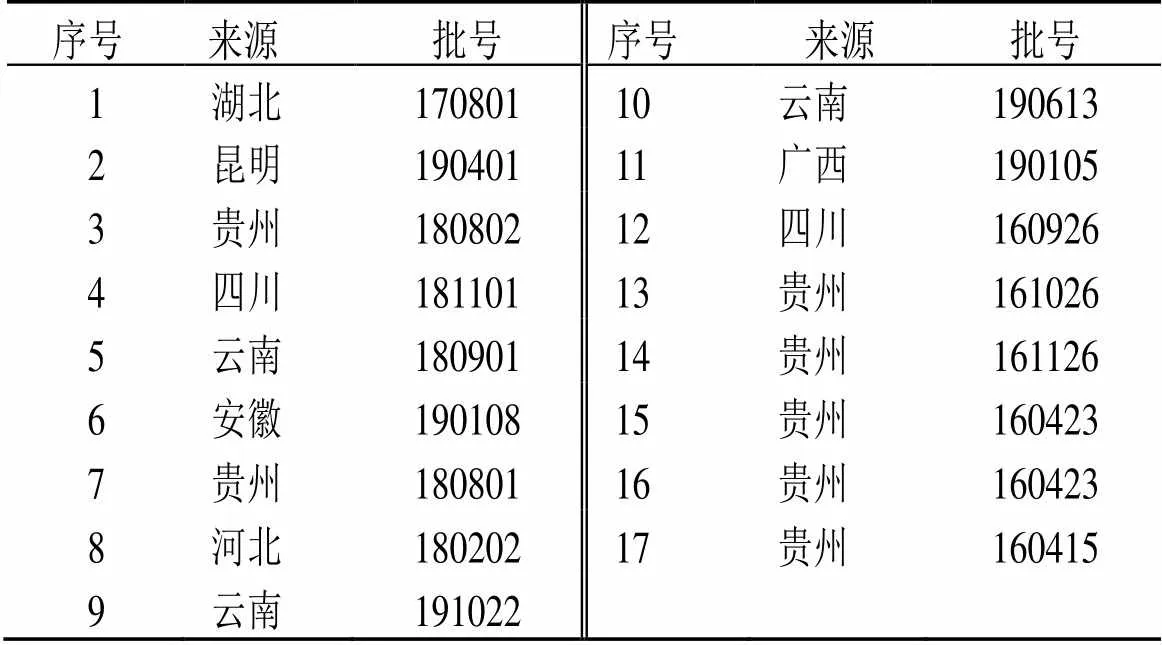
表1 17批白及饮片来源信息
2.2 2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物的标定
以2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷对照品为对照,测定白及对照提取物中4个2-异丁基苹果酸葡萄糖氧基苄酯类化合物的含量。
2.2.1 色谱条件 ZORBAX Eclipse Plus C18(100 mm×2.1mm,1.8 μm)色谱柱;流动相为0.05%磷酸水溶液(A)- 乙腈(B);梯度洗脱,洗脱程序:0~2 min,18%~20% B;2~3 min,20%~20% B;3~6 min,20%~22% B;6~7 min,22%~23% B;7~9 min,23%~24% B;9~12 min,24%~26% B;12~16 min,26%~28% B;16~20 min,28%~100% B;20~24 min,100% B;进样量2 μL;体积流量0.15 mL/min;柱温35 ℃;检测波长220 nm。混合对照品、饮片和白及对照提取物色谱图见图1。
2.2.2 混合对照品溶液的配制 分别精密称取2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷对照品适量,加50%乙醇溶解,配制成质量浓度分别为0.200 4、0.400 0、0.105 0、1.210 0 mg/mL的混合对照品溶液A。
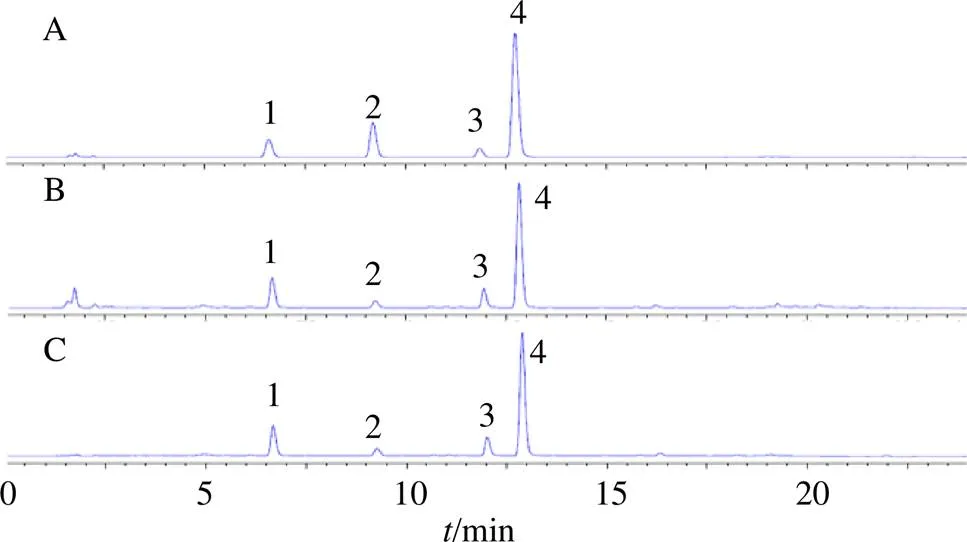
1-2-O-葡萄糖基白及苷 2-手参苷Ⅰ 3-手参苷Ⅲ 4-白及苷
2.2.3 对照提取物供试品溶液配制 精密称取白及对照提取物5.12 mg,置10 mL量瓶中,加50%乙醇溶解并定容至刻度、摇匀,经0.22 μm微孔滤膜滤过,取续滤液,即得供试品溶液。
2.2.4 线性关系考察 将上述混合照品溶液A分别稀释10倍、50倍得到混合对照品溶液B、C;按“2.2.1”项下色谱条件,混合对照品溶液A分别进样1、2、3、4、5 µL,混合对照品溶液B分别进样1、3、5 µL,混合对照品溶液C分别进样1、2、3 µL,测定各成分的峰面积,以各成分的进样量为横坐标(),峰面积为纵坐标(),绘制标准曲线,得回归方程:相关系数()均大于0.999 9,线性关系良好,结果见表2。
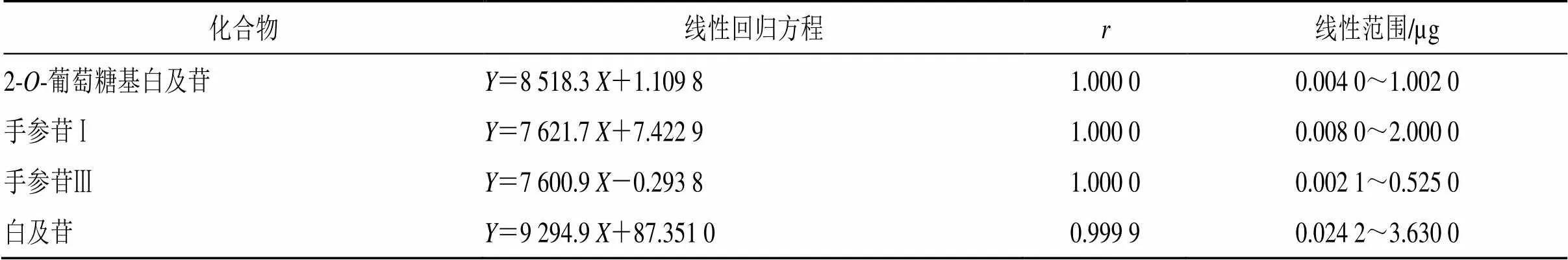
表2 4个指标成分的回归方程及线性范围
2.2.5 精密度试验 精密吸取“2.2.2”项下的混合对照品溶液,按“2.2.1”项下色谱条件连续进样6次,测定2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷的峰面积,计算峰面积的RSD值,结果分别为0.13%、0.20%、0.38%、0.11%,表明仪器精密度良好。
从香港到东莞,已有46年历史的金杯印刷一直坚守着要成为绿色印刷先驱的使命,并化身为“大使”,毫无保留传授己身经验。
2.2.6 重复性试验 取白及对照提取物按“2.2.3”项下方法平行制备6份白及对照提取物供试品溶液,按照“2.2.1”项下色谱条件进样,记录峰面积。计算供试品溶液中2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷的质量分数,其平均值分别为15.21%、4.47%、9.50%、58.22%,RSD值分别为1.08%、1.26%、1.08%、0.91%。
2.2.7 稳定性试验 按“2.2.3”项下方法制备白及对照提取物供试品溶液1份,按照“2.2.1”项下色谱条件,分别于0、2、6、8、10、24 h进样测定,记录峰面积。计算供试品溶液中2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷的峰面积的RSD值,分别为0.35%、0.14%、0.39%、0.28%,表明供试品溶液在24 h内稳定性良好。
2.2.8 加样回收率试验 取同一批已知含量的白及对照提取物5.25 mg,精密称定,置10 mL量瓶中,平行6份,分别精密加入不同浓度的2--葡萄糖基白及苷(0.767 00 mg/mL)、手参苷Ⅰ(0.220 0 mg/mL)、手参苷Ⅲ(0.484 80 mg/mL)、白及苷(2.984 00 mg/mL)对照品溶液各1 mL,再加入50%乙醇定容至刻度,摇匀,经0.22 μm微孔滤膜滤过。按“2.2.1”项下的色谱条件进样,记录各成分峰面积,计算2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷的加样回收率分别为97.16%、97.78%、104.10%、96.10%,RSD分别为2.23%、2.99%、2.02%、1.17%,表明该方法准确度良好。
2.2.9 2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物标定结果 取9批白及对照提取物,按“2.2.3”项下制备供试品,取适宜供试品按“2.2.1”项下色谱条件进样检测,测定9批白及对照提取物中2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷,含量结果见表3,4个指标成分的含量之和均大于70%,9批对照提取物的平均值为81.95%,说明该制备方法具备良好的稳定性和可重复性。
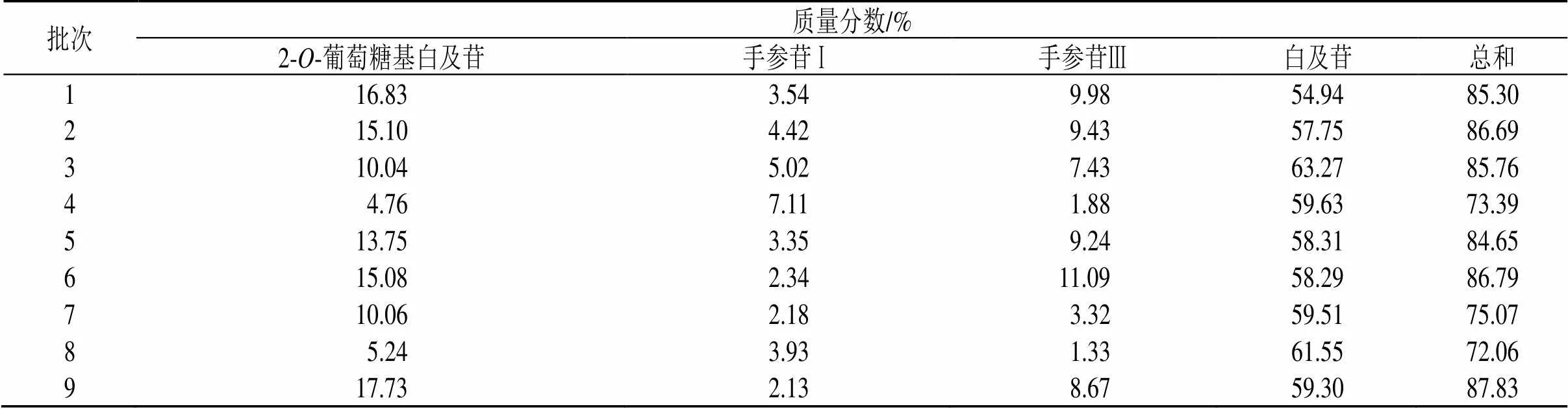
表3 9批对照提取物含量标定
2.3 对照提取物在白及饮片质量控制中的应用
以2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物为对照,测定白及饮片中2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷共4个成分的含量,并与单体对照品测得的结果进行比较,考察对照提取物用于饮片质量控制的科学性和可行性。
2.3.1 薄层鉴别 取白及饮片粉末(过三号筛)0.20 g,加入50%乙醇10 mL,超声处理(功率400 W、频率40 kHz)30 min,滤过,滤液蒸干,残渣加入1 mL甲醇溶解,作为供试品溶液。取白及2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物配制成33 mg/mL的溶液。对照薄层色谱法(通则0502)试验。吸取供试品溶液、对照提取物溶液各5 μL,分别点于同一硅胶GF254薄层板上,以三氯甲烷-甲醇-甲酸-水(6.5∶3.5∶0.1∶1)下层为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105 ℃加热至斑点显色清晰。供试品色谱中,在与对照提取物色谱相应的位置上,显相同颜色的斑点。
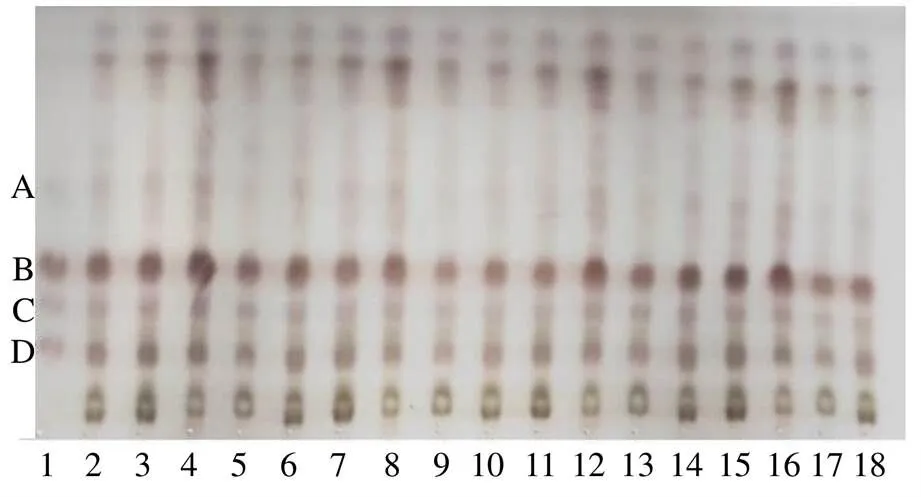
1-对照提取物(A-手参苷Ⅰ B-白及苷 C-手参苷Ⅲ D-2-O-葡萄糖基白及苷) 2~18-不同批次白及饮片
2.3.2 含量测定
(1)对照提取物溶液制备:精密称取白及对照提取物5.12 mg,置10 mL量瓶中,加50%乙醇溶解并定容至刻度,摇匀,制成2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷质量浓度分别为0.079 9、0.023 1、0.049 5、0.302 0 mg/mL的对照提取物溶液A;将上述对照提取物溶液A分别稀释10、50倍,作为白及对照提取物溶液B、C。
(2)白及饮片供试品溶液制备:取白及饮片粉末约0.20 g,精密称定,置具塞锥形瓶中,精密加入50%乙醇溶液10 mL,称定质量,超声(400 W、40 kHz)处理30 min,放冷。再称定质量,用50%乙醇补足减失的质量,摇匀,将提取液经0.22 µm微孔滤膜滤过,取续滤液,即得供试品溶液。
(3)色谱条件:同“2.2.1”项下的色谱条件。
(4)线性关系考察:将“(1)”项下的对照提取物溶液A分别进样1、2、3、4、5 µL;对照提取物溶液B分别进样1、2 µL;对照提取物溶液C进2 µL;以进样量为横坐标(),峰面积为纵坐标(),绘制标准曲线,得回归方程:相关系数()均大于0.999 9,线性关系良好,结果见表4。

表4 4个指标成分的回归方程及线性范围
(5)精密度试验:精密吸取“(1)”项下的对照提取物溶液,按“2.2.1”项下色谱条件连续进样6次,测定2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷的峰面积,计算峰面积的RSD,结果分别为0.28%、0.32%、0.58%、0.001%,表明仪器精密度良好。
(6)稳定性试验:取白及饮片粉末,按“(2)”项下的方法制备供试品溶液,按“2.2.1”项下色谱条件,分别于0、2、6、8、24、48 h进样测定,记录峰面积。计算供试品溶液中2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷的峰面积RSD,分别为0.66%、0.66%、0.67%、0.35%,表明供试品溶液在48 h内稳定。
(7)重复性试验:取同一批白及饮片粉末,按“(2)”项下方法制备6份供试品溶液,按“2.2.1”项下色谱条件进样,记录峰面积。计算供试品溶液中2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷的质量分数,其平均值分别为5.03、1.39、3.55、19.95 mg/g,RSD分别为0.48%、0.27%、0.53%、0.30%,表明该方法重复性良好。
(8)加样回收率试验:取已知含量的同一批白及饮片粉末约0.10 g,精密称定,置于10 mL具塞锥形瓶中,精密加入50%乙醇溶液9 mL,称定质量,超声(400 W,40 kHz)处理30 min,放冷。再称定质量,用50%乙醇补足减失的质量,再精密加入配制好的白及对照提取物溶液1 mL,摇匀,平行制备6份。按“2.2.1”项的色谱条件进样,计算2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷的加样回收率分别为101.53%、98.42%、101.44%、99.59%;RSD分别为1.06%、1.25%、1.47%、0.75%。表明该方法准确度良好。
(9)白及饮片含量测定:取17批购买的白及饮片,精密称定,按“(2)”项下方法制备白及供试品溶液,按“2.2.1”项色谱条件,进样测定峰面积,分别采用白及对照提取物法和单体对照品法计算样品中的(2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷)4个成分的含量,结果见表5。
根据表5中的结果,取2种方法测定的不同来源饮片中4个成分含量及4个成分含量总和的平均值(对照提取物法:0.60%、0.21%、0.35%、3.10%、4.26%;单体对照品法:0.57%、0.20%、0.32%、2.94%、4.04%),用SPSS 25.0进行配对样本检验,在配对样本相关性结果中<0.05,两组数据有显著的相关性,可进行配对检验。由配对样本检验的结果知=0.102,>0.05,说明两组数据无显著差异,两种检测方法结果具备一致性,进一步验证了白及对照提取物可替代单体对照品进行白及饮片含量测定的可行性。
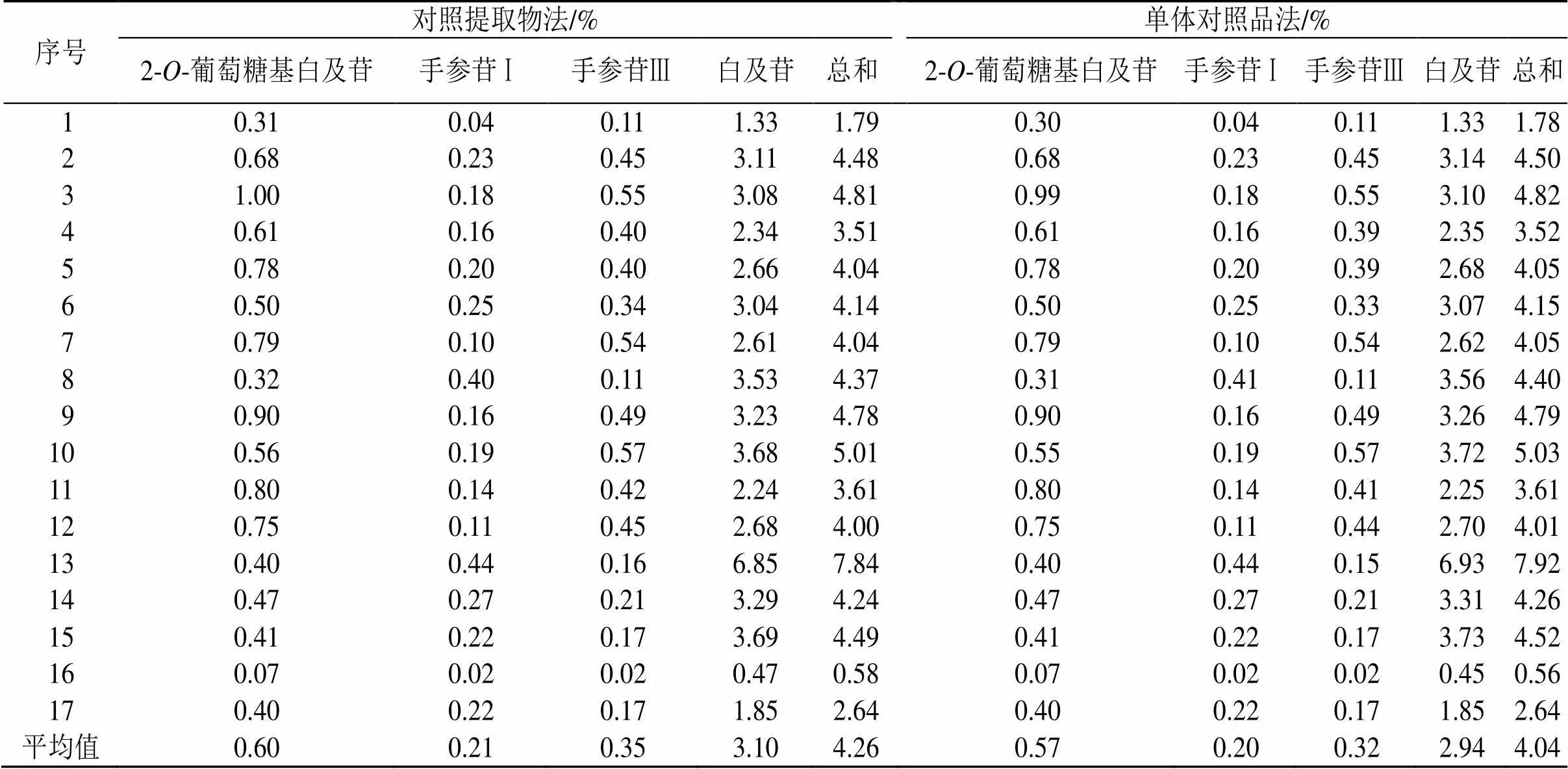
表5 17批白及饮片含量测定
3 讨论
本实验考察供试品和对照品在相同条件下使用不同展开系统的分离情况。分别考察三氯甲烷-甲醇-甲酸(3∶1∶0.1)、二氯甲烷-甲醇-甲酸(2.5∶1∶0.5)、乙酸乙酯-甲醇-甲酸(4∶1∶0.1)、三氯甲烷-甲醇-水(6.5∶3.5∶1)下层、三氯甲烷-甲醇-甲酸-水(6.5∶3.5∶0.1∶1)下层等5个展开剂下分离的情况。结果显示以三氯甲烷-甲醇-甲酸-水(6.5∶3.5∶0.1∶1)下层为展开剂的分离效果最好。此外,还考察不同硅胶薄层板对供试品和对照品分离效果的影响。取硅胶G薄层板、硅胶GF254薄层板、硅胶H薄层板、硅胶HF254薄层板在相同条件下对样品进行展开,结果以硅胶GF254薄层板分离效果最好。
本实验考察了乙腈-0.1%磷酸水、乙腈-0.2%磷酸水、乙腈-0.05%磷酸水、乙腈-0.05%甲酸水、乙腈-0.05%醋酸水、乙腈-水、甲醇-0.05%磷酸等流动相系统,结果表明,乙腈-0.05%磷酸水溶液为流动相梯度洗脱时色谱峰峰形较好,分离较好。考察了UPLC色谱柱在25、30、35 ℃温度下各成分的分离效果,结果显示在35 ℃下各个色谱峰分离较好。考察了在0.3、0.2、0.12、0.15、0.1、0.08 mL/min下各成分间的分离效果,结果显示在0.15 mL/min下各个色谱峰分离较好。
白及药材经过超声提取,经过一次柱色谱即可制备得到符合标准的以4个(2--葡萄糖基白及苷、手参苷Ⅰ、手参苷Ⅲ、白及苷)2-异丁基苹果酸葡萄糖氧基苄酯类成分作为总控成分的对照提取物。对照提取物制备简单,相对于单体化合物的制备节约了成本和时间。在对照提取物与单体对照品就含量测定结果的验证中,其两者结果经统计分析发现具有高度一致性,说明将制备得到的对照提取物,作为白及药材含量的测定指标具有可行性。在白及质量评价研究中,对照提取物法的操作步骤更为简便,在一定程度上降低了操作误差,其重复性及可靠性更高。
药物或组分的有效性是临床应用的基本要求,有研究报道2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物中的白及苷还具有改善慢性脑缺血大鼠的认知功能障碍及减轻脑白质缺血性损伤[20]、体外抗炎活性[21]、对PM 2.5诱导的BV-2细胞损伤有保护作用[22];2--葡萄糖基白及苷对HIV有潜在的抑制作用[23];手参苷Ⅰ还可缩短肝素化小鼠的出血时间和凝血时间[24]。综上,制备得到的2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物可代替单体化合物作为对照品进行含量测定的基础上,还可与安全性、有效性密切相关,可为后期开发应用及临床应用奠定基础。
基于2-异丁基苹果酸葡萄糖氧基苄酯类对照提取物建立的白及UPLC含量测定方法,可为白及质量控制评价方法进一步的完善提供参考。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典 [S]. 一部. 2020: 106-107.
[2] 孙爱静, 庞素秋, 王国权. 中药白及化学成分与药理活性研究进展 [J]. 环球中医药, 2016, 9(4): 507-511.
[3] 刘金梅, 安兰兰, 刘刚, 等. 白及化学成分和药理作用研究进展与质量标志物预测分析 [J]. 中华中医药学刊, 2021, 39(6): 28-37.
[4] 刘成才, 饶春梅, 宋昌俊, 等. 种植方式与栽培措施对白及产量和有效成分含量的影响研究 [J]. 中草药, 2021, 52(21): 6669-6676.
[5] 陈长芬, 蒋赛, 娄华勇, 等. 黔产白及中糖苷类化学成分研究 [J]. 中草药, 2019, 50(20): 4879-4883.
[6] 李正坤, 王铭爽, 刘传鑫, 等. 基于UPLC指纹图谱考察云贵产地白及药材大小与化学成分含量的关系 [J].药物评价研究, 2021, 44(3): 504-511.
[7] 黄良永, 毛闪闪, 陈黎. HPLC测定不同产地白及药材中1, 4-二[4-(葡萄糖氧)苄基]-2-异丁基苹果酸酯的含量 [J]. 现代中药研究与实践, 2013, 27(5): 16-19.
[8] 王爱民, 鄢艳, 兰波, 等. UPLC同时测定白及药材中9种指标成分的含量 [J]. 中国中药杂志, 2014, 39(11): 2051-2055.
[9] 刘刚, 丁志山, 刘育辰, 等. 白及药材的HPLC指纹图谱建立及聚类分析 [J]. 中国药房, 2018, 29(22): 3050-3053.
[10] 段营辉, 黄澜, 朱樵苏, 等. 基于液质联用法对白及中2-异丁基苹果酸葡萄糖氧基苄酯类成分的定性定量分析 [J]. 中国医院药学杂志, 2020, 40(9): 1009-1013.
[11] 刘金梅, 刘刚, 刘育辰, 等. 基于UPLC-Q-TOF/MS技术分析白及中的化学成分 [J]. 中华中医药学刊, 2022, 40(4): 72-76.
[12] 李丽敏. 白及中白及苷在大鼠体内代谢产物及药代动力学研究 [D]. 上海: 上海中医药大学, 2019.
[13] 鲁静, 付凌燕, 戴忠, 等. 定量用三七总皂苷对照提取物的协作定值 [J]. 中国药品标准, 2012, 13(3): 199-202.
[14] 何风艳, 戴忠, 马双成. 西红花苷对照提取物用于双红活血胶囊的质量控制研究 [J]. 药物分析杂志, 2016, 36(12): 2204-2208.
[15] 黄琴伟, 赵维良, 严爱娟, 等. 对照提取物在银杏叶制剂特征图谱中的应用 [J]. 医药导报, 2017, 36(7): 794-797.
[16] 陈沛, 金红宇, 孙磊, 等. 对照提取物在中药整体质量控制中的应用 [J]. 药物分析杂志, 2016, 36(2): 185-195.
[17] Zöllner T. Herbal Reference Standards: Applications, definitions and regulatory requirements [J]., 2013, 23(1): 1-21.
[18] 戴宇, 邓赟, 宋川霞, 等. 对照提取物的国内外发展研究概况 [J]. 中药与临床, 2015, 6(4): 49-53.
[19] 国家药品标准工作手册[S]. 第四版. 2013: 453.
[20] Luo Y, Diao H J, Xia S H,. A physiologically active polysaccharide hydrogel promotes wound healing [J]., 2010, 94(1): 193-204.
[21] 吴梅, 田守征, 郑永仁, 等. 白及苦味成分的分离、鉴定及抗炎药效学初研 [J]. 时珍国医国药, 2019, 30(2): 372-374.
[22] Tian S X, Cheng W, Lu J J,. Role of militarine in PM2.5-induced BV-2 cell damage [J]., 2021, 46(6): 1423-1434.
[23] Kumar Bhardwaj V, Purohit R, Kumar S. Himalayan bioactive molecules as potential entry inhibitors for the human immunodeficiency virus [J]., 2021, 347: 128932.
[24] 赵菲菲, 李靖, 徐国波, 等. 白及非多糖组分止血活性成分研究 [J]. 天然产物研究与开发, 2021, 33(3): 426-432.
Study on application of glucosyloxybenzyl 2-isobutylmalates reference extract in quality control of
LIU Gang,LIU Jin-mei, MU Kai-lang, LIU Yu-chen, SUN Qing-wen, ZHANG Yong-ping
Guizhou University of Traditional Chinese Medicine, Guiyang 550025, China
To establish of a quality control method forwith glucosyloxybenzyl 2-isobutylmalates reference extract as a control.A ZORBAX Eclipse Plus C18(100 mm×2.1 mm, 1.8 μm) column was used with the mobile phase of 0.05% phosphoric acid aqueous solution (A)-acetonitrile (B), gradient elution, column temperature of 35oC, flow rate of 0.15 mL/min, injection volume of 2 μL, detection wavelength of 220 nm. The contents of dactylorhin A, gymnoside I, gymnoside III and militarine in 17 batches oftablets were determined by the control method and the control extract method, respectively, and compared.The linearity of dactylorhin A, gymnoside I, gymnoside III and militarine in the reference extract of glucosyloxybenzyl 2-isobutylmalates was good (≥0.999 9), the precision of the injection RSD values were in the range of 0.001%—0.58%, the reproducibility RSD values were in the range of 0.27%—0.53%. The recoveries of the four components ranged from 98.42% to 101.53%, and the stability of the sample solutions was good within 24 h. The results of the two methods were determined by-test,>0.05, indicating that there was no significant difference between the two methods and the results of the two assays were consistent.This study verified the feasibility of glucosyloxybenzyl 2-isobutylmalates reference extract as a substitute for the monomeric control, which can be applied to quality control studies ofand its preparations.
(Thunb.) Reiehb. f.; glucosyloxybenzyl 2-isobutylmalates; reference extract; quality control; militarine;gymnoside I; militarine; gymnoside III; dactylorhin A
R286.12
A
0253 - 2670(2023)04 - 1260 - 07
10.7501/j.issn.0253-2670.2023.04.027
2022-08-09
国家自然科学基金项目(U1812403);贵州省科技计划项目(黔科合基础[2019]1027号);国家公益性行业科研专项经费项目(201507002)
刘 刚(1979—),男(汉族),吉林白城人,高级实验师,硕士研究生导师,研究方向为中药资源学和中药鉴定学。E-mail: liugang888_2000@163.com
刘育辰(1982—),女(汉族),吉林长春人,教授,博士,硕士研究生导师,研究方向为中药及民族药资源分类鉴定与质量控制。E-mail: lyc8564732@163.com
#共同第一作者:刘金梅(1997—),女(苗族),贵州贞丰人,硕士研究生,研究方向为中药及民族药化学及中药新药的研究。E-mail: 1943456442@qq.com;
[责任编辑 时圣明]
