聚合工艺对聚吡咯改性石墨毡电极结构及其氧还原性能的影响
2023-02-16郭华珍唐思扬钟山吴潘蒋炜吴可荆刘长军鲁厚芳梁斌
郭华珍,唐思扬,钟山,吴潘,蒋炜,吴可荆,刘长军,鲁厚芳,,梁斌,
(1.四川大学 化学工程学院,四川 成都 610207;2.四川大学 新能源与低碳技术研究院,四川 成都 610207)
H2O2在工业中应用广泛[1-4],就地生产避免了H2O2的运输储存,可降低使用成本和危险[5]。酸性溶液中,O2经2电子还原可生成H2O2,要提高其选择性需抑制4电子还原和析氢反应,减少分解。
碳纤维在电极中应用广泛,但其电化学活性低,电化学活性表面积小。氮原子掺杂可提高碳材料的电化学活性[6-10],促进H2O2生成[11-13]。吡咯氮具有优异的2电子氧还原催化活性。通过聚吡咯改性,引入吡咯氮对提高碳材料的电化学活性具有重要应用价值[14-15]。聚合条件对聚吡咯膜厚度与形貌有显著影响[16]。本文对电化学聚合法调控石墨毡(GF)表面聚吡咯结构和性能进行了系统研究。
1 实验部分
1.1 材料与仪器
无水乙醇、过氧化氢、硫酸钠、铁氰化钾、草酸钛钾、吡咯均为分析纯;实验室用水为超纯水;石墨毡(厚度5 mm);甘汞电极R0232;铂网电极Pt310(10 mm×10 mm)。
CHI660E型电化学工作站;UV-1500PC型紫外可见分光光度计;D07型气体质量流量计;D08-1F型流量显示仪;PHIBJ-260型pH计;KQ5200DE型超声波清洗仪;LX-705B型接触角测量仪;JEOL JSM7610F型扫描电子显微镜;iS50型红外光谱仪。
1.2 聚吡咯改性石墨毡电极的制备
石墨毡裁剪成2 cm×2 cm,分别经无水乙醇和超纯水超声清洗1 h,在60 ℃真空干燥8 h。
电化学聚合吡咯改性石墨毡在三电极无隔膜电解池中进行,工作液为50 mL含0.05 mol/L的硫酸钠和0.2 mol/L的吡咯的水溶液。在机械搅动下,以经过预处理的石墨毡为阳极,10 mm×10 mm铂网电极为阴极,在0.01 A的恒电流条件下进行电化学聚合。聚合时间(t1)、脉冲间隔时间(t2)以及脉冲次数(n)根据具体实验要求进行设定。聚合反应结束后,用去离子水将石墨毡电极冲洗干净,干燥后,得到聚吡咯改性石墨毡n(t1-t2)-GF。
1.3 结构形貌表征
石墨毡改性前后的表面形貌结构通过扫描电子显微镜获取;表面的官能团组成通过傅里叶变换红外光谱仪获得,样品由0.12 g干燥的KBr和0.01 g样品经研磨混合后压片制得。石墨毡电极材料的亲疏水性能由接触角测定仪测定。
1.4 电化学性能测定
1.4.1 循环伏安(CV)测试 在电解液中通10 min氧气,使溶解氧饱和,测试中以100 mL/min的流量持续往电解液中鼓入氧气,扫描范围为-1.4~0 V(vs.SCE,除特别说明外,均为相对SCE电极的电势),扫描速率为50 mV/s。
1.4.2 电化学活性比表面积测定 以K3[Fe-(CN)6]为探针分子,在三电极体系中进行循环伏安扫描所得峰电流(Ip,A),通过Randles-Sevcik方程计算得到。设定AV为单位体积石墨毡的电化学活性比表面积(cm2/cm3);VG为测试所用的石墨毡电极体积(2.0 cm3);则电化学活性面积A=AVVG(cm2)。电化学活性比表面积按照式(1)计算得到。测试的电解液为0.01 mol/L K3[Fe(CN)6]和 1.0 mol/L KCl 的混合电解质溶液,扫描速度为 10 mV/s,扫描范围为-0.3~0.8 V。
IP=2.69×102×AVVGD1/2n3/2γ1/2C
(1)
式中D——探针分子的扩散系数,在测试条件下为7.6×10-6cm2/s;
n=1——电极反应的电子传递数;
γ——电势扫描速度,10 mV/s;
C——探针分子的浓度,10-5mol/cm3。
1.4.3 氧还原活性测试 利用电化学工作站,以石墨毡样品为工作电极,铂网为对电极,以标准甘汞电极(SCE)为参比电极,0.05 mol/L的Na2SO4溶液为电解液构建三电极测试系统进行电极的氧还原活性测试。测试前,通10 min氧气使溶解氧饱和,测试中氧气以100 mL/min的流量由3 mm外径的聚四氟乙烯管以鼓泡的方式持续通至工作电极附近。阴极电势通过电化学工作站控制,并恒定为-0.45 V,每隔30 min从电解池中取1.4 mL样品,通过草酸钛钾分光光度法测定其中的H2O2浓度,并且根据式(2)计算电流效率(CE)。
(2)
式中n=2——生成过氧化氢所需的电子转移数;
F——法拉第常数,96 486 C/mol;
CH2O2——电解液中H2O2的浓度,mol/L;
i——电流,A;
t——反应时间,s。
2 结果与讨论
2.1 聚吡咯改性对石墨毡纤维表面结构的影响
2.1.1 SEM 聚吡咯改性前后石墨毡纤维表面形貌见图1。
由图1可知,未改性的石墨毡纤维表面光滑,纤维直径约为20 μm;聚吡咯改性的石墨毡纤维外壁均匀包覆了一定厚度的聚吡咯层。聚吡咯壳层与石墨毡纤维贴合紧密,但强的外力作用可使石墨纤维断裂,聚吡咯壳层碎裂,并从石墨毡纤维剥离。聚吡咯壳层的厚度随着聚合时间的延长而增厚,当聚合时间从500 s延长至1 000 s时,厚度相应从 240 nm 增大到640 nm。脉冲间隔时间的延长,会提高聚吡咯壳层的厚度,当脉冲间隔时间从60 s延长至120 s时,聚吡咯壳层厚度从400 nm增大到640 nm。

图1 石墨毡样品的SEM图Fig.1 SEM images of graphite felt a.GF;b.1(1 000 s-0 s)-GF;c、d.10(50 s-120 s)-GF;e.10(100 s-120 s)-GF;f.10(100 s-60 s)-GF
2.1.2 FTIR 未改性GF、1(1 000 s-0 s)-GF和10(100 s-60 s)-GF的红外光谱见图2。
(6a)The man(who ordered sandwich)is getting restless.

图2 GF、1(1 000 s-0 s)-GF、10(100 s-60 s)-GF 的FTIR图Fig.2 FTIR spectra of GF,1(1 000 s-0 s)-GF and 10(100 s-60 s)-GF

2.2 聚吡咯改性对石墨毡电极亲水性的影响
接触角测定结果见图3。
由图3可知,石墨毡GF和样品10(100 s-120 s)-GF的接触角分别是131°和73°,表明石墨毡为强憎水性材料,采用聚吡咯包覆改性后亲水性得到显著提高。电极材料亲水性的提高有利于石墨毡电极被电解液浸润,从而促进电解液中的溶解氧向石墨毡纤维表面扩散和产物H2O2向溶液主体的传递[18]。


图3 石墨毡样品与水的接触角Fig.3 Contact angle of GF,10(100 s-120 s)-GF with water a.GF;b.10(100 s-120 s)-GF
2.3 聚吡咯改性对石墨毡电化学活性比表面积的影响
电化学活性比表面积大小是反映电极的电化学性能的重要指标[19]。以K3[Fe(CN)6]为探针分子,通过循环伏安法对各石墨毡样品的电化学活性比表面积进行了测定,结果见图4。
由图4可知,聚吡咯改性能够显著提升石墨毡电极的电化学活性比表面积。聚吡咯改性的石墨毡材料的电化学活性比表面积先随着聚合时间(t1)的延长而先增大后减小。当聚合脉冲时间从50 s提高到100 s时,改性石墨毡的电化学活性比表面积从0.356 9 cm2/cm3提高到1.502 8 cm2/cm3。这主要是因为吡咯单体在石墨毡纤维表面的聚合包覆取决于电化学聚合时间和石墨毡电极附近可反应的吡咯单体量。聚合脉冲时间从50 s延长至100 s时,浸润石墨毡纤维的电解液中所含的吡咯单体能够更充分地通过电化学聚合包覆在碳纤维表面,石墨毡纤维的吡咯包覆率提高,聚吡咯膜层的厚度从 240 nm 增加到640 nm,同时石墨毡样品的电化学活性比表面积增大。进一步延长聚合脉冲时间,则出现石墨毡空隙内包含的吡咯单体被完全消耗,电化学聚合只能发生在石墨毡电极与电解液主体接触的部分表面,导致不均匀包覆,聚吡咯主要包覆在石墨毡电极的最外层纤维的表面,电化学活性面积并未得到有效提升。因此,对于5 mm厚度的石墨毡而言,以聚合脉冲时间为100 s,总聚合时间为1 000 s为宜,所得样品10(100 s-120 s)-GF的电化学活性比表面积最大,达到1.502 8 cm2/cm3。
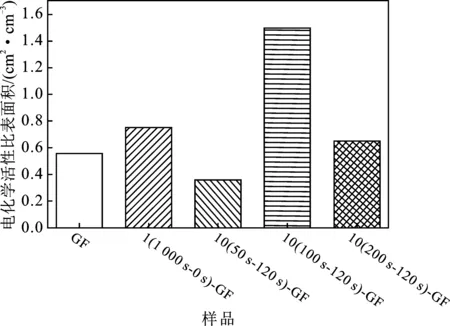
图4 不同聚合时间的石墨毡的电化学活性比表面积Fig.4 Electrochemical active specific area of graphite felt with different polymerization time
图5为脉冲间隔时间对聚吡咯改性石墨毡电化学活性比表面积的影响。
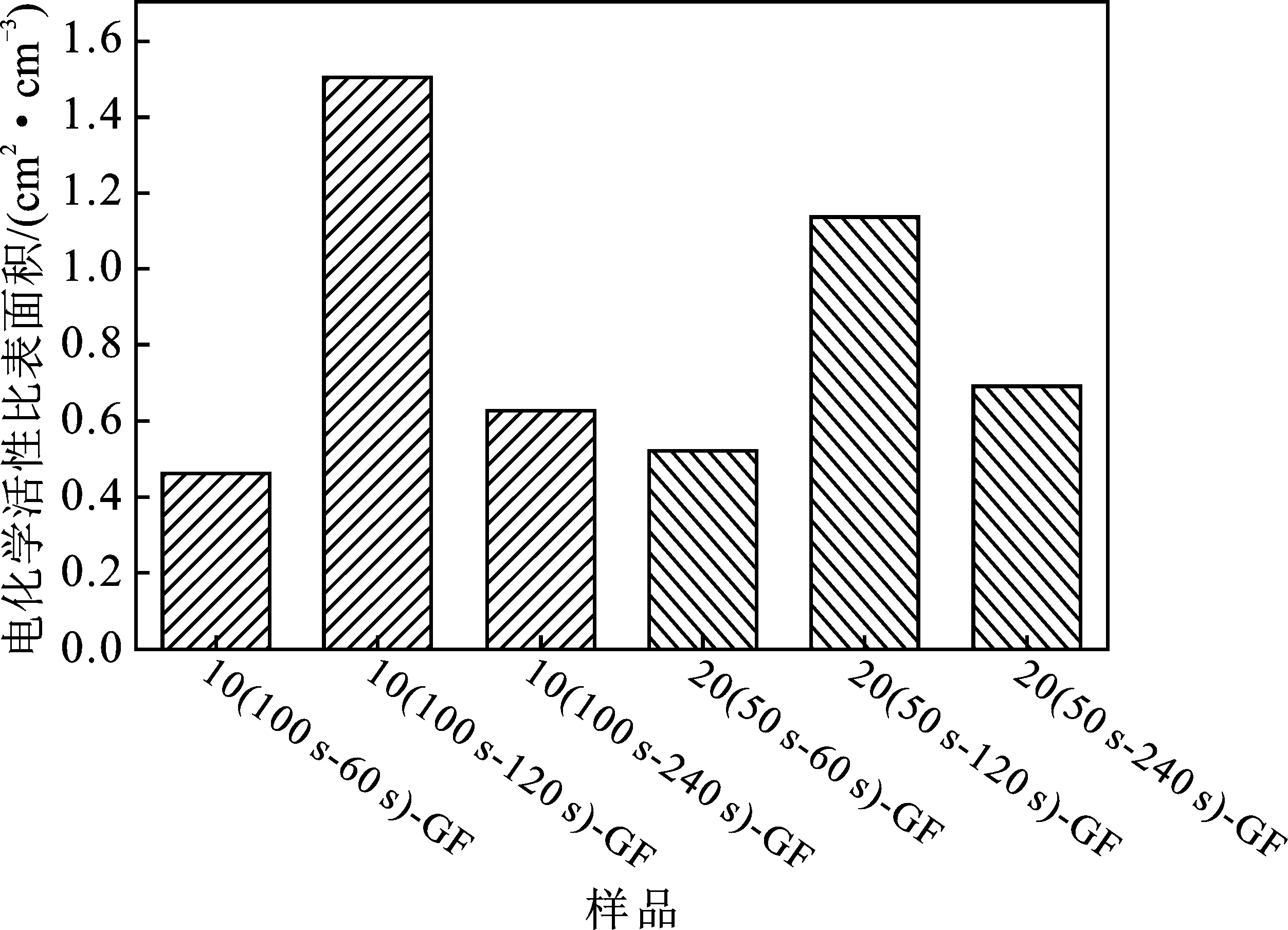
图5 不同脉冲间隔时间石墨毡的电化学活性比表面积Fig.5 Electrochemical active specific area of graphite felt with different pulse interval time
由图5可知,在聚合脉冲时间和总聚合时间相同的条件下,电化学活性比表面积会随着脉冲间隔时间的延长而先增大后减小,脉冲间隔时间120 s时,对应的比表面积最大。这是因为在脉冲间隔时间内,吡咯单体由高浓度的溶液主体向低浓度的石墨毡纤维内部扩散。间隔时间延长时,石墨毡纤维内部浸润的吡咯量增加,在进入聚合时间时,吡咯的包覆率增大,聚吡咯膜层厚度增大,改性石墨毡的电化学活性比表面积越大。间隔时间>120 s时,样品的电化学活性比表面积减小。
2.4 聚吡咯改性对石墨毡电极氧还原活性的影响
图6是在扫描速率50 mV/s,电势范围-1.4~0 V,pH维持在3,0.05 mol/L Na2SO4电解液中进行的循环伏安实验。

图6 石墨毡和改性石墨毡电极的循环伏安曲线Fig.6 CV curves of graphite felt and polypyrrole-modified graphite felts
由图6可知,聚吡咯改性使得氧还原反应响应的起始电位向正电位方向偏移,GF、1(1 000 s-0 s)-GF和10(100 s-120 s)-GF上氧还原反应的起始电位分别为-0.5,-0.45 V和-0.2 V。1(1000 s-0 s)-GF和10(100 s-120 s)-GF在-0.9~-0.3 V的范围内出现较宽的电流峰响应,主要对应于2电子氧还原反应,即H2O2的电化学生成过程[20],这表明聚吡咯改性石墨毡电极具有更强的2电子氧还原反应活性,其中10(100 s~120 s)-GF的电流响应最大,其2电子氧还原活性最高。
2.5 电化学聚合改性工艺条件对石墨毡电极电化学性能的影响
2.5.1 吡咯沉积量的影响 在-0.5~-0.2 V的范围内对应的是2电子氧还原反应,即H2O2的电化学生成过程,在-1.1~-0.9 V的区间内,对应的是4电子氧还原反应,即H2O的生成过程[20]。图7是在扫描速率50 mV/s,电势范围-1.4~0 V,pH维持在3的0.05 mol/L Na2SO4电解液中进行的循环伏安实验。
由图7可知,在2电子氧还原反应对应的区间内,样品10(50 s-120 s)-GF的电流响应依次高于 10(100 s-120 s)-GF、10(200 s-120 s)-GF、GF,电流响应随着聚合时间的增加而减小。随着聚合时间的增加,吡咯沉积量增加,石墨毡表面的聚吡咯膜层变厚,样品的电阻变大,电流响应逐渐减小[15]。对于样品10(50 s-120 s)-GF,在-1.1~-0.9 V的区间内电流响应也较强,说明样品10(50 s-120 s)-GF对2电子氧还原反应及其竞争反应即4电子氧还原反应都有促进作用,因此H2O2的产量的增长和电流响应的增长趋势有所不同。
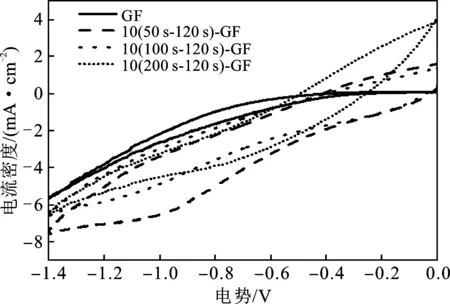
图7 不同吡咯掺杂量的石墨毡样品的循环伏安曲线Fig.7 CV curves of graphite felt with different pyrrole coated
图8是在扫描速 50 mV/s,电势为-0.45 V,氧气流量为100 mL/min,pH维持在3的0.05 mol/L Na2SO4电解液中进行的氧还原生成H2O2的实验。
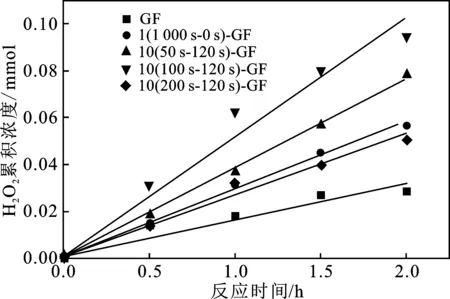
图8 聚合脉冲时间对石墨毡上H2O2累积速率的影响Fig.8 H2O2 Cumulative curves of graphite felts with different polymerization time
由图8可知,未改性的石墨毡(GF)的H2O2的累积速率为 8.130 mol/(m3石墨毡·h),而样品1(1 000 s-0 s)-GF上H2O2的累积速率为 13.335 mol/(m3石墨毡·h)。此外,H2O2的累积浓度随着吡咯聚合脉冲时间的延长先增大后减小,聚合脉冲时间100 s时,H2O2的累积速率最大,达到了25.775 mol/(m3·h)。这表明了聚吡咯改性显著提高了石墨毡电极的2电子氧还原性能,通过聚合脉冲时间可调控聚吡咯的包覆厚度,从而调变改性后石墨毡电极的电化学性能,并且存在一个最佳的聚吡咯层厚度。聚合脉冲时间较短时聚吡咯包覆率较低,可能导致电极表面未得到充分利用,这与电化学活性比表面积测试结果一致。而聚合脉冲时间较长时,聚吡咯层厚度显著增加,电极内阻变大,电化学性能也相应下降。
2.5.2 聚合脉冲时间对聚吡咯改性石墨毡氧还原活性的影响 总聚合时间一定的条件下,改变聚合脉冲时间和脉冲次数制备的改性石墨毡电极的循环伏安曲线见图9。扫描速率50 mV/s,电势范围 -1.4~0 V,pH 3,电解液为0.05 mol/L Na2SO4溶液。
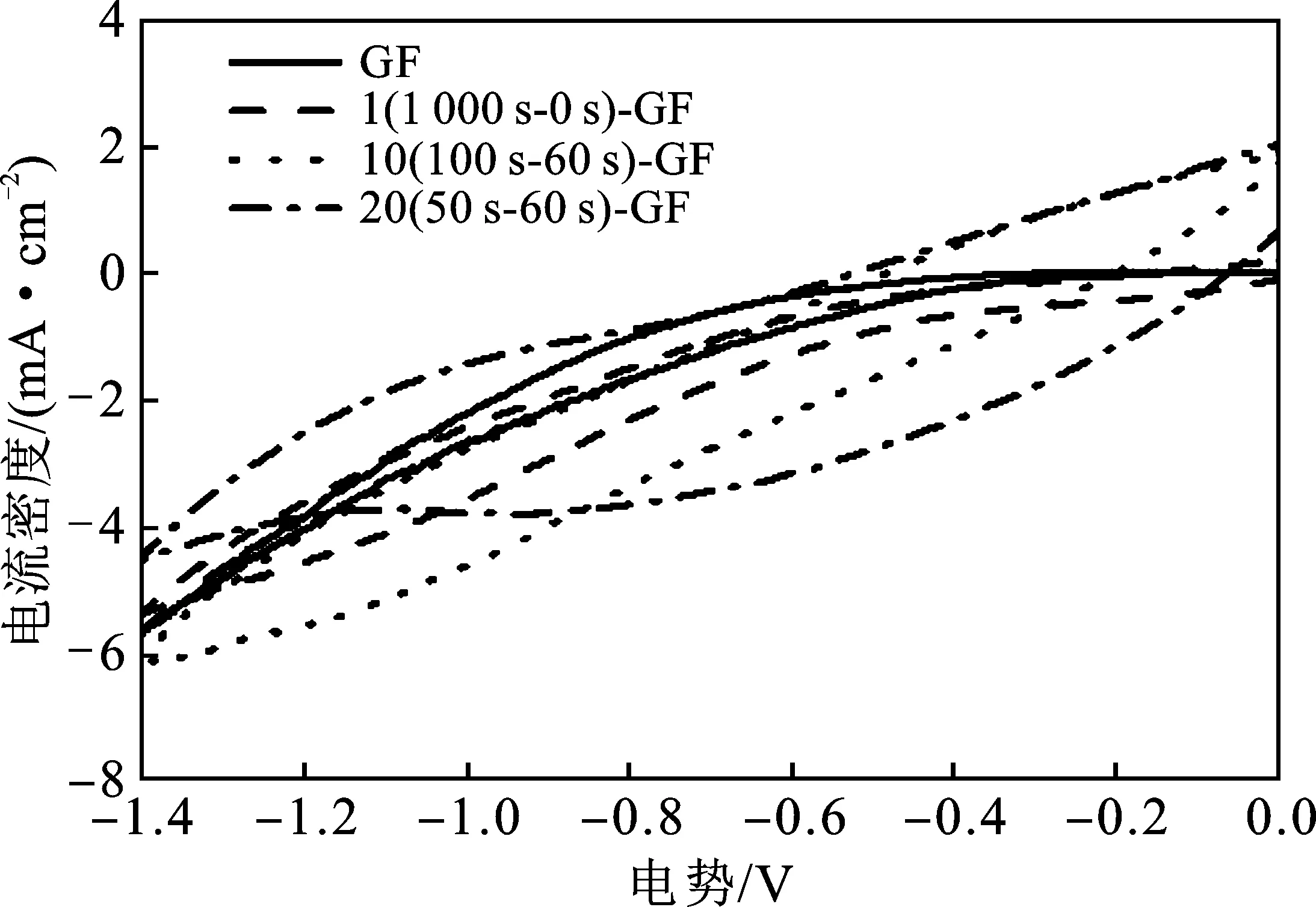
图9 不同脉冲次数的石墨毡样品的循环伏安曲线Fig.9 CV curves of graphite felts with different pulse number
在总聚合时间一定的情况下,脉冲次数的增加代表聚合脉冲时间的减少。由图9可知,电极在 -0.9~-0.3 V的电势范围内,氧还原响应电流随着脉冲次数的增加即聚合脉冲时间的减少而增强。聚合脉冲时间越短,能够进入石墨毡纤维内部的吡咯量越大,石墨毡纤维薄膜包裹的聚吡咯的膜层越厚,样品的2电子氧还原反应活性越高,电流响应越强。
在氧气流量为100 mL/min,电势为-0.45 V,pH维持在3的0.05 mol/L Na2SO4电解液中进行了氧还原生成H2O2的实验。氧还原生成H2O2实验结果(图10a)表明,H2O2的累积速率随着脉冲次数的减少即聚合脉冲时间的延长而减少。脉冲次数越多,聚合脉冲时间越短,石墨毡纤维表面的聚吡咯膜层越厚,样品的2电子氧还原反应活性越高,H2O2的累积浓度越大。当聚合脉冲时间分别为1 000,100,50 s时,H2O2的累积速率依次是 14.645,18.290,19.880 mol/(m3石墨毡·h),远大于初始石墨毡材料的8.130 mol/(m3石墨毡·h)。当循环次数从10次增加到20次,聚合脉冲时间从100 s减小到50 s时,H2O2产量的提升并不明显。图10b显示了不同聚合脉冲时间对应的样品的电流效率。
由图10b可知,2 h后,1(1000 s~0 s)-GF、10(100 s-60 s)-GF、20(50 s-60 s)-GF在同一条件下对应的电流效率分别达到了47.57%,56.68%,56.16%,电流效率会随着聚合脉冲时间的延长而减小。聚合脉冲时间越短,石墨毡纤维表面的聚吡咯膜层越厚,电阻越大,损耗越大,电流效率越低。
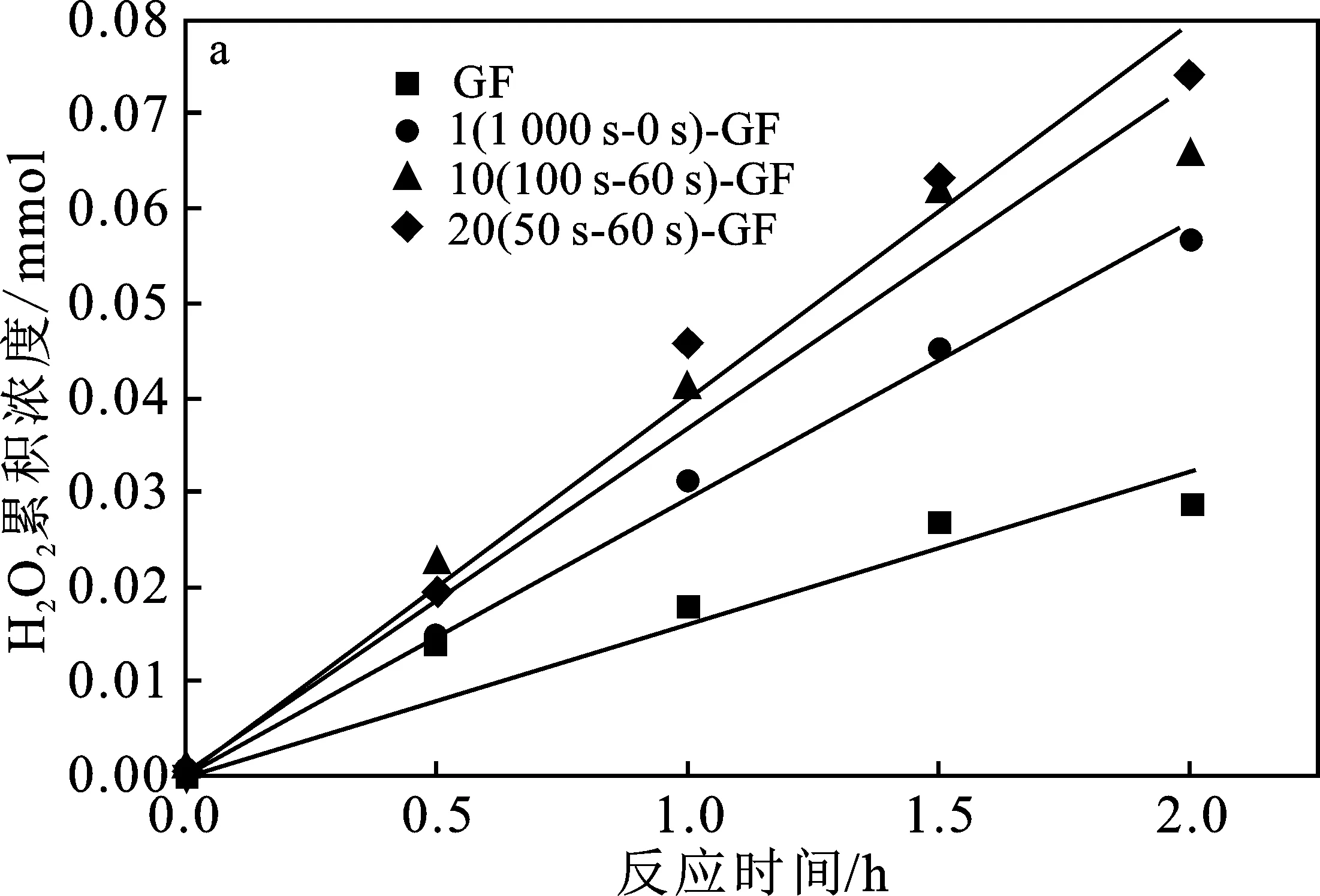
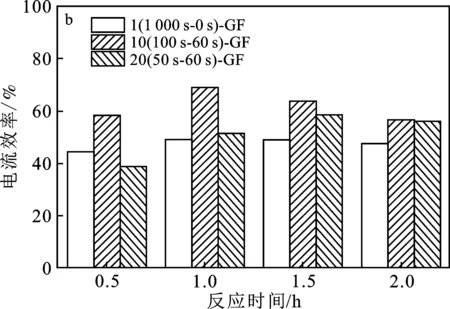
图10 不同脉冲次数的石墨毡电极样品的H2O2 累积浓度曲线(a)和电流效率(b)Fig.10 H2O2 Cumulative curves(a) and current efficiency diagram(b) of graphite felts with different pulse number
综合H2O2累积浓度曲线和电流效率可以发现,循环10次的样品的H2O2产量与循环20次的样品的H2O2产量差别较小,但前者对应的电流效率略高。因此,循环10次为最佳循环次数。
2.5.3 间隔时间对电极氧还原活性的影响 实验条件:扫描速率50 mV/s,电势范围-1.4~0 V,电解液为0.05 mol/L Na2SO4溶液,pH=3,氧气流量为100 mL/min。在相同聚合脉冲时间和脉冲次数,不同间隔时间下所得聚吡咯改性石墨毡上生成H2O2的活性见图11。
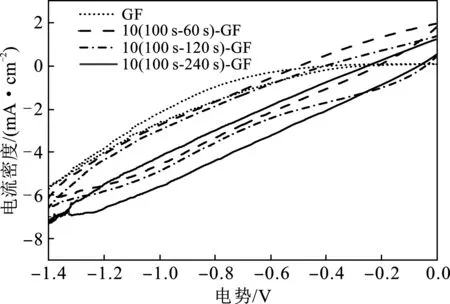
图11 不同间隔时间的样品的循环伏安曲线Fig.11 CV curves of graphite felts with different pulse interval time
由图11可知,在-0.9~-0.3 V范围内,样品的电极响应电流随着脉冲间隔时间的增加而增大,间隔时间增加时,吡咯单体在机械搅拌下更好地分散进入石墨毡纤维内部,在聚合时能够更加均匀地包覆石墨毡纤维,聚吡咯膜层厚度增大,电化学活性比表面积也增大。间隔时间增大,吡咯的掺杂量越大,样品的2电子氧还原反应活性越强,电流响应越强。
图12是在pH值为3,0.05 mol/L的Na2SO4作为电解液,氧气流量为100 mL/min,电势 -0.45 V 的条件下进行的氧还原生成H2O2实验,考察了不同间隔时间所得改性电极氧还原生成H2O2的性能。
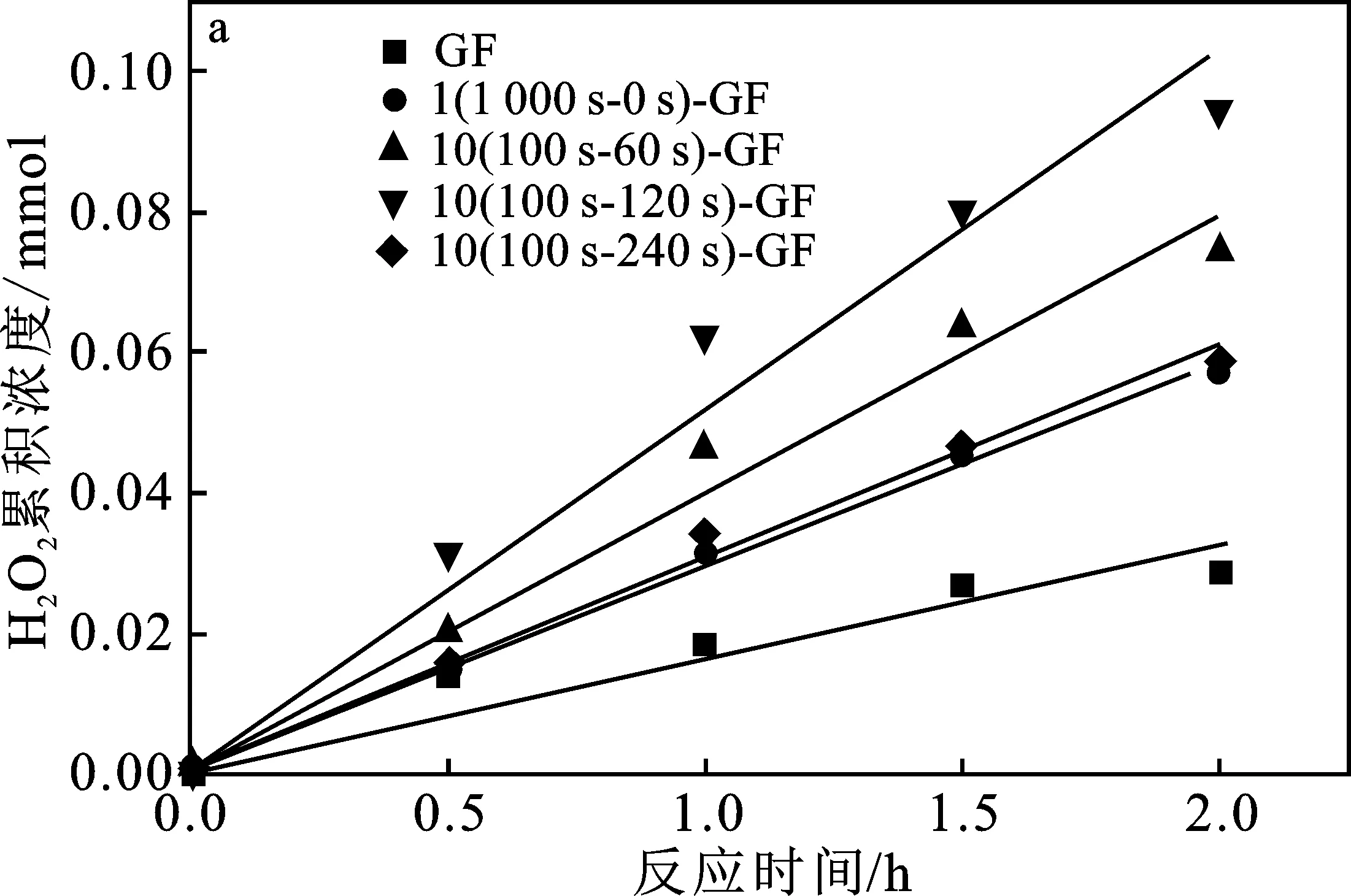

图12 石墨毡电极样品的H2O2累积浓度 曲线(a)和电流效率(b)Fig.12 H2O2 Cumulative curves(a) and current efficiency diagram(b) of graphite felts with different pulse interval time
由图12可知,电极上H2O2的累积速率随着间隔时间的增加而增大。当间隔时间从60 s延长到120 s时,所得石墨毡电极上H2O2的累积速率从 18.290 mol/(m3石墨毡·h)增加到 25.775 mol/(m3石墨毡·h)。延长脉冲间隔时间,使得聚吡咯膜层的厚度增大,吡咯掺杂量变大,对应样品的2电子氧还原活性变高,H2O2的累积浓度变大。
由上可知,样品10(100 s-120 s)-GF对应的聚吡咯膜层厚度最大,电阻最大,电流效率最小,同时吡咯掺杂量最大,2电子氧还原活性最大。聚吡咯的大量掺杂能够增强石墨毡样品的电化学活性,同时也增大了样品的电阻,增加了能耗,减小了电流效率。
3 结论
电化学聚合法沉积吡咯改性石墨毡电极,通过聚合脉冲时间、间隔时间和脉冲次数可以有效调控石墨毡纤维表面聚吡咯结构和电化学性能,在聚合时间为100 s、间隔时间为120 s,脉冲次数为10次的条件下,获得聚吡咯改性石墨毡电极2电子氧还原活性最佳和电化学活性比表面积最大达到 1.502 8 cm2/cm3,并且其H2O2累积速率最大,为25.775 mol/(m3石墨毡·h),是未改性石墨毡电极上H2O2累积速率的3.17倍。
