食品中邻苯二甲酸酯类塑化剂检测方法研究进展
2023-02-12王腾余逸飞王睿王鑫李昀怡陈洋程楠
王腾 , 余逸飞 , 王睿 , 王鑫 , 李昀怡 , 陈洋 , 程楠
中国农业大学食品科学与营养工程学院,食品质量与安全北京实验室,北京 100083
塑化剂是指在聚合物加工过程中添加的、能够改善产品塑型的物质[1]。塑化剂一般为低分子物质,夹在聚合物分子物质之间,使聚合物分子的分子间距增大、分子间作用力降低、相对滑动能力增强,从而降低聚合物成型的加工温度,最终改善产品的柔韧性和可塑性[2]。
塑化剂并不是一种食品添加剂,禁止在任何食品中使用,但在食品中仍可被检测到。食品中的塑化剂可能来源于生产、流通和餐饮三个环节。在生产过程中,由于部分车间生产风险管控不严的原因,各种劣质塑料制成的生产工具、生产管道中的塑化剂可能渗透到食品中[3];在流通过程中,由于部分包装材料本身存在安全问题,食品长期保存在问题塑料包装内,塑化剂随时间缓慢迁移至食品中[4];在餐饮行业,错误使用或使用劣质的外卖包装盒、塑料袋等包装烹饪后的食品,包装材料不能满足耐受高温的要求,导致塑化剂迁移进入食品[3]。
塑化剂种类繁多,目前全球范围内可用作塑化剂的化合物有上千种,其中超过500种化合物已被商品化[5],我国也有100余种已投入生产[6]。现有的数百种塑化剂中,最常用的是邻苯二甲酸酯类(phthalic acid esters,PAEs)[7],占塑化剂总用量的80%以上[8]。邻苯二甲酸酯类塑化剂包括邻苯二甲酸二(2-乙基己基)酯[Di(2-ethylhexyl)phthalate,DEHP]、邻苯二甲酸二丁酯(dibutyl phthalate,DBP)、邻苯二甲酸二异壬酯(diisononyl phthalate,DINP)、邻苯二甲酸甲苯基丁酯(butyl benzyl phthalate,BBP)等[9]。

图1 邻苯二甲酸酯结构式Fig. 1 Chemical structural for phthalate esters
邻苯二甲酸酯类塑化剂作为一种环境内分泌干扰物(environmental endocrine disruptors,EEDs)[10],通过干扰人体内激素分泌水平,会对人体生殖系统造成不可逆伤害,如引发女童早熟、子宫和卵巢过早发育[11]、损害男子睾丸和精子数量,进而导致生殖率的降低[7]。此外,还会增加心血管疾病的发病风险、损害肝脏和泌尿系统、引发感觉迟钝、神经炎[12]及免疫毒性[13]。2011年,台湾发生的“起云剂”风波就是一起滥用塑化剂造成的食品安全危机,多个企业和产业被波及,引起人们的广泛关注,使塑化剂问题走进大众视野,并越来越被重视[8]。有研究发现,长期摄入塑料制品中的饮用水会吸入邻苯二甲酸酯,即使在低浓度下,也会导致这些物质在人体中积累有机小分子,危害人体健康[14],因此食品中邻苯二甲酸酯含量的检测对保障生命健康至关重要。
本文概述了邻苯二甲酸酯类塑化剂的相关法规和标准以及检测邻苯二甲酸酯的前处理方式、传统检测方法,并按照检测方法输出信号类型分类,着重总结了近年来新出现的邻苯二甲酸酯的快速检测方法,以期为进一步开发塑化剂的检测方法提供参考。
1 邻苯二甲酸酯相关法规与标准
我国标准GB9685-2016规定了邻苯二甲酸酯类塑化剂在食品接触用材料中的使用要求,但未对其在食品中的残留量作出限制。目前,我国使用的邻苯二甲酸酯在食品中的残留量限制依然依据2011年台湾“起云剂”事件后卫生部紧急发布的卫办监督函[2011]551号公告,具体规定如表1。
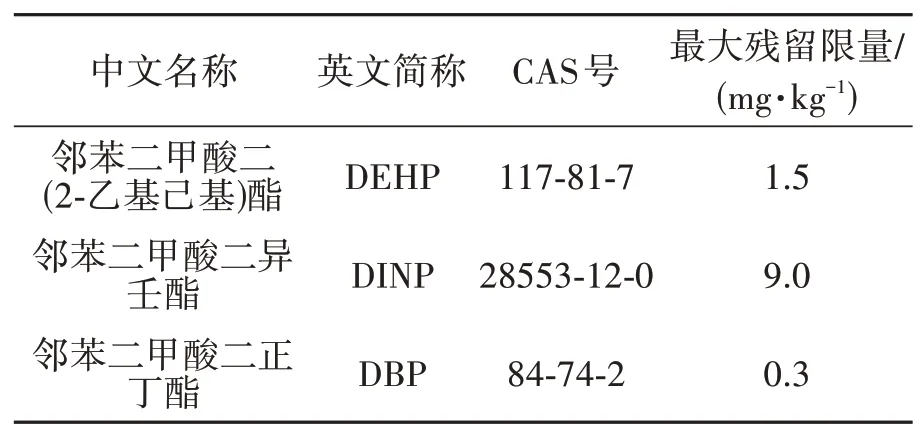
表1 食品及食品添加剂中邻苯二甲酸酯类最大残留量[15]Table 1 Maximum residual amount of phthalate esters in food and food additives[15]
2011年8月29日,卫生部发布了卫办监督函[2011]773号公告,回答了食品用香料香精中邻苯二甲酸酯的最大残留量等相关问题。公告指出:食品用香料香精中邻苯二甲酸酯的最大残留限量仍按卫办监督函[2011]551号公告执行,除此之外,国家已将食品、食品添加剂邻苯二甲酸酯类物质列入食品安全风险监测计划。对检出DEHP、DINP、DBP以外的其他14类邻苯二甲酸酯产品进行进一步追查,汇总相关监督监测数据,作为开展风险评估和制定限量值的科学依据[16]。
在国际上,许多国家和机构也对邻苯二甲酸酯在食品中的残留量做出了限制,如欧盟食品安全局(European Food Safety Authority,EFSA)、美国食品药物管理局(Food and Drug Administration,FDA)都制定了食品中塑化剂的人类安全摄入量。世卫组织也规定了饮用水中DEHP、DEP、BBP三种邻苯二甲酸酯类物质的每日允许摄入量[17]。
2 食品中塑化剂检测的前处理方法
前处理方法是影响食品中塑化剂检测结果准确度的关键因素之一。提取剂的选择、是否提取完全、杂质的引入和去除情况等都将影响最终的检测结果,同时还要考虑时间成本、价格成本及污染情况等因素。目前,常用的基本前处理方法主要有固相萃取法和液液萃取法。但为了进一步提高精确度和降低检测限,有不少研究者对传统的前处理方法进行了优化和改进,开发了更多、更高效的前处理方法。
2.1 固相萃取法
固相萃取(solid phase extraction,SPE)是对PAEs进行前处理最常用的方法之一。固相萃取技术基于液-固色谱理论,通过选择性吸附和选择性洗脱的过程对样品进行提取和纯化。固相萃取法选择性好、分离效果好,可同时进行富集和纯化,能够有效地降低基质干扰,提升检测方法的灵敏度。Wang等[18]首次制备了C8修饰的磁性氧化石墨烯(MGO-C8),建立了MGO-C8固相萃取-分散液-液微萃取法,以此提取水中的PAEs并进行检测,发现该方法准确性好、灵敏度高、精密度高,可使检出限降低至0.000 5~0.001 μg·L-1,同时具有较好的回收率,回收率达到90.6%~108.3%。
在固相萃取的基础上,进一步出现了固相微萃取(solid phase microextraction,SPME)的前处理方法,它不仅保留了SPE的优点,而且无需柱填充物和有机溶剂解吸,直接将高分子涂层涂渍在石英玻璃纤维上,在气相色谱的进样口进行热解吸,或以液相色谱的流动相使其解吸,大大缩短了前处理的时间[19]。Liu等[20]使用在线管内固相微萃取技术(in-tube solid-phase microextraction,IT-SPME)对瓶装水进行前处理,结合高效液相色谱测定了瓶装水中PAEs的含量,在最佳实验条件下,检测限为0.052~0.100 ng·mL-1,回收率为84.6%~111.6%。在线管内固相萃取技术结合了在线系统和固相微萃取的优点,实现了样品提取、纯化与分析的一体化和自动化,且精度和灵敏度极佳、溶剂消耗低,是一种绿色环保又高效的前处理方式。
2.2 液液萃取法
对于果汁、牛奶等液体样品中的PAEs,通常采用液液萃取法进行提取,一般使用乙腈、甲醇、丙酮等有机溶剂对目标物进行提取和分离,简单易行且回收率较好。但此法往往会消耗大量有机溶剂,增加环境污染的风险,持续时间长,操作步骤繁琐,而且其更适于大体积高含量的物质提取,不适于痕量分析。
近些年发展起来的液液微萃取(liquid-liquid microextraction,LLME)方法,可使用少量的有机溶剂萃取大量样品,从而得到较高的富集倍数,减少有机溶剂的消耗,再结合使用新型萃取溶剂,或超声、微波等辅助方法,进一步提高萃取效率。
Leng等[21]建立了全自动涡流辅助液-液微萃取(vortex assist LLME,VALLME)的前处理方法对白酒中的PAEs进行萃取,利用气相色谱-质谱联用(gas chromatography-mass spectrometry, GC-MS)法测定了白酒中PAEs的含量,通过对萃取剂、萃取时间、相分离的搅拌速度和时间等多项指标进行优化,最终得到检出限为0.003~0.006 μg·L-1,此法是一种简单快速、高效的痕量前处理方法,灵敏度和自动化程度较高。
共晶溶剂(deep eutectic solvent,DES)是一种新型环保溶剂萃取剂,具有制备简单、成本低、回收率高、低毒或无毒性等特点,Wang等[22]使用由薄荷醇和月桂酸组成的酸碱诱导共晶溶剂作为提取溶剂,建立了酸碱诱导共晶溶剂-涡旋辅助液-液微萃取(DES-VALLME)技术,对牛奶中的PAEs进行提取和检测,与其他方法相比,此法大大缩短了实验时间,且未使用有毒的有机溶剂,是一种快捷、绿色的前处理方法。
2.3 QuEChERS法
QuEChERS法是一种快速、简便、经济、高效、抗干扰、安全的前处理方法[23],一般以单一溶剂乙腈进行提取,再使用吸附剂与基质中的干扰物结合,最后通过离心方式去除溶剂达到纯化的目的。
Socas-Rodriguez等[23]采用QuEChERS方法对4种婴儿食品进行前处理,使用气相色谱-质谱联用法对PAEs进行检测,该方法最终检测限为0.03~1.11 μg·kg-1,相对回收率在70%~120%之间,相对标准偏差在19%以下。此法具有较高的提取效率,且具有更广泛的应用范围。
Sun等[24]结合分散固相萃取对QuEChERS法进行了改进,用乙腈提取高粱中的PAEs后,使用N-丙基乙二胺、C18和无水硫酸钠进行纯化处理,涡旋、离心后用气相色谱检验PAEs的含量。最终的检测限为0.4~0.8 g·kg-1,回收率在82.0%~120.2%之间。此法准确、有效,适用于谷物样品中PAEs的检验。
2.4 搅拌棒吸附萃取
搅拌棒吸附萃取法(stir bar sorptive extraction,SBSE)源于固相微萃取(SPME)技术,为了解决SPME方法萃取量小的缺陷[25],SBSE使用聚二甲基硅氧烷(polydimethylsiloxane,PDMS)涂层包裹搅拌棒,在搅拌过程中完成萃取,此法具有更大的固定相体积、萃取容量以及更高的萃取回收率[26]。
Shen等[27]开发了一种咪唑酸盐石骨架基氧化石墨烯复合材料(ZIF-8@GO)作为中空纤维搅拌棒的吸附剂,以此来提取儿童食品中PAEs并检测其含量,此法避免了吸附剂与样品直接接触对吸附剂造成的污染,且灵敏、快速,萃取效率高。
Wang等[28]首次制备了4,4′-二氨基对三联苯三嗪(4,4′-diaminop-ter phenyl triazine, PDT)涂层搅拌棒,对白酒和矿泉水样品中PAEs进行提取并使用高效液相色谱检测,PDT涂层中的氮原子可与PAEs中的苯环形成π-π共轭,也可以与PAEs的氧原子形成分子间氢键,因此PDT对于PAEs的吸附力较好。利用此法的萃取回收率大于65%,且具有更好的吸附动力,优于市售的两款搅拌棒(PDMS与EG-硅胶涂覆搅拌棒),同时合成材料较为廉价,降低了成本。
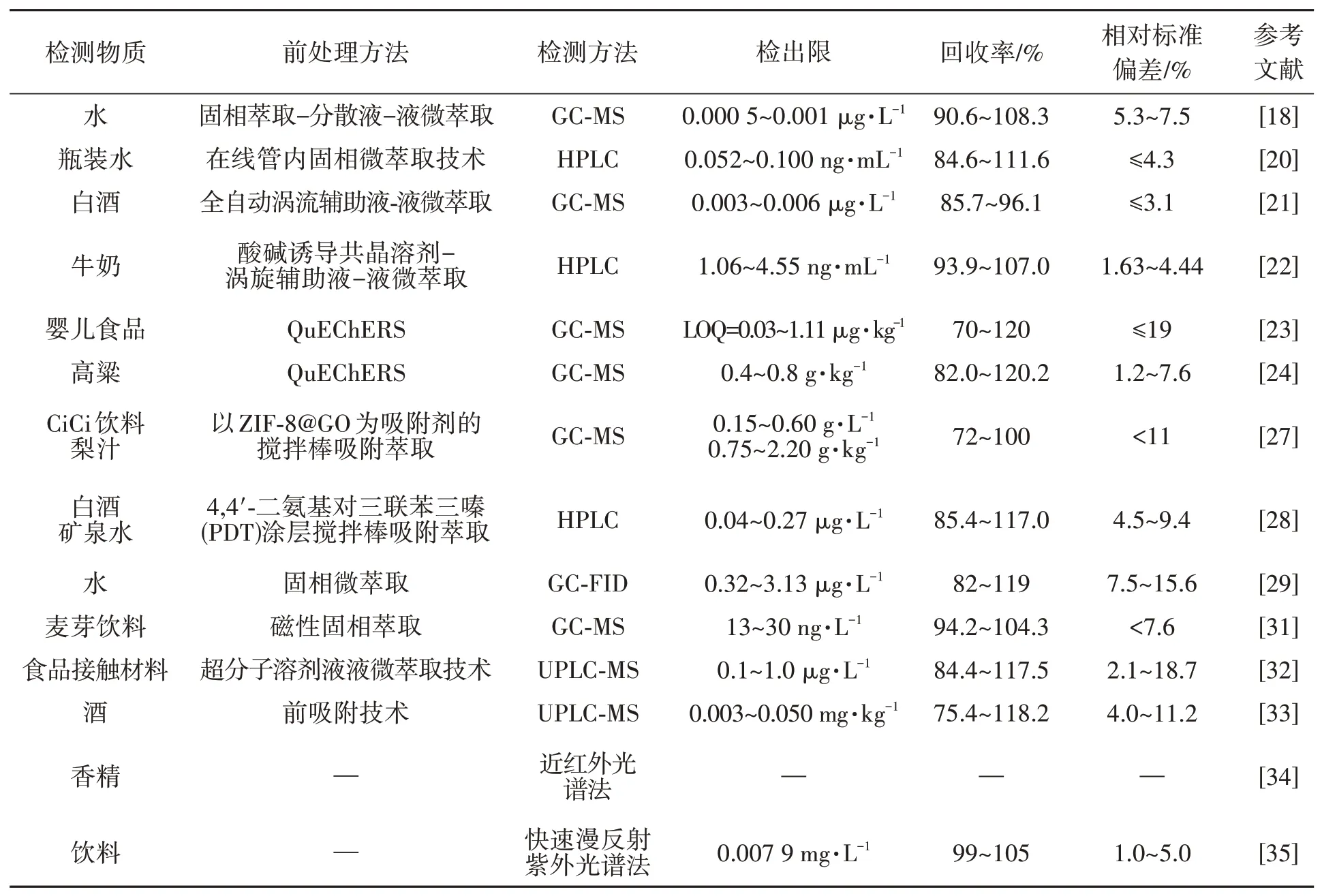
表2 食品中邻苯二甲酸酯含量测定的相关研究Table 2 Studies on determination of phthalate esters in food
3 食品中塑化剂的传统检测方法
目前在食品分析中常用的邻苯二甲酸酯类塑化剂的检测方法主要有气相色谱法、液相色谱法、气相色谱-质谱联用法和液相色谱-质谱联用法。尽管由于食品基质、环境因素等原因,各文献中选择的色谱柱和质谱条件有差异,但都会利用色谱的高分离度、高分辨率特性对样品分离后进行检测。
3.1 气相色谱法
气相色谱法(gas chromatography,GC)是以气体作为流动相,将色层分离以后进行分析的色谱分离方法。对于易挥发物质具有较好的分离能力,较高灵敏度和选择性,适宜多种混合的复杂组分之间的分离,在邻苯二甲酸酯类的定量分析中应用广泛。Wu[29]等采用SPME-GC对水样中的PAEs进行定量分析,以蜡烛烟灰制备的碳点作为SPME的涂层材料,搭配氢焰离子化检测器,最终5种PAEs的检出限和定量限分别为0.32~3.13 μg·L-1和1.07~10.43 μg·L-1,此方法线性良好,相对标准偏差较小,同时碳点涂层也为其带来了更低的检测限和高回收率。
3.2 液相色谱法
液相色谱法(liquid chromatography,LC)是最常用的塑化剂检测方法之一,与气相色谱不同的是,液相色谱以溶液作为流动相进行分离。由于邻苯二甲酸酯的中低极性,色谱柱通常选用低极性的反相柱进行洗脱,同样具有较好的分离度和选择性。
3.3 气相色谱-质谱联用法
气相色谱-质谱联用法(GC-mass spectrometry,GC-MS)广泛应用于PAEs的检测,同时也是国标GB31604.30-2016《食品接触材料及制品邻苯二甲酸酯的测定和迁移量的测定》使用的方法。将气相色谱的高分离度与质谱的定性能力相结合,相较于氢焰离子化检测器,质谱检测器更适用于种类繁多、结构相近的混合物定性检测,其中离子检测扫描模式的检测灵敏度和选择性更高[30]。Rezaei等[31]使用磁性固相萃取法提取瓶装麦芽饮料中的PAEs,并采用GC-MS技术检验PAEs的含量,选择离子检测扫描模式检测,最终得到的检测限为13~30 ng·L-1,定量限为39~90 ng·L-1。此法灵敏、经济且具有较低检测限。
3.4 液相色谱-质谱联用法
液相色谱-质谱联用法(LC-MS)是在液相色谱法基础上发展起来的,现已广泛应用于塑化剂等痕量物质的检测。相较于液相色谱,串联质谱进一步提高了检验的灵敏度,减少了基质中杂质对检测结果的干扰,更准确地进行定性和定量分析。王春等[32]使用UPLC-MS方法测定了食品接触材料中8种邻苯二甲酸酯的含量,配合超分子溶剂液-液微萃取技术,检出限为0.1~1.0 μg·L-1,8种邻苯二甲酸酯在各自浓度范围内均具有良好的线性关系,准确可靠。
由于液相色谱一般采用塑料管道输入溶液和样品,在测量过程中常需要做空白试验以减少管道中可能存在的塑化剂迁移对实际结果的影响,尤其是更换了新管道的仪器造成的误差会很大。吴敏等[33]采用前吸附技术,以Eclipse XDB-C18柱作为前吸附柱接在液相色谱的混合器和进样器之间,以此来减少塑料管道造成的误差,此技术检测了酒中的PAEs含量,得到了较低的定量限和较好的重复性。
3.5 红外、紫外光谱法
李祥辉等[34]运用近红外光谱法,无需对样品香精进行前处理,以空气作为测量背景,在室温下测定后用偏最小二乘法进行定量分析,根据模型预测未知样品中DEHP的含量。该方法检测结果与真实值相近,相对误差为15.8%~17.6%。Chen等[35]建立了一种快速漫反射紫外光谱法检测DEHP。该方法结合膜过滤富集和漫反射紫外光谱,对0.03~5.00 mg·L-1范围内饮料中DEHP的测定具有良好的灵敏度和选择性,DEHP的检出限为0.007 9 mg·L-1。该方法具有操作简单、无溶剂洗脱的优点。
4 快速检测方法
PAEs常用的检测方法大多使用大型仪器,虽然检测结果准确、反应灵敏,但具有仪器价格昂贵且操作过程繁琐、需要专业人员操作、样品前处理复杂等一系列问题,此外,最重要的是无法满足对食品中PAEs实时原位快速检测的迫切需求。相较于传统检测方法,荧光法、胶体金显色法、化学发光法、表面增强拉曼光谱法(surface-enhanced raman spectroscopy, SERS)等其他快速检测方法有着前处理相对简单甚至无需前处理,操作简便、快速等优势,在PAEs快速初检方面有着较好的应用前景。
4.1 基于荧光的快速检测法
荧光法利用羟基自由基进攻PAEs使其具有荧光性,或是合成外源强荧光物质,或是建立荧光分子印迹传感器识别荧光强度,均可间接检测PAEs的含量(表3)。

表3 几种荧光法检测邻苯二甲酸酯方法的特点Table 3 Characteristics of several fluorescence methods for determination of phthalate esters
宋玮等[36]合成了具有强荧光的超支化聚乙烯亚胺-铜纳米簇(hPEI-Cu NCs)。表面配体是金属纳米簇荧光的主要影响因素,hPEI中的富电子基团氨基与Cu NCs表面结合,促使其产生高强度荧光。Cu2+在和Cu NCs竞争性结合富电子基团氨基中占据优势,阻止氨基与Cu NCs结合,导致荧光淬灭;Cu2+与DEHP、UTP共同存在时会形成复杂化合物,阻止Cu2+与氨基结合,使荧光强度保持不变,因此在一定检测范围内可以根据荧光强度定量检测DEHP的质量分数。荧光铜纳米簇是较稳定的荧光纳米材料之一,与荧光染料、原子点相比,其具有毒性低、生物相容性高等诸多优点,同时由于铜的化学电位较低,其在空气中容易被氧化。此外,荧光铜纳米簇也有量子产率低的劣势,增加表面配体的给电子能力或许是解决问题的突破口。
原琳等[37]开发了一种基于DEHP可变构适配体耦合球型核酸(spherical nucleic acid, SNA)的荧光检测方法。将可变构适配体(variable structure aptamer,Vs-Apt)用于识别DEHP并将荧光信号放大。当没有DEHP时,将其加入AuNPs和Nt.BbvCI的溶液环境中,荧光基团从AuNPs表面脱落,产生荧光信号;当DEHP存在时,Vs-Apt与DEHP特异性结合,当加入Nt.BbvCI后,荧光基团与AuNPs保持紧密结合状态,不产生荧光信号变化。该方法具有较高的灵敏度和选择性,解决了以前生物传感检测在稳定性、重复性及检测限方面存在的不足,可设计为便携式荧光传感器应用于不同液体环境的DEHP快速分析。同时,适配体可以通过范德华力、氢键等与目标物质产生高亲和力、强特异性地紧密结合,相比于抗体,具有易于体外合成、易于储存、重复性好、稳定性高、操作简便特点。但该方法需要进行过滤、混合水样、去除悬浮污染物、消除其干扰荧光信号等前处理过程。
Li等[38]研发了一种新型的表面分子印迹技术。以邻苯二甲酸二丁酯为模板制备表面印迹聚合物(molecularly imprinted polymers, MIPs)。实验前需将样品在8 000 r·min-1下离心30 min以去除任何可能存在的杂质,取上清液进行检测。在检测范围5.0~50.0 μmol·L-1内,荧光强度随DBP浓度的增加线性减小,检出限为0.27 μmol·L-1。该方法弥补了普通分子印迹技术去除模板分子不完全、结合能力差、结合动力学慢等缺点,此外,MIPs具有较高的结合能力和快速的传质能力,同时与荧光量子点结合可以提高MIPs的选择性和敏感性。
Qiu等[39]通过调节晶体结构中官能团的运动产生荧光信号,研发了一种基于硝基苯基取代三芴分子端部的多孔晶体带荧光法来检测邻苯二甲酸盐,具有高灵敏度和选择性的优点。以DEHP为研究对象,最低检出限为1 μg·L-1。荧光法可以通过荧光强弱间接而直观地反映出PAEs的含量,有效地提高了选择特异性和灵敏度,但不论是合成外源的强荧光物质,还是建立荧光分子印迹传感器步骤都稍显繁琐,成本较高。
4.2 基于比色的快速检测法
比色法是通过比较或测量有色物质或溶液的颜色深度来确定待测组分含量的方法,利用有色物质对特定波长光的吸收特性来进行定性分析。比色法克服了传统方法操作耗时、预处理复杂、仪器体积大、成本高等缺点,因其简单、快捷的优势具有广阔的应用前景(表4)。

表4 几种比色法检测邻苯二甲酸酯方法的特点Table 4 Characteristics of several colorimetric methods for the determination of phthalate esters
4.2.1胶体金试纸条检测 胶体金法是由氯金酸在还原剂(如枸橼酸钠、鞣酸等)的作用下,聚合成为金颗粒,静电作用使其成为一种稳定的胶体状态,形成带负电的疏水胶溶液,称为胶体金。胶体金技术具有特异敏感、稳定性强、不需要特殊设备和试剂、结果判断直观等优点,因而特别适合于广大基层检验人员以及大批量检测和大面积普查等使用。
Guo等[40]研发了一种简单易行的胶体金显色法,将修饰了AuNPs的DNA探针用于邻苯二甲酸盐的检测。如果样品中存在PAEs,则探针与PAEs发生特异性识别,且随着PAEs浓度的增加,胶体金聚集,颜色由红变蓝。DEP、DBP和DEHP的检测限分别为0.026、0.077和0.144 mg·L-1。该实验灵巧、方便、快捷,但在实验前需要检验修饰了AuNPs的DNA探针的敏感性和选择性。朱帆等[41]以邻苯二甲酸二甲酯(DMP)为研究对象,利用免疫层析原理建立了DMP胶体金免疫层析检测试纸方法。进行检测时,如样品中没有DMP,试纸条检测线为红色且与质控线颜色一致,结果为阴性;如样品中存在DMP,检测线颜色较质控线颜色浅,为弱阳性,完全无色为强阳性。此方法操作简单、使用快捷、稳定可靠,适用于实际样品中DMP的现场快速检测。胶体金比色法因其稳定便捷的特性,适用于实时现场检测,但此方法仅能用于定性研究,在定量问题上稍有欠缺。
4.2.2酶联免疫检测 酶联免疫吸附剂测定(enzyme-linked immunosorbent assay,ELISA)是常见的抗体或抗原测定方法,基于相关联的酶对免疫复合物发生酶催化反应进行测定。待测抗体的量与有色产物成正比,因此可以定量计算待测抗体的含量。ELISA常用直接法、竞争法、双抗体夹心法等方法。
Feng等[42]开发了一种基于单克隆抗体的直接竞争性酶联免疫吸附法(direct competitive enzymelinked immunosorbent,dc-ELISA)检测MEHP,该方法具有较高的特异性和敏感性。实验前需将样品在4 ℃、3 000 r·min-1离心10 min,除去不溶性沉淀物,收集上清。实验制备了分泌抗MEHP单抗的杂交瘤细胞株4B9,用辣根过氧化物酶(horseradish peroxidase, HRP)标记抗原作为dc-ELISA探针,测量样品OD492值。Zhang等[43]研究了一种灵敏、特异的直接竞争酶联免疫吸附试验用于检测DEHP。在家兔体内培养DEHP特异性多克隆抗体,构建dc-ELISA检测DEHP,抗体与HRP的偶联物作为检测探针。该方法可用于婴幼儿用品中DEHP的测定。总体而言,dc-ELISA的优势在于操作步骤简短,无需使用二抗,减少交互作用,而缺点是实验中所有的一抗都需要用酶标记且费用相对较高。
Sun等[44]建立了一种间接竞争生物素-链霉亲和素酶联免疫吸附试验(biotin-streptavidin enzyme-linked immunosorbent, BA-ELISA),获得了针对DEHP的特异性多克隆抗体。该方法成功应用于饮料中DEHP的检测。在最佳条件下检测范围为0.021~12.948 μg·L-1,检出限为0.007 4 μg·L-1,中位抑制浓度IC50为0.526 μg·L-1。尚淑娜等[45]以邻苯二甲酸二丁酯(DBP)为研究对象,以4-氨基邻苯二甲酸为原料,利用重氮化法合成免疫抗原,进而得到抗DBP的抗体,建立间接竞争ELISA方法(indirect competitive enzyme-linked immunosorbent, ic-ELISA),用酶标仪测定OD450值。该方法的IC50值为40.68 μg·L-1,最低检测限为1.98 μg·L-1,对DBP特异性较好。此测定方法与直接法类似,区别是一抗没有酶标记,改用酶标记的二抗去识别一抗来测定抗原量。间接竞争ELISA法的优势在于二抗可以起加强信号的作用,不加酶标记的一级抗体则能保留它最多的免疫反应性,而缺点是加入二抗之后交互反应发生的机率较高。综上所述,酶联免疫检测法应用领域广阔,准确度高、特异性好,但是该方法前后耗时太长,无达到实时检测的目的,且相比于其他快检方法,实验成本较高。
4.3 基于表面增强拉曼光谱的快速检测方法
表面增强拉曼光谱(surface enhanced raman spectroscopy,SERS)是指当一些分子或官能团被吸附到某些金属或半导体的特殊表面上时, 其拉曼散射信号强度会大幅增加而产生一种奇特的光谱现象[45]。在一定条件下,拉曼散射光的强度与物质浓度呈正比,因此,SERS可以用于定量检测物质浓度[46]。SERS基于纳米粒子附近电磁场的局部高度增强,具有线宽窄、分子指纹识别、灵敏度高等优点[47],检测条件温和、操作简单、样品前处理步骤少或无,具有原位快速检测的潜力(表5,表6)。

表5 几种拉曼光谱法检测邻苯二甲酸酯方法特点Table 5 Characteristics of several unlabeled raman spectrometric methods for determination of phthalate esters

表6 几种电化学传感器的特点Table 6 Characteristics of several electrochemical methods for determination of phthalates
Wang等[48]构建了立方体等离子核壳AuNS@AgNCs,用于液体中的BBP检测。分别通过双金属复合体系和立方体结构避雷针效应增加局域表面等离子共振(localized surface plasmon resonance,LSPR)的频率范围、产生更多“热点”以增强拉曼信号。Xiang等[49]合成肌醇六磷酸(IP6)稳定立方体Au@Ag纳米粒子(Au@Ag@IP6),除通过Au与Ag长方体涂层壳的等离子体模式耦合和优化Ag壳层尺寸以提供了更广泛和更丰富的波段和更强的响应信号外,还用1-十二硫醇处理将其功能化为疏水表面,以降低检测限。Zhou等[50]通过自组装方法合成了β环糊精功能化的Ag@Fe3O4@Ag。通过β环糊精分子的疏水腔捕获BBP分子,利用磁分离的方式分离后进行SERS检测。
邻苯二甲酸酯水溶性低[51],上述两种方法通过增加非极性部分提高基底的疏水性,进一步降低了邻苯二甲酸的检测限。同时两种方法分别通过将样品基底复合物滴在铝箔表面室温干燥和磁分离的方式进行检测前的预处理,进一步简化了检测操作,使方法更适于现场原位检测。
Tu等[52]以5,5′-二硫代双-(2-硝基苯甲酸)作为拉曼报告分子,通过竞争性结合的原理构建了一种标记型适配体传感器。该方法通过二氧化硅包埋,防止拉曼报告分子解离以及额外的分子吸附在标签表面,获得可以提供稳定拉曼信号光谱信号的颗粒。通过竞争性结合反应,测量溶液中剩余二氧化硅颗粒的拉曼光谱信号强度间接得出样品DEHP浓度,从另一个角度解决了DEHP响应信号弱的问题。
目前对SERS检测邻苯二甲酸酯的研究多集中在制备具有显著增强信号效果及降低检测限基底方面,通过磁分离代替离心从而简化操作步骤也是快速检测方法开发的方向之一。SERS克服了传统检测方法需要使用有毒试剂的缺点,有着灵敏度高、操作简便等优点。然而,目前在SERS中常用的Au和Ag纳米颗粒在溶液中极易产生聚集[51],基底存在难以大规模生产、难以保存等问题。成分复杂的食品对SRES检测信号的干扰因素较多,也会导致检测结果的不准确。开发特异性识别邻苯二甲酸酯的标记型SERS检测方法,制备可批量生产、易稳定储存的信号基底或许是未来的研究方向。
4.4 基于电化学的快速检测方法
目前邻苯二甲酸酯的电化学检测方法多集中于构建电化学传感器。电化学传感器是利用电化学分析方法对目标检测物进行定量分析的装置,在电极上修饰的对目标分子特异性识别的原件与目标物特异性识别而引起信号的改变,并将信号转换成电流、电压、电阻、电容等信号[53]。
Lu等[54]使用SELEX技术筛选出了DEHP适配体,构建了电化学阻抗谱适配体传感器。该方法通过使用适配体代替抗体作为特异性检测使用的功能分子,在保证传感器选择性的同时降低了成本,使传感器更易储存。但电化学阻抗谱传感器需要更昂贵的额外恒电位仪模式,而且复杂的数据分析计算也会成为其应用于现场检测的阻碍[55]。
李颖等[56]用分子印迹聚合物(molecularly imprinted polymer,MIPs)作为传感器识别元件的敏感材料,制成用于检测DBP的分子印迹电化学传感器。印迹孔穴中的识别位点能够对DBP产生专一的响应电流,Fe3O4不仅使材料易于分离,还利于铁氰化钾探针在玻碳电极表面的吸附,与Au纳米粒子一同起到增强导电性的作用。该方法具有较好的选择性和稳定性,但没有解决电化学传感器普遍存在的寿命短的缺点。
El-sharif等[57]使用成本较低的一次性丝网刷电极,以4-氨基苯酚(4-AP)作为功能单体,构建了一种一次性MIP传感器。亚铁/铁氰化物作为氧化还原探针的使用解决了邻苯二甲酸酯在适合水溶液分析的电极电势范围内没有氧化还原活性的问题。构建价格低廉的一次性电化学传感器有效地避免了基于水基电解质溶液的电化学传感器寿命较短和成本高的问题[58]。但该传感器不适用于多次或连续检测,同时样品需要经过固相萃取等方法进行浓缩,操作较为繁琐。
电化学法是检测邻苯二甲酸酯灵敏度最高的快速检测方法。随着新材料的出现和电化学原理和方法的发展,解决电化学传感器寿命短、不易储存的缺点或许是未来电化学传感器的研究方向之一。
5 展望
塑化剂污染问题已成为当前食品安全卫生领域不可避免的话题之一。在塑料食品包装使用越来越普遍的今天,食品中塑化剂含量超标的问题更应该受到重视。随着“起云剂”事件将塑化剂安全问题引入消费者的视线,越来越多的消费者对食品中塑化剂的安全性,特别是对儿童食品中塑化剂是否超标愈发关注。目前,基于色谱、质谱和光谱技术的PAEs传统检测方法能够保证结果的准确性,但是大多需要大型专业仪器,且具有前处理过程复杂、操作繁琐、费时和成本高昂等缺点。相较于传统检测方法,现今存在的快速检测方法前处理过程更加简单,部分快速方法的准确性已经接近甚至超过传统检测方法。然而,基于荧光或拉曼光谱的快速检测方法仍需要专业设备支持;酶联免疫传感器、电化学传感器可以实现现场原位检测,但成本高、难以长期保存(表7)。现有的检测方法都对操作有一定要求,需要经过专业培训才能够完成检测。未来PAEs快速检测方法正在向更快速、成本更低廉、结果更准确的方向发展。与此同时,开发低成本小型化仪器或利用信息技术开发手机App、小程序辅助检测或将成为快速检测技术开发的又一方向。

表7 几种快速检测方法的不足Table 7 Shortcomings of several rapid detection methods
