人工智能赋能麻醉监护仪实现麻醉深度监测
2023-02-12郭艺杜秋晨吴朦朦李冠华
【作 者】 郭艺,杜秋晨,吴朦朦,李冠华
1 火箭军特色医学中心,北京市,100088
2 北京航空航天大学,北京市,100191
0 引言
麻醉是指由药物产生的中枢神经以及周围神经的临时性功能抑制,表现为可逆性意识消失、肌肉松弛等临床现象[1]。麻醉深度监测是手术中至关重要的环节,对手术的平稳进行和患者的术后康复起着决定性的作用。麻醉深度监测方式包括主观方式和客观方式,主观方式由麻醉医师通过观察给药后患者的心跳、呼吸、循环以及肌张力等生命体征来判断麻醉深度,虽然准确性高,但对麻醉医师经验要求较高;客观方式采用监护仪器监测患者的各项生命体征,通过特定算法给出麻醉深度的定量评价。客观方式直观反映麻醉深度的数值,减轻了手术中麻醉医师的工作量,已成为主要研究方向,研究重点在于建立生命体征与麻醉深度之间的关系。
目前由于麻醉药物的作用机制没有得到充分认识,麻醉深度监测没有形成统一的评价标准[2]。大量研究发现脑电(electroencephalogram,EEG)信号能够反映药物对患者中枢神经的影响,进而反映患者的意识状态,已成为主流的麻醉深度监测方法,其中应用最广泛的是脑电双频指数(bispectral index,BIS)。文献[3]提出基于BP(back propagation)神经网络的脑电图麻醉深度预测模型;文献[4]设计了用于麻醉深度检测的模糊神经网络模型。虽然脑电信号能够反映麻醉深度,但由于脑电监测仪成本较高,并且脑电信号容易受到年龄、低温和脑缺氧等因素影响,导致麻醉深度监测有较大局限性。
心电图(electrocardiogram,ECG)是围术期监测的生理特征之一,已作为国际公认标准方法[5]。由于心电图可通过普通麻醉监护仪低成本获取,并且心电图包含的信息能够反映麻醉深度,很多研究者从脑电图的研究转向心电图的研究。脑电信号和心电信号均具有非线性特征,用于脑电信号麻醉深度估计的人工智能方法同样可用于心电信号。文献[6]提出了基于心电图(ECG)和脉搏波(photoplethysmography,PPG)的麻醉深度预测,将一维ECG和PPG信号分段拼接成二维图像,利用多层卷积神经网络(convolutional neural network,CNN)进行麻醉深度预测;文献[7]利用心率变异度(heart rate variability,HRV)作为特征,基于人工神经网络实现麻醉深度判断。在上述方法的基础上,本研究充分考虑监护仪信号的时序性,提出了卷积神经网络(CNN)和长短期记忆网络(long and short-term memory network,LSTM)相融合的麻醉深度监测模型。
1 材料与方法
基于人工智能的麻醉深度监测方法的整体架构如图1所示。核心为基于卷积神经网络和长短期记忆网络的人工智能算法,算法输入为来自麻醉监护仪的ECG、PPG和HRV推导出的心率变异性,算法输出为麻醉深度分类,包括麻醉诱导、麻醉维持和麻醉苏醒3个阶段。
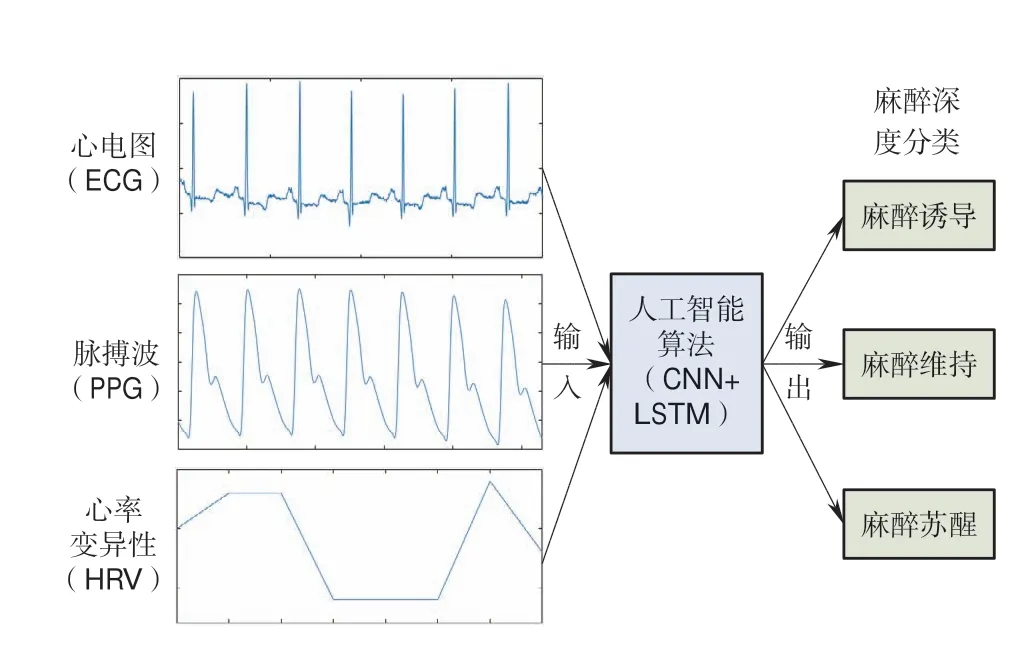
图1 人工智能麻醉深度监测方法整体架构Fig.1 Overall framework of artificial intelligence anesthesia depth monitoring method
心电图和脉搏波是围术期中重要的监测信号,能够直接反映麻醉深度。心率变异性指心跳周期之间的差异情况,能够反映中枢神经系统对心脏搏动节律的调整,已经作为自主神经功能评价中最准确的无创指标,与麻醉深度密切相关[8]。心率变异性虽然不能直接从麻醉监护仪中观察得到,但可以通过心电图中两个相邻的R波间隔计算得出。
人工智能算法采用基于CNN和LSTM的分类方法。CNN通过卷积操作提取3种输入信号的局部信息,LSTM通过复杂的门控结构学习长时间的时序信息,并且还可以对这些信息进行筛选,对序列数据具有很强的特征提取能力。因此,我们在文献[9]的模型基础上进行改进,设计了CNN和LSTM相结合的人工智能麻醉深度监测算法模型,如图2所示。
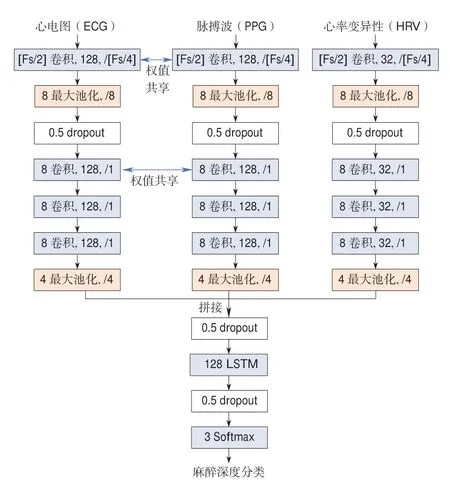
图2 人工智能麻醉深度监测算法模型Fig.2 Artificial intelligence anesthesia depth monitoring algorithm model
算法模型分为上下两个部分,上半部分采用CNN提取ECG、PPG和HRV的局部特征信息,对应上半部分的3个分支。3个分支的模型结构相同,均包含4个卷积层、2个最大池化层和1个dropout层。由于ECG和PPG的波形和采样频率相近,ECG和PPG分支采用相同的卷积核大小、数量和步长等参数。为了利用多任务学习的思想提高特征提取的有效性,使ECG和PPG分支的前两个卷积层共享权值,即采用相同的权值。前两个卷积层主要用于提取浅层特征,可看作提取不同信号特征的滤波器,通过ECG和PPG两个任务的训练,提取到的特征更具通用性,且降低了模型参数量。后两个卷积层用于提取深层特征,即ECG和PPG特有的特征,不采用共享权值方式,两者分别训练。由于HRV通过ECG计算得到,HRV的变化率低于ECG,所以提取HRV特征的卷积核数量较少,在降低模型参数量的情况下保证模型准确性。下半部分是上半部分的3个特征按通道拼接后,通过LSTM提取的时序特征,最后通过Softmax获取每个麻醉深度分类的概率,选择最大概率对应的类别作为麻醉深度分类。
人工智能算法模型采用迁移学习的方式进行训练。迁移学习利用麻醉深度监测方法之间的相关性,把已经训练好的模型参数迁移到新的模型中,赋予新的模型先验知识,从而提高分类精度。本研究提出的人工智能算法模型在文献[9]的基础上进行迁移学习,两者的模型结构基本相同,本研究在模型上半部分设计了3个分支,文献[9]上半部分是单个分支,因此3个分支采用相同值初始化。
在3种麻醉深度分类中,麻醉苏醒预测的准确性至关重要,因为患者可能会产生术中知晓,影响术后恢复,反之,麻醉诱导和麻醉维持之间分类错误并不会对患者产生较大影响。因此,模型训练中的损失函数采用加权Softmax函数对3种麻醉深度分类结果赋予不同的权重,即加大麻醉苏醒预测错误的惩罚。
2 实验结果
实验数据集的建立是开展实验的前提条件。从麻醉监护仪中采集了50例全身麻醉患者手术过程中的ECG和PPG数据,并计算出HRV作为算法模型的输入数据。由经验丰富的麻醉医生记录手术过程中患者的麻醉深度,作为算法模型的标签数据。由于输入数据和标签数据是连续的,按每5 s截取一段输入数据和对应的标签数据构建数据集,认为5 s之内麻醉深度保持不变。共提取出1000条数据构成数据集。
实验中所用的硬件平台CPU为Intel i7-7700K,16 GB内存,显卡为NVIDIA GTX1080,8 GB显存。软件系统为CentOS7,Python版本为3.6.8,深度学习框架为Tensorflow 1.11.0。实验数据集按照4∶1随机划分为训练集和测试集,即训练集800条数据、测试集200条数据。训练前需要选取合适的超参数,主要包括批尺寸和学习率。批尺寸的选择主要考虑显存容量,实验中设置最大批尺寸为32。学习率的选择由训练过程的误差曲线决定,曲线下降缓慢应增大学习率,曲线振荡较大应减小学习率,通过试验选择学习率为0.001,能保证模型稳定收敛。
为了证明本研究所提出的人工智能模型有效,以本研究中采集的数据集作为实验样本,对比了文献[6]和文献[9]的结果。同时为了证明迁移学习的有效性,对比了模型训练中没有使用和使用了迁移学习的情况,评价指标采用准确率和损失值,实验结果如表1所示。

表1 实验结果对比Tab.1 Comparison of experimental results
本研究提出使用人工智能技术赋能麻醉监护仪实现麻醉深度监测方法。该方法从麻醉监护仪中获取ECG和PPG,并从ECG中计算出HRV,将ECG、PPG和HRV作为人工智能模型的输入数据。人工智能模型采用CNN和LSTM相融合的结构,利用权值共享的方式减少训练参数并提高模型的麻醉深度分类能力。人工智能模型采用迁移学习的方法进行训练,采用加权Softmax损失函数,提升了麻醉苏醒状态监测的准确性,降低了患者术中知晓的风险。实验结果表明,本研究提出的方法能够有效监测麻醉深度,准确率达94.1%,优于所有对比方法,表明本方法能够实现准确的麻醉深度监测。
本研究的创新点在于:
(1)提出卷积神经网络和长短期记忆网络相融合的麻醉深度监测模型,具有提取长时间段内生理特征的能力,可结合过去和现在的生理特征,提高麻醉深度估计的准确性。
(2)采用ECG、PPG、HRV作为监测模型的输入,可通过普通麻醉监护仪采集到这些信息,不增加额外的监护仪器,降低了手术成本。
本方法虽然在麻醉深度监测方面取得了较好的效果,但由于仅使用了EGG、PPG作为判断麻醉深度的条件,没有充分利用麻醉监护仪的数据。后续研究中应考虑血氧饱和度等麻醉监护数据,进一步提高麻醉深度监测的准确性。
