肠道菌群视角下非酒精性脂肪性肝病的治疗策略
2023-02-11傅伟强周剑波吴雄健黄才斌
傅伟强,周剑波,吴雄健,黄才斌*
非酒精性脂肪性肝病(NAFLD)是指除外酒精和其他明确的损肝因素,以肝脏脂肪沉积超过5%为主要特征的临床综合征,其疾病谱主要包括非酒精性肝脂肪变、非酒精性脂肪性肝炎(NASH)、肝硬化以及肝细胞癌(HCC)[1]。NAFLD与肥胖、胰岛素抵抗、2型糖尿
病及心脑血管疾病等密切相关,被认为是代谢综合征的肝脏表现[2]。基于此,专家共识提议将NAFLD改名为代谢相关性脂肪性肝病(MAFLD)[3]。据统计,目前NAFLD的全球患病率在成年人中约为25%,已成为最常见的慢性肝病,且预计未来10年NASH的发病率将增加56%[4]。NAFLD在南美洲、北美/欧洲、非洲等地区的患病率分别为30%、24%、13%,在亚洲患病率为5%~51%[2]。我国NAFLD的患病率为6%~27%,已超过慢性乙型肝炎成为第一大慢性肝病,可导致肝硬化、HCC等严重后果,严重影响国民健康和经济发展[5]。
NAFLD涉及肝脏脂肪沉积、炎性反应、肝细胞变性坏死、纤维化等一系列病理过程[6]。目前治疗相关的研究主要集中在改善肝脏炎症和纤维化,尚无批准上市的治疗药物[7]。近年研究揭示肠-肝轴与NAFLD发生发展相关,调控肠道微生物可能会成为NAFLD治疗新靶点[8-9]。运动、饮食、微生态制剂、抗生素、粪菌移植、噬菌体等干预措施均可通过改变肠道菌群缓解NAFLD。本文就肠道菌群与NAFLD的关系、以调整肠道菌群为NAFLD治疗靶点的研究进展进行综述,并基于肠道菌群治疗NAFLD绘制简要机制图(图1),以期为临床防治NAFLD提供思路及参考。
本文文献检索策略:以“Intestinal flora,metabolic syndrome,probiotics,probiotics,synbiotics,metazoa,antibiotics,exercise,diet,Microecological preparation,FMT,bacteriophage,NAFLD”为英文关键词检索PubMed、Medline、Web of Science;以“肠道菌群、代谢综合征、微生态制剂、益生菌、益生元、合生元、后生元、抗生素、运动、饮食、粪菌移植、噬菌体、非酒精性脂肪性肝病”为中文关键词检索中国知网、万方数据知识服务平台及中国生物医学文献服务系统。检索时间为建库至2022-06-15。文献纳入标准:基于肠道菌群防治NAFLD的临床研究、基础研究及文献研究。文献排除标准:未涉及肠道菌群、与NAFLD防治相关性较弱、数据记录不详细、观点有重叠、文献质量差。
1 肠道菌群与健康
人体肠道内生活着数以百万计的微生物动态群落,超过500个种类,包含的基因是人基因的100倍[10]。肠道菌群中超过99%为专性厌氧菌,其余包括需氧菌、兼性厌氧菌或其他种类微生物[11]。正常情况下,尽管受到年龄、生活习惯、情绪等因素的影响,这些肠道菌群仍可保持动态平衡,与人体长期互利共生,在维持肠道微生态平衡和维护人体健康方面发挥着积极作用[12-13]。一旦这种平衡被破坏,可能导致一系列疾病的发生[10]。甚至有研究证明,结直肠癌的发病与肠道菌群的失衡有直接关系[12]。
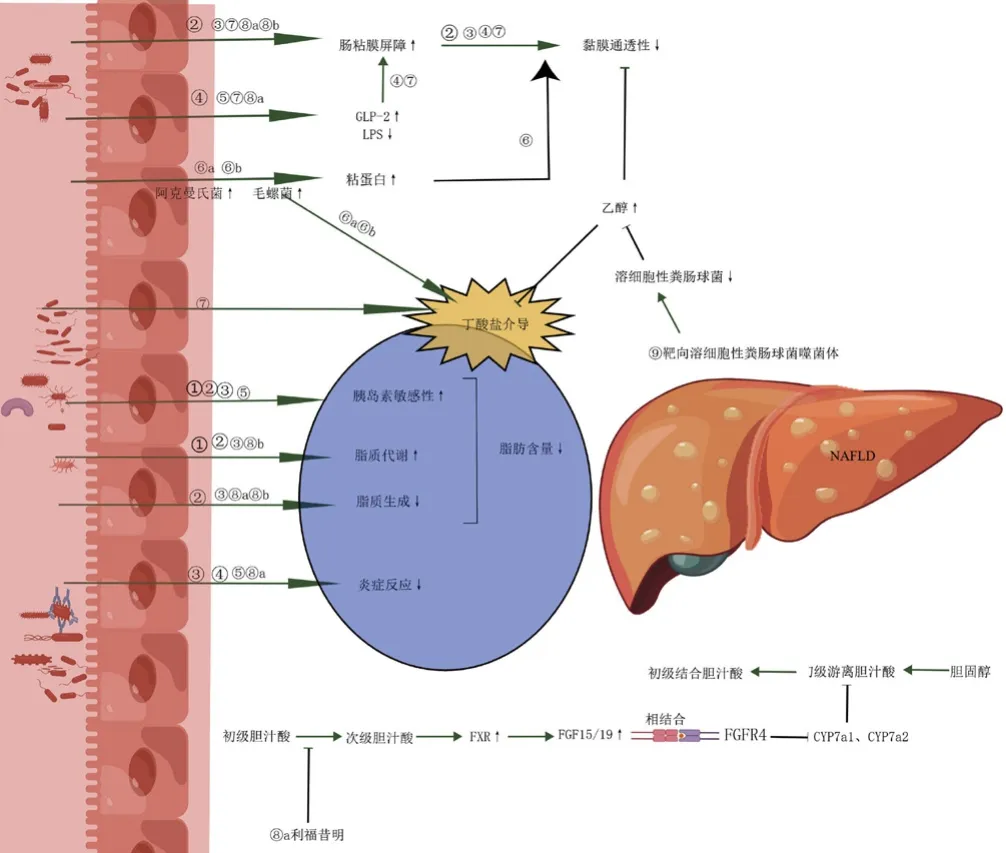
图1 基于肠道菌群治疗NAFLD的机制图Figure 1 The mechanism of action of NAFLD treatment targeting the intestinal microbiota
2 肠道菌群与NAFLD
研究证实NAFLD患者肠道菌群多样性及优势菌群构成比降低,与健康人群相比,反刍菌科、拟杆菌和普氏杆菌减少,而变形菌、大肠埃希菌、瘤胃球菌和厚壁菌增加[14-15]。然而,也有研究发现NASH患儿肠道拟杆菌增多而厚壁菌减少。此外,一项研究发现,约60%的NAFLD患者的肠道中有能够产生高浓度酒精的肺炎克雷伯菌,而只有6%的健康人携带了这种细菌[16]。上述差异可能与两种人群的饮食结构、生活环境、年龄及基因遗传等异质性相关,前者的肠道环境可能比其他人更适合肺炎克雷伯菌的生长和定植。多项横断面研究表明,肠道菌群的扰动与NAFLD严重程度存在关联,拟杆菌和大肠埃希菌丰度增加与NAFLD晚期纤维化密切相关,而厚壁菌在轻中度NAFLD患者丰度更高,提示与疾病严重程度相关[17]。尽管NAFLD患者存在肠道菌群失调,但通过调控肠道菌群改善NAFLD已成为治疗新靶点。
3 肠道菌群介导NAFLD发生的机制
肠道和肝脏通过肠-肝轴双向关联,肝脏将合成的胆汁酸和其他生物活性物质分泌至肠道,这些成分被肠道菌群分解代谢可随门静脉吸收入血重新回流至肝脏。肠道菌群介导NAFLD发生的机制可能包括以下几种,(1)肠道通透性增加:NAFLD患者肠道菌群失衡会导致肠道屏障完整性受损,细菌及其代谢物从肠腔转移到固有层,同时产生的毒素通过门静脉进入肝脏激发炎性反应[18]。(2)增加内生乙醇的生成:肠道菌群产生过多的内源性乙醇能增加肠道通透性,促进肠内有害物质进入肝脏,并阻碍脂质代谢、产生氧自由基,加速肝脏脂肪变性及炎性反应进程[16]。(3)调节胆汁酸代谢:胆汁酸可以通过法尼酯X受体(FXR)和G蛋白胆汁酸偶联受体5(TGR5)信号通路减少肝脏炎症和纤维化,当肠道菌群紊乱时,可通过影响胆汁酸代谢下调FXR信号增强脂肪生成并抑制脂肪酸β氧化而促进NAFLD发展[19]。(4)参与胆碱代谢:胆碱是细胞膜的一种成分,肠道菌群多样性改变导致细菌合成所需胆碱增多,肝脏产生极低密度脂蛋白(VLDL)所需的胆碱减少,使得肝细胞内的三酰甘油(TG)向外周转运障碍,在肝内沉积,从而导致NAFLD的发生[20]。(5)短链脂肪酸:短链脂肪酸可激活肠道L细胞释放类胰高血糖素样肽1(GLP-1)和胃肠激素酪酪肽(PYY)调节代谢,同时直接抑制组蛋白去乙酰化酶上调脂质氧化基因的表达,促进肝脏脂质氧化[21]。
4 基于肠道菌群治疗NAFLD的方式
4.1 运动 目前研究表明,运动不仅直接影响代谢反应,而且影响肠道微生物组结构和功能,后者可能是运动改善NAFLD的机制[22]。与久坐不动的人群相比,保持积极训练的运动员肠道内阿克曼菌和粪杆菌丰度显著增加,这种情况也见于肥胖患者和进行体育锻炼的非肥胖人群,这两种菌群可以促进肝脏脂质代谢,对健康有积极影响[23-24]。CARBAJO-PESCADOR 等[25]建立高脂饮食诱导的NAFLD大鼠模型,将其分为对照组和实验组,对照组保持大鼠久坐不动,实验组接受为期5周的有氧和阻力训练,评估运动对大鼠肠道微生物组成和功能平衡的益处,以及对早期肥胖和NAFLD发病的后续影响。该研究发现,经过5周训练的大鼠最终体质量低于对照组,肠道拟杆菌和变形杆菌的相对丰度提高,芽孢杆菌、疣微菌和厚壁菌丰度降低,显著纠正高脂饮食引起的微生物失衡。进一步分析发现,对照组大鼠表现出微泡和大泡肝脂肪变性,NAFLD活动评分显著增加,而实验组大鼠肝脂滴存在减少,并且空腹胰岛素和胰岛素敏感性均有所提高,结果证实了运动可通过调控肠道菌群改善NAFLD代谢紊乱。近期的一项随机对照试验显示,NAFLD患者在为期8.6个月的有氧运动后,肠道微生物组成发生了显著变化,瘤胃球菌、拟杆菌属成员的丰度增加,而瘤胃球菌科与纤维化严重程度呈负相关,且肝脏脂肪含量下降了24.4%,表明运动干预明显改变了微生物组的丰度和功能[26]。但目前关于NAFLD患者肠道菌群的研究主要集中在分类水平而不是功能能力上,运动调节肠道菌群改善NAFLD的具体机制仍不清楚,仍需进一步的研究加以解析,但目前研究仍肯定了适量运动对NAFLD患者的发生和进展有积极的影响,因此推荐NAFLD患者适当的有氧运动,且长期维持。
4.2 饮食调节 饮食调节及体育锻炼仍然是NAFLD管理的基石,其中饮食调节是简单、有效调节肠道菌群的方法之一[27]。高脂饮食已被证实与肝脂肪变性、炎症和肝纤维化有关[28]。动物实验显示长期高脂饮食可使肠道微生物的多样性下降,减少双歧杆菌和拟杆菌菌群数量,影响胆汁酸代谢,导致FXR信号下调,脂肪生成增加并抑制脂肪酸β氧化,促进NAFLD发展[19]。而高糖饮食则可以降低胰岛素敏感性,提高肝脏脂肪生成,促进NAFLD发生。因此NAFLD患者饮食管理建议采用低脂肪、低碳水化合物饮食并限制每日热量[29]。一项横断面研究显示,长期坚持地中海饮食是超重者肝纤维化和非酒精性脂肪性肝炎的独立保护因素[30]。有学者探究地中海饮食与有氧运动结合对NAFLD患者肠道菌群的影响,发现地中海饮食组肠道菌群α多样性提高,瘤胃球菌、厚壁菌及拟杆菌菌群丰度相对增加,而瘤胃球菌可通过改善胃肠道屏障完整性、调节肠道微生态来保护肝脏,此外,研究发现当饮食干预与有氧运动相结合时,地中海饮食的有益效果会更大[19,31]。然而,即使在相同饮食模式下,个体间的反应存在差异,因此,实行个体化饮食治疗,对识别预测饮食相关肠道菌群,为NAFLD患者制定干预措施提供依据是有必要的。
4.3 微生态制剂 鉴于肠道菌群与NAFLD发生、发展密切相关,调节肠道菌群更为直接的微生态制剂已在NAFLD的防治中进行了相关研究。微生态制剂主要包括益生菌、益生元、合生元及后生元等,目前最常见且临床上应用最多的是益生菌。
4.3.1 益生菌 根据世界卫生组织定义,益生菌是指足量摄入时对健康有益的活微生物[32]。目前关于益生菌对NAFLD防治的研究主要集中在动物实验方面,临床试验较为有限。有研究发现益生菌可以增加肠道菌群多样性和有益菌相对丰度,改善黏膜通透性,抑制脂质合成及促进脂质氧化代谢,降低肝脏的炎症和纤维化[33-35]。AHN等[36]研究发现,给予益生菌的肥胖NAFLD患者的嗜酸乳杆菌、鼠李糖乳杆菌、戊糖假单胞菌、乳酸双歧杆菌的相对丰度增加,且其肝内脂肪分数及体质量较安慰剂组下降。DUSEJA等[37]一项关于评估益生菌对成年人NAFLD患者疗效的随机、双盲、安慰剂对照试验,随访1年后发现益生菌组生化标志物丙氨酸氨基转移酶(ALT)和天冬氨酸氨基转移酶(AST)、瘦素、肿瘤坏死因子α(TNF-α)和内毒素水平均有下降,肝活检显示,益生菌组肝细胞气球样变(P=0.036)、小叶炎症(P=0.003)和NAFLD活动性评分(NAS)(P=0.007)与基线相比显著改善,与安慰剂相比改善更为明显。相关荟萃分析同样证实益生菌的使用显著降低了NAFLD患者的体质指数(BMI)、ALT、AST、胰岛素抵抗和脂肪肝的超声分级,但由于益生菌菌株的不同、剂量模式和治疗持续时间的差异,不同研究显示的改善幅度并不统一[38]。因此,未来需要就益生菌的类型、剂量和治疗时间达成共识,并进行更为完备的大样本、多中心前瞻性研究来验证其有效性。
4.3.2 益生元 益生元本身不能被人体消化吸收,但可选择性地刺激有益细菌的生长和活性来改善宿主健康[39]。大量试验支持益生元在治疗NAFLD上的有效性。在动物实验中,益生元已被证明可诱导啮齿动物肠道菌群组成的变化,增加双歧杆菌及乳杆菌丰度,并刺激GLP-2的产生,调节内毒素易位,从而改善肠道屏障的功能[40]。此外,GLP-2还可影响血浆脂多糖水平,降低肝脏炎症和氧化应激,减轻肝脏脂质积累和脂肪性肝炎[41]。在临床试验中,BOMHOF等[42]研究表明益生元能够增加NASH患者肠道粪杆菌和双歧杆菌的丰度,并降低血清AST、ALT水平,改善经组织学证实的肝脂肪变性。CHONG等[43]临床试验同样支持益生元在调节肠道菌群及改善脂肪变性等方面的疗效。
4.3.3 合生元 合生元是益生元和益生菌的组合,可用于替代功能失调的肠道菌群,改善胰岛素抵抗,降低促炎因子和内毒素水平,改善肝脏组织学[44-45]。SCORLETTI等[46]发现补充合生元能够改变NAFLD患者原有的肠道菌群,增加放线菌和双歧杆菌相对丰度,降低颤螺菌相对丰度。FEROLLA等[47]进行了一项关于合生元对NAFLD患者的随机双盲试验,在补充由罗伊乳杆菌、瓜尔豆胶和菊粉组成的合生元后,观察到促炎细胞因子IL-6、TNF-α水平显著下降,血清AST、ALT及碱性磷酸酶(ALP)水平得到改善,中度和重度脂肪变性患者的比例从40.7%下降到18.5%,轻度脂肪变性患者从59.2%增加到81.5%,显著改善了脂肪性肝炎患者的肝纤维化。相关荟萃分析同样证实,补充合生元可诱导肠道菌群发生改变,有效降低BMI和肝酶水平,改善肝脏脂肪变性[48]。
4.3.4 后生元 后生元是近年来新提出的概念,包括在宿主中具有潜在生物活性的细菌代谢产物和细胞成分,包括某些维生素、短链脂肪酸、多胺、支链氨基酸或细菌细胞壁的成分,通过刺激免疫系统影响肠黏膜屏障的完整[49-50]。目前关于后生元在NAFLD疗效的数据仍然很少,主要限于临床前研究。在老年小鼠中,热灭活副干酪乳杆菌D3-5中的脂磷壁酸可使肠道内阿克曼菌丰度增加,黏蛋白显著表达,增强黏膜屏障功能,预防高脂饮食喂养引起的代谢功能障碍[51]。MA等[52]研究发现多胺亚精胺给药可改变肥胖小鼠肠道菌群的组成和功能,特别是产生丁酸盐的毛螺菌属丰度增加,显著改善肠道屏障功能及代谢表型。
4.4 粪菌移植(FMT) FMT是指将供体粪便中的功能菌群移植至患者肠道中,改善原有肠道菌群失调,重建正常肠道微生态,实现疾病的治疗[53]。动物实验方面,高脂饮食喂养的小鼠在FMT干预后,肠道拟杆菌门减少,厚壁菌门增加,肠道屏障功能和内毒素血症改善,肝脏脂质积累减少和促炎细胞因子水平降低,脂肪性肝炎减轻[54]。一项针对代谢综合征患者的研究表明,来自瘦供体的FMT改善了胰岛素敏感性及肝内脂质代谢,而这与产生丁酸盐的菌株增加有关[55]。WITJES等[56]一项随机双盲对照试验,比较了3个为期8周的素食供体FMT与自体FMT对NAFLD严重程度的影响,研究发现FMT干预后肠道菌群发生显著变化,且向供体微生物菌群特征趋同,在拟杆菌及厚壁菌上这种趋势更为明显。然而整体NAFLD活动评分及纤维化评分在统计学上并无明显差异,但值得注意的是,坏死性炎症评分(包括小叶炎症和肝细胞气球样变)有改善的趋势。一项针对21例NAFLD受试者的试验显示,FMT可改善NAFLD患者的肠道通透性,但随访6个月未见胰岛素敏感性增加或肝内脂质含量降低[57]。FMT疗效与“供体”特征密切相关,特别是粪便微生物群的丰富度、多样性和相容性等,所以FMT治疗NAFLD是否可以在临床上应用,仍需要大量的临床试验提供依据。
4.5 抗生素 利福昔明是衍生于利福霉素的非全身性抗生素,其在胃肠道中几乎不被吸收,不会显著影响肠道微生物组的多样性[58]。在对NAFLD模型小鼠的实验中发现,口服利福昔明可降低肠道通透性及内毒素水平,减少肝内脂质沉积,并降低NASH小鼠AST、ALT水平,同时减轻肝脏炎症和纤维化。此外,肠道菌群发生改变,并减少回肠末端的次级胆汁酸水平,逆转Fxr-FGF15信号的激活,促进肝脏中的CYP7a1和CYP7b1的表达,这可能是利福昔明缓解NASH的机制[59],与FUJINAGA等[60]研究相一致。而在评估利福昔明对人类NASH治疗的疗效上研究结论相互矛盾。GANGARAPU等[61]研究纳入42例经活检证实为NAFLD的患者,利福昔明(1 200 mg/d)短期给药28 d后发现,内毒素水平、AST、ALT、促炎细胞因子以及NAFLD活动评分显著下降,抗生素的这种改善归因于肠道微生物群和胆汁酸代谢的改变,以及FXR信号传导的下调。然而,在COBBOLD等[62]研究中,接受为期6周利福昔明(400 mg,2次/d)治疗后,患者血清ALT水平及胰岛素抵抗增加,提示对NASH没有益处,且治疗后粪便微生物群的相对丰度没有差异。以上差异可能与不同的治疗剂量和持续时间相关。同样有研究发现三氯生可增加NAFLD模型小鼠肠道有益菌的相对丰度,包括乳酸杆菌、双歧杆菌和毛螺菌科,同时增加拟杆菌门/厚壁菌门的比例,显著改善肝脏脂肪变性,提示三氯生可以调节肠道菌群为靶点治疗NAFLD[63]。然而,抗生素可能具有不同的作用,MAHANA等[64]研究发现,用抗生素治疗的小鼠表现出严重的胰岛素抵抗,同时增加NAFLD组织学病变的发生率和严重程度,这与抗生素扰动肠道菌群导致双歧杆菌和普雷沃菌的变化有关。因此,抗生素是一把双刃剑,一方面可以通过灭活有害菌群调节肠道菌群紊乱达到缓解或者治疗的目的,另一方面长期使用抗生素可能会导致细菌耐药的发生,影响体内有益菌的生长,产生新的菌群紊乱。
4.6 噬菌体 噬菌体对细菌具有特异性,可靶向编辑肠道微生物群落结构,目前这种方法尚未在NAFLD中进行评估,但临床前研究支持其对酒精相关性肝病的有效性[65]。DUAN等[66]使用酒精性肝病患者的粪便定植无菌小鼠,研究靶向溶细胞性粪肠球菌的噬菌体的疗效,发现这些噬菌体消除了乙醇诱导的肝损伤和脂肪变性,而不影响肠道菌群的整体组成。这种溶细胞性粪肠球菌的存在已被证明与酒精性肝病的严重程度以及死亡率有关。然而,针对肝病的噬菌体疗法目前仅在小鼠模型中进行了研究,还需要进行临床试验来评估其有效性,以及对NAFLD患者的疗效及安全性。
5 小结与挑战
肠道菌群在维持肠道平衡及NAFLD发生发展中具有重要作用,运动、饮食、益生菌制剂、FMT、抗生素等以调整肠道菌群为靶点的干预措施可有效缓解NAFLD,噬菌体有效性还需进一步明确,但目前有关其在NAFLD治疗上的相关试验存在异质性,而这种异质性可归因于多个方面。首先,通过锻炼、饮食、益生菌制剂及FMT等疗法虽可短暂改变肠道菌群结构,但当干预消失时这种改变并不能长期维持,疗效受到制衡。其次,以上干预措施在具体方案上并未达成共识,如饮食模式的改善、锻炼的强度和持续时间、微生态制剂的菌群种类、剂量及频率等;另外,评估疗效使用的是血清学生物标志物,而非作为金标准的肝活检,这些差异均可能会对试验结果造成影响。最后,尽管现有的横断面研究体现出相关性,但建立肠道菌群-NAFLD的因果关系仍然是一个挑战,具体哪些菌株可能驱动NAFLD的一些关键特征,如脂肪变性、炎症、胰岛素抵抗或纤维化的进程仍有待进一步阐明。
作者贡献:傅伟强负责文章的构思和设计、文献整理、撰写论文;周剑波负责文献收集;吴雄健负责论文修订;黄才斌负责文章的质量控制及审校,对文章整体负责、监督管理。
本文无利益冲突。
