术前颈椎椎体CT值与颈椎前路椎间盘切除融合术后邻近椎间隙高度变化的相关性研究
2023-02-09凯依塞尔阿布都克力木李磊杨晓凯任军刘帅
凯依塞尔·阿布都克力木,李磊,杨晓凯,任军,刘帅
1958年SMITH和ROBINSON首次提出了颈椎前路椎间盘切除融合术(anterior cervical discectomy and fusion,ACDF)[1],现已逐渐成为治疗多种颈椎退行性疾病的标准术式,其有效性及安全性得到了广泛的认可[2]。该术式是对被压迫的脊髓、神经根进行减压,恢复正常的椎间隙高度和生理曲度,使相应的节段维持稳定。邻近节段退变(adjacent segment degeneration,ASD)是ACDF术后远期严重并发症之一,主要表现为邻近椎间隙退变,即椎间盘变形、突出,椎间隙变窄,骨赘形成,邻近椎体的不稳、滑移等[3-4],部分有神经功能障碍的ASD患者需再次行手术治疗,严重影响ACDF 术后疗效[2]。
骨密度是影响脊柱融合术后疗效的重要因素之 一[5-6]。定量计算机断层扫描(quality control technology,QCT)和双能X射线吸收法(dual-emission X-ray absorptiometry,DXA)是目前测量骨密度的代表性方法。DXA最常用于髋部或腰椎骨密度的检测[3-4],但在椎体压缩性骨折、血管钙化、椎体退行性病变等患者中DXA误差较大,其结果不如QCT可靠。由于QCT辐射量较大,临床上实际应用较少。颈椎椎体CT值与T值之间存在密切关系,可在一定程度上反映椎体骨密度。术前测量颈椎椎体CT值可能对患者术后邻近椎间隙丢失有一定的预测作用。国内外有关ACDF前颈椎椎体CT值与术后邻近间隙高度关系的研究较少。本研究旨在探讨ACDF术前颈椎椎体CT值与上邻近椎间隙高度丢失之间的关系。
1 对象与方法
1.1 研究对象 选取2017年1月至2021年1月在新疆医科大学第六附属医院脊柱外科明确诊断为脊髓型或神经根型颈椎病,并接受单节段ACDF治疗的86例患者为研究对象。纳入标准:(1)明确诊断为脊髓型或神经根型颈椎病并接受单节段ACDF前路钛板固定;(2)既往无颈椎前路或后路手术史;(3)术前行三维CT扫描,随访资料齐全。排除标准:(1)患有颈椎感染、使用零切迹融合器、颈椎肿瘤、创伤、颈椎结核者;(2)术前诊断为骨质疏松症,并接受抗骨质疏松药物治疗者;(3)术前邻近间隙存在严重退行性改变的患者;(4)融合器或钛板位置欠佳,术后有切口感染等严重并发症者。
1.2 手术方法 患者均采用标准Smith-Robinson颈前入路术式,透视下确定责任间隙后进行椎间盘切除术,通过切除后纵韧带及增生的骨赘,使受压的脊髓和神经根获得充分的减压。去除椎间隙上、下的软骨终板,选择适合的椎间融合器,钛板固定。透视确认后,放置引流,无菌敷料包扎。并根据术后状况,术后3 d佩戴颈托下床活动。术后1周视切口状况予以拆线。出院后定期门诊复查。随访截至2022-02-01。
1.3 临床资料 收集患者年龄、性别、随访时间和体质指数(BMI),并测量术前颈椎椎体CT值和术后1周与末次随访时的上邻近椎间隙高度,计算椎间隙高度丢失值。患者术前CT资料均由新疆医科大学第六附属医院影像中心CT设备(Definition Flash双源CT,西门子,德国,管电压 120 kVp)扫描获得,采用 Senyint PACS workstation ver 2.0标准图像存档软件〔心医国际数字医疗系统(中国)有限公司〕测量每个椎体的上终板正下方(刚好不包括上终板的一层)、椎体中央、下终板正上方3个CT值,记录每位患者上邻近间隙头侧和尾侧两个椎体共6个CT值,并取其平均值作为术前颈椎椎体CT值。横断面松质骨内圈定的尽量大的椭圆形敏感区,不包括皮质骨,以及骨岛、空洞、静脉窦等骨质异常区(图1)。采用侧位X线测量融合节段上邻近椎间隙的前、中、后高度(图2)。上、下终板最前点间的距离为椎间隙前高度,上、下终板中点间的距离为椎间隙中高度,上、下终板最后点间的距离为椎间隙后高度。计算其平均值作为上邻近椎间隙高度。

图1 椎体CT值的测量Figure 1 The measurement of HU values
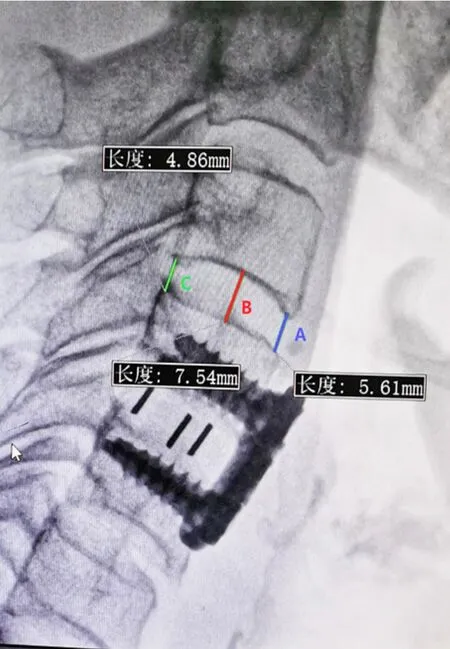
图2 上邻近间隙高度的测量Figure 2 Measurement of upper adjacent segment height
1.4 分组方法 将术后1周与末次随访时的侧位X线进行对比,测量融合节段上邻近椎间隙高度。若末次随访的椎间隙高度丢失值>术后1周时测量值的20%,则诊断为上邻近椎间隙退变,纳入A组,如果<20%则纳入B组。依据椎间隙高度丢失值计算结果,15例患者纳入A组,71例患者纳入B组。
1.5 统计学方法 采用SPSS 26.0统计学软件分析数据,计量资料采用(±s)表示,两组间比较采用独立样本t检验,计数资料的分析采用χ2检验。采用二元Logistic回归分析探讨上邻近椎间隙退变的影响因素;术前颈椎椎体CT值与上邻近节段高度丢失值的相关性分析采用Pearson相关分析;绘制术前颈椎椎体CT值预测患者术后上邻近椎间隙丢失的受试者工作特征曲线(receiver operating characteristic curve,ROC)。 以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床资料 86例患者平均随访时间为(12.45±1.51)个月,A 组患者手术节段 C4~5,C5~6,C6~7分别为 3、8、4例,B 组患者手术节段为 C4~5,C5~6,C6~7分别为 9、37、25例。两组患者年龄、性别、随访时间和BMI比较,差异无统计学意义(P>0.05);两组患者术前颈椎椎体CT值、术前颈椎椎体CT值分布比较,差异有统计学意义(P<0.05),见表1。
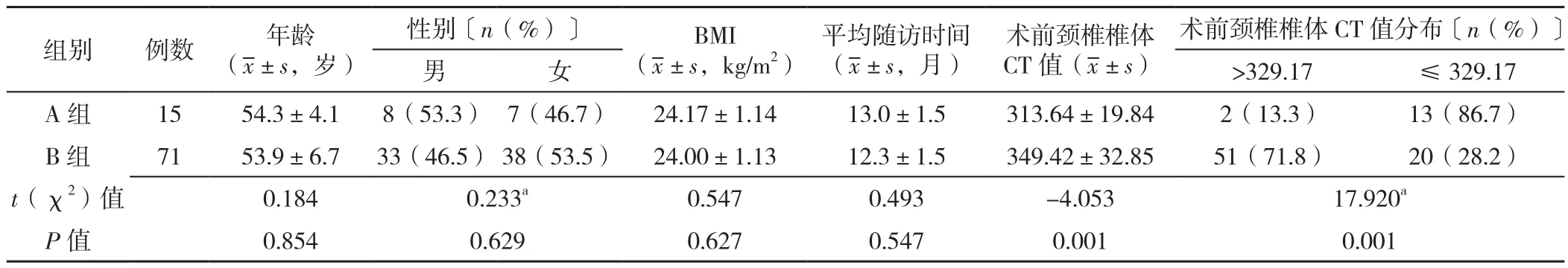
表1 两组患者临床资料比较Table 1 Comparison of clinical data between two groups of patients
2.2 二元Logistic回归分析 以上邻近间隙退变为因变量(赋值:0=否,1=是),以年龄(赋值:实测值)、性别(赋值:0=女性,1=男性)、BMI(赋值:实测值)、术前颈椎椎体CT值(赋值:实测值)为自变量,纳入二元Logistic回归模型,结果显示,术前颈椎椎体CT值较低是上邻近椎间隙退变的危险因素(P<0.05),见表2。

表2 患者术后上邻近间隙退变影响因素的二元Logistic回归分析Table 2 Binary Logistic regression analysis of influencing factors of postoperative adjacent space degeneration
2.3 术前颈椎椎体CT值与椎间隙高度丢失值的相关性分析 患者术前颈椎椎体CT值为(343.18±33.76),术后上邻近椎间隙高度丢失值为(0.66±0.31)mm。Pearson相关分析结果显示,患者术前颈椎椎体CT值与术后上邻近椎间隙高度丢失值呈负相关(r=-0.844,P=0.001)。
2.4 术前颈椎椎体CT值对患者术后上邻近椎间隙退变的预测价值 ROC曲线结果显示,术前颈椎椎体CT值预测患者术后上邻近间隙退变的曲线下面积(AUC)为 0.830〔95%CI(0.732,0.928)〕,最佳截断值为329.17,灵敏度为71.8%,特异度为86.7%,见图3。

图3 术前颈椎椎体CT值预测患者术后上邻近间隙退变的ROC曲线Figure 3 ROC curve of preoperative vertebral CT values for predicting postoperative adjacent space degeneration
3 讨论
有症状的ASD也称邻椎病,一项包括了34 716名脊柱融合术后患者有关ASD发病率的meta分析显示,颈椎融合术后ASD和邻椎病的发生率分别为32.8%和6.3%[6]。LEE等[5]报道,邻椎病在颈椎融合术后5年的发病率可高达50%。目前,ASD的发病机制尚无定论。相关生物力学研究指出,融合节段的活动度大幅度降低使邻近节段的应力过度集中,代偿性增加了其活动范围,从而引起原有矢状位平衡和生物力学的改变,这可能是ASD加速发生的重要原因[7-9]。也有研究者认为,术后ASD是持续的自然退行性过程[10]。综合现有的研究观点,影响ASD发生的因素除了年龄、BMI、骨质疏松、术前是否已有相邻节段的退变、生理曲度异常(矢状位平衡参数)等患者本身因素以外,还可能与术中操作不当,如邻椎解剖结构的过度破坏、手术间隙撑开过大、钛板位置欠佳(钛板上或下缘距邻近椎间盘的距离<5 mm)和融合节段数量等有关[11-15]。
ASD的影像学评估目前仍无统一的标准,但大部分文献除了参考颈椎X线外,还要评估颈椎磁共振成像(MRI)、颈椎动力位X线检查结果等。既往研究报道,MRI评估的早期颈椎间盘退变,即髓核信号强度的改变与X线下颈椎间盘高度的丢失有显著的相关性,即对于尚未发生退变的邻近间隙而言,椎间隙高度的丢失可在一定程度上准确反映椎间盘的退变[14]。考虑大多数患者随访时只复查X线,故本研究仅评估了X线下的邻近间隙变窄程度,以反映椎间隙退变。
部分研究把邻近椎间隙高度丢失值≥原高度的30%[15]或25%[16]作为影像学评估ASD的重要条件之一,而本研究把邻近椎间隙高度丢失值是否大于原高度的20%作为分组标准,以确保有足够的样本量进行对比,从而进一步得出对ASD的进展更为敏感的CT阈值。相关研究指出,融合术使邻近节段的运动负荷增大,尤其是对上邻近节段应力作用更明显,从而使ASD在上邻近节段更容易发生[17-18]。此外,对于手术节段为C6~7的部分患者,X线检查难以评估下邻近间隙,为了减少测量误差,本研究仅对上邻近节段进行了评估。
骨密度是影响脊柱融合术后的重要因素之一,KWOK等[19]的一项纳入395例老年人的研究发现,腰椎骨密度越低,椎体和椎间盘体积下降趋势更明显。HARAD等[20]对86例绝经后妇女影像学腰椎间盘退变程度与腰椎骨密度行相关性分析表明,骨密度与椎间盘退变程度呈负相关。DXA因具有结果可靠、使用简便、辐射剂量低等优点被认为是诊断骨量减少或骨质疏松的最佳方法,但其结果可能受到骨骼体积、BMI、血管钙化、退行性改变和脊柱手术史等的影响,导致检查结果与真实值存在一定的误差[21,23]。然而DXA不是颈椎骨密度的常规检测方法。使用DXA测量包括胸1在内的整个颈椎在技术上具有一定的难度。此外颈椎目前尚无广泛接受的骨密度阈值。相关研究表明,不仅是腰椎,颈椎椎体CT值与T值之间存在密切的关系[21-23],即CT值在一定程度上可以准确反映椎体骨密度。此外,CT在重度脊柱侧弯患者中没有禁忌证,不受椎体退行性变、压缩性骨折、血管钙化等病变的影响,并且CT值的获取简便,患者无需再进行额外的检查,因此可作为较好的替代检查方法。由于CT值测量的数值范围远大于DXA的T值范围,因此可以更准确地反映椎体骨密度。
然而CT值的标准测量目前仍没有一个普遍接受的方法。SCHREIBER等[24]最先提出了腰椎CT值的测量方法,并指出观察者的多次测量和单侧测量的组内相关系数(ICC)分别为0.964和0.975,说明一致性良好,且在别的研究中得到了证实[25-26]。其次,此方法操作相对简便,而且椎体单个轴位测量的CT值与3个轴位上测量的平均CT值一样可靠[27]。虽然颈椎体积比腰椎小,但并不影响多个不包括终板的平行轴位测量CT值。然而颈椎矢状位、冠状位重建面获得的CT值可能包含终板在内的硬化骨赘或Schmorl结节等结构,这会错误地抬高CT值。因此,为了尽量减少测量误差,本研究选择椎体矢状面重建的3个横断面获取CT值,取其平均值作为椎体的CT值。DEMIR等[28]对16例腰椎融合术后患者的术前与术后1年CT值进行比较后发现,所有手术节段及邻近节段椎体CT值呈持续下降,并提出邻近节段椎体骨密度降低可能是ASD的主要诱发因素之一。WANG等[29]对91例接受单节段ACDF治疗的患者术前CT值与1年后融合节段高度丢失的相关性进行研究发现,融合节段上下椎体CT值<343.7与融合器下沉有关。此外,本研究发现术前颈椎椎体CT值与术后上邻近节段高度丢失值呈明显负相关。
总之,单节段ACDF患者术前较低的椎体CT值与术后上邻近节段高度丢失有关。测量术前颈椎椎体CT值可能有助于预测ACDF术后ASD等并发症。术后上邻近间隙高度丢失与术前颈椎椎体CT值相关。根据CT阈值大小,术前或术后给予抗骨质疏松等治疗可能有助于减少术后ASD等并发症。
本研究存在以下局限性:为了正确评估邻近椎间隙退变情况,长期的随访、MRI等检查是必不可少的,本研究仅采用X线来评估椎间隙高度丢失可能不够充分。此外,本研究仅对上邻近椎间隙进行了评估,椎间隙高度丢失病例较少,可能对结果产生影响。
作者贡献:凯依塞尔·阿布都克力木、李磊负责文章的构思、设计、实施、收集并整理数据、撰写论文;杨晓凯进行数据收集和统计学处理;任军、刘帅负责数据质量控制;李磊负责论文的修订、监督管理,对文章整体负责。
本文无利益冲突。
