奥马珠单抗在儿童过敏性哮喘及其过敏性共病中的应用评价
2023-02-08郑乐乐解龙花张美乐叶妍贞史瑞明
谭 璐,郑乐乐,解龙花,张美乐,叶妍贞,史瑞明
(1.西安交通大学第一附属医院儿科,陕西 西安 710061;2.南昌市第三医院儿科,江西 南昌 330000;3.赣州市信丰县人民医院儿科,江西 赣州 341600)
支气管哮喘是具有多种不同表型的异质性疾病,95%的儿童病例初发年龄在6岁之前。超过90%的哮喘儿童具有潜在的过敏反应,虽经吸入糖皮质激素(inhaled corticosteroids,ICS)、糖皮质激素联合长效β2受体激动剂(inhaled corticosteroid-long acting β2 agonist,ICS-LABA)、白三烯受体拮抗剂等控制类药物治疗,但仍有19.9%的患儿哮喘未得到控制。在我国每年约77.0%和47.3%的哮喘患儿因急性发作就诊或急诊入院[1]。近年来不断涌现过敏性共病如变应性鼻炎、结膜炎、鼻窦炎、肺炎、特应性皮炎、嗜酸性食管炎、食物过敏等,可能影响哮喘的临床表现并导致哮喘控制不佳的证据。国际儿童哮喘和过敏研究机构发现,15%~40%的哮喘儿童曾被诊断过变应性鼻炎;亚洲人种哮喘合并过敏性鼻炎共患率更高,达36.0%~64.3%,这也成为日本学龄儿童哮喘未控制的重要危险因素[2]。选择综合性治疗策略已成为哮喘合并过敏性共病的重要参考因素。免疫球蛋白E(immunoglobulin E,IgE)在过敏性疾病的病理生理学中起着重要作用,靶向IgE已被证明是对常规治疗反应不佳的过敏性疾病的一种成功治疗方法。代表性药物奥马珠单抗(Omalizumab)的批准适应症目前仅限于过敏性哮喘和慢性荨麻疹,但其在治疗其他过敏性共病方面的潜力正变得越来越明显。有证据表明,用奥马珠单抗治疗过敏性哮喘不仅能改善哮喘症状,而且可改善任何共存疾病的预后[2]。奥马珠单抗在我国正式获批应用于临床仅3年多时间,中国儿童过敏性哮喘合并过敏性共病方面临床治疗经验和相关检查数据仍十分缺乏。本课题对西安交通大学第一附属医院儿童哮喘门诊就诊患儿的相关临床资料展开研究,以期为临床广泛应用奥马珠单抗提供参考依据。
1研究对象与方法
1.1研究对象
收集2020年7月至2021年3月在西安交通大学第一附属医院儿童哮喘门诊就诊符合中重度哮喘合并过敏性共病诊断的患儿15例。纳入标准:①符合《中国哮喘防治指南(2016版)》的中度或重度诊断标准,并同时伴有变应性鼻炎、食物过敏、湿疹或特应性皮炎等;②年龄为6~14岁;③患儿经吸入ICS-LABA治疗至少6个月以上,仍不能有效控制症状;④过敏源检测阳性,皮肤点刺试验阳性、血清过敏源特异性IgE水平升高或血清总IgE升高;⑤外周血嗜酸性粒细胞(eosinophil,EOS)计数升高;⑥呼出气一氧化氮浓度(exhaled nitric oxide,eNO)水平升高。排除标准:①对奥马珠单抗活性成分或任一辅料过敏;②血清总IgE<30IU/mL,或>1 500IU/mL;③患自身免疫性疾病,或重要脏器功能损害;④哮喘急性发作期或哮喘持续状态。
1.2奥马珠单抗给药方案
①严格遵循奥马珠单抗(进口药品注册证号S20170042)说明书对药品进行存贮;②根据患儿体重及治疗前血清总IgE水平,并对照奥马珠单抗说明书剂量表选取适合的给药剂量和给药频率,若剂量>150mg,则按需分1~4个部位皮下注射;③皮下注射部位为上臂三角肌区;④注射地点在西安交通大学第一附属医院儿科日间病房,配备过敏性休克抢救的相关医疗设施;⑤注射后需在院观察2小时;⑥由经过培训的哮喘门诊专科医生及护士完成上述操作。在接受奥马珠单抗治疗的24周中未见患儿发生不良反应。
1.3观察指标
收集患儿在初次行奥马珠单抗注射治疗前及治疗4周、8周、12周、16周、20周及24周时的下述指标,并进行回顾性分析。①儿童哮喘控制测试(childhood asthma control test,C-ACT):评估过去4周内哮喘控制情况,满分为27分,≤19分提示哮喘未控制,20~22分提示哮喘部分控制,≥23分提示哮喘完全控制。②儿童哮喘生活质量问卷(Pediatric Asthma Quality of Life Questionnaire,PAQLQ):针对哮喘患儿生活质量的调查问卷,包括症状(用S表示)、活动受限(用A表示)、情感功能(用E表示)3个方面23个条目;问卷均采用7分制评分,最低1分,最高7分,各条目得分相加即为总分,得分越高提示生活质量越好。③儿童鼻-结膜生活质量问卷(Pediatric Rhinoconjunctivitis Quality of Life Questionnaire,PRQLQ):包括鼻部症状、眼部症状、非鼻-结膜炎症状、鼻炎相关行为问题及情感反应5个方面23个条目,每个问题根据其代表功能损害的严重程度,采用1~7分评分,评分越低,所代表的功能损害越轻,生活质量越好。④变应性鼻炎视觉模拟评分(visual analog scale,VAS)。⑤湿疹面积及严重指数评分(Eczema Area and Severity Index score,EASI)。⑥皮肤病生活质量指数评分。
收集患儿在初次行奥马珠单抗注射治疗前及治疗8周、16周及24周时的下述指标,并进行回顾性分析。①肺功能:包括第1秒用力呼气量占预计值百分比(forced expiratory volume in one second in percentage of predicted,FEV1%pred),1秒率(FEV1/forced vital capacity,FEV1/FVC),最大呼气流量占预计值百分比(peak expiratory flow percentage of predicted,PEF%pred),呼出25%肺活量时的最大呼气流量(maximum expiratory flow rate at 75% of vital capacity,MEF75),呼出50%肺活量时的最大呼气流量(maximum expiratory flow rate at 50% of vital capacity,MEF50),呼出75%肺活量时的最大呼气流量(maximum expiratory flow rate at 25% of vital capacity,MEF25)。②呼出气一氧化氮浓度:包括流速为50mL/s呼出气一氧化氮浓度(fractional exhaled nitric oxide,FeNO)和鼻呼出气一氧化氮浓度(nasally exhaled nitric oxide,nNO)。
1.4统计学方法

2结果
2.1一般临床资料
本研究共纳入15例患儿,其中男性12例,女性3例;年龄为6~14岁,平均年龄(8.76±2.09)岁;体质量指数(body mass index,BMI)为13.33~29.05kg/m2,平均(18.91±5.13)kg/m2;嗜酸粒细胞计数为(0.10~1.47)×109/L,平均(0.47±0.43)×109/L;IgE水平<500IU/mL 有10例,500~1 000IU/mL 有2例,>1 000IU/mL 有3例,IgE为157~1 270IU/mL,平均(464.82±377.40)IU/mL。
在过敏源中:①吸入变应原12例,分别为葎草2例次、复叶槭/桑槐榆柏构树3例次;蒿4例次;户尘螨、粉尘螨、热带无爪螨3例次;念珠菌点青霉分枝孢霉黑曲3例次;苋1例次;猫皮毛屑1例次。②食入变应原2例,分别为牛奶鸡蛋1例次;小麦荞麦1例次。③无明确变应原,仅血清总IgE明显升高1例。
在所有患儿中,合并变应性鼻炎15例,合并特应性皮炎3例,合并过敏性结膜炎1例。
2.2奥马珠单抗治疗前后患儿临床疗效改善情况
与奥马珠单抗治疗前相比,治疗后哮喘症状控制及生活质量评价C-ACT、PAQLQ的评分均有升高,鼻部及眼部症状评价PRQLQ、VAS的评分均有下降,差异均有统计学意义(P<0.05),见表1。

表1 奥玛珠单抗治疗前后多组间临床疗效评分的比较[分,M(P25,P75)]Table 1 Efficacy evaluation between groups before and after treatment with Omalizumab[score,M(P25,P75)]
进一步行C-ACT、PAQLQ、PRQLQ和VAS的各评估时间节点两两比较:
C-ACT评分在治疗4周开始改善,并逐步提高,至治疗20周达满分,与治疗前及治疗4周、8周、12周、16周比较差异均有统计学意义(Z值分别为-2.668、-2.536、-2.032、-2.060和-2.070,P<0.05);在治疗8周、12周及16周3个评估时间节点两两比较差异均无统计学意义(Z值分别为-1.857、-1.163和-0.552,P>0.05);提示奥马珠单抗至少用药至20周才能持续获益,哮喘症状持续缓解;至治疗24周,15例患儿哮喘症状均控制良好,日间、夜间及运动后未再有喘息、咳嗽、胸闷等症状发作。
PAQLQ评分在治疗4周开始提高,至治疗24周评分接近满分,与治疗前及治疗4周、8周、12周、16周比较差异均有统计学意义(Z值分别为-2.803、-2.807、-2.521、-2.533和-2.060,P<0.05);在治疗12周与治疗16周、治疗16周与治疗20周、治疗20周与治疗24周3个评估时间节点比较差异均无统计学意义(Z值分别为-1.757、-1.841和-1.633,P>0.05);提示奥马珠单抗治疗4周患儿生活质量就有改善,且随治疗时间的延长,患儿生活质量改善越明显;治疗12周后评分上升缓慢,至治疗20周后评分持续稳定在该水平,该时期扣分项主要为担忧哮喘再次发作,其哮喘症状未再发作,运动无受限。
PRQLQ评分在治疗初始阶段鼻部及眼部临床症状改善不明显,治疗4周与治疗8周比较差异无统计学意义(Z=-1.729,P>0.05);治疗12周的临床症状明显控制,此后进入治疗平台期(治疗12周、16周),经比较差异无统计学意义(Z=-1.246,P>0.05);治疗20周鼻部及眼部临床症状控制良好,评分进一步降低,与治疗前及治疗4周、8周、12周、16周比较差异均有统计学意义(Z值分别为-3.408、-3.408、-3.298、-3.306和-3.074,P<0.05);至治疗24周,患儿鼻部及眼部临床症状消失。
VAS评分随着治疗周期的延长逐渐下降,治疗20周的鼻部临床症状明显缓解,评分降至最低值并持续保持在该水平,治疗24周与治疗20周比较差异无统计学意义(Z=-1.841,P>0.05)。
C-ACT、PAQLQ、PRQLQ及VAS评分变化趋势一致,奥马珠单抗治疗20周后患儿临床症状得到明显控制,生活质量明显提高,见表2。

表2 奥马珠单抗治疗前后临床疗效评分组间两两比较Table 2 Comparison of clinical efficacy between groups before and after treatment with Omalizumab
2.3奥马珠单抗治疗前后特应性皮炎及过敏性结膜炎改善情况
在3例合并特应性皮炎患儿中,有2例轻度患儿治疗4周皮肤瘙痒消失,皮损范围明显缩小,1例重度患儿治疗16周后相应的症状及体征才有明显改善。治疗前EASI评分分别为3.6、3.6、33.6分,皮肤病生活质量指数分别为10、9、27;治疗4周EASI评分分别为0.6、0.6、21.6分,皮肤病生活质量指数分别为0、0、22;治疗8周EASI评分分别为0、0、21.6分,皮肤病生活质量指数分别为0、0、22;治疗12周EASI评分分别为0、0、18.9分,皮肤病生活质量指数分别为0、0、20;治疗16周EASI评分分别为0、0、8.0分,皮肤病生活质量指数分别为0、0、11;治疗20周EASI评分分别为0、0、6.8分,皮肤病生活质量指数分别为0、0、8;治疗24周EASI评分分别为0、0、1.8分,皮肤病生活质量指数分别为0、0、6。因病例数较少,未进行统计学分析。1例合并过敏性结膜炎患儿治疗4周临床症状消失,眼部症状评估包括在PRQLR评分中,故不再单独统计。
2.4奥马珠单抗治疗前后患儿肺功能的改善情况
经奥马珠单抗治疗,对所有患儿每8周评估1次肺功能,结果显示,治疗8周FEV1%pred中位数较治疗前有所下降,治疗16周及24周其中位数较治疗前均有所提高,但组间比较差异无统计学意义(χ2=8.265,P>0.05);FEV1/FVC、MEF75及MEF50在治疗8周、16周、24周较治疗前均有升高,但组间比较差异均无统计学意义(F值分别为0.945、1.507和2.703,P>0.05);进一步行组间两两比较显示,MEF50治疗8周与治疗前比较差异无统计学意义(t=-1.511,P>0.05),而治疗16周、24周分别与治疗前比较差异均有统计学意义(t值分别为-2.351和-2.561,P<0.05),但治疗24周与治疗16周比较差异无统计学意义(t=-0.211,P>0.05);PEF%pred及MEF25在治疗8周、16周、24周较治疗前均有升高,组间比较差异均有统计学意义(F值分别为3.685和3.727,P<0.05),见表3、表4。治疗8周,PEF%pred及MEF25均有明显改善,与治疗前比较差异均有统计学意义(t值分别为-2.467和-2.102,P<0.05),治疗8周后各评估时间节点比较差异均无统计学意义(t值分别为0.064、-0.604、-0.668;-0.670、-0.893和-0.223,P>0.05);且PEF%pred治疗16周均数略有下降,见表5。
2.5奥马珠单抗治疗前后患儿一氧化氮呼气试验改善情况
FeNO和nNO治疗8周、16周、24周与治疗前组间比较差异均无统计学意义(χ2=8.106,F=1.944,P>0.05),见表3。
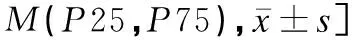
表3 奥玛珠单抗治疗前后肺功能及一氧化氮呼气试验各指标的比较[分,Table 3 Comparison of pulmonary function and indexes of nitric oxide breath test before and after treatment with Omalizumab[分,
进一步行FeNO、nNO的各评估时间节点两两比较:
FeNO从治疗前[13.50(8.75,29.50)]ppb降至治疗24周的[12.00(10.00,16.25)]ppb,但在8周FeNO中位数值略有上升,造成治疗24周与治疗8周比较差异有统计学意义(Z=-2.201,P<0.05),其余各评估时间节点两两比较差异均无统计学意义(Z值分别为-0.153、-0.204、-0.461、-1.123和-1.832,P>0.05)。nNO从治疗前(536.70±174.05)ppb降至治疗24周的(398.20±85.36)ppb,治疗24周与治疗前比较差异有统计学意义(t=2.287,P<0.05),其余各评估时间节点两两比较差异均无统计学意义(t值分别为0.674、1.534、0.778、1.530和0.753,P>0.05),见表4、表5。

表4 奥玛珠单抗治疗前后非正态分布肺功能指标的两两比较Table 4 Comparison of non-normal distribution indexes of pulmonary function between groups before and after treatment with Omalizumab
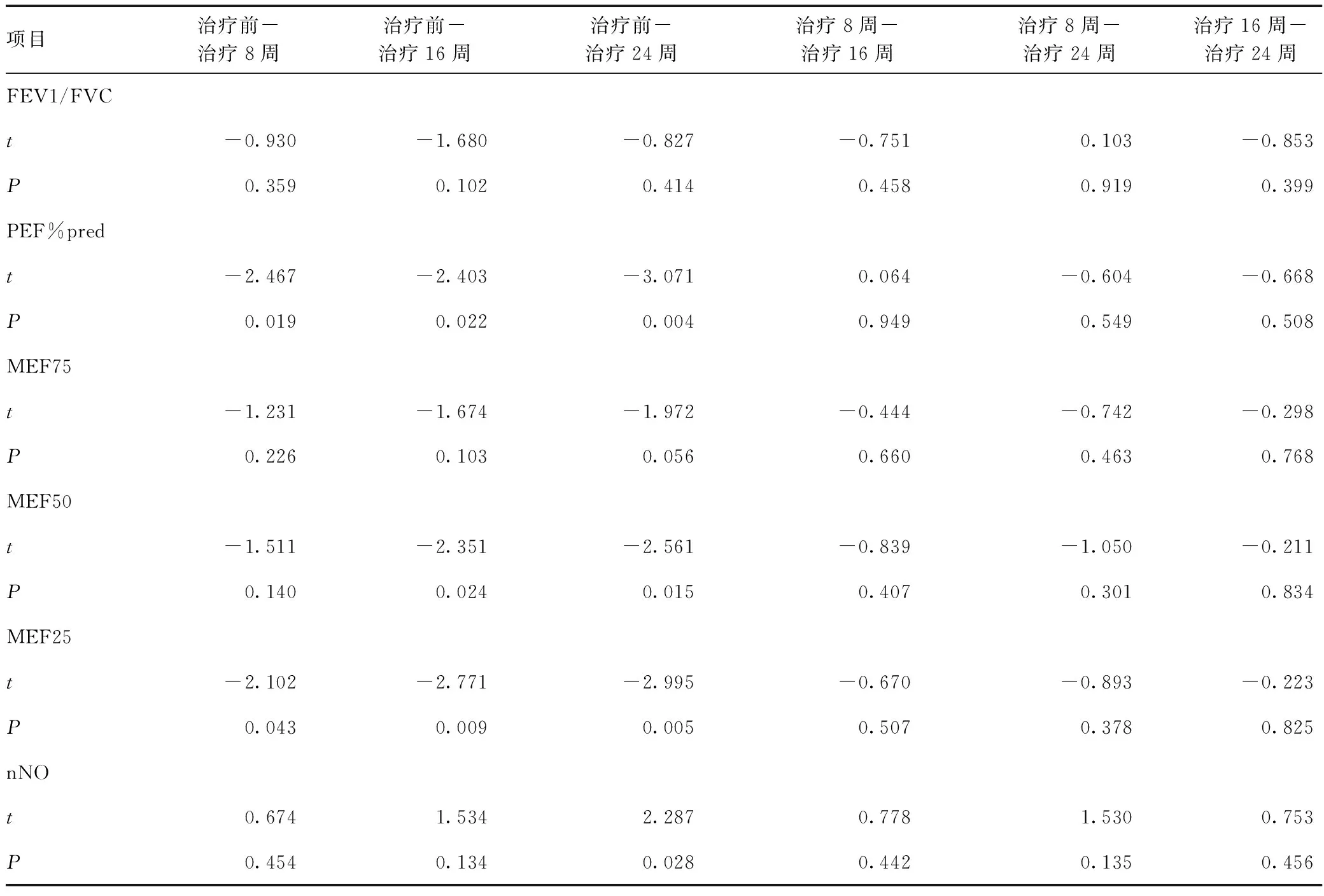
表5 奥玛珠单抗治疗前后正态分布肺功能指标的两两比较Table 5 Comparison of normal distribution indexes of pulmonary function between groups before and after treatment with Omalizumab
3讨论
3.1 IgE与过敏性疾病的关系
IgE介导的过敏性疾病涉及多种遗传和环境因素,这些因素相互作用决定疾病的表达,并导致异质性发生。过敏性疾病,如哮喘、鼻炎、结膜炎和食物过敏,可能与过敏源特异性IgE及非过敏性机制有关,这些机制可在同一患者中共存。研究表明约38%的过敏性共病与IgE致敏有关[3]。靶向IgE已被证明是对常规治疗反应不佳过敏性疾病的一种成功治疗方法。奥马珠单抗是一种抗人IgE的单克隆抗体生物制剂,2005年欧洲药品管理局(European Medicines Agency,EMA)首次批准用于治疗青少年严重持续性过敏性哮喘,2016年美国食品药品监督管理局(Food and Drug Administration,FDA)批准用于6岁以上儿童[4]。尽管目前奥马珠单抗批准的适应症仅限于过敏性哮喘和慢性荨麻疹,但在治疗其他过敏性共病方面的潜力正变得越来越明显。有证据表明,奥马珠单抗治疗过敏性哮喘不仅能改善哮喘症状,而且能改善任何共存疾病的预后[5-8]。
变应性鼻炎是暴露于过敏源后,由IgE介导的鼻黏膜慢性炎症。因为上下呼吸道具有相似的假复层纤毛柱状上皮细胞结构,因此变应性鼻炎和哮喘的炎症反应过程相似。流行病学的研究为哮喘和变应性鼻炎间的联系提供了有力证据。2002年至2003年的国际儿童哮喘和过敏性共病的流行病学研究表明,与5年前相比,哮喘、变应性鼻炎、过敏性结膜炎和其他过敏性疾病的患病率有所上升。高达40%的变应性鼻炎患者发生了哮喘,高达80%的哮喘患者合并有变应性鼻炎。共同的流行病学、病理学和生理学特征更加支持“一个气道,一种疾病”的假说,也是变应性鼻炎和哮喘采用共同治疗方法的理论基础[5]。
3.2奥马珠单抗临床疗效评价分析
本研究纳入的15例中重度过敏性哮喘合并过敏性共病患儿中,合并变应性鼻炎15例,合并特应性皮炎3例,合并过敏性结膜炎1例。过敏源中以吸入性变应原为主。在接受奥马珠单抗治疗的24周中,所有患儿耐受性良好,未发生不良反应。短期疗效表现为哮喘发作频率的降低,长期疗效表现为哮喘症状控制的改善及生活质量的提高,这与既往文献[5,7,9-10]一致。本研究中15例中重度过敏性哮喘合并变应性鼻炎患儿的C-ACT、PAQLQ评分显示,治疗前基线值失分项主要在运动诱发哮喘发作、夜间憋醒和因哮喘导致躯体及情感上的不适。奥马珠单抗治疗4周C-ACT及PAQLQ评分与基线值比较差异均有统计学意义,提示奥马珠单抗治疗后哮喘症状很快得到控制,生活质量由此得到改善;至治疗20周后,患儿哮喘症状几乎完全控制,活动力明显提高,对情感认知功能影响降至最低,生活质量明显提高。本研究中15例患儿的PRQLQ评分显示,治疗前基线值失分项主要在鼻部症状明显,如鼻塞、鼻痒、清水涕、喷嚏,以及因鼻部症状长期困扰导致患儿出现相关行为问题和情感反应。所有患儿治疗初期鼻部症状有缓解,但改善缓慢;唯一1例共患过敏性结膜炎患儿在治疗4周,眼痒及眼红肿症状消失。至治疗12周鼻部症状明显控制,但因上述症状导致的相关行为情感问题仍然存在,直至治疗20周后,所有症状明显改善,不再因症状而尴尬,生活质量明显提高。本研究显示,15例中重度过敏性哮喘合并过敏性共病患儿PRQLQ和VAS的变化与C-ACT、PAQLQ的变化一致。C-ACT、PAQLQ、PRQLQ及VAS评分在治疗后期失分项中的行为及情感反应均占有一席之地,这也提示过敏性哮喘合并过敏性共病的治疗目的不应仅停留在症状的缓解或控制上,要注重改善疾病对患儿情感及行为的影响。从3例合并特应性皮炎患儿可以看出,奥马珠单抗可以降低EASI总分,改善患儿生活质量,但因样本量过少,尚缺乏统计学依据。
3.3奥马珠单抗与肺功能和一氧化氮呼气试验关系的分析
本研究显示,FEV1%pred从治疗前[90.80(45.60,93.60)]%增加至治疗24周的[94.00(91.00,97.00)]%,虽有改善,但差异无统计学意义;这与部分文献[8-9,11]一致。但最近的研究显示,奥马珠单抗给药1年后肺功能才有明显改善,提示持续用药的必要性[7]。本研究显示,FEV1%pred在治疗8周中位数较治疗前有所下降,但差异无统计学意义,考虑与患儿治疗8周时值蒿类花期,环境暴露可能影响FEV1%pred,但并未造成哮喘急性发作。本研究显示,气道通畅性评估指标PEF%pred提示在治疗8周气道阻力明显降低,而小气道功能评估指标MEF50及MEF25分别在治疗16周和治疗8周改善明显,与临床症状缓解程度相一致,提示奥马珠单抗在改善哮喘患儿气道阻塞及气流受限方面有一定作用。本研究显示,治疗16周PEF%pred数值略下降,推测与初冬为呼吸道感染高发季节,部分患儿处于呼吸道感染恢复期,气道内仍有少许分泌物有关。但MEF75治疗前后变化无统计学意义,考虑与样本量较小存在一定偏倚有关。
FeNO主要与过敏性气道炎症相关,有助于判断气道炎症类型,指导哮喘治疗策略。本研究显示,除治疗8周外,与治疗前相比,FeNO在治疗后下降幅度较小且组间差异无统计学意义,考虑与吸入ICS可能使FeNO短期迅速下降有关。因此,当FeNO被用作奥马珠单抗疗效的指标时,必须考虑ICS伴随使用的影响[7]。FeNO在治疗8周中位数有所上升,与治疗24周比较差异有统计学意义,考虑与病例收集季节为7月,时值蒿类花期,可使FeNO暂时性上升,与既往不同的是,即便环境过敏源暴露,但并未造成患儿哮喘急性发作,这与前述FEV1%pred在治疗8周略有下降相一致,提示奥马珠单抗季节性应用的可行性。鼻窦是nNO的主要来源,当鼻腔黏膜发生炎性反应时,诱导型一氧化氮合成酶表达增加,导致nNO也增加,且nNO升高早于急性鼻炎症状的产生。本研究中的15例患儿均合并变应性鼻炎,nNO治疗24周明显下降,与治疗前比较差异有统计学意义。但治疗前nNO基线值并未见明显升高,考虑与儿童呼吸道黏膜生理特点有关。儿童鼻腔及鼻窦黏膜柔嫩,发生炎症时极易充血水肿,分泌物增多,窦口堵塞,导致一氧化氮排出受阻。随着治疗时间的延长,鼻部黏膜炎症反应消退,鼻阻逐渐缓解,窦口得以开放,一氧化氮排出量先增多后逐渐降至正常水平[8]。由于本研究中并非每个治疗周期均监测nNO,其峰值出现的时间节点未知,故不能真实反应nNO的变化趋势,这也可以解释为治疗后nNO下降缓慢,至治疗24周才与治疗前基线值的差异存在统计学意义。故不建议以nNO用作短期疗效评价指标。
综上,奥马珠单抗对中重度过敏性哮喘合并过敏性共病患儿治疗有效,且起效较快,未见发生明显不良反应[9-14]。治疗4周即可见效,至治疗20周后,患儿伴随的情感行为问题有明显改善,提示奥马珠单抗的治疗不仅使临床症状得以良好控制,更重要的是改善了患儿生活质量,提高了患儿及家长的治疗信心,且应给予足够长的疗程才能持续获益;这与2021版《中国奥马珠单抗儿童用药指南》[15]一致,其建议疗程持续12个月以上,而12个月的后半年时间可维持原剂量治疗方案,也可酌情采用每次给药量减半或间隔时间延长1倍的治疗方案;对季节性加重的患儿建议酌情在秋季和/或春季前加用奥马珠单抗4~6周[13,15]。同时也启发了奥马珠单抗在过敏性哮喘外过敏性疾病中的应用[3,6-8,13]状况。随着今后治疗样本量的不断扩大,临床医师将积累更多哮喘合并过敏性共病患儿的临床证据和治疗经验,为我国的哮喘患儿,甚至一些IgE介导的非哮喘性过敏性疾病的靶向治疗提供更为全面的统计学依据[2,16],使更多患儿长久受益。
