基于15N 示踪技术的盐渍土壤氮素转化模拟
2023-01-30洪明海魏文杰汪仕伟王兴建冯楚桥
洪明海,严 涛,刘 辉,魏文杰,汪仕伟,王兴建,冯楚桥
(贵州省水利水电勘测设计研究院有限公司,贵州 贵阳 550002)
0 引言
土壤盐渍化是干旱半干旱地区农业发展的主要限制因素[1]。我国盐渍土总面积超过1 亿hm2,广泛分布在西北、华北、东北以及沿海地区,其中西北内陆地区盐渍化耕地面积占总耕地面积的15%[2]。在一定的盐度范围内,施加氮肥能够有效缓解盐分对作物生长的不利影响,提高作物产量[3]。曾文治等[4]通过田间实验发现增施氮肥可提高盐渍地区向日葵对氮肥的利用率,得出河套灌区135 kg/hm2是较合理的施氮水平。
土壤氮素转化研究是作物估产、环境评价、农田管理、农业相关政策和盐碱地治理措施的重要依据,由于各氮素参与的反应过程受到土壤水分[5]、盐分[6]、温度、微生物活动[7]、通气等众多因素影响,监测困难。因此,建立氮素转化数值模型成为十分有效的研究手段[8,9]。最早出现基于单个土壤氮循环过程方面的报道是1954 年Kirkham 和Bartholomew[10]考虑了矿化氮和有机氮,从解析方程上进行分析计算,1955 年他们又对模型的假设进行了修正[11]。60多年来,基于Kirkham 和Bartholomew 的研究出现了大量的土壤氮循环模型[12-15]。1973 年Stanford 和Smith[16]提出了氮素矿化的一阶动力学反应模型,Myrold 和Tiedje[15]首次采用数值方法计算了氮的总转化速率,Wessel 和Tietema[17]同时考虑了铵态氮和硝态氮的同化,氮的矿化硝化过程,建立了新的概念模型;1998年Marry等[14]人采用同位素氮示踪的方法开展裸土实验,开发了FLUAZ 土壤氮转化模型,从机理上较系统地分析了土壤中存在的主要氮素转化过程并在后续的实验中得到验证,得到了非常广泛的应用;2004 年Muller等[13]人指出FLUAZ模型并不能模拟土壤氮素动态转化,分别对草原土壤采用标记同位素搜集数据,开发了氮素示踪模型[13,18],2005 年Jesper Luxhoi[19,20]认为Muller 的数值模型无法同时求解9个过程,并对该模型的部分转化过程产生质疑;为了进一步完善模型的求解过程,2007 年Muller 等人结合马尔科夫链蒙特卡洛随机采样算法优化模型的求解参数过程[21,22],提高了氮素总转化速率的计算个数和精度,使土壤氮的总转化速率计算更加接近真实情形。2013 年Inselsbacher 等[12]人考虑了作物对土壤中氮素的吸收开发了新一代的氮素示踪模型,分析和验证了土壤氮循环中存在的14个转化过程。
尽管已有的研究反映了氮素转化的部分规律,推动了土壤氮素转化的研究,但是一方面,解析模型在推导过程中并未考虑同位素标记氮的再矿化或反硝化再次回到标记氮库的影响,难以用于计算发生这一转化过程之后(时间难以确定)的氮素转化率;另一方面,现有的氮素转化模型多在非盐渍土地区获得,不同地区对土壤氮素转化的过程不全相同,因此对于盐渍土壤氮素转化过程的数值模拟方法还有待进一步的验证和完善。
1 实验与方法
1.1 研究区概况及实验土样
研究区位于内蒙古河套灌区五原县永联实验基地(108°00'16.14″E,41°04'11.57″N)。该地区海拔约为1 030 m,地处黄河北岸,是河套灌区主要的盐渍土分布区。供试土样选取研究区盐分含量较低的沙壤土(ECe=2.01 dS/m,S1),其pH 值为8.71~8.80,呈弱碱性,容重为1.35 g/cm3;土壤中交换性钙、镁、铁3 种元素含量较高(44.44、8.03、12.46 cmol/kg),钾、钠元素则较少(0.39、2.02 cmol/kg),总氮、总碳分别为0.7、20.3 g/kg,含量最多的是碳元素,为2.03%,此外,土样中铵态氮、硝态氮(亚硝态氮)的分别为3.66 mg/kg和33.92 mg/kg。
1.2 盐分设置和处理
实验以基础土样的盐度值为基本处理(S1),其饱和浸提电导率值ECe为2.01 dS/m为S1处理,根据基础土样中的交换性钾、钠、钙、镁等的含量,添加硫酸钾(K2SO4)、硫酸镁(MgSO4)、碳酸钠(Na2CO3)、碳酸氢钠(NaHCO3)、氯化钙(CaCl2)5 种盐分以形成6 个不同的盐度值(S1:ECe=2.01 dS/m,S2:ECe=6 dS/m,S3:ECe=12 dS/m,S4:ECe=16 dS/m,S5:ECe=20 dS/m,S6:ECe=25 dS/m),其所对应的各盐度的添加值如表1所示。
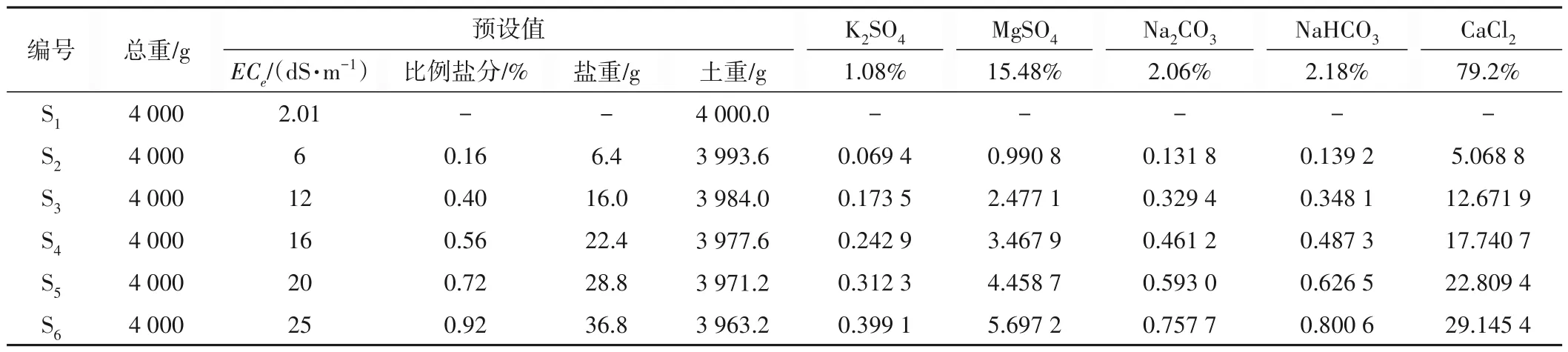
表1 盐分设置情况Tab.1 Setting of salt
培养容器直径5 cm,高10 cm 的圆柱形有机玻璃容器,每个填土高度为3 cm。各培养容器中以每克干土对应7.14 μmol N的比例添加3 种不同15N 标记的硝酸铵,其中标记15N 的原子百分数(atom %)分别为15NH4NO3:10.12、NH415NO3:10.18 和15NH415NO3:10.18。
1.3 实验步骤
(1)土样预处理。取土,称取约80 g 相应盐分水平的土,晒干、磨碎、过2 mm筛,按照质量含水量为25%添加约20 mL去离子水,充分混匀后封口放入培养箱培养24 h。
(2)填土培养。将培养土填装进Φ5×10 cm 的培养容器,土装3 cm 高,按照7.14 μmol/g 分3层(0.5、1.5、2.5 cm)用注射器添加同位素氮。
(3)取样。依次在4、24、72、144、288 h(12 d)5 个时间点取样,同时测定取样时培养箱中的温度、湿度、二氧化碳浓度等环境变量参数。
(4)氮素浸提。对以上各时间点取出的培养容器9 个(3 个硝酸铵标记各3个),按照土水比1∶5用高纯度2 mol/L KCl 溶液浸提氮素,将滤液调转移到离心管(10~12 mL)送检。
2 氮素转化模型
2.1 同位素稀释原理
同位素稀释法是测定土壤中氮素转化速率最重要的方法之一[23]。其基本原理为:某一形态的氮库用15N 标记后,当未标记的其他形态的氮转化为该标记状态的氮素时,此时,标记态的氮素15N 总量不变,而标记状态的氮总量增大,这样就形成分子不变,分母增大,从而导致标记态的氮素15N 被稀释;当标记状态的氮素向其他形态的氮素转化时,其14N 和15N 被利用的情况是等可能性的,因此这一转化过程被标记状态的14N 和15N 同时下降;综上,标记状态的14N 增加的同时15N 在减少,因此形成了标记状态的同位素15N 被稀释,结合氮库的含量变化即可计算土壤氮素的总转化速率。
根据同位素稀释原理,可得总矿化速率m、总同化速率i如式(1)、(2):
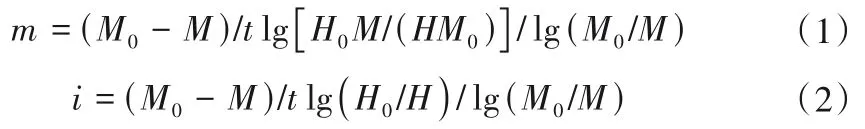
当i<m和i=m时,也可推导出相应的总矿化速率和总同化速率计算公式[10,11]。
2.2 一阶动力学方程
根据同位素稀释原理以及质量守恒有:
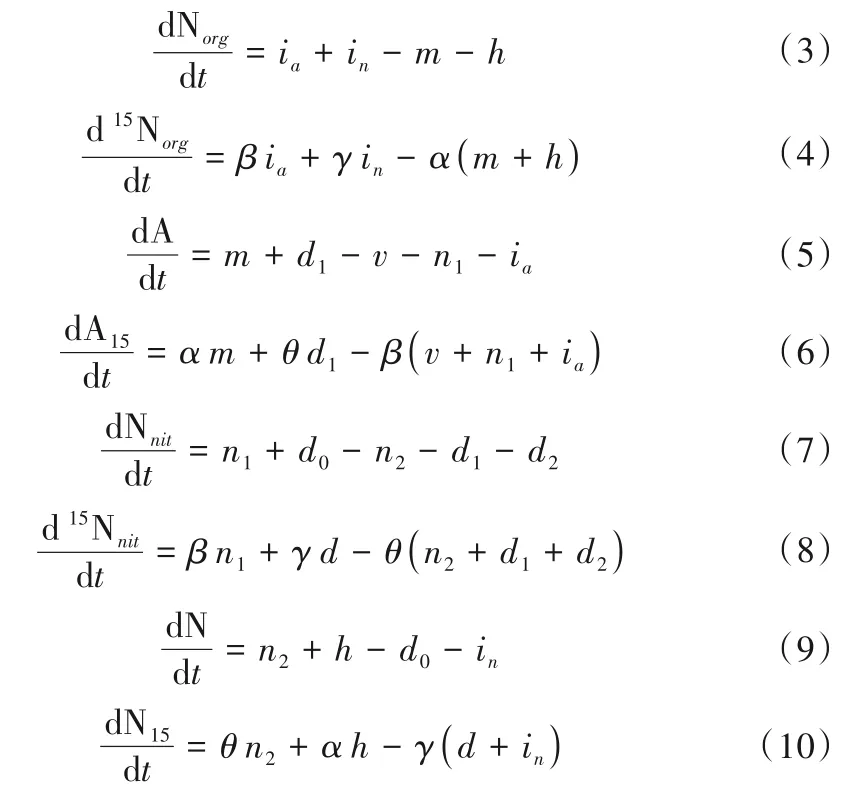
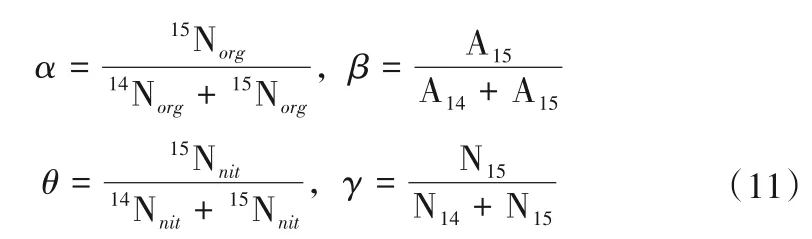
式中:A、A14、A15、N、N14、N15、Norg、14Norg、15Norg、Nnit、14Nnit、15Nnit分别表示铵态氮库、硝态氮库、有机氮库及亚硝态氮库的总量、14态氮的量以及15 态氮的量(mg/kg);m、h、v、n1、ia、d1、d2、n2、d0、in分别表示矿化速率、异养硝化速率、氨挥发速率、第一阶段硝化速率、铵态氮同化速率、异化还原为铵第二阶段速率、反硝化第二阶段速率、硝化第二阶段速率、反硝化或者异化还原为铵第一阶段速率、硝态氮同化速率[mg/(kg·h)],按照式(12)计算,其中α、β、θ、γ为对应的15N/(14N+15N)的比值。
大量研究表明土壤氮素转化过程可以通过一阶或者零阶动力学方程进行描述[13,14,24],但是Muller等人建议,在对超过两个数据点的长时间计算和模拟中一阶动力学方程是比较合适的选择[13],Watson等[25]也证明了采用零阶方程会低估土壤氮素转化过程中NO3-的消耗量,因此本文均假设各个过程满足一阶动力学方程,则有:
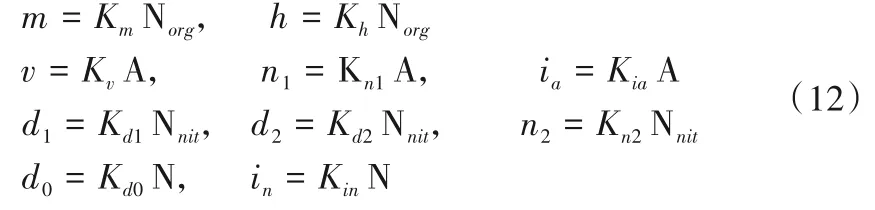
式中:Km、Kh、Kv、Kn1、Kia、Kd1、Kd2、Kn2、Kd0、Kin分别为对应速率的一阶动力学常数,也即是所有的一阶动力学常数k随时间不变,速率仅和氮库的状态量有关。
2.3 模型及初始化参数
因此,最终考虑10个转化过程的模型如图1所示。
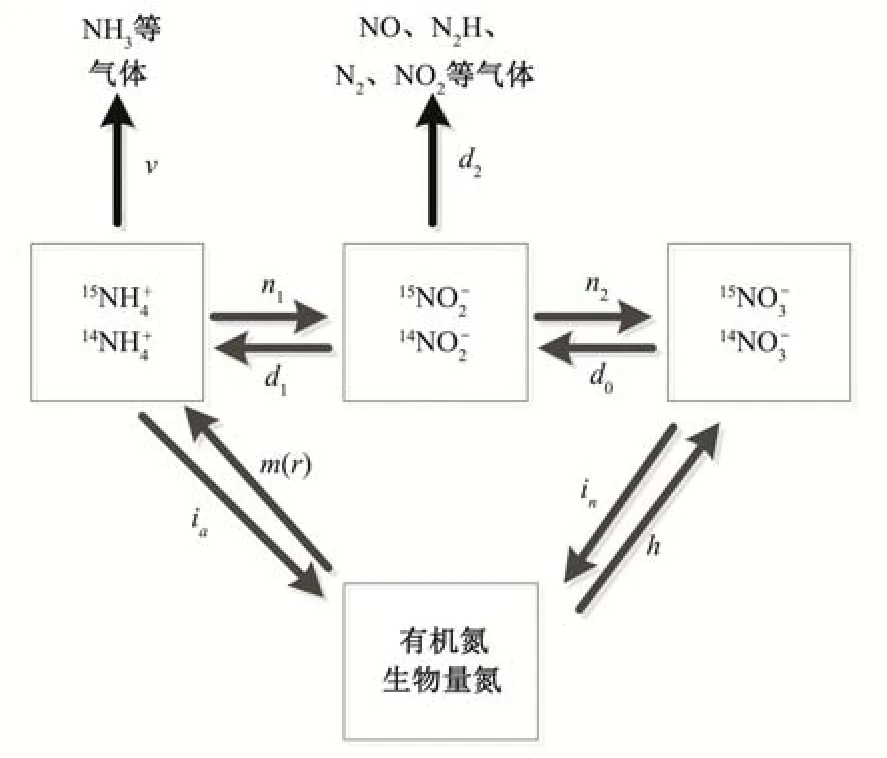
图1 氮素转化模型Fig.1 Nitrogen transformation model
数据的输入分别为3 种标记的铵态氮和硝态氮(包括14N和15N),具体的参数值请参见表2,模型的建立是利用Matlab R2017b软件编程完成。
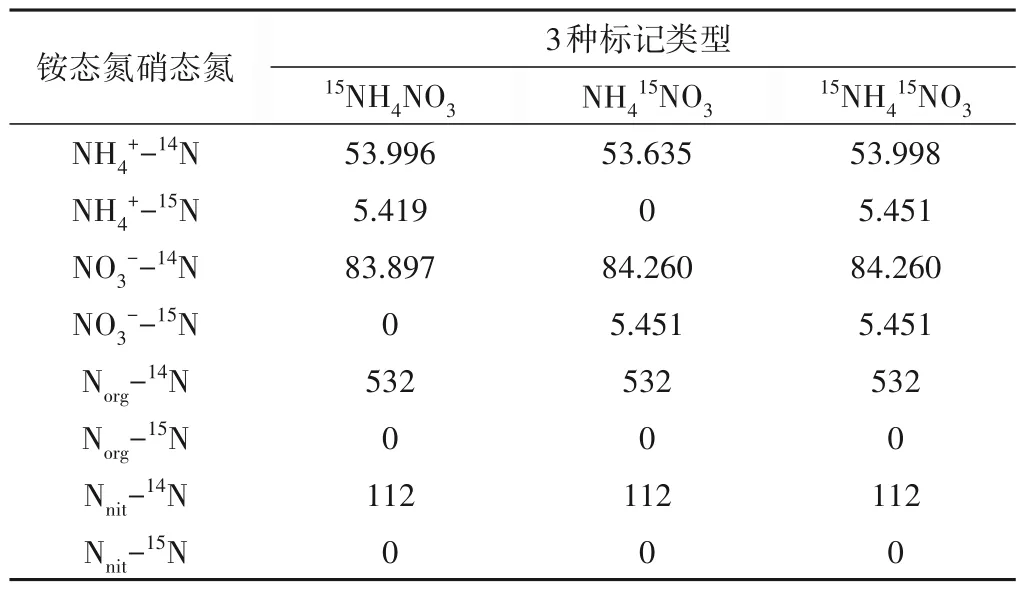
表2 初始的14N和15N输入 mg/kgTab.2 Initial input 14N and 15N
3 结果与分析
不同标记和不同盐分的铵态氮和硝态氮观测值和模拟值的如图2所示。4幅图中,其决定系数R2均大于0.5,说明模型模拟值和观测值相关性程度高,而S2铵态氮(14N+15N 和15N)的观测值和模拟值、S4(15NH4NO3)硝态氮(14N+15N 和15N)的观测值和模拟值其决定系数均大于0.9,表明模型反映的观测值和模拟值之间的离散程度很小,效果好;其中,铵态氮(15N)的观测值和模拟值的拟合相关性系数达0.91。从图2中的所展示的纳什系数来看,它们均大于0,说明模型可以接受[26,27],且图2(d)的纳什系数更是达到了0.71,表明该模型对于S4盐分处理硝态氮的模拟效果很好。偏差Bias为模拟值与观测值的偏差程度,大的偏差值表明模拟值没有很好地逼近观测值,模拟效果差,图2(a)~(d)的偏差依次为-3.46、-0.48、-0.53和1.39。
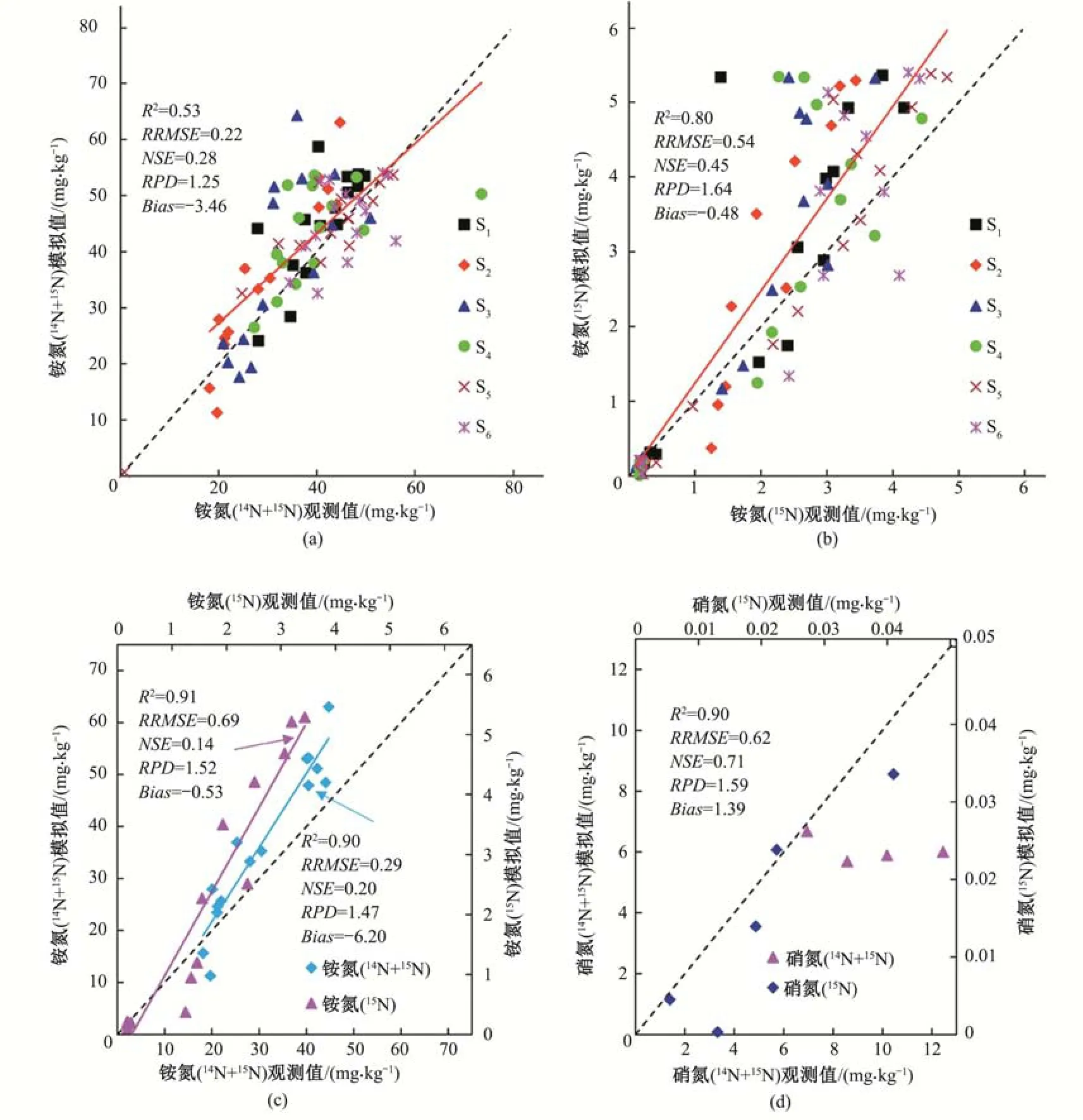
图2 铵态氮和硝态氮观测值和模拟值结果比较Fig.2 Comparison of observed and simulated values of ammonium nitrogen and nitrate nitrogen
S6盐分处理的3 种标记的15N 含量与14N+15N 含量的比值如图3 所示。4 个比值中,α 最小,该比值不仅取决于其15N 的含量,还和总的有机氮含量有关,如添加15NH415NO3标记的土样,铵态氮和硝态氮通过铵同化过程和硝同化过程转化为带标记的有机氮(即15Norg),因此有机氮库中15Norg的含量逐渐上升。同时,有机氮也通过矿化(再矿化)和异养硝化过程转化为铵氮和硝氮消耗有机氮库未标记的有机氮,根据同位素等可能性原则,有机氮库中的14N 和15N 的消耗比例是相同的,且有机氮库的14Norg含量(其初值为532 mg/kg)大于15Norg含量(初始含量为0 mg/kg),因此14Norg的含量下降肯定大于15Norg含量的下降,这样α比值的分子增大,分母减小,引起α增大[图3(a)~(c)];又因为有机氮库中的14Norg含量都比其他3个氮库中的14N含量多,铵氮库最初的含量为59.45 mg/kg,仅为有机氮库的11.18%,亚硝氮库最初的含量为112 mg/kg,为有机氮库的21.05%,硝氮库最初的含量为89.71 mg/kg,占有机氮库的16.86%,且铵态氮和硝态氮还在不断转化为有机氮,因此α始终最小,15NH4NO3标记土样α的最大值为288 h时的0.07%。
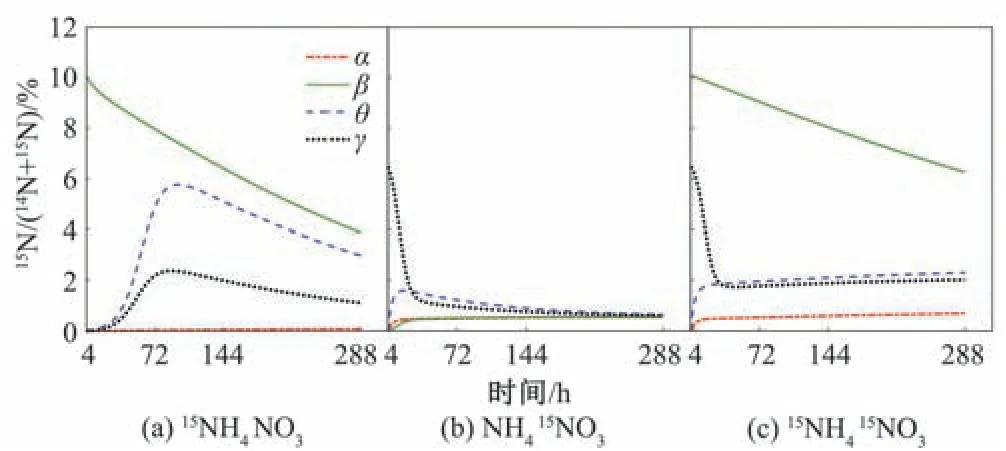
图3 S6氮库15N与14N+15N的比值变化Fig.3 Changes in the ratio of 15N to 14N +15N in S6 nitrogen pool
同样,其他3 个氮库的参数β、θ、γ的变化也类似,如添加NH415NO3标记土样中的γ,实验开始后硝态氮库中标记态的氮(15NO3-)通过反硝化、硝氮同化以及异化还原为铵等过程转化为其他形态氮素离开硝氮库,使15NO3-含量减小,另一方面,其他形态氮素通过硝化、异养硝化等过程不断转化进入硝态氮库,但其他氮库中均不含标记氮(15N),结合氮同位素等可能性原则这样引起硝氮库中的14NO3-含量增加,就形成分子减小,分目增大导致γ不断减小,因此,氮库中15N 含量与14N+15N 含量的比值变化关系很好地解释了同位素稀释原理。
氮素转化速率是反映土壤中氮素转化过程的实际速率,图4 是本研究的10 个不同一阶动力学常数与盐分之间的拟合曲线及相关性,虽然氨挥发过程受到盐分的促进作用,但是其一阶动力学常数和盐分之间的拟合关系的决定系数R2并不高,只有0.36,可能的原因是氨挥发过程不仅受到盐分的影响,同时也和其他本研究没有涉及的因素存在很大的关系;而除了氨挥发的一阶动力学常数之外,其余9 个一阶动力学常数和盐分之间的拟合曲线的R2均在0.65 以上,表明盐分和一阶动力学常数之间均有较好的拟合关系。其中,硝化作用第二阶段的一阶动力学常数Kn2和盐分之间呈负相关关系,其拟合决定系数R20.98是所有拟合关系中最高的,观测值和拟合曲线之间也很贴近,其误差限Δ平均值为0.017,Kn2和盐分的关系可以通过公式Kn2=39.59(lnS)2-244.27 lnS+393.86确定。
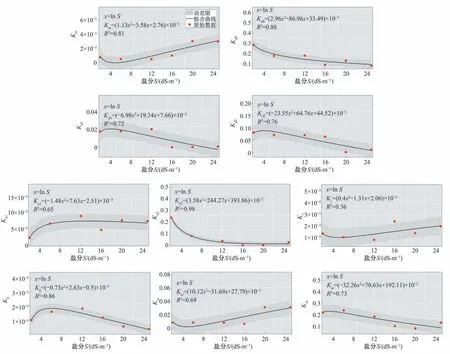
图4 一阶动力学常数和盐分的拟合关系Fig.4 Fitting relationship between first order kinetic constant and salinity
4 结论
以内蒙古河套灌区盐渍土为研究对象,采用同位素标记法开展室内培养实验,基于同位素稀释原理和一阶动力学方程建立了包含氨挥发v、反硝化第一阶段或异化还原为铵第一阶段d0、异化还原为铵第二阶段d1、反硝化第二阶段d2、矿化m、硝化第一阶段n1、硝化第二阶段n2、铵态氮同化ia、硝态氮同化in、异养硝化h等10 个土壤氮素转化过程的模型。通过初始化模型参数和调试,使模型较好地反映了同位素稀释原理以及盐渍土壤氮素转化的各过程,较好地模拟了实验观测值的趋势变化,且对于标记的和未标记的铵态氮和硝态氮均得到了较优的评价结果。
