某些功能饮料中共存胭脂红及酒石黄的检测
2023-01-18何树华
何树华, 江 虹
(长江师范学院化学化工学院,重庆 408100)
食品中的色素分为天然色素和合成色素,天然色素在加工或储存过程中易褪色,而合成色素则具有色泽鲜艳、稳定性好、价格低廉等优点。在食品加工业中,常添加各种合成色素来刺激食欲,提高消费者的购买欲望。然而,当色素被超量使用时,可能导致人体中毒、致癌或死亡。由此各国对合成色素的使用作了严格规定,我国GB 2760-2014《食品安全国家标准 食品添加剂使用标准》规定饮料中胭脂红的含量不得超过0.05 g/kg,酒石黄的含量不得超过0.10 g/kg。可见,研究食品中共存胭脂红和酒石黄的含量有着重要意义。目前报道合成色素检测方法主要有高效液相色谱法[1 - 4]、液相色谱-质谱联用法[5,6]、电化学法[7 - 9]、荧光法[10,11]和紫外-可见分光光度法[12 - 16]。高效液相色谱法和液相色谱-质谱联用法存在成本高、操作繁琐、费时等不足;电化学法需特殊电极材料;荧光法对所用试剂有特殊要求;紫外-可见分光光度法所用设备价廉易购、操作简单、快速,但在食品色素的检测中,常因食品成分复杂,有的共存色素间存在严重的吸收光谱重叠现象,以至于很难用紫外-可见分光光度法进行共存色素的定量分析。文献[14 - 16]报道的分光光度法是用求解复杂的联立方程,文献[12,13]是通过复杂的色素分离措施来实现分光光度法测定共存色素的问题,可见这两种分光光度法均很麻烦。本工作首先将被分析物进行光谱定性分析,确定样品中可能的共存色素,再进行定量分析,这不仅可以大大简化工作流程,还可提高该法的选择性。该法用于实际样品分析,结果满意。
1 实验部分
1.1 仪器与试剂
U-3010型紫外可见分光光度计,购自日本日立公司;pHS-3C型酸度计,购自上海虹益仪器仪表有限公司;KQ-200VDE型超声波清洗机,购自昆山超声仪器有限公司。
胭脂红(Carmine,CAR,纯度≥98%)标准物质,购自上海源叶生物科技有限公司;酒石黄(Tartrazine,TAR,纯度≥98%)标准物质,购自北京普析科技有限公司;碱性艳绿(Alkaline Brilliant Green,ALKG,纯度99%),购自上海迈瑞尔化学技术有限公司;氨丁三醇(Tris,纯度≥99.8%),购自上海阿拉丁生化科技股份有限公司;HCl(分析纯),购自重庆川东化工有限公司。水为自制超纯水。
样品为市售东鹏功能饮料(1#)和红牛功能饮料(2#和3#)。
1.2 溶液制备
CAR、TAR标准溶液贮备液:1.00×10-3mol/L水溶液(CAR、TAR的质量浓度分别为562.5 mg/L和534.4 mg/L),操作溶液浓度均为1.00×10-4mol/L(用贮备液稀释),于冰箱4 ℃保存。Tris溶液为0.20 mol/L水溶液,HCl浓度为0.10 mol/L。Tris-HCl溶液:pH 3.0~9.8,通过酸度计测量Tris和HCl混合溶液的pH。ALKG溶液:1.00×10-3mol/L水溶液。
1.3 样品的制备
准确移取30.0 mL 1#~3#功能饮料,称量(精确到±0.000 1 g),于超声仪45 ℃超声20 min,取出,冷却后用NH3·H2O调至近中性,60 ℃水浴加热,加入1g已调成糊状的聚酰胺粉末,搅拌、抽滤,用60 ℃ pH 4.0的水(柠檬酸调pH)洗3~5次(5 mL/次),再用6∶4(体积比)的甲醇-甲酸混合物洗涤3~5次(5 mL/次),最后用水洗至洗脱液为无色。再用7∶2∶1(体积比)的乙醇-氨水-水混合液解吸3~5次(5 mL/次)至色素完全解吸。合并解吸液,用乙酸中和至近中性,水浴70 ℃蒸发至近干,加适量水溶解并稀至5.0 mL,取定容溶液4.0 mL用水稀释至25.0mL,得1#~3#待测液,储于4 ℃冰箱中。
1.4 实验方法
取适量1#~3#待测样液于分光光度计上扫描(以水作参比),根据吸收曲线的形状及最大吸收波长确定样液中可能存在的色素。于10 mL比色管中,分别准确加入1.00×10-4mol/L CAR和TAR标准溶液0~1.80 mL、1.00×10-3mol/L ALKG溶液2.00 mL及pH 3.80 Tris-HCl溶液1.00 mL,用水定容。10 min后,于分光光度计上扫描吸收光谱(以试剂空白作参比),在521 nm测定CAR体系的吸光度,在426 nm测定TAR体系的吸光度。
2 结果与讨论
2.1 CAR、TAR及与ALKG反应的吸收光谱特征
图1中曲线1和2分别是胭脂红和酒石黄标准溶液的吸收曲线,胭脂红的最大吸收波长为504 nm,酒石黄的最大吸收波长为428 nm。曲线3~5分别是1.4节中制得的1#、2#和3#样液的吸收曲线,根据吸收光谱定性分析依据,将样液及标准溶液的吸收曲线形状及最大吸收峰相比较,可以判断1#~3#样中只含CAR和TAR,不含其它色素。由此确定色素范围,有针对性的制定CAR与TAR共存时的定量分析方案,大大简化了分析流程。

图1 胭脂红、酒石黄及1#~3#样品的吸收光谱Fig.1 The absorption spectra of carmine,tartrazine,and 1#-3# samples1.CAR(6.04 mg/L);2.TAR(5.34 mg/L);3-5.1#-3# sample liquid;against water.
ALKG为三苯甲烷类碱性染料,可与酸性染料CAR、TAR以静电引力相作用,生成离子缔合物。图2A表明,CAR和TAR与ALKG在pH 3.80条件下均可发生反应。曲线1是CAR与ALKG反应生成的缔合物的吸收曲线,在可见光区除有2个较大的正吸收峰外,还有较小的正吸收和负吸收峰,最大正吸收峰位于521 nm(相对于ALKG蓝移101 nm,ALKG的最大吸收峰位于622 nm),次大正吸收峰位于660 nm;曲线2是TAR与ALKG反应生成的缔合物的吸收曲线,在可见光区有2个明显的正吸收峰,最大正吸收峰位于426 nm(紫移196 nm),次大吸收峰位于628 nm;两体系的波移现象表明,CAR和TAR是可以与ALKG反应生成新物质二元离子缔合物。
当选择在521 nm处测定CAR时,CAR-ALKG体系有大的吸光度,而TAR-ALKG体系的吸光度近于0,即共存TAR不干扰CAR的测定;当选择在426 nm处测定TAR,TAR-ALKG体系有大的吸光度,而CAR-ALKG体系的吸光度近于0,即共存CAR不干扰TAR的测定。从图2可知,在其它吸收峰处测定CAR和TAR,两缔合物的吸收曲线重叠较大,相互间干扰大,不能分别测定共存的CAR和TAR。故选择521 nm作为CAR的测定波长,426 nm作为TAR的测定波长,可实现共存色素CAR与TAR的分别测定。
由图2B可知,在521 nm和426 nm处分别测定CAR与TAR,缔合物均有好的线性关系和较高灵敏度,能用于定量分析共存色素CAR和TAR。吸收光谱特征见表1。
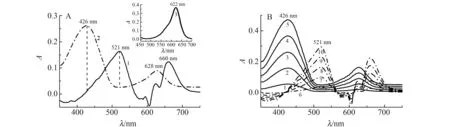
图2 胭脂红、酒石黄与碱性艳绿反应的吸收光谱Fig.2 The absorption spectra of the reaction of carmine,tartrazine with alkaline brilliant greenA:1.CAR(6.04 mg/L)-ALKG(2.00×10-4 mol/L),pH 3.80,against reagent blank;2.TAR(5.34 mg/L)-ALKG(2.00×10-4 mol/L),pH 3.80,against reagent blank;3.ALKG(2.00×10-5 mol/L),pH 3.80,against water;B:1-5.TAR(1.07,3.21,5.34,7.48,9.62 mg/L),ALKG(2.00×10-4 mol/L);6-10.CAR(1.21,3.63,6.04,8.45,10.9 mg/L),ALKG(2.00×10-4 mol/L);pH 3.80,against reagent blank.
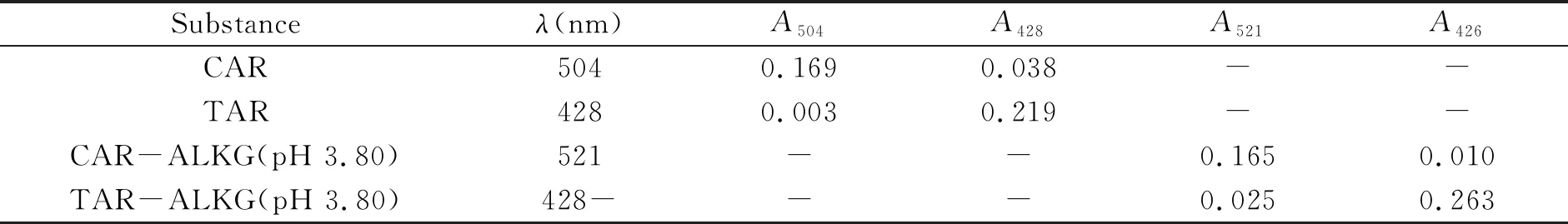
表1 胭脂红、酒石黄的吸收光谱特征
2.2 溶液酸度
室温下,考察了1.00 mL不同pH 的Tris-HCl(pH 3.0~9.8)溶液对1.00 mL CAR或TAR(1.00×10-4mol/L)与2.00 mL ALKG(1.00×10-3mol/L)反应生成的离子缔合物的吸光度的影响。结果表明,在pH 3.80的条件下,当测定波长为521 nm时,可单独测定CAR,TAR不干扰;当测定波长为426 nm时,可单独测定TAR,CAR不干扰(图2A曲线1和2),故选择1.00 mL pH 3.80 Tris-HCl溶液作为两体系的反应介质。
2.3 反应时间
室温下,考察了选定酸度下5 min~120 min内不同反应时间对两体系吸光度的影响。结果表明,CAR-ALKG体系与TAR-ALKG体系的反应在10 min内均可进行完全;在10 min~60 min内,两体系的吸光度达最大且基本稳定;60 min后,随着时间的增加,两体系吸光度均有降低趋势。故测定时间选在10 min后的稳定区。
2.4 方法学考察
2.4.1 标准曲线及灵敏度移取1.00×10-4mol/L CAR、TAR标准溶液0.0、0.20、0.60、1.00、1.40、1.80 mL,分别置于比色管中,加入2.00 mL ALKG(1.00×10-3mol/L)溶液和1.00 mL pH 3.80 Tris-HCl 溶液,用水定容至10 mL。参照1.4 项下的测定方法测定两体系标准系列溶液的吸光度,作标准曲线。结果显示,CAR与TAR两种体系的表观摩尔吸光系数分别为1.26×104L/(mol·cm)、2.63×104L/(mol·cm)。CAR与TAR体系方法有很好的线性关系、较宽的线性范围及较高灵敏度(表2)。

表2 胭脂红及酒石黄的标准曲线相关参数
2.4.2 方法的选择性室温下,考察了某些常见阴阳离子、氨基酸、糖类及某些常见色素对测定6.04 mg/L CAR和5.34 mg/L TAR的影响,见表3。结果表明,当相对误差≤±5%时,常见阴、阳离子及氨基酸、糖类的允许倍数均较大,而常见共存色素中,除日落黄、亮蓝有较大允许倍数外,苋菜红、诱惑红及赤藓红允许倍数相对较小,但被测溶液的定性结果表明样液中不含此3种红色色素。

表3 共存物质的影响
2.4.3 样品测定、准确度及精密度取1#~3#待测样液各2.00 mL,加入2.00 mL ALKG溶液及1.00 mL pH 3.80 Tris-HCl溶液,用水定容至10 mL,在选定测定波长及反应时间下测定各溶液的吸光度(n=5),并与GB 5009.35-2016法(HPLC法)结果比较,同时作加标回收试验(n=5)。结果见表4,可见,新方法测定结果与国标法相近,并有较高的准确度和精密度,可用于共存CAR和TAR的定量分析。
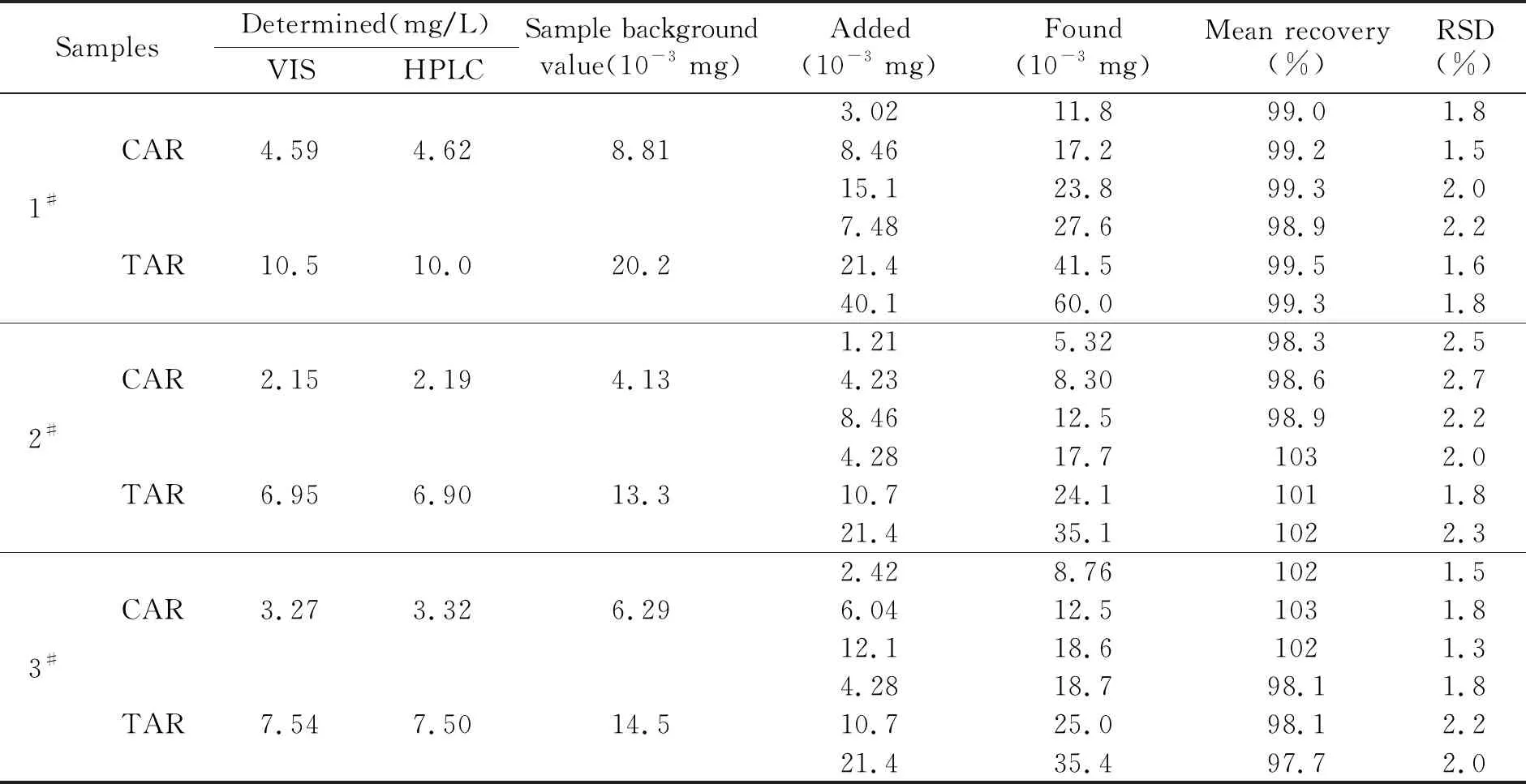
表4 样品分析结果及回收试验(n=5)
3 结论
在定性分析基础上,针对样品中存在的色素进行定量分析,不仅可以大大减小分析工作量,而且还可提高光度分析方法的选择性。以ALKG作探针的酸度控制吸收光谱法,不仅简便、快速,有较高灵敏度、较好选择性及较宽线性范围,而且成本低、仪器价廉易于普及;新方法检测结果与国标法基本一致,准确度和精密度符合定量分析要求。
