膳食补充剂β -烟酰胺单核苷酸辅助预处理高龄合并医源性卵巢储备功能减退不孕症的1例报道
2023-01-13杨志勇王桂芳
杨志勇, 王桂芳
(同济大学附属第十人民医院生殖医学中心,上海 200072)
体外受精-胚胎移植(俗称“试管婴儿”)技术成功解决了数百万不孕不育夫妻的妊娠问题,但治疗卵巢储备功能减退的不孕患者,目前仍较为棘手,表现为: 体外获取的卵子数量少和/或卵子质量差,导致可移植胚胎的数量与发育潜能均明显降低,治疗成功率远低于其他病因不孕。导致卵巢储备功能减退的原因以高龄和医源性为主。近些年,伴随国家人口政策的调整,追求二胎/三胎的女性逐渐增多,导致试管婴儿治疗中,卵巢储备功能减退的不孕夫妇比例呈现逐年升高趋势。目前生殖医学面临的最大挑战之一是如何改善这类人群的助孕结局,但遗憾的是,迄今为止改善卵巢功能和提升卵母细胞质量的治疗方法极为有限。本研究回顾性报道1例由于高龄(年龄>35岁)合并医源性卵巢储备功能减退的女性不孕患者,既往接受11次体外受精-胚胎移植治疗失败后,自行补充膳食补充剂β-烟酰胺单核苷酸(nicotinamide mononucleotide, NMN)3个月后,再接受第12次试管婴儿治疗成功并活产1名女婴的病例,以期为临床寻找解决卵巢储备功能减退不孕患者的助孕难题开拓思路。
1 资料与方法
1.1 一般资料
患者夫妇婚后性生活正常,自然流产后未避孕5年未孕,于2018年求治于同济大学附属第十人民医院生殖医学中心。
女方患者38岁,身高168 cm,体质量70 kg,体质量指数(body mass index, BMI)24.8 kg/m2。平素月经周期尚规律,周期35 d左右,经期5 d,经量适中,无痛经等明显经期不适症状。生育史目前足月分娩0,早产0,流产1,生育儿童0。2013年自然妊娠后于孕8周因稽留流产行清宫术治疗,术后未采取避孕措施5年未孕。2017年患者因多囊卵巢综合征曾经进行双侧卵巢楔形切除术联合双侧输卵管通液术,术中提示双侧输卵管通畅,术后联合克罗米芬促排卵治疗仍未成功建立妊娠。我院妇科查体: 阴道畅通,子宫颈光滑,子宫前屈前倾位、大小正常、质地中等无压痛,双附件区未明显探及异常。2018年6月在月经周期第2天检查基础性激素水平如下: 促卵泡激素(follicle-stimulating hormone, FSH)9.75 IU/L,促黄体生成素(luteinizing hormone, LH)3.79 IU/L,雌二醇137.7 pmol/L,孕酮0.48 nmol/L;外周血抗缪勒管激素(anti-Müllerian hormone, AMH)0.8 ng/mL;经阴道超声显示双侧卵巢基础窦卵泡计数(antral follicle count, AFC)共计4枚;外周血染色体检查示女性正常核型: 46,XX。其临床诊断: 继发不孕,卵巢储备功能下降(卵巢楔形切除术后),多囊卵巢综合征术后。
男方患者43岁,否认勃起功能障碍,否认射精障碍。男科体检外生殖器正常,双侧睾丸体积正常,附睾区无结节和压痛。既往在外院多次进行精液常规检测提示弱精症。根据男性精液正常参考标准(世界卫生组织第5版),我院精液常规检测显示: 精液量1.8 mL,精子浓度93.7×106/mL,前向运动精子比例(progressive motility, PR) 5.3%,非前向运动精子比例(non-progressive motility, NP) 12.3%,正常形态精子比例2%;精子DNA碎片指数(DNA-fragmetation-index, DFI)16.08%;男方外周血染色体检查示男性正常核型: 46,XY;Y染色体微缺失检测未见异常。其临床诊断为继发不孕,重度弱精症、畸形精子症。
夫妻双方否认近亲结婚,否认家族重大遗传病史,传染性疾病及生殖道感染性疾病检测均未见明显异常;在无治疗禁忌的情况下,患者夫妇开始接受体外受精-胚胎移植术治疗。
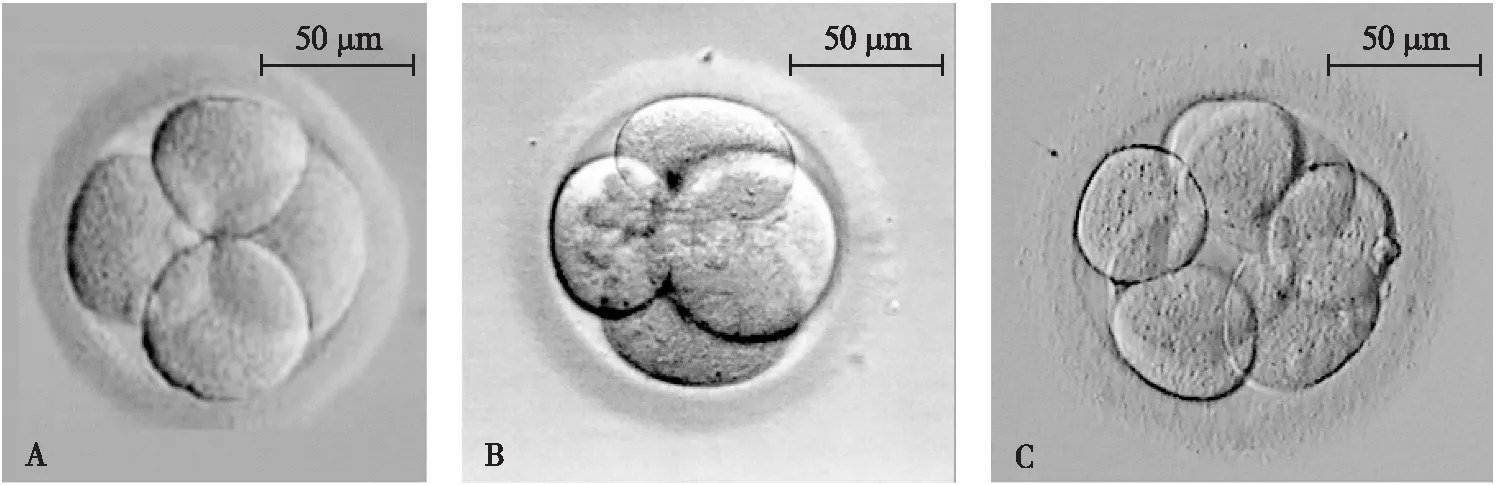
图1 患者第12次取卵形成的胚胎Fig.1 The morphology of embryo from the 12th oocyte retrievaA: 第2天胚胎,4细胞,Ⅰ级;B: 第2天胚胎,4细胞,Ⅱ级;C: 第3天胚胎,8细胞,Ⅰ级
1.2 总体治疗经过
患者夫妇整个治疗时间跨度4年,自2018年6月至2021年12月。女方患者共计进行了12次促排卵取卵和6次胚胎移植治疗,具体采用的辅助生殖治疗技术详情见表1。男方患者因重度弱精,且精子质量(前向运动比例和正常形态)均未得到明显改善,因此体外授精方式全部采用单精子卵母细胞质注射方法(intracytoplasmic sperm injection, ICSI)。患者在12次促排卵治疗中: 温和刺激方案6次,GnRH拮抗剂方案3次,长效GnRH激动剂长方案2次,GnRH激动剂短方案1次。患者12次促排卵治疗均呈现卵巢反应不良,符合波塞冬低预后4型特征[1]。12次促排卵均达到取卵标准,无取消周期发生,每取卵周期获卵数均≤4枚,平均2枚,其中获卵1枚的周期为3个(GnRH拮抗剂方案2个,温和刺激方案1个),获卵2枚的周期为7个(GnRH拮抗剂方案1个,温和刺激方案5个,长效GnRH激动剂长方案1个),获卵3枚的周期为1个(长效GnRH激动剂长方案1个),获卵4枚的周期为1个(GnRH激动剂短方案1个)。第6次和第7次取卵均未获得正常受精卵,6次取卵周期中即使获得2枚成熟的卵子,也仅能获得1枚正常受精卵。其中7次促排卵治疗周期没有可移植胚胎形成(Ⅰ、Ⅱ、Ⅲ级为可移植胚胎),第5次促排卵治疗周期至第11次促排卵治疗周期均未获得可移植胚胎。患者自第11次取卵后,自行开始口服补充膳食补充剂β-烟酰胺单核苷酸150 mg每日2次,至第12次取卵时,已口服β-烟酰胺单核苷酸3个月。2021年12月取卵,获得4枚成熟卵子,4枚卵子均正常受精,最终形成3枚优质可移植胚胎,见图2。移植其中2枚后,确立双胎妊娠,于妊娠8周后转至产科进行产前检查直至活产分娩。患者自首次接受试管婴儿治疗时34岁,至第12次取卵时38岁,4年时间卵巢功能发生进一步减退,卵巢功能评估参数见表2,至第12次取卵前AMH由最初治疗时的0.8 ng/mL降至0.5 ng/mL。
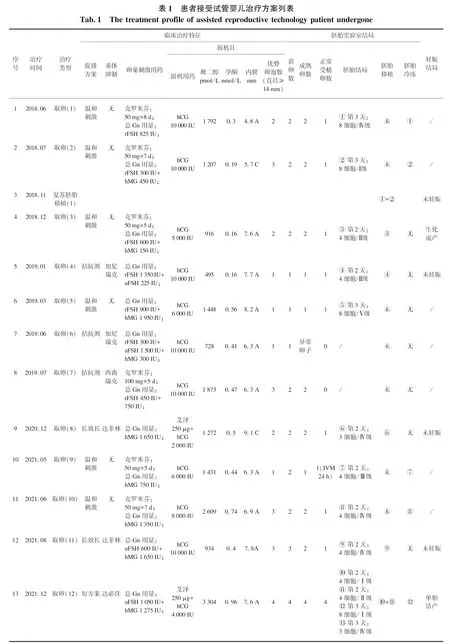
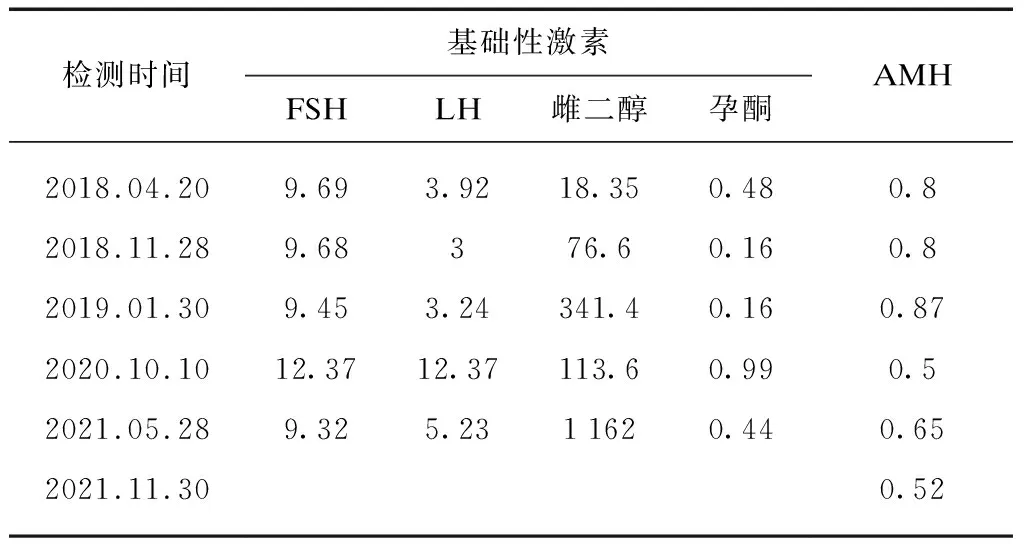
表2 患者卵巢功能评估参数表
1.3 治疗结局
患者于2021年12月11日移植2枚D2胚胎,移植后第11天血β-hCG 253.2 IU/L,确认妊娠。移植后第14天血β-hCG 638.6 IU/L显示翻倍良好。孕6周时首次超声确认宫内双胎妊娠(双胎类型: 双羊膜囊双绒毛膜),孕囊大小分别为11 mm×7 mm×11 mm(可见心管波动)和14 mm×11 mm×15 mm(未见心管波动);孕8周时第2次超声随访: 宫内双胎妊娠,孕囊大小分别为18 mm×16 mm×27 mm(可见心管波动)和22 mm×14 mm×36 mm(可见心管波动);孕12周时超声随访显示头臀径(crown-rump length, CRL)52 mm,胎心可见,颈后透明带扫描(nuchal translucency, NT)1.2 mm和CRL 51 mm(胎心可见,NT 3.8 mm)。因1胎NT异常,患者在孕24周时进行经腹壁羊膜穿刺术对羊水细胞染色体核型分析,结果显示NT异常胎儿为21-三体型,于孕28周时行减胎术。患者最终于2022年9月7日孕40周+6 d因“珍贵儿,孕晚期减胎”选择剖宫产终止妊娠,术中分娩1名活女婴,新生儿出生体质量3 055 g,身长50 cm,Apgar评分10分,外观检查及超声检测未见畸形。
2 讨 论
卵巢储备功能减退性不孕患者的助孕结局低于预期或常规人群的治疗结局,成为临床较为棘手的难题之一。目前针对改善这类人群卵子质量的方法有: (1) 更换促排方案;(2) 线粒体置换术;(3) 联合使用生长因子;(4) 中医药调理;(5) 膳食补充剂,如: 辅酶Q10、维生素E、DHEA等。但这些方法的临床效果有限,而且异体线粒体置换术还存在生殖伦理的问题,因此临床亟需寻找其他合适的解决方法。
作为膳食补充剂,β-烟酰胺单核苷酸因其可以逆转衰老诱发线粒体功能的下降和体内烟酰胺腺嘌呤二核苷酸(nicotinamide adenine dinucleotide, NAD+)水平的下降,目前较多用于抗衰老领域的辅助治疗,并取得了一系列的研究进展。因其对线粒体作用的广普性,线粒体功能的改善是否会影响卵巢功能,本课题组进行了Pubmed检索,发现β-烟酰胺单核苷酸对女性生殖衰老的预防作用和改善卵母细胞质量已有动物实验证据,但尚未检索到相关的临床研究报道。因此,本文是首次报道应用膳食补充剂β-烟酰胺单核苷酸后助孕结局得到改善的病例。鉴于此,本研究从其可能的作用机制和未来还需要临床进一步明确的科学问题进行探讨。
2.1 β-烟酰胺单核苷酸的作用机制
NMN是一种具有生物活性的核苷酸吡啶碱,相对分子质量为334.22,以α和β两种异构体形式存在,其中β异构体形式具有生物活性,其化学结构[2]见图2。NMN是由烟酰胺磷酸基转移酶(nico-tinamide phosphoribosyl transferase, NAMPT)催化1个磷酸基和1个由烟酰胺(维生素B3的酰胺形式)与核糖组成的核苷的反应产物[3]。
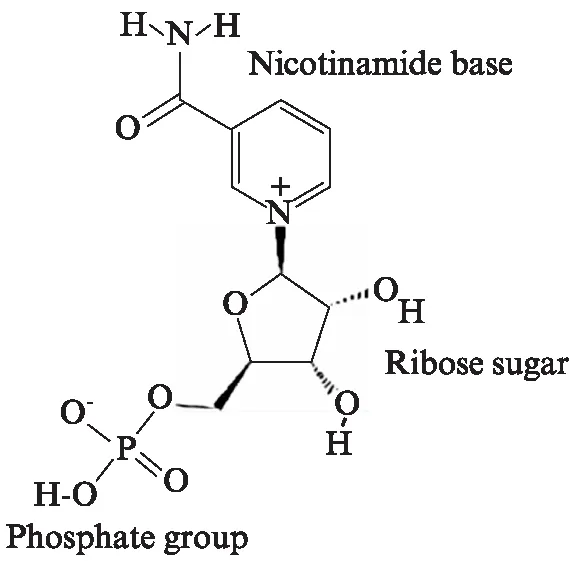
图2 β-烟酰胺单核苷酸的化学结构Fig.2 Chemical structure of NMN
NMN是NAD+生物合成的前体,NAD+是真核生物中一种非常重要的氧化还原辅酶,是大量酶促反应的必需成分,参与细胞代谢的多个方面[4-5],在细胞死亡、衰老、自噬、适应性应激反应、基因组稳定性和DNA修复等多种机体生物学过程中发挥着重要作用[6]。事实上,许多细胞和组织的NAD+水平随着年龄的增长而下降,这种下降被认为与多种相关疾病有关。NAD+水平的下降会改变NAD+/SIRT1轴,导致神经退行性变、血管炎症、脂肪生成与储存增加、胰岛素抵抗、疲劳和肌肉力量丧失的发生[7-10]。因此,恢复细胞内NAD+的水平是一种有效的抗细胞衰老干预手段。NMN可以逆转由于NAD+不足导致的线粒体稳态失衡、活性氧(ROS)过量产生、DNA修复障碍和细胞存活方面的缺陷[11]。近期一项对高龄小鼠补充NMN改善生殖老化的基础研究发现: (1) 补充NMN改善了线粒体的功能,逆转了高龄卵母细胞内NAD+水平的下降;(2) NAD+水平的提升降低了卵母细胞内ROS的蓄积,维持纺锤体与染色体正常结构和皮质颗粒成分的动力学变化,不仅提高了卵子成熟率、而且改善了卵子的受精能力和后续胚胎发育潜力[12]。国内学者[13]进一步通过小鼠着床前胚胎发育的代谢动力学对表观遗传学的影响研究发现: 卵子NAD+的合成对胚胎着床前的发育是必不可少的,NAD+通过与SIRT1的配合,去除受精后合子的H3K27ac,从而退出小合子基因组激活阶段(合子的S期和2细胞胚胎的G1期之间发生的基因组激活阶段[14],此阶段被认为与后续胚胎发育密切相关[15])。对于人类,NAD+的补充可以促进受精后合子H3K27ac的去除,有利于胚胎着床前的发育。综上,推测NMN对于改善卵子质量的机制可能为: (1) 通过线粒体代谢途径,逆转了卵巢功能下降导致的卵母细胞内NAD+水平的下降,继而降低了ROS的蓄积,维持受精后涉及胚胎发育的重要结构的正常,如细胞骨架纺锤体与染色体的结构和皮质颗粒的动力学变化。(2) 通过代谢-表观遗传重塑途径,加速合子H3K27ac的去除,影响合子基因组激活,有利于着床前胚胎的发育。
2.2 改善卵巢储备功能减退患者卵子质量的方法

3 结 语
在本病例报道之前,尚未见到应用NMN预处理改善卵巢储备功能减退患者的相关报道。因此该患者显示的应用NMN后助孕结局得到改善之间的因果关系还需要严谨的随机双盲临床对照试验或者前瞻性队列研究进行明确。同时,对于卵巢储备功能减退的不同程度,NMN的适用剂量也需要进一步通过研究确定。有限的NMN改善卵母细胞质量的研究样本来源于动物小鼠,因此对于人类卵母细胞,NMN是否也是通过相似机制来改善卵母细胞质量和胚胎发育潜能需要在人类卵子身上进行验证。
最后,作为病例报告,本文的局限性明显,如: 不能明确NMN的确切效果和相应机制,但在当下面对缺少有效的改善卵巢储备功能减退性不孕患者助孕结局的方法,其价值在于可以提供一个未来值得深入研究的方向和潜在的改善方法。
