CuCo2O4/SBA-15负载型催化剂的制备及其催化氧化苄醇的研究
2023-01-13杨琪杰陈威韦俐霞李悦心仇丹李亚王灵辉
杨琪杰,陈威,韦俐霞,李悦心,仇丹,李亚,王灵辉
(宁波工程学院 材料与化学工程学院,浙江 宁波 315211)
0 引言
混合金属氧化物(mixed metal oxide,MMO)材料具有可调节的电子能带结构,能够表现出与相应的单组分氧化物及其混合物明显不同的化学性质,同时还能为各种催化反应提供新型的表面活性位点。MMO这种性质使其在催化[1-2]、选择性吸收涂层[3]、磁性应用[4]、太阳能海水淡化[5]、医药等领域具有广阔的应用前景。在MMO类型的材料中,不同金属离子之间在原子水平上发生相互作用,使MMO表现出与相应的单组分氧化物及其混合物不同的化学性质。此外,MMO还能为各种催化反应提供新的表面活性位点,使其具有更好的催化性能。
单独的MMO粒子较为细小,回收较为困难,无法重复使用,而将其负载在介孔模板上可解决该问题。目前,负载MMO纳米粒子的介孔材料,引起了人们的广泛关注。这种介孔材料具有比表面积大、热稳定性好、孔隙均匀等特点[6],并且具有极高的表面暴露率,同时其纳米级颗粒尺寸可以为催化剂提供丰富的反应活性位点[7]。通过控制改变介孔负载混合金属氧化物的粒径大小、表面状态以及形貌等参数,也可以提高其催化活性[8]。现在的化工工艺通常以介孔二氧化硅或碳为模板,采用纳米浇铸法合成MMO负载催化剂[9-11]。纳米铸浇法的优点包括催化剂具有更大的表面积以及均匀、可调的孔径,其大粒径有利于后续操作。
苯甲醛作为一种最简单的芳香醛,是苄醇选择性氧化的主要产物,广泛应用于制造医药、染料、香料以及农药等各个领域[12-14]。苯甲醛通常是通过苄醇的选择性氧化来生成的[15]。传统的醛类制备方法需要消耗大量的铬酸盐或高锰酸盐氧化剂,这些氧化剂毒性大,使用过程中会产生很大的安全隐患并对环境造成严重污染。以纯氧或过氧化氢[16-18]为氧化剂的苄醇选择性氧化反应则被认为是一种更环保的策略,已成为制备“绿色”产品的主要途径之一[19-20]。近年来随着社会对环保关注度的不断提高,以及更为严格的环保法律法规的实施,工业上迫切需要寻找一种经济、环保的非均相催化剂替代传统的均相催化剂,而CuCo2O4/SBA-15正是一种易于分离回收的环保型非均相催化剂[21]。
本文提出了以SBA-15为介孔模板,制备混合金属氧化物CuCo2O4负载催化剂,并以质量分数为30%过氧化氢溶液为氧化剂,探究其催化苄醇氧化为苯甲醛的性能。
1 试验条件及方法
1.1 仪器与试剂
Bruker D8 advance X射线衍射仪(XRD)、NOVA2000e比表面积分析仪、JEM-2100F透射电镜(TEM)、Thermo Scientific Nexsa X射线光电子能谱(XPS)、飞纳Pro扫描电子显微镜(SEM)、GC-2014气相色谱仪。
所用试剂均为分析纯。
1.2 SBA-15的制备
SBA-15采用水热法合成[22-23],将45 g蒸馏水和30 g的盐酸(4 mol·L-1)加入圆底烧瓶中,然后加入2 g P123模板剂,最后加入4 g甘油,常温搅拌12 h后加入3.1 g正硅酸四乙酯(TEOS)。35℃水浴反应12 h,然后将混合物加入到水热反应釜中,100℃反应12 h。固体产物用乙醇清洗后过滤,然后在100℃下干燥,除去多余的水分和乙醇,500℃煅烧6 h,得到SBA-15。
1.3 CuCo2O4/SBA-15的合成
将0.09 g三水合硝酸铜(0.375 mmol)和0.22 g六水合硝酸钴(0.750 mmol)用蒸馏水定容到5 mL,制得前驱体溶液。将0.5 g SBA-15载体加入到15 mL正己烷中,高速搅拌,缓慢加入0.5 mL前驱体溶液。由于毛细效应,前驱体溶液自发进入介孔氧化硅的孔隙内。搅拌1 h后,在100℃下干燥,去除多余的水分和大部分结晶水,然后将产品在600℃空气下煅烧4 h,制得CuCo2O4/SBA-15负载型催化剂。
1.4 催化氧化性能评估
典型的催化氧化过程如下:以质量分数为30%的过氧化氢溶液为氧化剂,在圆底烧瓶中加入0.1 g CuCo2O4/SBA-15,再加入80.0 g蒸馏水,超声10 min,再加入1.08 g苄醇(10.0 mmol)和3.0 mL质量分数为30%过氧化氢溶液,反应一定时间后取出冷却,通过气相色谱法得到苄醇的转化率和苯甲醛选择性。
2 结果与讨论
2.1 载体和催化剂的表征
图1为SBA-15载体的小角XRD谱图,由图可以看到在1.02°、1.74°和1.96°出现了3个明显的衍射峰,分别对应于二维六方p6 mm有序介孔结构的(100)、(110)和(200)晶面,与文献报道一致[24]。图中的衍射峰较尖锐,说明制备的SBA-15规整性好。通过Scherrer公式可以计算出制备的SBA-15的平均孔径大小为7.88 nm,这远远大于苯甲醇和苯甲醛的尺寸,利于反应产物和底物自由进出孔道,利于反应的发生。

图1 SBA-15的小角XRD谱图
焙烧过后催化剂CuCo2O4/SBA-15的广角XRD谱图如图2所示。可以看到,样品在18.9°、31.2°、36.7°、44.7°、55.5°、65.0°、68.4°、73.9°、78.2°和82.4°时出现了衍射峰。这些衍射峰与Cu0.92Co2.08O4(PDF卡片号37-0878)位置一致,表明成功通过纳米浇铸法实现CuCo2O4在介孔SBA-15孔道内的生成。由图可观察到峰的强度较小,这是因为SBA-15孔道小,使得生成的CuCo2O4晶体较细,且金属氧化物含量也较低。

图2 CuCo2O4/SBA-15的广角XRD谱图
图3是SBA-15负载催化剂CuCo2O4前后的SEM照片,从图3(a)中可以看到SBA-15具有明显的短棒状结构,颗粒直径在0.7~1.1 μm之间,从图3(b)中可以看到负载催化剂也具有明显的短棒状结构,颗粒直径也在0.7~1.1 μm范围,说明负载CuCo2O4后,载体SBA-15的结构未被破坏。合适大小的颗粒一方面使得催化剂在反应体系中具有较高的分散性和比表面积,利于提高催化效率,另一方面也便于催化剂的回收利用。

图3 SBA-15负载前后的SEM照片:(a)SBA-15;(b)CuCo2O4/SBA-15
图4为SBA-15负载催化剂CuCo2O4前后的TEM照片,由图4(a)可以看出SBA-15的直形管状结构,呈二维六方通孔结构,具有P6 mm空间群,管径为6 nm,这与图1的小角XRD结果一致。图4(b)为CuCo2O4/SBA-15的HRTEM照片,可以找到明显的晶体结构,图中0.28 nm和0.20 nm分别对应于尖晶石结构CuCo2O4晶体的(220)和(400)晶面,这进一步证明了CuCo2O4晶体结构的生成,与图2的广角XRD结果一致。该二维六方通孔结构可以大大降低物质在孔内的扩散阻力,利于反应底物和产物的自由扩散,对提高催化效率具有重要的意义。

图4 SBA-15负载前后的TEM照片:(a)SBA-15;(b)CuCo2O4/SBA-15
在液氮温度下对多孔材料进行N2吸附-脱附分析是表征多孔材料性质的有效手段,SBA-15和CuCo2O4/SBA-15的N2吸附-脱附等温线如图5所示。SBA-15和CuCo2O4/SBA-15的等温吸附曲线都是具有H1滞后环的Ⅳ型吸附曲线,在相对压强为0.5~0.8之间有明显的滞后环,这是由于吸附分子延迟凝聚的结果,说明两种材料都为介孔结构。CuCo2O4/SBA-15在相对压强为0.4~0.6之间有额外的滞后环,这是由于孔道内负载的CuCo2O4产生了类似于墨水瓶的效应,使得脱附的阻力较大,需在更低的压力下才能发生脱附。
通过DFT计算得到SBA-15和CuCo2O4/SBA-15的孔径分布曲线,如图5所示。SBA-15的孔径主要集中在6.9 nm,且分布较窄,这与XRD和TEM的结果相符。负载CuCo2O4后,孔径有所变小,主要集中5.0 nm,这说明CuCo2O4主要在SBA-15的孔内生成。同时,经过CuCo2O4负载后,孔容从0.582 cm3·g-1降低到了0.544 cm3·g-1。可以看到孔容下降幅度很小,这是由于CuCo2O4颗粒小,负载量少,使得负载催化剂仍然保持SBA-15的介孔结构。

图5 N2吸附-脱附等温线(液氮77k)及其相应的孔径分布曲线:(a)SBA-15;(b)CuCo2O4/SBA-15
另外,根据BET方程可以计算得到SBA-15和CuCo2O4/SBA-15的比表面积分别为441.3 m2/g和581.7 m2/g,负载后的催化剂比表面积有所增加,这是由于当SBA-15内有CuCo2O4负载后,在孔道内CuCo2O4也占有了部分表面积,提高了比表面积。
CuCo2O4/SBA-15的XPS谱图如图6所示。从图6(a)可以看到Cu、Co、Si和O元素的信号,表明SBA-15和CuCo2O4都存在于样品中。从图6(b)的O1s高分辨谱中,可以看到在529 eV和533 eV处出现了峰,其分别对应于SBA-15中的Si-O和CuCo2O4的晶格氧[25]。图6(c)的Cu2p高分辨谱显示,在933 eV和954 eV处出现了峰,分别对应于Cu2p3/2和Cu2p1/2[26],另外在942 eV和962 eV观察到两个强卫星峰,表明了样品中的铜处于氧化状态。在图6(d)Co2p的高分辨谱中可以看到结合能为779 eV和794 eV有两个特征峰,分别是Co3+和Co2+的特征峰[27],这说明CuCo2O4/SBA-15中含有Co3+和Co2+两种离子,且Co3+的峰比Co2+的峰面积大,即Co3+的含量比Co2+高,这与XRD表征的结果一致。

图6 CuCo2O4/SBA-15的XPS谱图:(a)XPS全谱;(b)O1s;(c)Cu2p;(d)Co2p
2.2 催化性能
以上表征结果说明所制备的CuCo2O4/SBA-15负载催化剂具有比表面积大、孔径大等特点,可以使得催化剂与反应底物接触面积大,反应物易通过。因此进一步以质量分数为30%过氧化氢溶液为氧化剂,考察苄醇的催化氧化反应特点。
从表1可以清楚地看到铜钴硝酸盐金属离子的摩尔组成比例为n(Cu):n(Co)=1∶2时催化效率最高,转化率在50%以上,而偏离这个比例的负载催化剂效果都明显较差。这是因为在CuCo2O4中,Cu和Co的摩尔比为1∶2。若前驱体中铜钴的摩尔比不满足1∶2时,会导致产生的CuCo2O4量变少,而CuO或Co2O3的催化效率较低,因此会导致总的反应效率下降。

表1 铜钴摩尔比对苄醇催化氧化转化率的影响
通过不加催化剂、添加载体和添加催化剂,考察催化剂的催化效果(表2,序号1~3)。可以看到,不加催化剂和添加SBA-15模板的催化效果都很差,反应6 h后的转化率都只有10%左右,而添加催化剂的转化率达到了60%以上。当同时考虑选择性时,含复合催化剂的反应体系的产率仍然是不含催化剂的4倍左右。这说明所制备的混合金属氧化物催化剂具有显著的催化效果。
另外,考察了反应时间对催化氧化反应的影响(表2,序号3~6)。结果表明,反应2 h后的转化率已经达到44%左右,继续延长反应时间到3 h,转化率提高到50%左右,且选择性变化不大。进一步延长反应时间,可以看到反应选择性下降,而转化率增加不是那么明显,这是由于此时反应体系中的苯甲醛浓度比较高,容易进一步被氧化成为苯甲酸。
本文进一步考察了反应温度对混合金属氧化物催化苄醇体系的影响(表2,序号6~8)。可以看到,随着温度的升高,苄醇的转化率逐渐增大,但是苯甲醛的选择性逐渐下降。这是由于温度对苯甲醇和苯甲醛的氧化反应都起着促进作用,但是对苯甲醛的催化氧化促进作用更加明显,从而导致了选择性的下降。

表2 反应温度和时间对苄醇催化氧化转化率和选择性的影响
进一步考察了混合金属氧化物负载催化剂对苄醇衍生物催化氧化反应(反应通式如图7所示)的适用性,如表3所示。可以看到,混合金属氧化物催化剂对其他4种苄醇衍生物都具有一定的催化氧化作用。当取代基为—H和—CH3时,转化率都比较高(表3,序号1~2),而当取代基为—CF3和—NO2时,转化率降为40%及以下(表3,序号3~4)。这是由于苄醇在氧化反应过程中为失电子组分,给电子基团使其苯环电子云密度升高而更容易失去电子,导致氧化反应速率增大,而吸电子基团使得苯环电子云密度下降而难以失去电子,导致氧化反应速率下降。虽然—OH为较强的给电子基团,但是对羟基苄醇的转化率最低,这可能是由于酚羟基具有一定的酸性,会对CuCo2O4有部分的破坏作用,使得催化效率大大下降。

图7 CuCo2O4/SBA-15对苄醇衍生物催化氧化反应通式
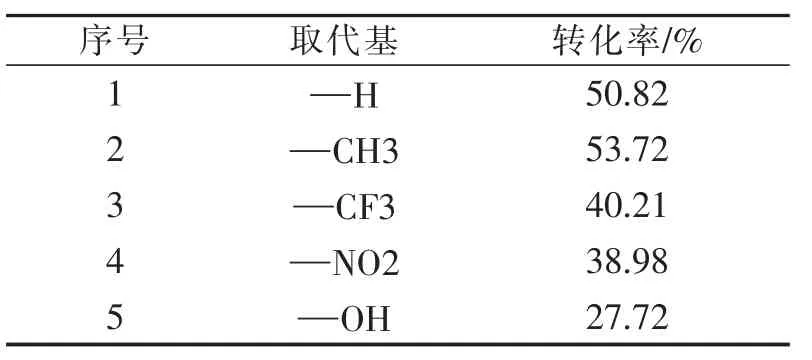
表3 不同取代基苄醇的选择性氧化(80℃下反应4 h)
3 结论
本研究通过纳米浇铸法制备出了对苄醇具有较好催化氧化效果的CuCo2O4/SBA-15负载型催化剂,主要得到以下结论:
(1)CuCo2O4/SBA-15负载型催化剂的孔径为5.0 nm左右,比表面积可达581.7 m2/g,有利于反应底物和产物的自由扩散和充分接触。
(2)该催化剂对苄醇及其衍生物具有较好的催化氧化效果,当反应温度为80℃、反应时间为4 h时,苄醇的转化率大于50%,而不含催化剂的转化率只有10.19%。
由于H2O2在金属氧化物催化剂的存在下可能会发生迅速分解,使得总体的转化率较低,后续仍然需要进一步研究H2O2和苄醇加料方式等,以进一步提高催化效果。
