液相色谱-串联质谱法测定动物源性食品中糖皮质激素类药物残留
2023-01-11黄婷谭磊何玉榆陈彤丁燕玲钟名琴
黄婷,谭磊,何玉榆,陈彤,丁燕玲,钟名琴*
(1.深圳市质量安全检验检测研究院,广东 深圳 518000;2.广东省市场监督管理局食用农产品监管重点实验室,广东 深圳 518000)
糖皮质激素(glucocorticoid,GCS) 又名“肾上腺皮质激素”,具有调节人体三大物质(糖、蛋白质、脂肪)代谢的生理作用,还能调节钾、钠和水的代谢,用来维持机体内外环境的平衡,是机体应激反应最主要的调节激素,也是临床上最常用和有效的抗炎、免疫抑制剂[1]。常见的糖皮质激素类药物主要是地塞米松、倍他米松,若人长期使用可能会出现不良反应,还可能会降低机体免疫力,人类食用后可导致机体代谢紊乱和发育异常,或潜在致癌、致畸风险[2]。目前,糖皮质激素常被用于治疗家畜的炎症反应、免疫性疾病、牛的酮病等,属于生产常用的药物。糖皮质激素的非法用途是为了增加家畜的采食量,从而达到增重的目的。因此,世界各国都制定了对于动物源性食品中各种激素的最大残留量,欧盟第96/22/EC 指令、美国食品与药品管理局、日本政府都禁止在食品源性动物中使用激素类药物[3]。我国GB31650-2019 《食品安全国家标准食品中兽药最大残留限量》规定,猪肉中地塞米松的最大残留量为1.0 μg/kg,倍他米松的最大残留量为0.75 μg/kg[4]。
目前,测定动物源性食品中糖皮质激素类药物残留的方法主要有酶联免疫法、高效液相色谱法[5]和液相色谱-串联质谱法。其中,酶联免疫法只能用于筛查,液相色谱法的检测项目比较单一,灵敏度低,耗时长,选择性和特异性差,已达不到用于痕量兽药残留分析的要求。液相色谱-串联质谱法是一种分析动物源性食品中痕量兽药残留的重要方法,具有灵敏度高、选择性和特异性好的特点,对低浓度样本有很好的检测率,还可用于测定不同基质中的糖皮质激素类药物。针对动物源性食品,常用标准的前处理过程耗时长[6],经济成本高,过程繁琐,不能满足目前对动物源性食品的高效、快速检测的需求。为加强对动物源性食品兽药的监控,有效监督我国兽药滥用质量现状,我们对糖皮质激素类药物中的地塞米松、倍他米松进行检测,前处理过程操作简单,耗时短,有机溶剂用量少,成本低,还能将两物质进行分离,且结果可靠,灵敏度高,检出限低。
1 材料与方法
1.1 样本准备
取适量新鲜猪肉组织,将其充分绞碎且均质,-20 ℃避光保存。
1.2 仪器
TQ-XS 液相色谱-串联质谱联用仪(美国Waters 公司)、多管漩涡混合仪(杭州奥盛仪器有限公司)、电子天平(感量0.01 g、感量0.000 1 g) [ 梅特勒托利多(Mettler Toledo) 集团]、3K15冷冻离心机[ 适马(Sigma)股份有限公司]、Millipor 超纯水仪、奥特赛斯AS 系列超声波清洗机、OAN-EVAP 24 型可控温的氮吹浓缩仪。
1.3 主要试剂与耗材
1.3.1 实验室用水
符合GB/T 6682《分析实验室用水规格和试验方法》规定的一级水。
1.3.2 试剂
甲醇(CH3OH)、乙腈(C2H3N)、甲酸(HCOOH)为色谱纯,购自德国默克公司。
1.3.3 乙腈水提取溶液
乙腈水提取溶液:80%乙腈水+0.2%甲酸。
甲醇水复溶液甲醇+水+甲酸(10 ∶90 ∶0.09,V/V/V)。
Waters PRIME HLB(6 cc,200 mg)固相萃取柱(美国沃特世公司);
滤膜(津腾,0.22 μm,水系);
标准物质:地塞米松、倍他米松(纯度>98%,购自德国DR 公司)。
1.4 标液配制
准确称适量的地塞米松、倍他米松的标准品,用甲醇分别配成100 μg/mL 的标准储备液,-18 ℃冰箱中保存,有效期6 个月;分别移取适量地塞米松、倍他米松标准储备液,用甲醇逐级稀释成适当浓度的地塞米松、倍他米松标准工作液,置于-18 ℃冰箱中保存。
1.5 样本前处理
准确称取试样2.00 g 于50.00 mL 离心管内,加入10.00 mL 乙腈水提取溶液,震荡摇匀30 s,超声波清洗仪超声5 min,于高速离心机8 000 r/min 离心5 min,备用。
于上述离心后提取液中移取4.00 mL 上清液过Waters PRIME HLB 固相萃取柱,保持1 滴/s 的速度。移出2.50 mL 至15 mL带刻度的离心管中。流出液在40 ℃水浴下氮气吹至少于0.50 mL。残留液用甲醇水复溶液定容至1.00 mL,震荡2 min,过0.22 μm 滤膜,供液相色谱-串联质谱仪测定。
1.6 仪器条件
1.6.1 液相色谱条件
a)色谱柱:BEH C18(100 mm×3.0 mm,1.7 μm)(美国Waters 公司);
b)流速:0.30 mL/min;
c)柱温:40 ℃;
d)进样量:2.00 μL;
e)流动相及梯度洗脱程序(表1)。
1.6.2 质谱参考条件(表2、图1、图2)
a) 离子源:电喷雾离子源(electron spray ionization,ESI);
b)扫描方式:负离子扫描;
c)检测方式:多反应离子监测(multiple reaction monitoring,MRM);
d)毛细管电压:1.00 kV;
e)离子源温度(TEM):550 ℃;
f)去溶剂气体流量:氮气,1 000 L/h;
g)碰撞气:氩气。

2 结果
2.1 标准曲线
按方法条件设置仪器参数,量取适量糖皮质激素类药物标准溶液,将其用空白基质溶液制备成浓度为0.20 ng/mL、0.50 ng/mL、1.00 ng/mL、2.00 ng/mL、5.00 ng/mL、10.00 ng/mL 的混合系列标准工作溶液进行上机测定,绘制标准曲线[7],测得地塞米松的相关系数为0.999 2,倍他米松的相关系数为0.999 6。


图1 阴性样本添加0.50 ng/mL 地塞米松离子通道色谱图

图2 阴性样本添加0.50 ng/mL 倍他米松离子通道色谱图
2.2 方法检出限测定(表3)
以空白猪肉样本为基质,添加浓度为0.50 μg/kg,按照“1.5 样本前处理”中介绍的试验方法处理和测定,平行样本7 个(n=7),根据各样本检测值计算出平均值及标准偏差。再根据公式检出限MDL=(k×Sb×C)/X(式中:k 为置信因子,一般取3),测定地塞米松、倍他米松检出限分别为0.046 4 μg/kg 和0.047 3 μg/kg。
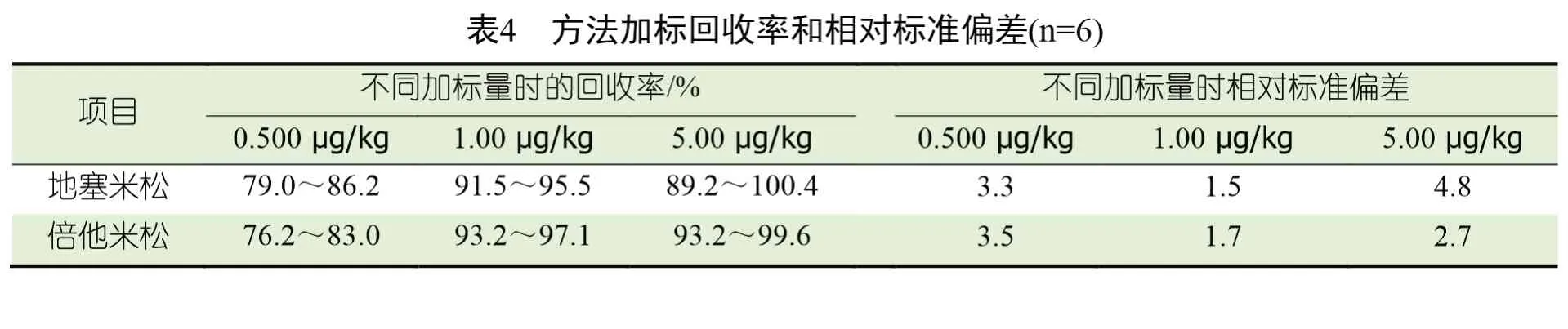
2.3 回收率及精密度确定(表4)
用空白猪肉样本进行0.50、1.00 和5.00 μg/kg,3 个水平阳性添加回收实验,每个水平取6 个平行样,按“1.6.2 质谱参考条件”处理和测定。地塞米松、倍他米松平均回收率和相对标准偏差结果见表1。3 个水平的阳性添加回收率为76.2%~100.4%,相对标准偏差为1.5%~4.8%。
3 结论
本试验建立了一种检测动物源性食品中糖皮质激素的液相色谱串联质谱的测定方法。结果表明,该方法解决了现行检测方法定性定量过程繁琐复杂、耗时长的问题,节省了人力、物力和财力,具有前处理过程简单、溶剂使用量少、稳定性好、定量准确等优点[8],能满足对动物源性食品糖皮质激素类药物进行快速定性定量检测的要求,为兽药残留防控监管提供强有力的技术支撑。