DR 联合MRI 诊断不典型肺结核球与周围型小细胞肺癌的临床价值
2023-01-11张治勤
张治勤
甘肃省第二人民医院,甘肃 兰州 730020
肺结核和肺癌是临床上常见的呼吸系统疾病。肺结核球属于肺结核的一种特殊形态,在病理上是干酪样病灶被纤维膜或类上皮肉芽组织包围形成,其发病率及死亡率较高[1]。近年免疫抑制及抗菌药物滥用,导致患者逐年递增,严重危害人们健康[2]。周围型小细胞肺癌指发生于支气管末端及肺段以下肺叶直径≤3cm的肺癌,以腺癌较常见[3]。不典型肺结核球和周围型小细胞肺癌早期发病隐匿,症状不典型,易漏诊、误诊,是临床影像学诊断的难题。数字化X 射线摄影(DR)和磁共振成像(MRI)是临床上诊断肺部疾病较常用的方法。DR 较普通X 射线摄影系统具有更高的动态范围,且在X 线透过人体后,经X 线探测器刺激和计算机系统处理可在短时间内成像,但对重叠部位检查存在局限性[4]。MRI 利用原子核共振产生的型信号进行成像,对疾病的诊断具有明显优越性,可直接对矢状面、冠状面及各种斜面进行体层成像,但MRI 禁忌证较多,对肺部疾病研究较少[5]。本研究旨为探讨DR 联合MRI诊断不典型肺结核球与周围型小细胞肺癌的临床价值。
1 对象和方法
1.1 研究对象 选择我院2018 年2 月至2020 年8月收治的不典型肺结核球患者37 例,周围型小细胞肺癌 41 例,共 78 例。其中男 51 例,女 27 例,年龄 38~71岁,平均(56.29±8.16)岁。
纳入标准:①经临床手术、穿刺活检等确诊为不典型肺结核球及周围型小细胞癌患者;②不典型肺结核球患者符合《中国结核病病理学诊断专家共识》[6]中相关诊断标准;③周围型小细胞肺癌患者符合《中华医学会肺癌临床诊疗指南(2018 版)》[7]中相关诊断标准;④患者均为初诊,无既往放化疗史。排除标准:①伴有心、肝等脏器功能严重障碍者;②对DR 及MRI检查存在禁忌证者;③DR 及MRI 图像存在伪影无法分析及诊断;④典型肺结核。
1.2 方法
1.2.1 DR 影像检查。78 例患者取站立位,采用DR 系统(南京贝登医疗股份有限公司,SONTU100-Polaris50型)检测,管电压设置为120kV,正位摄片电流320mA,侧位摄片电流400mA,自动调节时间。
1.2.2 MRI 检查。78 例患者取仰卧位、头部进入,采用磁共振扫描仪(德国西门子,Siemens Magnetom Avanto 1.5T 型)行18 通道体部高分辨扫描,扫描范围从双肺尖至膈肌水平。常规平扫冠状位T2WI 成像:HASTE TR 1000ms、TE 90ms,层厚 5.5mm、间距 1mm,层数 18,视野(FOV)360mm×320mm,激励次数 1;轴位 T1WI 成像:GRE(压脂用 SPAIR)TR 160ms,TE 4.9ms,层数 30,FOV 380mm×360mm;轴位 T2WI 成像:FSE TR 2200ms,TE 90ms。轴位弥散加权成像(DWI):EPI TR 1500ms,TE 82ms、激励次数 2,b 值为 50、800s/mm2扫描。增强扫描采用VIBE-T1WI 序列,采用高压注射器经肘静脉注射 0.2mL/kg 对比剂 Gd-DTPA,速度 2.5mL/s,15s、30s、60s、5min 进行屏气扫描,部分延迟至30min。
1.3 观察指标 由两名具有丰富经验的高年资医师分别对78 例患者DR、MRI 成像进行阅片。观察DR、MRI、DR 联合MRI 检测结果、检出率、误诊率及漏诊率进行比较。以手术病理、支气管镜活检、肺穿刺活检等检查作为临床确诊金标准。
1.4 统计学分析 采用SPSS19.0 软件进行统计学分析。计数资料用百分比表示(%),组间差异采用χ2检验,P<0.05 为差异具有统计学意义。
2 结果
2.1 不典型肺结核球、周围型小细胞肺癌病变部位不典型肺结核球患者与周围型小细胞肺癌患者病变部位差异无统计学意义(P>0.05)。见表1。
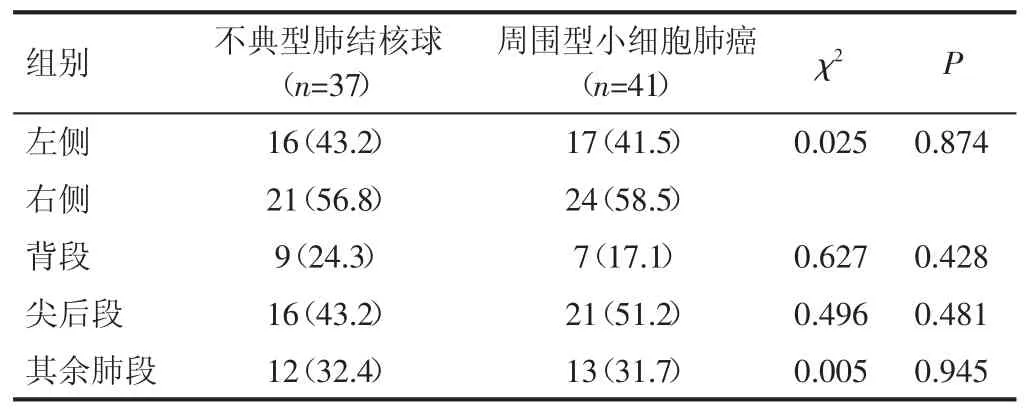
表1 不典型肺结核球、周围型小细胞肺癌病变部位[例(%)]
2.2 不典型肺结核球、周围型小细胞肺癌形态学征象不典型肺结核球患者形态学征象中胸膜凹陷、血管集束、分叶、空洞及钙化数量少于周围型小细胞肺癌患者,差异具有统计学意义(P<0.05)。见表2。
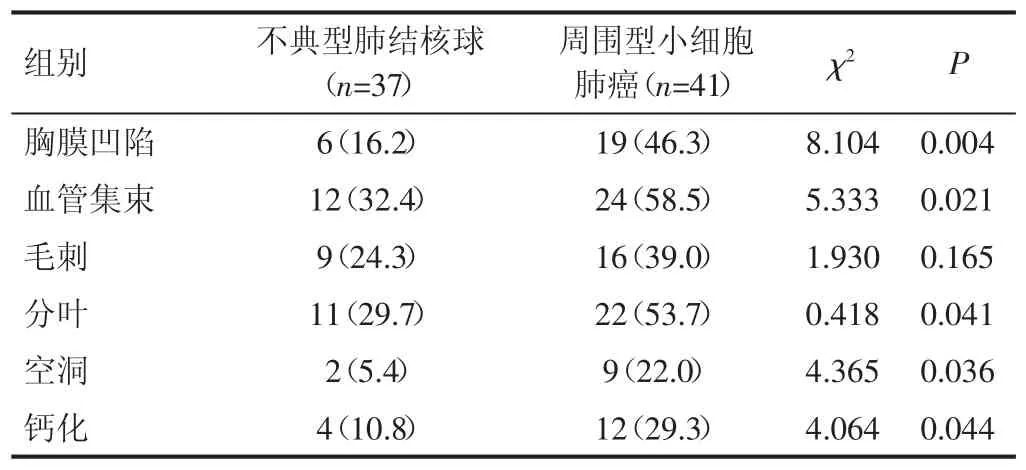
表2 不典型肺结核球、周围型小细胞肺癌形态学征象[例(%)]
2.3 不典型肺结核球、周围型小细胞肺癌检出率比较 联合组不典型肺结核球、周围型小细胞肺癌及总检出率均高于DR 组和MRI 组,差异具有统计学意义(P<0.05)。见表 3。
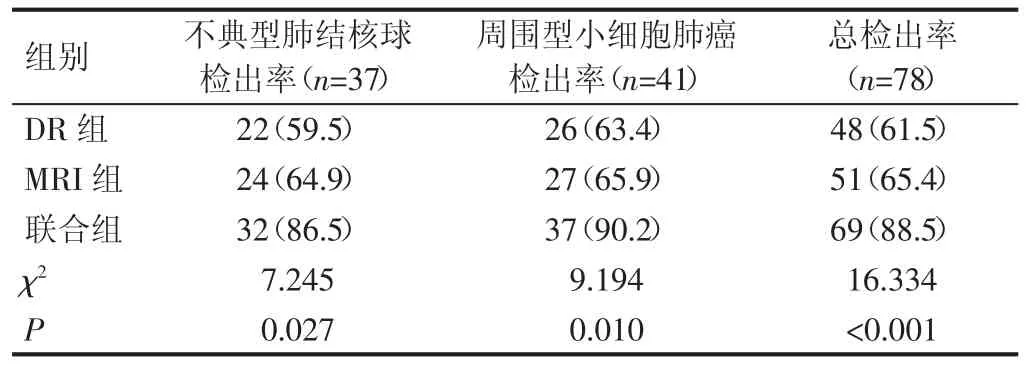
表3 不典型肺结核球、周围型小细胞肺癌检出率比较[例(%)]
2.4 漏诊、误诊率比较 本研究中DR 组漏诊6 例(7.7%)、MRI 组漏诊 5 例(6.4%)、联合组漏诊 2 例(2.6%),差异无统计学意义(P>0.05);联合组总误诊率低于DR 法和MRI 组,差异具有统计学意义(P<0.05)。见表4。

表4 三种方法的漏诊、误诊率比较[例(%),n=78]
3 讨论
肺结核属于慢性肺部感染性疾病,经呼吸道传播,由结核分枝杆菌感染引起,可引起肺部钙化和纤维化,是全球三大传染病之一,有研究显示每年约13 万人死于结核病[8-9]。肺结核球患者临床表现、发病部位等都缺少典型性,临床诊断易与肺癌、感染性病灶混淆,延误最佳救治时机[10]。肺癌在全球范围内的发病率和死亡率逐年上升,五年存活率仅为13%,是严重威胁人群生命健康的恶性肿瘤之一,其中男性肺癌患病率和死亡率居恶性肿瘤第一[11-12]。周围型小细胞肺癌是原发于肺段支气管以下肿瘤直径<3cm 肺癌。有研究显示当肺肿瘤直径>3cm 时,恶性程度和癌症因子增殖转移能力明显增强,严重影响预后[13]。不典型肺结核球及周围型小细胞肺癌临床表现均无特异性,影像形态学征象相似,易发生漏诊、误诊[10]。
本研究采用DR 和MRI 诊断不典型肺结核球及周围型小细胞肺癌,结果联合组不典型肺结核球、周围型小细胞肺癌及总检出率均高于DR 组和MRI 组,差异具有统计学意义,结果说明DR 联合MRI 诊断不典型肺结核球、周围型小细胞肺癌较单独采用DR、MRI诊断有效率更高。原因可能是DR 胸片在正侧位可完整显示胸廓及肋骨结构,对周围型肺癌侵及肋骨显示较好,而对不典型肺结核球诊断成像速度较快,且成像清晰,层次相较常规X 线摄影丰富,但仍对重叠部位存在局限性[14]。MRI 检查可弥补 DR 的不足,其具有多参数、多序列成像优势,在一定程度上可反应病理改变,提供更多特征性征象。
本研究结果显示,不典型肺结核球患者与周围型小细胞肺癌患者病变部位差异无统计学意义;不典型肺结核球患者形态学征象中胸膜凹陷、血管集束、分叶、空洞及钙化数量少于周围型小细胞肺癌患者,差异具有统计学意义。说明周围型小细胞肺癌与不典型肺结核球在发病部位、影像形态征象中相似,周围型小细胞肺癌形态征象较不典型肺结核球形态学征象更明显。形态学征象中胸膜凹陷是由于病灶内成纤维反应使与胸膜之间形成喇叭口状间隙,引起生理性液体积聚[15]。血管集束是因肺病变血管代偿性增粗导致,而边缘模糊不清或癌性因子生长速度不同影像表现为分叶征,分叶越明显提示肿瘤恶性程度越高[16-17]。不典型肺结核球毛刺是病灶炎症、纤维反应所致,在诊断过程中颗粒聚集形成不规则小簇状,而周围型小细胞肺癌患者出现毛刺影与癌症因子沿血管、肺泡浸润生长相关[18]。本研究结果显示,本研究中DR 组漏诊6例(7.7%),MRI 组漏诊 5 例(6.4%),联合组漏诊 2 例(2.6%),联合组总误诊率低于DR 组和MRI 组。其中不典型肺结核球采用DR 诊断时被误诊为肺炎4 例,周围型肺癌6 例,肺脓肿3 例,周围型小细胞肺癌被误诊为肺炎 3 例,肺结核球 4 例,错构瘤 4 例;MRI 诊断不典型肺结核球误诊肺炎3 例,周围型肺癌5 例,肺脓肿4 例,周围型小细胞肺癌被误诊为肺炎5 例,肺结核球3 例,错构瘤2 例;DR 联合MRI 诊断不典型肺结核球误诊肺炎1 例,周围型肺癌2 例,肺脓肿1 例,周围型小细胞肺癌被误诊为肺炎1 例,肺结核球1 例,错构瘤1 例。结果显示DR 联合MRI 较单独使用DR 或MRI 检测能有效降低误诊率。原因可能是DR 诊断对于小病灶或隐藏病灶成像不明显,极易被原发肺部病变掩盖,导致检出率较低,同时DR 胸片无法清晰显示病灶处肺组织,且在诊断过程中扫描时间较长,具有一定的辐射[19]。但DR 对于早期周围型小细胞肺癌患者主要表现为颗粒征、小空洞或小结节影等,且操作简单、费用低,与常规X 线诊断比较成像速度快,层次相较丰富。MRI 通过多方位、多序列扫描,可弥补DR 检查的不足,在一定程度上反映患者的病理改变。
综上所述,DR 和MRI 均可对肺部疾病做出诊断,但联合诊断具有较高的检出率,DR 是临床诊断肺部疾病的基础,而MRI 对肺结核的诊断有特殊优势,单一检查误诊率及漏诊率较高,联合诊断可互相弥补,具有较好的临床价值。除影像学检查外,应根据患者病症体征联合影像学及实验室检查等多种方式进行诊断,提高检出率。
