马钱内生真菌Exserohilum rostratum次生代谢产物研究
2023-01-10曹海燕陈科良杨晨宇刘云宝
易 诚,曹海燕,陈科良,杨晨宇,刘云宝
马钱内生真菌Exserohilum rostratum次生代谢产物研究
易 诚,曹海燕,陈科良,杨晨宇,刘云宝*
中国医学科学院 北京协和医学院 药物研究所 天然药物活性物质与功能国家重点实验室,北京 100050
对有毒植物马钱内生真菌的次生代谢产物进行研究。通过硅胶柱色谱及反相HPLC等多种色谱分离方法进行分离纯化,运用高分辨质谱、核磁共振波谱、红外、紫外及圆二色谱等分析方法对所分离的化合物进行结构鉴定。采用Griess法对化合物进行抗炎活性测试。从有毒植物马钱内生真菌的发酵产物中分离得到6个化合物,分别鉴定为exserone A(1)、(3,4)-4,8-二羟基-3-[()-2-羟基戊基]-6,7-二甲氧基异色满-1-酮(2)、(+)-monocerin(3)、11-hydroxymonocerin(4)、5-丁基-6-(羟甲基)-4-甲氧基-2-吡喃酮(5)和setophapyrone B(6)。化合物1为新的聚酮类化合物,命名为突蠕孢酮。化合物3具有潜在的抗炎活性。
马钱;内生真菌;次生代谢产物;抗炎;突蠕孢酮;(+)-monocerin;5-丁基-6-(羟甲基)-4-甲氧基-2-吡喃酮
植物内生真菌广泛存在于健康植物的各种组织和器官内部。在长期的与宿主植物协同进化过程中,内生真菌会产生结构多样和生物活性良好的次生代谢产物[1-3]。马钱科植物马钱L是一种乔木植物,全株均有毒性,广泛分布于南亚及东南亚地区,在我国云南、广东及海南等地有引种栽培,其种子马钱子为我国传统中药,始载于《本草纲目》,性寒味苦,归肝、脾经,具有通络止痛、散结消肿的功效。现代研究表明,马钱种子、根皮、茎皮和叶中均含有吲哚类生物碱,其中主要有毒成分是士的宁和马钱子碱[4-6]。马钱植株体内特征性的活性成分,为其内生真菌提供了独特的生长环境,然而尚未有对其内生真菌次生代谢产物的报道。本研究针对新鲜马钱叶片进行内生真菌分离,获得一株突脐蠕孢属真菌。国内外研究者从该属真菌的次生代谢产物中发现了一系列具有抗菌活性的聚酮及生物碱类化合物[7-8]。本研究对该株真菌的次生代谢产物进行了系统研究,从其95%乙醇提取物中分离鉴定了6个聚酮类化合物(图1),分别鉴定为exserone A(1)、(3,4)-4,8-二羟基-3-[()-2-羟基戊基]-6,7-二甲氧基异色满-1-酮((3,4)-4,8-dihydroxy-3-[()-2-hydroxypentyl]- 6,7-dimetho-xyisochroman-1-one,2)、(+)-monocerin(3)、11-hydroxymonocerin(4)、5-丁基-6-(羟甲基)-4-甲氧基-2-吡喃酮[5-butyl-6-(hydroxymethyl)-4- methoxy-2-pyran-2-one,5] 和setophapyrone B(6)。其中化合物1为新化合物,命名为突蠕孢酮。

图1 化合物1~6的结构
1 仪器与材料
安捷伦6205 Q-TOF高分辨质谱仪;Nicolet 5700 FT-IR红外光谱仪;Rudolph Autopol V旋光仪;JASCO J-810圆二色谱仪;安捷伦DD2-500或布鲁克 AVⅢHD-600及700核磁共振光谱仪;安捷伦HP1100型高效液相色谱仪;岛津LC-6AD 制备液相,SPD-20A紫外检测器;OSB-2200型旋转蒸发仪(日本EYELA公司);Sartorious GL124-1SCN型万分之一电子分析天平(北京赛多利斯仪器有限公司);YMC-Pack ODS-A型(250 mm×10 mm,5μm)半制备柱;大赛璐 CHIRAPAK AD-H型(250 mm×10 mm,5μm)半制备柱;硅胶(200~300目)、硅胶GF254预制板(青岛海洋化工集团公司);色谱甲醇、色谱乙腈(Mreda公司);姜黄素(上海麦克林生化科技股份有限公司,批号c12811019);其他试剂若无特别说明的均购于北京通广精细化工公司,级别为分析纯。
2 方法
2.1 菌种来源
新鲜的马钱叶片采自广西省,叶片经广西中医药大学韦松基教授鉴定为马钱科植物马钱L.,样品标本(S2506)现保存于北京协和学院药物研究所植物标本室。
菌株12-1-2是从马钱L.健康叶片中分离获得的一株内生真菌。根据形态学特征以及ITS序列同源对比鉴定该菌株为突脐蠕孢属真菌。该菌株现保存于中国医学科学院、北京协和医学院药物研究所刘云宝课题组。
2.2 提取和分离
将菌种转接至PDA培养基中,28 ℃下培养5 d,再将其接种于PDB培养基中于28 ℃下培养、7 d作为种子液。将其转接于1 L的三角烧瓶中(每瓶中含100 g大米、100 mL水;高压蒸汽灭菌15 min,共3瓶),置于室温下培养30 d。室温下用3倍量95%乙醇对发酵好的菌丝体超声提取3次,每次30 min,滤过后进行减压浓缩,回收溶剂至无醇味,共得到20.1 g浸膏。将所得浸膏用5倍量水分散,经醋酸乙酯反复萃取3次,得到醋酸乙酯部位粗膏3.7 g。采用硅胶色谱柱对醋酸乙酯部位样品进行分离,以二氯甲烷-甲醇(200∶1、150∶1、100∶1、75∶1、50∶1、25∶1、15∶1、10∶1、5∶1、2∶1、1∶1、0∶1)作为洗脱剂进行梯度洗脱得12个流分(每个洗脱体积1000 mL),以薄层色谱进行检识,合并流分得到8个不同极性组分(Fr. 1~8)。Fr. 6(930.3 mg)经制备液相色谱(C18半制备柱,流动相45%乙腈-55%水)纯化,得到化合物1(R=17.6 min,1.5 mg)和2(R=30.5 min,643.3 mg)。Fr. 7(140.8 mg)经制备液相色谱(C18半制备柱,流动相30%乙腈-70%水)分离,得到化合物3(R=21.2,4.2 mg)。Fr. 8(180.6 mg)经制备液相色谱(C18半制备柱,流动相20%乙腈-80%水)分离,得到化合物4(R=53.4 min,1.3 mg)、5(R=64.3 min,5.4 mg)和6(R=74.4 min,10.4 mg)。
2.3 体外抗炎活性测试
根据文献报道方法[9]进行体外抗炎活性测试,首先细胞按2×105/孔接种于96孔板中,每孔100 μL,贴壁4 h后,加入50 μL的10 μmol/L的目标化合物(对照孔或模型孔中加入等体积的培养基)孵育2 h,再加入50 μL终质量浓度为10 g/L的脂多糖(lipopolysaccharide,LPS)诱导(对照孔中加入等体积培养基)24 h,Griess法测定上清中NO2−的含量,用以反映NO水平。姜黄素(终浓度为200 μmol/L)作为阳性对照药物。
3 结果
3.1 结构鉴定

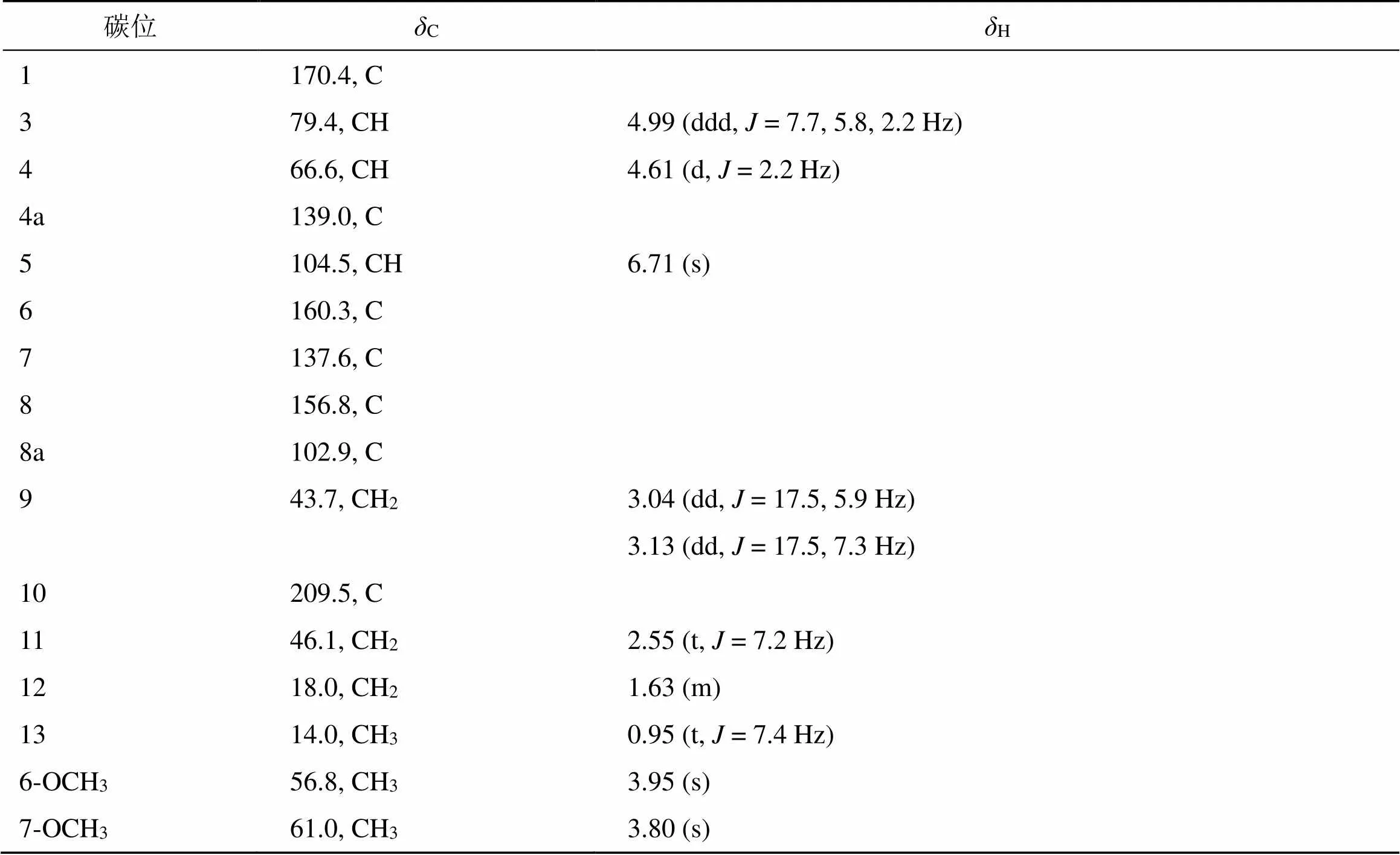
表1 化合物1的1H- 及13C-NMR数据(700/175 MHz Methanol-d4)
根据高分辨质谱,确定化合物1的分子式为C16H20O7,含有7个不饱和度。化合物1的IR谱显示化合物1的结构中存在羟基(3 362.3 cm−1)、羰基(1 715.1 cm−1)和苯环(1 668.6 cm−1)。1H-NMR和13C-NMR数据显示化合物1含有1个酮羰基,1个酯羰基,6个芳香碳,2个连氧次甲基,3个亚甲基,2个甲氧基,1个甲基(表1);1H-NMR数据H6.71 (1H, s) 和13C-NMR数据C137.6, 104.5, 160.3, 139.0, 156.8, 102.9 表明化合物1中存在1个五取代的苯环;结合13C-NMR和HSQC谱分析可知,碳谱中共有16个碳信号,包括1组五取代苯碳信号C160.3 (C-6), 156.8 (C-8), 139.0 (C-7), 137.6 (C-4a), 104.5 (C-5), 102.9 (C-8a);1个酯碳基碳信号C170.4 (C-1);1个羰基碳信号C209.5 (C-10);1个甲基碳信号C14.0 (C-13);3个亚甲基碳信号C43.7 (C-9), 46.1 (C-11), 18.0 (C-12);2个次甲基碳信号C79.4 (C-3), 66.6 (C-4)。结合上述数据推断该化合物为monocerin[11]类衍生物;由1H-1H COSY和HSQC图谱可推断结构中含有α(H2-11/H2-12/H3-13)和β(H-4/H-3/H2-9)2个自旋系统(图2);由H-3与C-1/C-4/C-4a以及H-5与C-1的HMBC相关信号推测结构中的吡喃酮环和苯环通过C-4a和C-8a骈合。根据已鉴定的2个自旋系统α和β,以及H2-9、H2-11、H2-12和C-10的HMBC信号,确定了C-9/C-3的结构片段;通过H2-9和C-3、C-4的HMBC信号,确定C-9/C-13片段通过C-3与吡喃酮环连接;通过6-OCH3和C-6、7-OCH3和C-7的HMBC信号与6-OCH3和H-5的NOE效应分别确定了2个甲氧基的连接位置(图3)。因此,化合物1的平面结构鉴定为4,8-dihydroxy-6,7-dimethoxy-3-(2-oxopentyl) isochroman-1-one。通过H-3和H-4的偶合常数(= 2.2 Hz)可以确定H-3和H-4的相对构型为[10]。化合物1的绝对构型通过计算ECD确定,将化合物1的其中一种构型(3,4) 的计算ECD谱图与实验测得的CD谱图相比对,两者具有一致的Cotton效应(图4)。因此,化合物1的结构确定为 (3,4)-4,8-二羟基-6,7-二甲氧基-3-(2-氧代戊基) 异色满-1-酮,命名为突蠕孢酮。
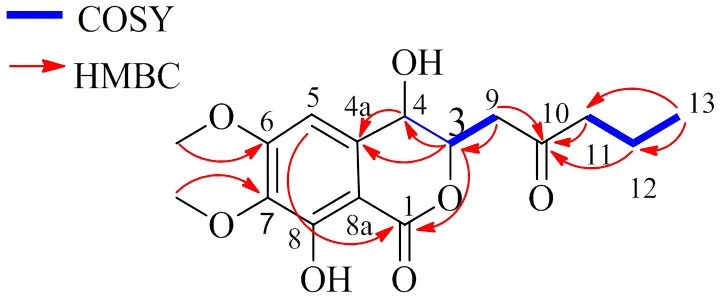
图2 化合物1的主要1H-1H COSY和HMBC相关信号

图3 化合物1的主要ROESY相关信号
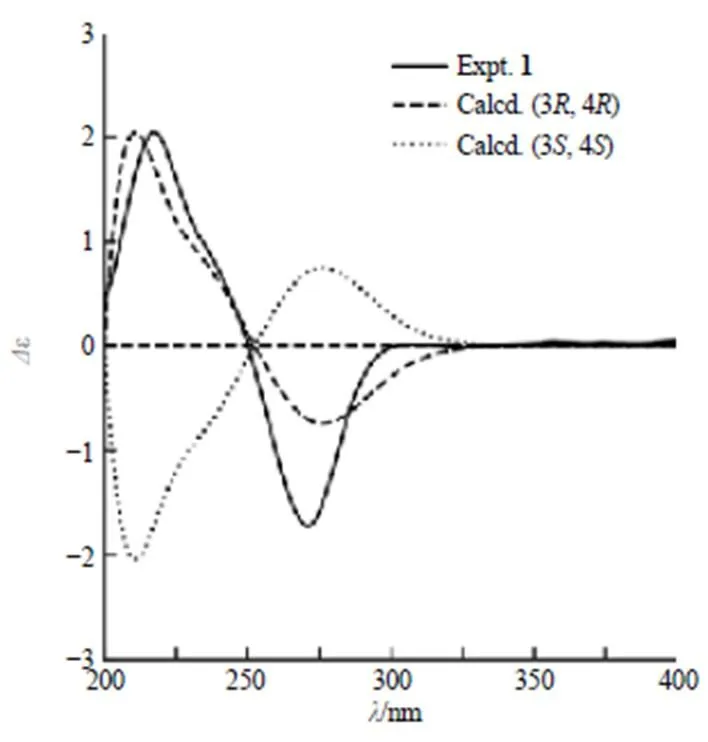
图4 化合物1的实验ECD谱图及其计算ECD谱图
化合物2:无色油状物。[α]20 D−8.62(0.25,CH3OH)。HR-ESI-MS327.143 6 [M+H]+(计算值C16H23O7,327.143 8)。1H-NMR (600 MHz, CDCl3): 11.05 (1H, s, 8-OH), 6.56 (1H, s, H-5), 4.73 (1H, ddd,= 8.0, 5.4, 2.2 Hz, H-3), 4.65 (1H, m, H-4), 3.97 (1H, m, H-10), 3.93 (3H, s, 6-OCH3), 3.87 (3H, s, 7-OCH3), 3.13 (1H, d,= 6.0 Hz, 4-OH), 2.59 (1H, d,= 2.3 Hz, 10-OH), 2.16 (1H, ddd,= 14.6, 8.3, 1.9 Hz, H-9β), 1.86 (m, 1H, H-9α), 1.54 (2H, m, H-11), 1.47 (1H, m, H-12β), 1.39 (1H, dddd,= 15.7, 10.5, 7.3, 5.2 Hz, H-12α), 0.95 (3H, t,= 7.1 Hz, H-13);13C-NMR (150 MHz, CDCl3): 169.0 (C, C-1), 158.9 (C, C-8), 156.1(C, C-6), 136.8 (C, C-7), 136.6 (C, C-4a), 102.9 (CH, C-5), 102.0 (C, C-8a), 79.6 (CH, C-3), 67.8 (CH, C-10), 67.0 (CH, C-4), 60.9 (CH3, 7-OCH3), 56.4 (CH3, 6-OCH3), 40.6 (CH2, C-9), 37.7 (CH2, C-11), 18.8 (CH2, C-12), 14.1 (CH3, C-13)。以上数据与文献报道数据基本一致[10],确定化合物2为(3,4)-4,8-dihydroxy-3-[()-2-hydroxypentyl]- 6,7-dimethoxyisochroman-1-one。
化合物3:无色油状物。[α]20 D+43.25(0.25, MeOH)。HR-ESI-MS309.132 2 [M+H]+(计算值C16H21O6,309.133 2)。1H-NMR (500 MHz, CD3OD): 6.75 (1H, s, H-5), 5.05 (1H, m, H-3), 4.60 (1H, d,= 2.9 Hz, H-4), 4.10 (1H, ddt,= 8.7, 7.2, 5.6 Hz, H-10), 3.92 (3H, s, 6-OCH3), 3.79 (3H, s, 7-OCH3), 2.62 (1H, ddd,= 14.6, 8.7, 6.0 Hz, H-9β), 2.01 (1H, ddd,= 14.4, 5.6, 1.0 Hz, H-9α), 1.55 (2H, m, H-11), 1.35 (2H, m, H-12), 0.89 (3H, t,= 7.3 Hz, H-13);13C-NMR (125 MHz, CD3OD): 169.5 (C, C-1), 160.2 (C, C-6), 156.9 (C, C-8), 138.1 (C, C-7), 133.4 (C, C-4a), 106.1 (CH, C-5), 103.0 (C, C-8a), 83.1 (CH, C-3), 79.8 (CH, C-10), 75.7 (CH, C-4), 61.0 (CH3, 7-OCH3), 56.9 (CH3, 6-OCH3), 40.0 (CH2, C-9), 39.5 (CH2, C-11), 20.2 (CH2, C-12), 14.3 (CH3, C-13)。以上数据与文献数据基本一致[11],确定化合物3为(+)-monocerin。
化合物4:无色油状物。[α]20 D+26.45(0.05,CH3OH)。HR-ESI-MS/325.128 1 [M+H]+(计算值C16H21O7,325.128 1)。1H-NMR (500 MHz, CDCl3): 11.31 (1H, s, 8-OH), 6.62 (1H, s, H-5), 5.12 (1H, ddd,= 6.0, 3.3, 1.7 Hz, H-3), 4.62 (1H, d,= 3.3 Hz, H-4), 4.10 (1H, m, H-10), 3.98 (3H, s, 6-OCH3), 3.93 (3H, s, 7-OCH3), 3.74 (1H, dq,= 8.0, 4.0 Hz, H-11), 2.52 (2H, m, H-9), 1.80 (1H, d,= 3.5 Hz, 11-OH), 1.55 (1H, m, H-12β), 1.45 (1H, ddq,= 14.5, 8.6, 7.4 Hz, H-12α), 1.01 (3H, t,= 7.4 Hz, H-13);13C-NMR (125 MHz, CDCl3): 167.6 (C, C-1), 158.8 (C, C-6), 156.3 (C, C-8), 137.4 (C, C-7), 130.6 (C, C-4a), 104.3 (CH, C-5), 102.1 (C, C-8a), 81.5 (CH, C-3), 80.7 (CH, C-10), 74.6 (CH, C-4), 73.0 (CH, C-11), 60.8 (CH3, 7-OCH3), 56.3 (CH3, 6-OCH3), 33.8 (CH2, C-9), 26.0 (CH2, C-12), 10.1 (CH3, C-13)。以上数据与文献数据基本一致[12],确定化合物4为exserolide E。
化合物5:棕色无定形粉末。HR-ESI-MS/213.112 1 [M+H]+(计算值C11H17O4,213.112 1)。1H-NMR (600 MHz, CD3OD): 5.63 (1H, s, H-3), 4.37 (2H, d,= 1.2 Hz, H-11), 3.88 (3H, s, 4-OCH3), 2.43 (2H, dd,= 8.6, 6.9 Hz, H-7), 1.42 (2H, m, H-8), 1.35 (2H, m, H-9), 0.92 (3H, t,= 7.3 Hz, H-10);13C- NMR (150 MHz, CD3OD): 173.0 (C, C-4), 166.9 (C, C-2), 160.0 (C, C-6), 115.1 (C, C-5), 89.9 (CH, C-3), 59.2 (CH2, C-11), 57.3 (CH3, 4-OCH3), 33.3 (CH2, C-8), 24.2 (CH2, C-7), 23.6 (CH2, C-9), 14.2 (CH3, C-10)。以上数据与文献数据基本一致[13],确定化合物5为5-butyl-6-(hydroxymethyl)-4-methoxy-2- pyran-2-one。
化合物6:棕色无定形粉末。[α]20 D+2.28(0.05,CH3OH)。经手性柱色谱分析,确定化合物6为一对对映异构体。拆分后,分别测得旋光值为:9-(+)-setosphapyrone B(5.4 mg):[α]20 D+7.2 (0.05, MeOH);9-(−)-setosphapyrone B(3.9 mg):[α]20 D−9.6 (0.05, MeOH)。HR-ESI-MS/213.112 0 [M+H]+(计算值C11H17O4,213.112 1)。1H-NMR (600 MHz, CD3OD): 5.56 (1H, s, H-3), 3.87 (3H, s, 4-OCH3), 3.70 (1H, ddd,= 7.8, 6.2, 4.6 Hz, H-9), 2.52 (1H, ddd,= 13.9, 10.1, 5.6 Hz, H-7β), 2.40 (1H, ddd,= 13.9, 10.0, 6.4 Hz, H-7α), 2.26 (3H, s, H-11), 1.51 (2H, m, H-8), 1.17 (3H, d,= 6.2 Hz, H-10);13C-NMR (150 MHz, CD3OD): 173.3 (C, C-4), 167.4 (C, C-2), 159.9 (C, C-6), 113.3 (C, C-5), 88.4 (CH, C-3), 68.0 (CH, C-9), 57.1 (CH3, 4-OCH3), 39.1 (C, C-8), 23.6 (CH3, C-10), 21.6 (CH2, C-7), 17.1 (CH3, C-11)。以上数据与文献数据比对基本一致[14],确定化合物6为setophapyrone B。
3.2 药理活性
对上述6个化合物进行体外抗炎活性测试,显示化合物3在10 μmol/L的浓度下,对LPS诱导的RAW 264.7细胞的NO生成抑制率为66.9%。其余各化合物均无显著抑制作用,抑制率均低于5%。
4 讨论
近年来,植物内生真菌研究已成为天然产物领域的一大热点,国内外研究者已从植物内生真菌中发现了一系列活性良好[15-17]、骨架新颖[18-19]的次生代谢产物。本研究综合利用多种分离技术从有毒植物马钱内生真菌中分离鉴定了6个聚酮类化合物,其中1为新化合物。活性测定结果表明化合物3具有一定抗炎活性。以上研究结果在一定程度上丰富了植物内生真菌次生代谢产物的化学结构和活性的多样性。
利益冲突 所有作者均声明不存在利益冲突
[1] Strobel G, Daisy B, Castillo U,. Natural products from endophytic microorganisms [J]., 2004, 67(2): 257-268.
[2] Cao H Y, Yi C, Sun S F,. Anti-inflammatory dimeric tetrahydroxanthones from an endophytic[J]., 2022, 85(1): 148-161.
[3] Yang H X, Ai H L, Feng T,. Trichothecrotocins A-C, antiphytopathogenic agents from potato endophytic fungus[J]., 2018, 20(24): 8069-8072.
[4] 宝乐尔, 毕力格, 孟香花, 等. 马钱子研究进展 [J]. 中国民族医药杂志, 2021, 27(8): 41-45.
[5] 吴小娟, 马凤森, 郑高利, 等. 马钱子吲哚类生物碱毒性研究进展 [J]. 中药药理与临床, 2016, 32(6): 231-235.
[6] 贾旋旋, 李文, 李俊松, 等. 马钱子的毒性研究进展 [J]. 中国中药杂志, 2009, 34(18): 2396-2399.
[7] Sappapan R, Sommit D, Ngamrojanavanich N,. 11-Hydroxymonocerin from the plant endophytic fungus[J]., 2008, 71(9): 1657-1659.
[8] Tan R X, Jensen P R, Williams P G,. Isolation and structure assignments of rostratins A-D, cytotoxic disulfides produced by the marine-derived fungus[J]., 2004, 67(8): 1374-1382.
[9] 李晓红, 齐云, 蔡润兰, 等. 芦荟大黄素对LPS诱导的RAW264.7细胞NO生成及iNOS表达的影响 [J]. 中国药理学通报, 2010, 26(4): 488-492.
[10] Zhang W, Krohn K, Draeger S,. Bioactive isocoumarins isolated from the endophytic fungus[J]., 2008, 71(6): 1078-1081.
[11] Ghosh A K, Lee D S. Enantioselective total synthesis of (+)-monocerin, a dihydroisocoumarin derivative with potent antimalarial properties [J]., 2019, 84(10): 6191-6198.
[12] Li R X, Chen S X, Niu S B,. Exserolides A-F, new isocoumarin derivatives from the plant endophytic fungussp [J]., 2014, 96: 88-94.
[13] Metwaly A M, Fronczek F R, Ma G Y,. Antileukemic α-pyrone derivatives from the endophytic fungus[J]., 2014, 55(24): 3478-3481.
[14] Pang X Y, Lin X P, Yang J,. Spiro-phthalides and isocoumarins isolated from the marine-sponge-derived fungussp. SCSIO41009 [J]., 2018, 81(8): 1860-1868.
[15] Yin G P, Gong M, Xue G M,. Penispidins A-C, aromatic sesquiterpenoids fromand their inhibitory effects on hepatic lipid accumulation [J]., 2021, 84(10): 2623-2629.
[16] Zhang W G, Lu X X, Huo L Q,. Sesquiterpenes and steroids from an endophytic[J]., 2021, 84(6): 1715-1724.
[17] Daley S K, Cordell G A. Biologically significant and recently isolated alkaloids from endophytic fungi [J]., 2021, 84(3): 871-897.
[18] Song B, Li L Y, Shang H,. Trematosphones A and B, two unique dimeric structures from the desert plant endophytic fungus[J]., 2019, 21(7): 2139-2142.
[19] Yan B C, Wang W G, Hu D B,. Phomopchalasins A and B, two cytochalasans with polycyclic-fused skeletons from the endophytic fungus. shj2 [J]., 2016, 18(5): 1108-1111.
Investigation on secondary metabolites of endophytic fungushosted in
YI Cheng, CAO Hai-yan, CHEN Ke-liang, YANG Chen-yu, LIU Yun-bao
State Key Laboratory of Bioactive Substance and Function of Natural Medicines, Institute of Materia Medica, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 100050, China
To study secondary metabolites of endophytic fungushosted ineparation and purification were carried out by various chromatographic separation methods such as silica gel column chromatography and HPLC.The structures of the isolated compounds were identified byHR-ESI-MSNMR,IR, UV, and ECDThe compounds were tested for their anti-inflammatory activity by the Griess method.Six compounds, exserone A (1), (3,4)-4,8-dihydroxy-3-(()-2-hydroxypentyl)-6,7-dimetho-xyisochroman-1-one (2), (+)-monocerin (3), 11-hydroxymonocerin (4), 5-butyl-6-(hydroxymethyl)-4-methoxy-2-pyran-2-one (5) and setophapyrone B (6), were isolated from the fermentation products of endophytic fungus.Compound 1 is a new polyketide and named exserone A. Compound 3 has potential anti-inflammatory activity.
L; endophytic fungus; secondary metabolites; anti-inflammation; exserone A; (+)-monocerin; 5-butyl-6-(hydroxymethyl)-4-methoxy-2-pyran-2-one
R284.1
A
0253 - 2670(2023)01 - 0035 - 06
10.7501/j.issn.0253-2670.2023.01.005
2022-10-11
中国医学科学院医学与健康科技创新工程项目(CIFMS-2022-I2M-JB-009)
易 诚,中国医学科学院药物研究所硕士研究生。E-mail: yicheng@imm.ac.cn
通信作者:刘云宝,博士,研究员,研究方向为特殊生境微生物中新颖结构活性分子的发现及其形成机制研究。Tel: (010)83162679 E-mail: liuyunbao@imm.ac.cn
[责任编辑 王文倩]
