SlCOMT1基因克隆及在番茄组织器官中的表达和褪黑素生物合成变化
2023-01-10叶欣悦闫见敏杨雪莲李云洲
叶欣悦, 闫见敏,2, 杨雪莲, 李云洲,2, 须 文,2
(1.贵州大学农学院,贵州贵阳 550025; 2.贵州大学蔬菜研究院,贵州贵阳 550025)
褪黑素(melatonin)化学名为N-乙酰基-5-甲氧基色胺(N-acetyl-5-methoxytryptamine),分子式为C13H16N2O2,相对分子质量为232.27,是一种高度保守的小分子色氨酸吲哚类衍生化合物。由褪黑素及其代谢产物组成的持续性清除活性氧(ROS)或活性氮(RNS)的过程被称为自由基清除级联(free radical scavenging cascade)[1]。据估计,通过这种自由基级联清除,1分子的褪黑素可以清除多达10个ROS或RNS分子,这使得褪黑素能够在较低的剂量下也能够有效保护生物免受氧化应激[2-3]。研究表明,外源褪黑素的应用可以减缓不同非生物胁迫诱导的衰老,因此也被称为植物非生物胁迫的通用调节剂[4-6]。除此之外,褪黑素还作为一种多功能信号分子,参与植物昼夜节律[7]、外植体生长、开花[8]和种子萌发[9]等生理过程。
近年来,植物褪黑素合成途径已被阐明。植物褪黑素的合成主要由6种不同的酶参与,包括色氨酸脱羧酶(tryptophan decarboxylase,简称TDC)、色氨酸羟化酶(tryptophan hydroxylase,简称TPH)、色胺5-羟化酶(tryptamine 5-hydroxylase,简称T5H)、血清素N-乙酰基转移酶(serotoninN-acetyltransferase,简称SNAT)、乙酰5-羟色胺甲基转移酶(acetylserotonin methyl transferase,简称ASMT)、咖啡酸-O-甲基转移酶 (caffeic acidO-methyltransferase,简称COMT)[8]。根据Byeon 等的研究[10],COMT与ASMT同属于O-甲基转移酶家族,能够甲基化苯丙烷类化合物、黄酮类化合物和生物碱,而能够甲基化N-乙酰血清素的COMT则被重新命名为COMT1。过表达番茄咖啡酸-O-甲基转移酶基因(SlCOMT1)提高了番茄内源褪黑素的含量,并通过提高抗坏血酸(ASA)-谷胱甘肽(GSH)循环减轻多菌灵带来的药害[11]。而通过病毒诱导的基因沉默(VIGS)技术沉默SlCOMT1基因减少了内源褪黑素的含量,并加剧了番茄在高温胁迫下诱导的衰老[12]。
番茄(Solanumlycopersicum)是我国重要的经济作物,同时也是茄科的模式作物。Micro-Tom作为一种小型栽培品种具有株型小和生长周期短等特点,被广泛用作番茄研究的模式作物[13]。目前,关于SlCOMT1基因的研究主要集中在番茄栽培变种Ailsa Craig中[14]。本试验以研究较少的番茄品种Micro-Tom作为试验材料,通过设计特异性引物,克隆SlCOMT1基因。利用qRT-PCR技术和酶联免疫法探讨SlCOMT1基因在不同组织器官、不同生育时期的表达模式和褪黑素含量变化,以期为深入研究SlCOMT1基因的功能以及番茄的抗逆育种和栽培提供借鉴和参考。
1 材料与方法
1.1 番茄幼苗的培养
2021年9月,于贵州大学农学院园艺系实验室将番茄(Lycopersiconesculentumvar. Micro-Tom)种子经过50 ℃的无菌水温汤浸种10 min后,在恒温25 ℃的黑暗条件下进行催芽。2 d后将萌发的种子置入装满基质的50穴穴盘中,并置入培养室中进行培养,2叶1心后将番茄幼苗移栽至10 cm宽的圆形营养钵中,并置于贵州大学农学院园艺系温室中,每5 d施用1次霍格兰德营养液,培养室温度为恒定25 ℃,光暗周期为16 h/8 h。
1.2 样品的取样分析
分别取4叶1心番茄幼苗的同一叶位的幼叶、成熟叶和衰老叶为待测叶片样品;在花期分别取花苞、正在开放的花和开放后5 d衰老的花为待测花样品;在结果期分别取绿熟期、破色期、红熟期的番茄果实为待测果实样品。所有样品从正常生长的番茄植株上取下后迅速用液氮速冻后置于-80 ℃超低温冰箱中保存备用。
1.3 番茄总RNA提取及逆转录
使用RNA提取试剂盒(DP432,北京天根)对番茄样品进行总RNA的提取,通过1%琼脂糖凝胶电泳确定RNA质量。使用cDNA第一链合成试剂盒(KR118,北京天根)完成RNA的逆转录。获得的cDNA保存在-20 ℃的冰箱中待用。
1.4 SlCOMT1基因的克隆
从番茄基因组数据库(https://solgenomics.net/)中获得SlCOMT1基因(Solyc03g080180)的蛋白质编码区(CDS)序列,通过Primer 5.0设计全长引物并使用Primer-BLAST进行检测引物特异性后交由生工生物工程(上海)股份有限公司合成。以番茄叶片cDNA为模板,在BIO-RAD T100 Thermal Cycler平台进行RT-PCR克隆SlCOMT1基因序列,反应总体系为20 μL,其中cDNA 2 μL,正、反引物各 0.5 μL,2×TaqPCR 10 μL,ddH2O 7 μL;PCR反应程序:94 ℃ 预变性3 min;94 ℃ 30 s,56 ℃ 30 s,72 ℃ 5 min,共35个循环;72 ℃ 延伸5 min。PCR产物经1.2%琼脂糖凝胶电泳分离,回收所需的条带并连接到pMD18-T克隆载体上交由北京擎科生物科技有限公司进行测序。SlCOMT1基因克隆所使用的引物见表1。
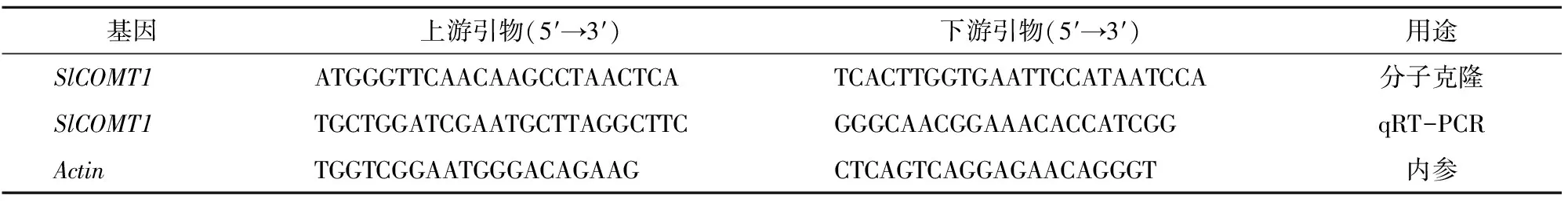
表1 本研究中使用的引物
1.5 SlCOMT1蛋白的生物信息学分析
通过番茄基因组数据库(https://solgenomics.net/)获得SlCOMT1(Solyc03g080180.2.1)编码的碱基序列和氨基酸序列;使用NCBI中的Batch CD-Search(https://www.ncbi.nlm.nih.gov/)搜索COMT1蛋白质保守结构域,拟南芥和西瓜的COMT1蛋白序列分别参考Byeon[10]、Chang等的序列[15],经过MUSLE多序列比对后使用Tbtools MSA trimmer修剪后进行可视化;使用ExPASy(https://web.expasy.org/)分析SlCOMT1蛋白的理化性质;使用TMHMM 2.0(https://services.healthtech.dtu.dk/)预测SlCOMT1蛋白的跨膜区域;使用NCBI的Protein BLAST工具寻找同源蛋白序列,通过ClustalW进行多序列比对后使用MEGA(V.10.2.6) 采用邻接法(Neighbor-Joining)构建系统发育树(bootstrap=1 000);使用Plant-mPloc(http://www.csbio.sjtu.edu.cn/)预测亚细胞定位;用SOPMA(https://npsa-prabi.ibcp.fr/)和SWISS-MODEL(https://swissmodel.expasy.org/)预测SlCOMT1的二级及三级结构。
1.6 番茄内源性褪黑素含量的检测
分别精确称取0.3 g番茄各组织样品,添加 3 mL 磷酸缓冲溶液,在冰上研磨成匀浆,3 000 r/min 离心10 min取上清液。按照植物褪黑素(MT)ELISA试剂盒(深圳子科生物科技有限公司)说明书上的方法检测褪黑素含量,在多功能酶标仪Multiskan FC(赛默飞世尔科技公司)测定 450 nm 波长下上清反应液的吸光度,计算不同组织中内源性褪黑素的含量,每个组织部位含3次生物学重复。结果通过DPS软件采用最小显著性差异(LSD)法检验不同组织内源性褪黑素含量的差异显著性(α=0.05)。
1.7 SlCOMT1基因的表达模式分析
用qRT-PCR检测SlCOMT1基因在不同组织的表达情况。以Actin(Solyc03g078400)为内参基因,用SYBR-Green染料在FQD-96A(BIOER,杭州)平台进行qRT-PCR。体系及步骤参照周露等的方法[16],用2-ΔΔCT法计算相对表达倍数。每个处理3次生物学重复,每次生物学重复3次技术重复。结果通过DPS软件用LSD法检验不同组织或处理间SlCOMT1基因相对表达量的差异显著性(α=0.05)。
2 结果与分析
2.1 SlCOMT1基因克隆及序列分析
为了从番茄中获得SlCOMT1基因,以成熟Micro-Tom番茄叶片的cDNA为模板,使用特异性的SlCOMT1引物(表1)进行PCR,在1.2%的琼脂糖凝胶上检测到预期大小的条带(图1),并对其进行测序和特征分析。SlCOMT1基因全长为1 074 bp,编码357个氨基酸。保守结构域分析结果表明,与其他COMT1类似,番茄SlCOMT1蛋白序列在第28~79氨基酸和第134~338氨基酸处分别含有二聚化保守结构域和甲基转移酶2保守结构域,属于SAM(S-腺苷甲硫氨酸)依赖型甲基转移酶超家族成员(图2),表明该基因在不同物种中较为保守。多序列比对结果(图3)表明,番茄SlCOMT1的S-腺苷甲硫氨酸(SAM)结合位点、催化残基和酚类底物结合位点,都显示出较高保守性。根据ExPASy预测对蛋白质理化性质进行分析,结果表明,SlCOMT1蛋白分子量为38.95 ku,结构式为 C1 746H2 740N448O513S23,理论等电点(PI)为5.63,负电荷残基(Asp+Glu)总数41个,正电荷残基(Asp+Glu)总数33个。不稳定系数为29.20,属于稳定蛋白。脂肪系数为88.26,表明SlCOMT1蛋白脂溶性很强。


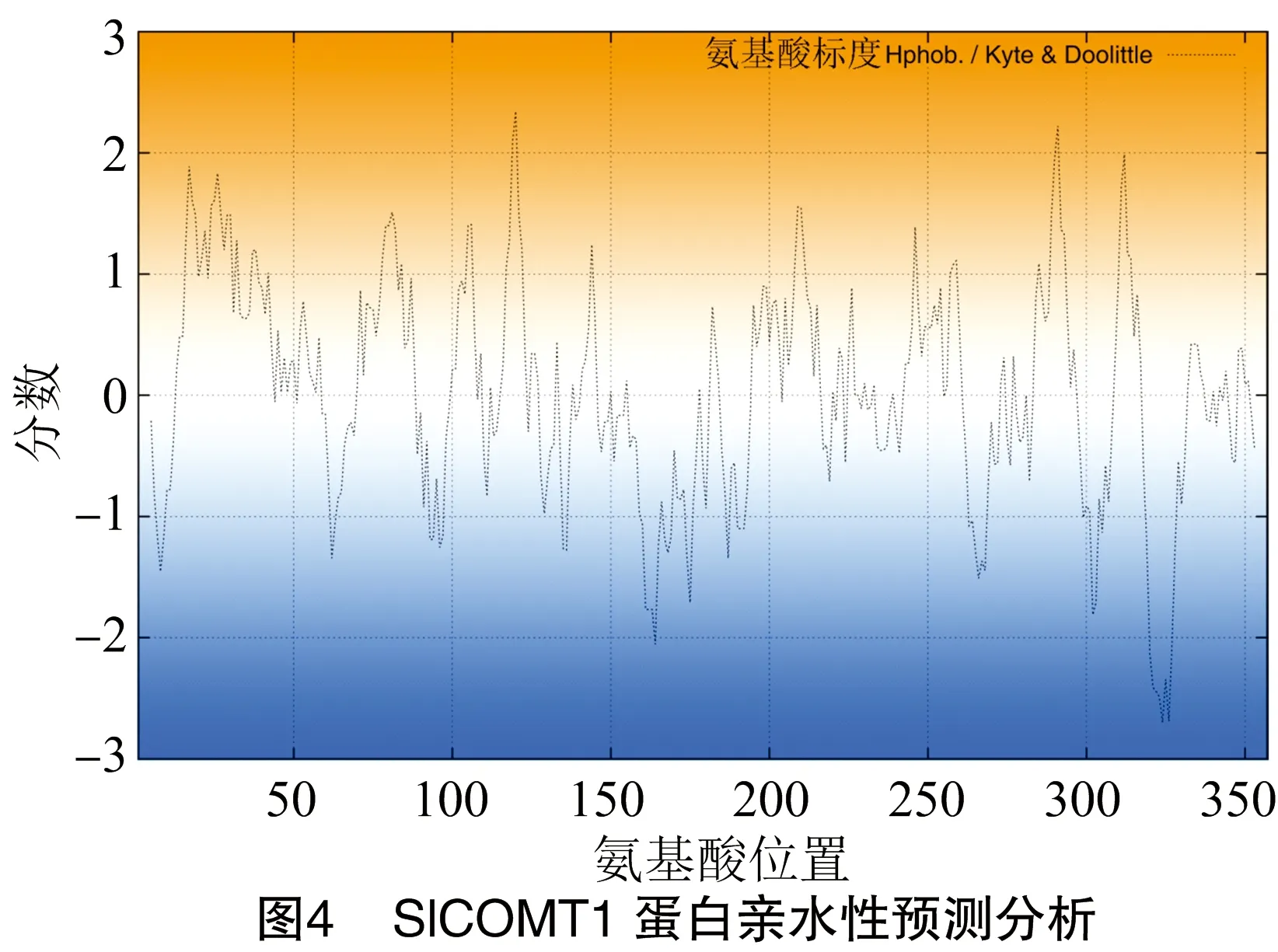
2.2 SlCOMT1蛋白亲水性分析
用ProtScale对SlCOMT1蛋白亲水性预测结果(图4)表明,SlCOMT1的亲水性均值(GRAVY)为0.020,表明该蛋白为疏水性蛋白。其中,多肽链第120位的脯氨酸具有最高的疏水性(2.344),第324位的精氨酸具有最高的亲水性(-2.700)。
2.3 SlCOMT1跨膜结构预测
通过TMHMM 2.0对番茄SlCOMT1进行蛋白质跨膜区域预测,结果(图5)表明SlCOMT1蛋白不含有跨膜区域,属于非跨膜蛋白。
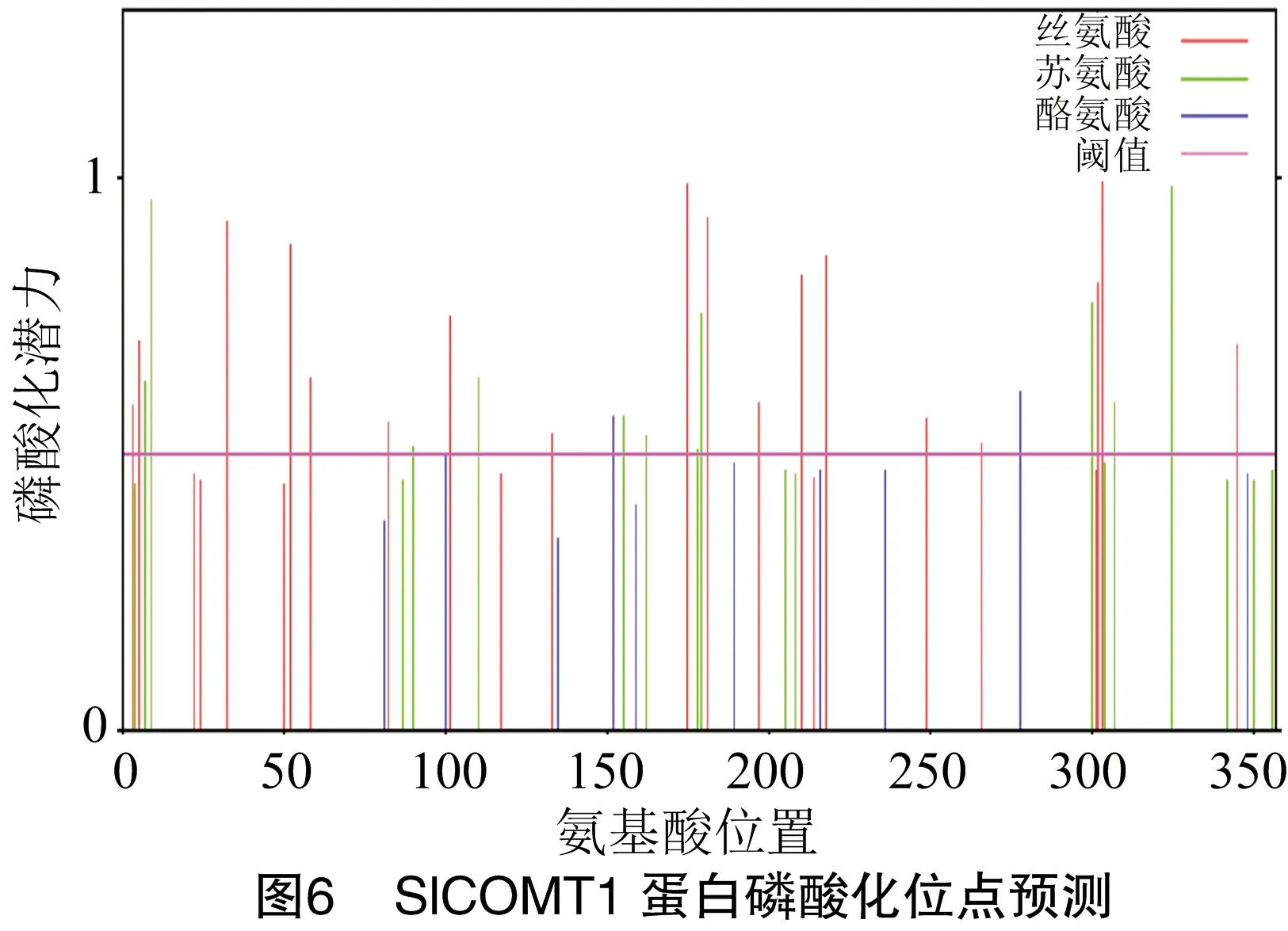
2.4 SlCOMT1蛋白磷酸化位点预测
使用NetPhos预测了SlCOMT1蛋白的磷酸化位点,结果(图6)表明,SlCOMT1含有预测的磷酸化位点31个,其中丝氨酸磷酸化位点18个;苏氨酸磷酸化位点11个;酪氨酸磷酸化位点2个。
2.5 SlCOMT1亚细胞定位预测
使用Plant-mPloc预测SlCOMT1的亚细胞定位,结果表明,SlCOMT1定位于叶绿体中。
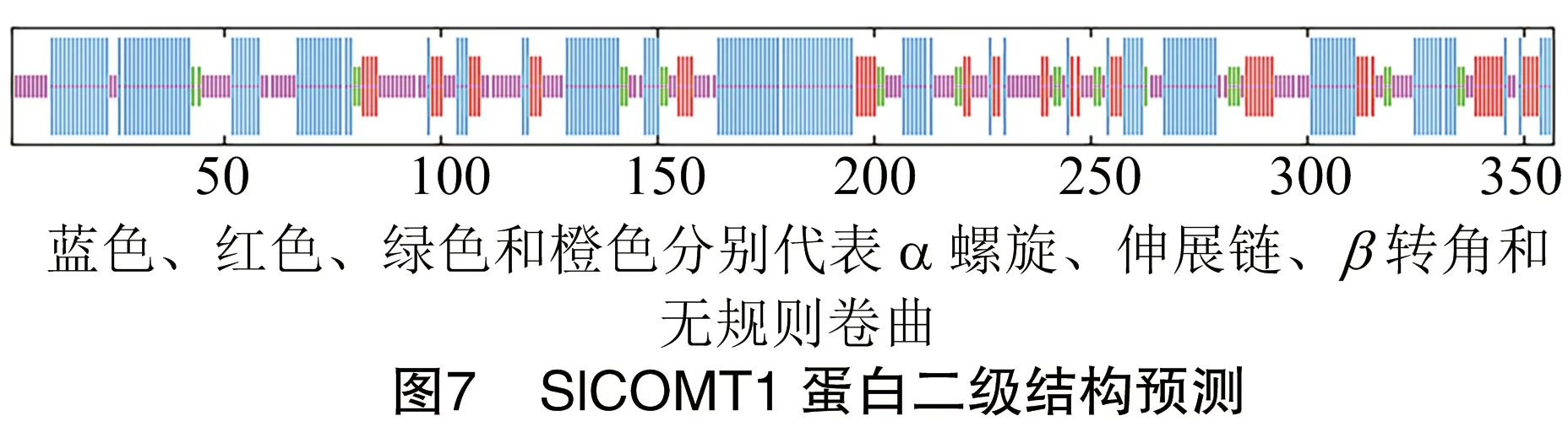
2.6 SlCOMT1蛋白的二级、三级结构预测
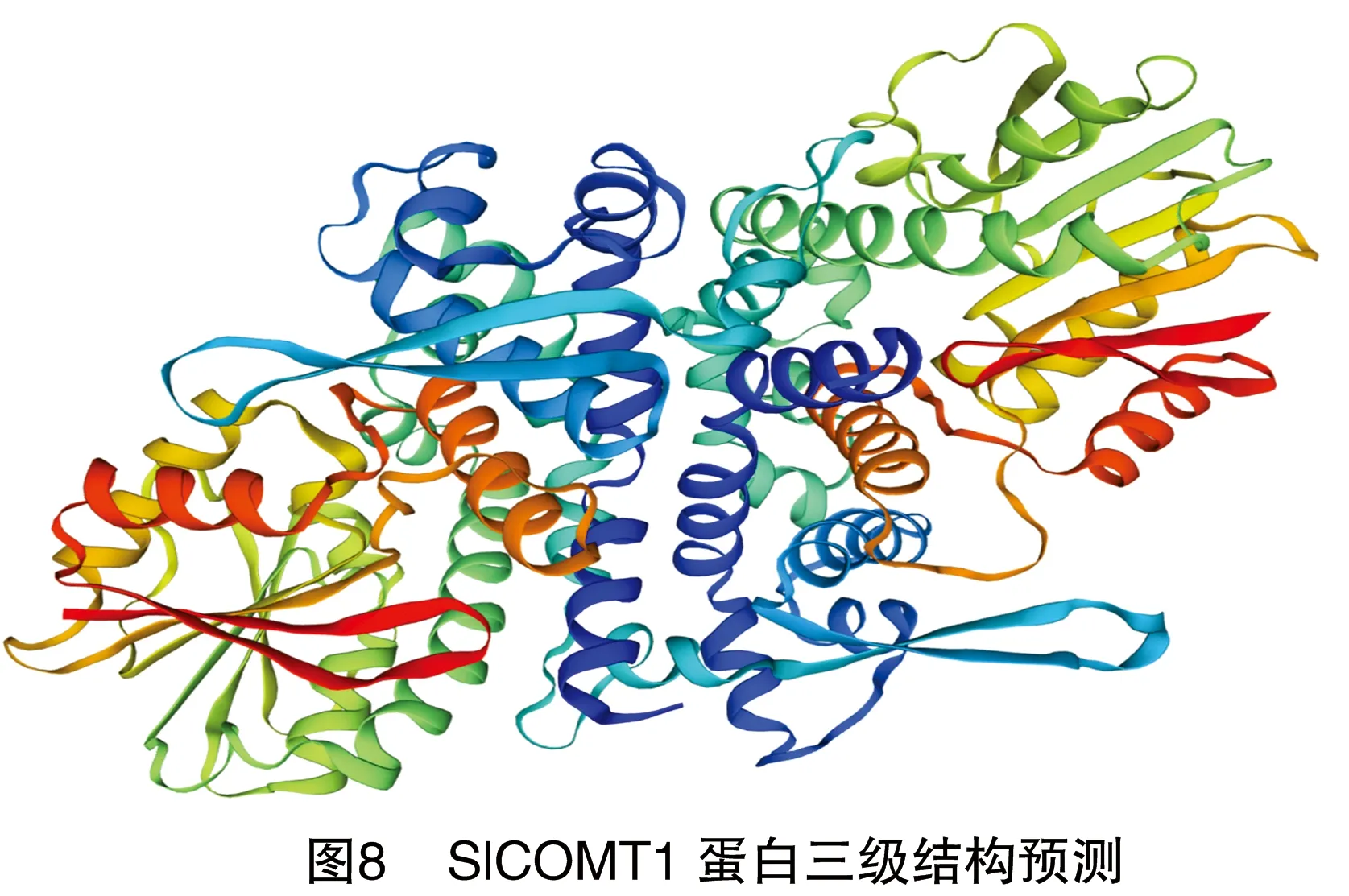
使用SOPMA预测SlCOMT1蛋白的二级结构(图7),在SlCOMT1的二级结构中,α螺旋占45.10%,无规则卷曲占32.77%,延展链占15.41%,β转角占6.72%,推测SlCOMT1蛋白主要由α螺旋和无规则卷曲组成。使用SWISS-MODEL预测SlCOMT1蛋白的三级结构,结果见图8。

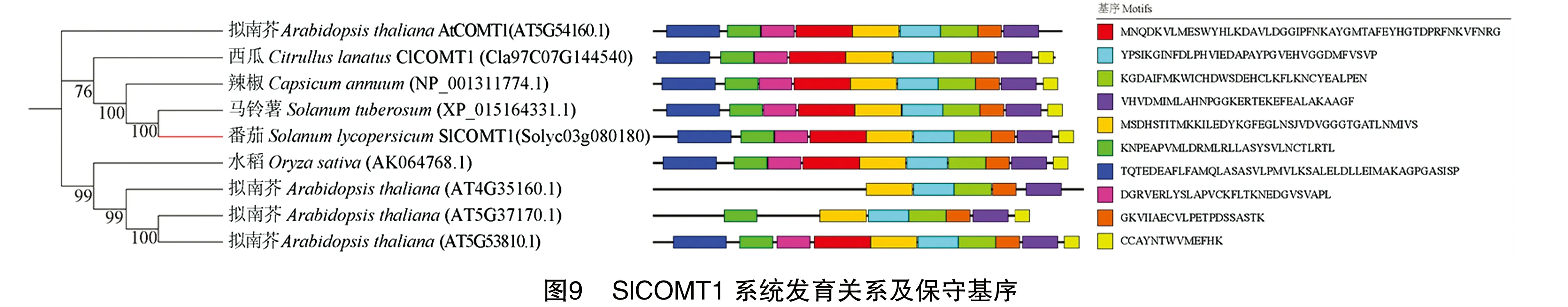
2.7 SlCOMT1的系统发育树及保守基序分析
通过系统发育树及MEME保守基序分析SlCOMT1,结果(图9)表明,番茄SlCOMT1与同科的辣椒和马铃薯具有较高的亲缘关系且具有相同的保守结构域数量。
2.8 SlCOMT1在番茄不同组织器官中的表达模式及褪黑素含量变化
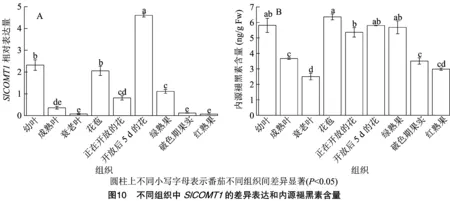
采用qRT-PCR技术,笔者检测了不同发育阶段的番茄叶片、花和果实中SlCOMT1基因的相对表达量、内源性褪黑素的含量。结果(图10)表明,SlCOMT1基因在番茄幼叶、成熟叶、衰老叶、花苞、开放当天的花、开放后5 d的花、绿熟果、破色期果实、红熟果等不同组织器官中都有表达,而且表达量不同。在叶片和果实的不同发育阶段,SlCOMT1的表达随着叶片和果实器官的发育其相对表达量显著降低。不同组织器官中内源褪黑素的含量变化也表现出类似的变化趋势,表明番茄叶片和果实中SlCOMT1基因的表达与内源褪黑素的生物合成密切相关。而在花器官中,SlCOMT1的表达随着花的发育呈现出先下调后上调的变化趋势,并在衰老花(开放后5 d的花)中表达量最高。而衰老花的内源褪黑素含量与其他时期的花之间没有显著差异,表明褪黑素在花发育进程中发挥的功能可能有别于其他组织。
3 讨论与结论
褪黑素是一种重要的信号分子,在植物响应非生物和生物胁迫中具有多种生理功能[19]。番茄SlCOMT1是与拟南芥褪黑素合成相关的AtCOMT1核苷酸序列最相似的基因,通过过表达和基因沉默技术证明了SlCOMT1与番茄褪黑素合成有关[14]。本研究发现SlCOMT1在Micro-Tom不同时期的组织器官中表达水平与内源性褪黑素的含量存在一定的关联,并在幼嫩组织中SlCOMT1的相对表达和褪黑素含量最高,这可能与SlCOMT1参与组织发育以及褪黑素的代谢水平有关,因为这些组织的代谢活动较高。Okazaki 等采用酶联免疫吸附剂测定(ELISA)方法[20],在Micro-Tom所有器官中均检测到褪黑素含量在1.5~66.6 ng/g之间,种子中褪黑素的含量最高,其次是发芽后生长4 d的幼苗,叶片中的含量高于花中的含量。Liu等采用实时荧光定量PCR方法[14]检测Ailsa Craig番茄中SlCOMT1的时空表达情况。结果表明,SlCOMT1在番茄的根、芽、叶、花、果实等组织中具有时空特异性,在这些组织中表达水平不同。在根中表达量最低,在果实中表达量最高,说明SlCOMT1可能参与了果实发育的调控。本研究结果是Micro-Tom正在开放的花和开放后5 d的花中褪黑素含量高于成熟叶片,红熟果中的褪黑素含量显著低于绿熟果,这与Liu等的研究结果[14,19]不太一致,这可能与分析的样品、植株生长发育的状态不同有关。Okazaki等的研究是取包括花苞到开放了的花,也就是全部花的混合样品进行分析;他们对不同成熟阶段的果实褪黑素含量分析结果表明,进入绿熟阶段后,随着果实的进一步成熟,果实中褪黑素含量有所增加,但是差异并不显著[19]。Liu等没有对SlCOMT1的表达量进行差异显著性分析[14]。本研究和Okazaki等的研究[19]一致表明在番茄叶、花、果实中均检测到褪黑素,且褪黑素在幼叶中的积累量高于成熟叶,并和Liu等的研究[14]一致表明,褪黑素在番茄花中的积累量高于叶片。褪黑素的浓度因番茄发育阶段的不同而不同,表明褪黑素在番茄发育过程中起着作用,可能参与番茄成熟的一些过程。
番茄SlCOMT1蛋白具有SAM(S-腺苷甲硫氨酸)依赖型甲基转移酶超家族典型的保守结构域,不含跨膜结构,是一种稳定的高脂溶性蛋白。SlCOMT1基因及褪黑素在矮生型番茄Micro-Tom的叶片、花、果实等不同组织器官中都有表达和积累,SlCOMT1的表达和内源褪黑素生物合成在番茄不同发育时期的叶片和果实之间存在一定的相关性,并在幼嫩组织中检测到SlCOMT1较高表达和褪黑素积累,这可能与SlCOMT1参与组织发育以及褪黑素的代谢水平有关,SlCOMT1在花发育过程中的生物学功能将是进一步研究的重点。
