可吸收胶原膜在累及前联合的声门型喉癌手术中的应用
2023-01-06闫静张慧慧任晓勇闫妍杜小滢孔德敏杨敏娟侯瑾
闫静,张慧慧,任晓勇,闫妍,杜小滢,孔德敏,杨敏娟,侯瑾
(西安交通大学第二附属医院 耳鼻咽喉头颈外科,陕西 西安 710004)
声门型喉癌占喉癌的60%[1],其扩散、转移发生率低,在治疗方面,理想的是切除肿瘤,尽量保存喉功能完整性[2]。目前对于早期声门型喉癌无颈部淋巴及远处转移者的治疗,使用经口CO2激光或等离子切除等微创的手术方法在临床上取得了较好的疗效[3]。而累及前联合的单侧或双侧声门型喉癌术后易发生声带粘连,阻碍声带的精确运动,影响发音或呼吸质量。如何防止术后瘢痕粘连仍是一个难题。本研究对于19例累及前联合声门型喉癌患者,在全麻支撑喉镜下行CO2激光切除病变并一期行可吸收胶原膜置入获得良好疗效,现报道如下。
1 资料与方法
1.1 病例选择
选取2016年2月—2020年10月在西安交通大学第二附属医院耳鼻咽喉头颈外科病院住院治疗的累及前联合的声门型喉癌患者19例,均为男性,年龄42~71岁,中位数为50岁。确诊为T1b型声门癌8例,T2型声门癌10例,T3型声门癌1例。影像学检查未发现癌灶淋巴结转移和/或其他器官组织转移征象,术前病理活检为鳞状细胞癌;无其他部位恶性肿瘤及对本研究产生影响的其他系统疾病,如甲状腺相关疾病、中枢神经系统疾病、心血管系统疾病及严重的胃溃疡等。所有患者在手术后随访过程中无误访、漏访情况,所有临床资料完整。除1例T3型声门癌患者术前先行尼妥珠单抗靶向治疗2个疗程后行手术治疗,余18例患者于住院手术之前未行相关辅助治疗。
1.2 手术方法
1.2.1 CO2激光联合低温等离子行声门型喉癌切除术 患者取仰卧位,给予全身麻醉,经口气管插管,选用直径为6.0 cm或6.5 cm的麻醉插管,具体视患者情况而定。麻醉起效后,经口插入 Storz支撑喉镜,暴露声门;然后调整喉镜位置,完整暴露声带病变部位或者在喉外按压的情况下完整的暴露前联合;整个显微内镜操作的完整影像资料由ZISS S7高清数字手术监视系统记录。完善所有的激光防护措施,将激光设置为单发模式,一般选择3.5W激光切除肿瘤。所有患者均行IV型声带切除术,沿肿瘤后及外侧保留3~5 mm的切缘,标出切除范围,完成后及外侧边界的切除后,牵拉病变组织或者按压喉部完整暴露前联合,前界切除至甲状软骨板,牵拉暴露下切缘,按3~5 mm安全界完整切除。激光切除病变后,对于可疑病变切除不彻底,尤其是前联合部位受到肿瘤侵犯者,将低温等离子刀头的前端弯曲,彻底将前联合残余甲状软骨膜消融及激光碳化组织至完全裸露骨面。术中有出血者可直接使用等离子刀进行止血。用显微杯状钳钳取异常切缘,送冷冻切片及常规病理检查。
1.2.2 可吸收胶原膜一期置入 以50 mL注射器针头分别于环甲膜中点左右旁开0.5 cm刺入喉腔内(图1a),2根0号可吸收线穿针孔进入,支撑喉镜下将2根线分别钳夹至口外,拔出穿刺针,将口外2线的一端于制备好的可吸收胶原膜的两侧分别穿过并进行固定,拉紧两根线的另一端,把2 cm×3 cm可吸收胶原膜修剪合适大小放置在喉腔的声带平面(图1b),用7-0polin线将胶原膜的后缘与声带切除残端固定,依靠胶原膜的支撑力将声门两侧分离开,避免创面之间接触、粘连(图1c)。将预留在颈部的可吸收缝线外端固定置于颈前,避免其在喉腔内可能发生移位或脱落,检查无活动性出血后撤出支撑喉镜。手术中出血或渗血明显处给予止血,操作尽可能细致、轻柔、准确。术后根据喉镜下胶原膜贴敷创面是否良好,选择在1~2周内拆除颈外缝线,术后1个月进行电子喉镜观察检查,观察喉腔恢复情况及胶原膜的吸收情况并嘱患者进行适当的发音训练。

图1 术中可吸收胶原膜置入过程
1.3 术后护理及随访
1.3.1 术后护理 术后常规给予心电监护、持续低流量吸氧及相关对症支持治疗,观察24 h,若无异常可出院。嘱患者禁声1周,并给予抗生素口服预防感染,口服质子泵抑制剂、多做深呼吸减少手术部位肉芽组织生成。
1.3.2 术后随访 按照出院后第1年前半年每个月复查1次,后半年开始每3个月来院复查1次;手术1年后,每半年门诊复查1次,通过电话和门诊随访。
1.4 术后疗效评估
1.4.1 呼吸功能 评定指标为1周内患者是否出现呼吸困难,若出现可详细记录出现的时间、轻重程度和原因等。
1.4.2 疼痛程度 应用疼痛数字分级法(NRS)进行术后24 h疼痛评估,用 0~10 代表疼痛的不同程度,0 为无痛,10 为剧痛。疼痛程度分级标准:0:无痛;1~3:轻度疼痛;4~6:中度疼痛;7~10:重度疼痛。以术后复查及随访时患者主观标出的疼痛程度数字为准。
1.4.3 黏膜功能 术后通过电子纤维喉镜观察黏膜愈合的情况。分别记录患者在入院前、术后1个月以及每次门诊随访时喉镜检查结果。
1.4.4 发音功能 记录患者术前及半年后黏膜稳定状态下主客观嗓音分析检查结果,观察的指标主要有嗓音障碍指数(voice handicap index,VHI)、最长发音时间(maximum phonation time,MPT) 、嗓音障碍严重指数( dysphonia severity index,DSI)。
1.5 统计学方法
采用SPSS 26.0 软件进行统计学分析,首先对两组计量资料差值进行正态性检验,对符合正态性分布资料采用配对t检验进行组间比较;不满足正态性分布则采用配对样本Wilcoxon符号秩检验进行组间比较,检验统计量为T。检验水准α=0.05,P<0.05为差异具有统计学意义。
2 结果
2.1 一般情况
19例患者术后24 h内呼吸均平稳、进食饮水正常,无呛咳,并于术后1~2日顺利出院。术后疼痛评分,其中17例(89.5%)轻度疼痛,2例(10.5%)中度疼痛,无重度疼痛患者。术后1~2周根据喉镜下胶原膜贴敷程度,拆除颈部缝线,均无脱落情况。
2.2 黏膜功能
术后1个月电子喉镜下观察胶原膜基本吸收,腔内无明显肉芽组织增生。除1例T2期声门癌患者术后前联合复发,3例前联合粘连超过声带前三分之一,其余15例(78.9%)患者声带前联合于术后6个月至1年均获得良好三角形形态(图2、3)。
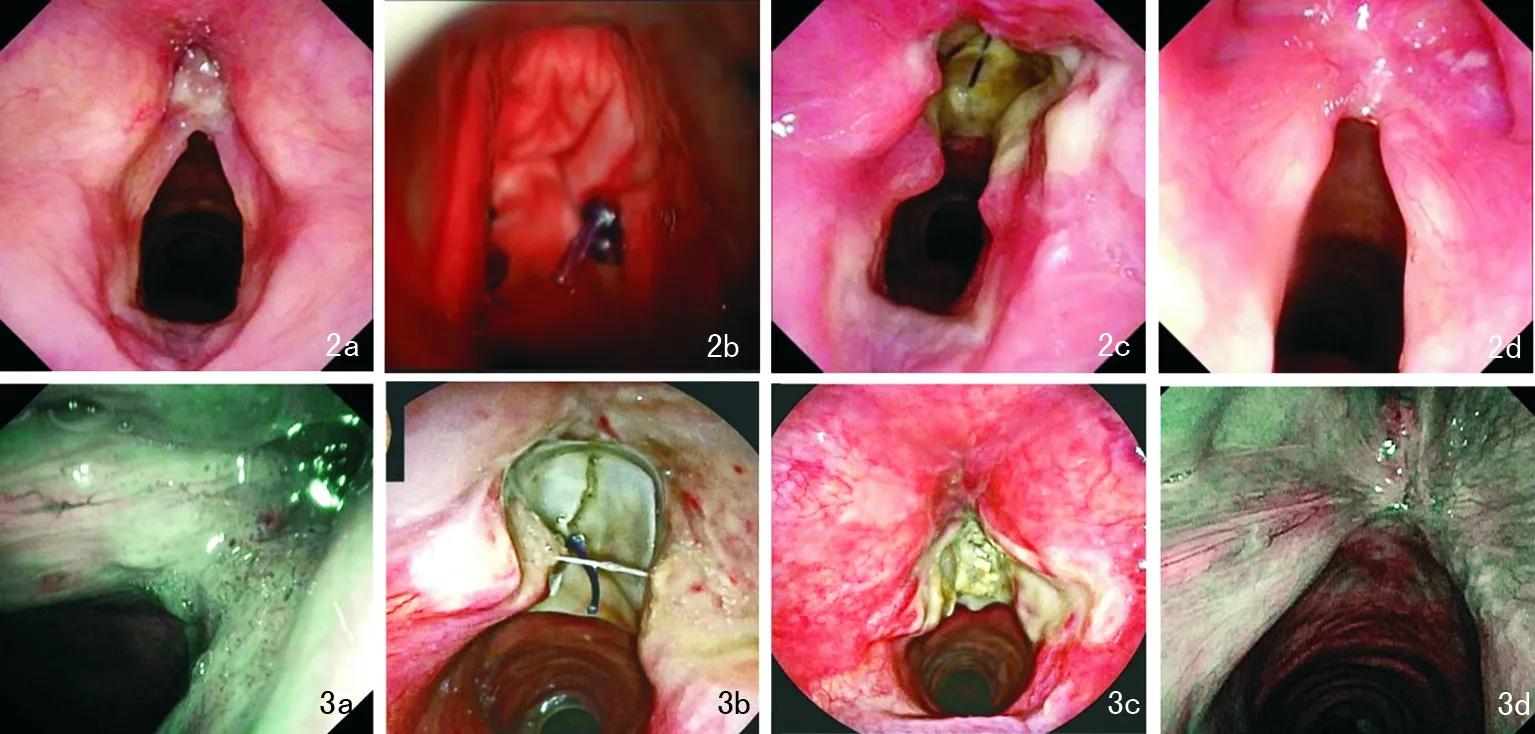
图2 1例T1bN0M0声门癌患者
2.3 发音功能评估
患者术前及术后半年黏膜功能稳定后行动态喉镜检查及嗓音分析,患者发音功能较术前明显好转,差异均具有统计学意义(P<0.001)。具体数值见表1。
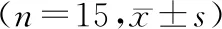
表1 手术前后嗓音参数比较
3 讨论
因声音嘶哑出现较早,声门型喉癌易早期发现,诊断时大多数呈早期病变;且声门区淋巴分布较少,加之喉部解剖结构的保护作用,颈部淋巴结在声门型喉癌中转移的几率较低[4]。目前对于早期声门型喉癌的治疗,主要方式有放射治疗,开放性手术和微创手术。放疗可较好的保护患者声音质量,但是治疗周期较长,且部分患者放疗反应重,甚至少数患者可出现呼吸困难,从而部分患者接受度低。经典的开放性手术有喉裂开声带部分切除术、喉部分切除术,患者均需要行暂时性气管切开术,术后大约需要2周时间恢复,对患者的吞咽、呼吸和发声功能影响较大,且部分患者难以适应气管切开,给其带来明显的生理和心理打击[5]。CO2激光或等离子切除术是近些年来在早期声门型喉癌的微创治疗中比较提倡的术式,CO2激光切除术的优点是手术精确度高、损伤小[6-7]。低温等离子优点包括射频消融刀头能够灵活弯曲,对于激光切除困难及隐匿的病灶可予以彻底切割,从而减少术后由于病变切割不彻底引起的复发;同时等离子刀集切割、吸引、止血及创面冲洗功能为一体,在狭窄的咽喉腔空间里操作更为方便[3];且支撑喉镜下的微创手术不需要进行预防性气管切开,术后恢复时间短,患者接受度高,成为治疗早期声门型喉癌的主要选择方式之一[8]。
在早期声门型喉癌中,对于其手术治疗效果的评估指标[9],除了术后肿瘤的复发率、手术创伤造成的疼痛之外,术后患者的呼吸、吞咽及发音等相关喉功能的恢复情况也是非常重要,这些因素严重影响患者手术后的生活质量。在这些影响因素中,喉狭窄无疑是手术后影响喉功能的最主要因素,而对于该并发症的预防,主要取决于术中对于前联合部位的妥善处理以及术后喉粘连的预防[10]。纵观国内外研究,在声门型喉癌术后喉狭窄的预防措施中,较多的是在手术过程中置入喉支架和喉膜,材质有硅胶及镍钛合金[11-12];术中置入这些材料,可以起到支撑喉腔、维持喉腔形态、保持气道通畅的作用,从而避免术后喉腔黏膜粘连,出现喉腔狭窄。徐文等[13]观察了15例喉蹼患者在支撑喉镜下行喉硅胶膜置入手术的疗效,其中14例患者取得了良好的声门形态,需术后3~4周行全麻手术取出置入物。魏春生等[14]利用Lichtenberger喉内缝合器固定硅胶膜的方法治疗3例声带息肉术后粘连患者,这种方法创伤小、操作相对方便,效果良好,但器械的特殊性限制了该手术的开展,硅胶膜也需二次手术取出;王燕等[15]在支撑喉镜下置入硅胶膜的方法治疗21例继发性喉粘连患者,其中20例患者在术后半年恢复了较好的声门形态以及主观嗓音功能,其G评分从术前的2.7±0.4到1.6±0.1,B评分从术前的2.1±0.3到1.4±0.2。这些研究表明硅胶膜置入能够较好的避免声带粘连、保持良好的声门形态并恢复发音功能。我们参照既往研究者的经验,也进行了硅胶膜置入预防声带粘连的尝试,发现硅胶膜需要二次全麻或表麻取出,给患者带来一定的负担。遂思考是否有应用可吸收材料作为“喉膜”置入术腔的可能性。
选择合适的修补材料是影响患者术后喉功能恢复的关键之一。考虑到喉部黏膜非常敏感,若置入物选择不当或大小不合适,会引起剧烈呛咳,严重者可能出现置入物脱落引起窒息的情况,所以置入物需要有一定的柔韧性;置入物长期与创面摩擦,应具有良好的组织相容性,避免引起排异反应。可吸收胶原膜最早应用于脑外科及骨科,作为引导组织再生的材料,用于修补硬脑膜、神经断裂修复后再生、防止术后粘连等[16]。也有文献报道[17-18],将可吸收胶原膜应用于鼻科及耳科相关手术,例如脑脊液漏修补术、乳突根治术、鼻中隔穿孔、腮腺、甲状腺手术等,在组织修复及防止粘连上均获得较好的疗效。胶原蛋白是可吸收胶原膜的主要成分,并去除胶原蛋白末端的抗原肽,降低了免疫原性,因而生物相容性良好,且不会引起机体产生免疫反应和毒性作用,在植入后降解的速度与组织再生的速度相匹配,在完全吸收之前可以有效防止粘连;具有良好的柔韧性,可随声门形态进行缝合塑形,增加了患者的舒适感。本研究的19例患者,在支撑喉镜下行声门型喉癌切除时同期置入胶原膜,术后均无刺激性咳嗽及异物感等不适。全部患者疼痛评估均为中度以下程度,其中绝大多数患者为轻度疼痛。该胶原膜于术后1个月左右吸收消失,无需二次取出,操作简便且无二次创伤。其中15例患者术后半年喉部黏膜状态稳定,患者均获得良好的三角形声门形态;3例患者术后声带瘢痕粘连约声带前三分之一,但未影响呼吸。15例患者MPT从术前的(10.07±1.47)s延长到术后(14.40±1.48)s,DSI手术前后分别为(-1.52±4.20)和(0.97±2.12),客观声学参数改善明显;3例患者由于声带前段粘连,声嘶改善不明显。
综上所述,可吸收胶原膜可应用于早期声门型喉癌的微创手术治疗中,使大部分患者在手术后避免喉狭窄的发生,声门保持三角形形态,发音功能较术前明显改善,在预防声门型喉癌术后前联合瘢痕粘连中有较好的效果,可作为治疗部分声门型喉癌患者的有益选择。对比既往研究中硅胶膜的疗效,虽然稍有逊色,但在治疗过程中使患者的舒适度明显提高,且无需二次取出,减轻患者负担的同时使其对该术式的接受度提高。但是对于肿瘤范围较大,切除组织过多,胶原生物膜存在吸收过快,稳定性不如硅胶膜的缺点。另外,由于本研究的样本量相对较小,更进一步的效果需要在临床实践中持续证实和改进。
