Zn2+掺杂对LiNiO2正极材料性能的影响*
2023-01-06张清波李东林高建行李童心
张清波,李东林,高建行,李童心,张 龙
(长安大学 材料科学与工程学院,新能源材料和设备实验室,西安710061)
0 引 言
LiNiO2(LNO)因具有高放电比容量和高能量密度的特点被认为是最有前景的锂离子电池正极材料。然而,LNO较差的循环稳定性限制了其实际应用[-3]。目前,研究人员已经研究了诸多提高LNO循环性能方法。体相掺杂作为一种有效的策略,已被广泛用来抑制Li+/Ni2+阳离子混排并稳定层状晶体结构,从而提高层状高镍材料的电化学性能[4]。电化学惰性的非过渡金属离子,特别是Mg2+和Al3+,作为正极材料的掺杂剂已经被广泛研究[5]。然而,Zn2+作为非过渡金属离子,目前只有很少的研究报道过Zn2+掺杂改性层状正极材料。Chen等[6]合成了Zn2+掺杂的LiZnyNi0.8-yCo0.2O2正极材料,发现Zn2+掺杂的材料在第1和第100次的放电容量分别为170和138 mAh/g,容量保持率为81%,未掺杂材料的相应值为158和97 mAh/g,容量保持率为61.4%。姚升超等[7]研究了锌掺杂对LiNi0.6Co0.2Mn0.2O2正极材料结构和电化学性能的影响,结果表明Zn2+掺杂之后的材料表现出更优异的倍率和循环性能,10C下放电比容量提升了37%,1C下循100圈之后容量保持率提高了12%。基于前人的研究,可以知道Zn2+掺杂对镍基正极的电化学性能有积极影响。基于此,本文重点研究了Zn2+掺杂对LNO结构和电化学性能的影响。
1 实 验
1.1 LiNi1-xZnxO2正极材料的合成
LNO和Zn2+掺杂的LNO样品均使用溶胶-凝胶法合成,路线如下所述:首先,将化学计量比的LiCH3COO·2H2O、Ni(CH3COO)2·4H2O和Zn(CH3COO)2·4H2O溶解在30 mL去离子水中。其中Li过量5%,以补偿在高温下发生的损失。其次,再向溶液中加入柠檬酸,柠檬酸与过度金属离子的摩尔比为1∶1。最后加入氨水调节溶液pH值为7~8,反应2h后在95 ℃下搅拌蒸干,转移到鼓风干燥箱中150 ℃下干燥12 h。干燥的前驱体粉末经研磨均匀后,在空气中加热至450 ℃预煅烧3h,后续在725 ℃下,氧气中热处理12 h。最终得到的样品LiNi1-x-ZnxO2(x=0、0.01、0.02、0.03),将其命名为LNO、LNO-1Zn、LNO-2Zn和LNO-3Zn。
1.2 材料的表征
样品的物象和结构分析采用Broker公司的型号为AXSD8的X射线衍射仪(Cu靶Kα为辐射源,λ=0.15406 nm)。样品的形貌分析采用日本JSM-4800型场发射扫描电子显微镜(FESEM),其中工作电压为5 kV,工作电流为10 μA。
1.3 材料的电化学性能测试
活性物质是本次实验所合成的LNO及其改性样品,导电剂是由SupeP和Ks6按照4∶1的比例混合而成。按照7∶2∶1的比例称取活性物质、导电剂、PVDF,并在研钵中研磨均匀,随后加入NMP制成浆料,将混合浆料涂敷在铝箔上。随后将涂敷好的正极极片放置在100 ℃真空干燥箱中,氩气气氛下烘12 h。以金属锂作为负极,1mol/L LiPF6的碳酸甲乙酯(DMC)-乙烯碳酸酯(EC)-碳酸甲乙酯(V(DMC)∶V(EC)∶V(EMC)=1∶1∶1)为电解液,在充满氩气的手套箱中完成CR2025扣式半电池的组装。充放电测试由NEWARE软件在2.5和4.5 V电压范围内在室温下进行。电化学阻抗谱(EIS)测量由电化学工作站在0.1~105Hz的频率范围内进行。循环伏安法(CV)测试使用电化学工作站进行。
2 结果与讨论
2.1 材料的表征和分析
2.1.1 XRD分析
图1(a)为未掺杂和掺杂Zn2+正极材料典型X射线衍射图。所有样品的衍射峰基本保持一致,且与LNO的标准PDF#74-0919卡片相对应,为α-NaFeO2层状结构。其次,所有材料的特征峰尖锐且无明显杂相峰存在,表明Zn2+掺杂未改变主体材料的结构。4个样品的特征峰(006)/(102)和(108)/(110)分裂明显(图1(c)),证明了4种正极材料均具有良好的层状结构。(003)特征峰放大之后,可以清楚地发现随着Zn2+掺杂量的增加,(003)峰产生了向小角度偏移的现象(图1(b)),这可能是由于Zn2+(0.074 nm)的半径大于Ni2+(0.069 nm)的半径,Zn2+掺入LNO晶格中导致(003)晶面间距增大[7]。图1(d)显示了所有样品特征峰(003)和(104)强度比值,用来衡量这些层状材料阳离子的混排程度[8]。当I(003)/I(104)的比值>1.2时,说明该种材料的阳离子混排程度较低。阳离子混排通过阻止锂离子的迁移导致层状正极材料的电化学性能下降[9]。LNO、LNO-1Zn、LNO-2Zn和LNO-3Zn样品的I(003)/I(104)的比值分别为1.148、1.315、1.316和1.296,其中Zn2+掺杂之后样品的I(003)/I(104)的比值大于原始样品,表明Zn2+掺杂降低了Li/Ni混排程度,从而使LNO样品可能具有更优异的电化学性能。其中LNO-2Zn的阳离子混排程度最低,预示着LNO-2Zn具有最佳的倍率性能和循环性能。
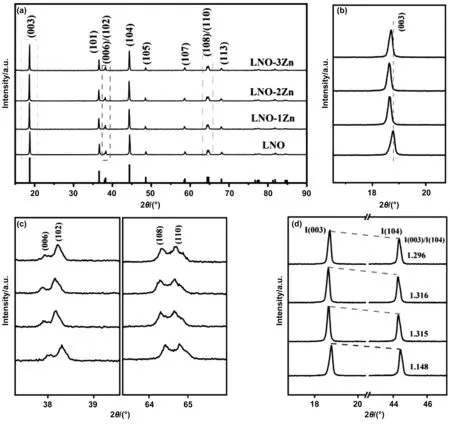
图1 (a) 样品的XRD图,(b) (003)衍射峰的放大图, (c) (006)/(102) 和 (108)/(110)衍射峰的放大图,(d) (003) 和 (104) 衍射峰的强度比示意图Fig.1 (a) XRD patterns of all samples, magnifications of (b) (003) peaks, (c) (108) and (110) peaks, and (d) the intensity of the peak ratio between (003) and (104)
2.1.2 SEM分析
图2为原始样品和Zn2+掺杂样品的SEM图像。从图中可以看出所有样品均由具有良好结晶和光滑表面的初级颗粒组成,这些初级颗粒形状为多面体,尺寸约为300~400 nm。如图2(a,e)所示,原始LNO样品初级颗粒聚集严重,颗粒间没有明显的边界,而掺杂之后的样品初级颗粒有明显的边界(图2(b,f)、(c,g)和(d,h)),且分布比较均匀。随着Zn2+掺杂量的增加,样品的形貌没有明显变化。

图2 样品的SEM图像:(a,e) LNO;(b,f) LNO-1Zn;(c,g) LNO-2Zn和(d,h) LNO-3ZnFig.2 SEM images of samples: (a), (e) LNO;(b), (f) LNO-1Zn; (c), (g) LNO-2Zn and (d, h) LNO-3Zn
2.2 电化学性能测试及分析
2.2.1 恒流充放电测试
(1)首次充放电曲线及循环性能分析
在0.1C(20 mA/g)电流密度下,获得初始充放电曲线如图3(a)所示。LNO、LNO-1Zn、LNO-2Zn和LNO-3Zn的初始放电容量分别为230.8,234,237和217 mA/g,库伦效率分别为89.6%、92.2%、90.5%和86.3%。上述结果表明,适量Zn2+掺杂能够增加首圈放电比容量和提高库伦效率。但是掺杂3%(摩尔分数) Zn2+后,发现LNO的放电比容量减少,库伦效率降低,这可能是由于过多非活性的Zn替代了部分提供容量的Ni元素。图3(b)显示了所有正极材料在1C下的循环性能。LNO、LNO-1Zn、LNO-2Zn和LNO-3Zn循环100次前后的充/放电比容量分别为171.2/128.3,181.6/131.7,167.2/133.8和156.4/91.3 mA/g,容量保持率分别为74.8%、72.94%、80.0%和58.3%。LNO-2Zn正极材料具有最优异的循环性能。
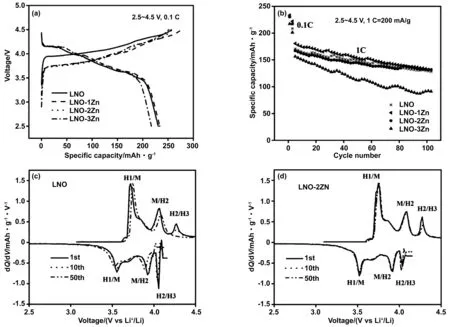
图3 (a) 在0.1C电流密度下,2.5和4.5 V之间的初始充放电曲线;(b) 1C倍率下循环100次的循环寿命;(c) LNO和 (d) LNO-2Zn在不同循环圈数下的微分容量曲线Fig.3 (a) Initial charge and discharge curves at 0.1 C between 2.5 and 4.5 V, (b) cycling performance at 1 C, dQ/dV profiles obtained by differentiating charge-discharge curves at different cycle numbers for the (c) LNO and (d) LNO-2Zn cathodes
为了研究Zn2+掺杂在循环过程中对LNO结构稳定性的影响,由第1、10和50次 的充电/放电曲线获得了dQ/dV曲线,如图3(c)和(d)所示。LNO正极通常会经历以下几个相变,包括初始充电阶段的六方相(H1)、单斜晶相(M)和后续充电阶段的六方相(H2/H3)[10]。H2-H3相变伴随着层间距离和晶胞体积的剧烈变化,快速的体积收缩可能导致材料晶体结构恶化,从而加速容量衰减[11]。从图3(d)可以看出,LNO-2Zn正极的氧化还原峰在循环过程几乎保持不变,且dQ/dV曲线重合度较好,表明该材料的相变过程具有良好的可逆性。然而,原始的LNO正极氧化还原峰强度随着循环次数增加而逐渐降低,当循环50次后,H2→H3的峰几乎完全消失,表明其相变可逆性差。由上述分析可得,Zn2+掺杂抑制了有害的相变,维持了晶体结构的稳定,从而在循环过程中使LNO获得了优异的容量保持率。
(2)倍率性能分析
所有样品的倍率性能如图4(a)所示,4个样品中LNO-2Zn的倍率性能最好,尤其是在大电流密度下。在2.5~4.5 V电压范围内,LNO、LNO-1Zn、LNO-2Zn和LNO-3Zn在0.1,0.2,0.5,1,2,5和10C电流密度下首次放电比容量分别为239.5/227.2/231.5/216.7,204.3/201.4/212.5/184.7,182.3/182.1/191.5/155.8,171.6/165.5/178.4/133.2,150.1/151.2/162.1/112.6,116.1/127.2/140.7/70.2和48/91.5/112.4/4.99 mAh/g。上述结果显示,在0.1倍率下,未掺杂LNO样品具有较高的放电比容量,但随着电流密度增大,LNO-2Zn正极显示出最高的放电比容量,这意味着Zn2+掺杂可以有效改善材料大电流密度下的充放电性能。倍率性能的改善可能是由于Zn2+掺杂之后的样品具有更少的锂镍混排和更宽的锂离子扩散通道,促进了Li+嵌入和脱出[12]。此外,从图4(b-e)可以很直观地发现,4个样品的放电电压随着电流密度的上升而急剧下降,电压平台也随之消失,其中未掺杂的LNO正极放电电压下降更为明显,电压平台衰减更为迅速,这可能是由于在大电流密度下,材料在充放电过程中发生极化现象所致[13-15]。而LNO-2Zn电压平台衰减较为缓慢,表明Zn2+掺杂减小了电化学极化,因而表现出更优异的倍率性能。

图4 (a) 在不同电流密度下的所有样品倍率性能,(b-e)不同电流密度下的首次放电曲线Fig.4 (a) Rate performance of all samples, and (b-e) discharge curves at different current density
2.2.2 循环伏安测试
图5(a-d)显示了LNO、LNO-1Zn、LNO-2Zn和LNO-3Zn在2.5~4.5 V的电压区间,0.1 mV/s的扫描速率下测试的循环伏安图(CV)。对于所有掺杂样品,在嵌锂/脱锂过程中均观察到与LNO相变过程相对应的典型行为。每条CV曲线的三对氧化还原峰代表了从原始六方相(H1)到新单斜相(M)、从单斜相到第二六方相(H2)和H2到第三六方相(H3)的相变过程[16]。从图中可以看出,除第一次循环外,第二次循环和第三次循环的氧化还原峰都向较低的电位移动,这是因为第一次循环中的CV行为与相转变过程中材料内部结构调整和SEI膜的形成密切相关[17-19]。对比LNO的CV曲线,发现Zn2+掺杂LNO正极的CV曲线在第二和第三圈良好重叠,这表明Zn2+掺杂的正极具有更好的可逆性。此外,氧化峰和还原峰之间的电位差(ΔE)用来揭示电极反应的可逆性和电化学极化的程度[20]。图中显示了第三条CV曲线上的H-M相变的氧化还原峰之间的差值,可以看出Zn2+掺杂之后的样品ΔE均小于未掺杂样品,这说明Zn2+掺杂有助于减小电化学极化并且提高相变的可逆性。在4个样品中,LNO-2Zn的电化学极化最小,表明其具有更好的倍率性能。Zn2+掺杂减小电化学极化可以解释为:(1) Zn2+掺杂抑制了有害相变过程,从而维持层状结构的稳定;(2) Zn2+减少了阳离子混排,促进了锂离子的传输。

图5 前三个循环的伏安图:(a) LNO;(b) LNO-1Zn;(c) LNO-2Zn和 (d) LNO-3ZnFig.5 Cyclic voltammograms of the first three cycles of (a) LNO, (b) LNO-1Zn, (c) LNO-2Zn, and (d) LNO-3Zn
2.2.3 交流阻抗测试
循环3次和循环100次后两个正极的奈奎斯特图如图6(a)和(b)所示。奈奎斯特图由两部分组成,中高频区域的半圆和低频区域的斜线[21]。Z′轴上半圆直径的数值近似为电荷转移电阻(Rct)。直线代表Warburg阻抗(Zw),这与锂离子在电极中的扩散有关。
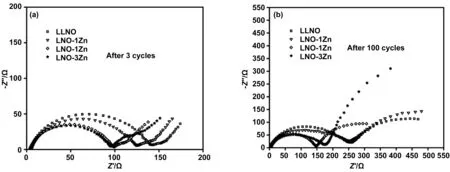
图6 (a) 循环3次和 (b) 循环100次后正极的Nyquist图Fig.6 EIS profiles after (a) 3 cycles and (b) 100 cycles
在循环3次后,LNO样品的Rsf和Rct值分别为4.312和130.9 Ω。LNO-2Zn的Rsf和Rct的值分别为4.307 和89.3 Ω。100次循环后,LNO样品的Rsf和Rct值分别为4.602 和219.8 Ω,LNO-2Zn的Rsf和Rct的值分别为4.803 和132.7 Ω。上述结果表明,两个样品的Rsf值相差不大,表明其对应电池的溶液阻抗基本一致。但是,无论是循环3次还是循环100次之后,LNO-2Zn的Rct值均小于LNO的值,这说明Zn2+掺杂可以阻碍循环过程中阻抗的增加。Zn2+掺杂减小阻抗的原因归结如下:(1) 可能是因为Zn2+阻碍H2-H3相变的发生。在电池的充放电过程中,由于发生严重的电解质-正极反应,正极颗粒会被一层高电阻岩盐相钝化[22]。此外,严重的颗粒破裂会不断暴露更多的正极颗粒到电解质中,加速阻抗的形成。Zn2+抑制了H2-H3相变过程,晶体内部的应力应变随之减小,从而抑制了颗粒破裂,减轻了接触损耗和电极/电解质副反应会抑制裂纹的产生;(2) Zn2+抑制了阳离子混排。阳离子混排在LNO的合成和充放电过程中均存在,且随着循环的进行逐渐加剧,从而导致阻抗不断增加。阳离子混排被抑制,从而抑制了阻抗的增加。
3 结 论
采用溶胶凝胶法合成了Zn2+掺杂的LNO正极材料,通过XRD、SEM和恒流充放电测试等对该材料进行分析,结果表明:
(1) Zn2+成功掺入LNO晶格中并导致LNO的晶面间距增大以及锂镍混排度的降低,并且未破坏主体材料的层状结构。此外,Zn2+掺杂之后样品的颗粒分布更加均匀。
(2)掺杂了2% (摩尔分数)Zn2+的LNO正极材料(LNO-2Zn)具有最好的倍率性能和循环性能。在1C的电流密度下循环100次后,LNO-2Zn的容量保持率为80%,高于LNO的74.8%;在较大的电流密度下,LNO-2Zn具有140.7 mAh/g(5C)和112.4 mAh/g(10C)的放电比容量,远远高于相同倍率下未掺杂LNO的放电比容量。
(3) LNO-2Zn具有较小的电化学极化和较高的充放电可逆性,因此其具有较好的倍率性能。Zn2+掺杂能够抑制有害相变,从而提高LNO的循环稳定性。Zn2+掺杂可以抑制循环过程中阻抗的增加,增大锂离子扩散系数,这也有利于提高LNO正极材料的电化学性能。
