青翘感冒颗粒微生物限度检查方法的建立
2023-01-06宋增炫邓映明通信作者
宋增炫,陈 媛,米 玲,邓映明(通信作者)
(梅州市食品药品监督检验所生测室 广东 梅州 514071)
青翘感冒颗粒为梅州市中医医院的医院制剂,其标准为广东省药监局的《医疗机构制剂注册标准》粤ZB20110012。青翘感冒颗粒由大青叶、连翘、马鞭草等5 味中药经现代制药工艺制成,具有清热与解毒和解表的功效,主要用于治疗常见的风热感冒及上呼吸道感染、急性扁桃体炎、咽喉炎。医院制剂为了确保患者临床使用的安全性,必须为其制定微生物限度检查方法(照《中国药典》2020 年版)以控制其微生物限度[1]。常规微生物限度检测目前尚无其微生物限度检查方法的报道。中药成分较复杂,不同药味组方常常含有抑菌物质,且有些制剂含有防腐剂,常规微生物检验法检验往往会显示假阴性的结果,发生微生物污染漏检的情况[2-7]。本实验建立了青翘感冒颗粒适合的微生物限度方法,提高了医院制剂的质量标准,为监管机构提供了参考。
1.仪器与材料
1.1 仪器
电子天平(AE ADAMHighlandHCB602H)、CL-40M 立式压力蒸汽灭菌锅(高山有限公司)、GHO-9080N-3 恒温培养箱(中国上海一恒公司)、BPMJ-250F霉菌培养箱(中国上海一恒公司)、THERMO 1384 A2 生物安全柜(THERMO(上海)仪器有限公司)、BPC-150F 生化培养箱(中国上海一恒公司)。
1.2 培养基
胰酪大豆胨培养基TSA(批号:1097453)、TSB胰酪大豆胨培养基(批号:1107232)、SDA 沙氏葡萄糖培养基(批号:1097161)、SDB 沙氏葡萄糖培养基(批号:1085972)、麦康凯MCB(批号:1093641)、麦康凯MAC(批号1095291)、肠道菌增菌液体培养基(批号1196031)、VRBGA(紫红胆盐葡萄糖)(批号1094631)、RV 沙门菌培养基(批号1106591)、XLD 琼脂培养基(批号1090311)均购自环凯微生物广东有限公司。经过适用性检查,符合药典四部通则1101、1102、1103 规定。
1.3 试剂
稀释液:pH 7.0无菌氯化钠- 蛋白胨缓冲液,批号1085991。
1.4 菌种
金黄色葡萄球菌〔CMCC(B)26003-5a8〕,铜绿假单胞菌〔CMCC(B)10104-2a5〕,大肠埃希菌〔CMCC(B)44102-3a〕,枯草芽孢杆菌〔CMCC(B)63501-2a22-3〕均购于中国食品药品检定研究院。白色念珠菌〔CMCC(F)98001-2a〕,购与广东环凯微生物有限公司。
黑曲霉定量工作菌株 菌种编号:CMCC(F)98003批号:1450-2014,由杭州微球科技有限公司提供。
1.5 供试品
青翘感冒颗粒,由梅州市中医医院提供,批号20220309、20220323、20220412。
2.方法与结果
2.1 试验菌液的制备
取新鲜培养物(铜绿菌、金葡菌、枯草菌)接种至10 mL TSB(胰酪大豆胨)培养基中,35 ℃培养24 h,取此培养液1 mL 加pH7.0 无菌Nacl-蛋白缓冲液9 mL,采用10 倍递增稀释法制成1 000 ~10 000 cfu/mL 的菌悬液;取新鲜培养物(白念珠菌),接种至10 mL SDB 沙氏葡萄糖培养基中,25 ℃培养48 h,取此培养液1 mL 加pH7.0 无菌NaCl-蛋白缓冲液9 mL,采用10 倍递增稀释法制成每1 000 ~10 000 cfu/mL 的菌悬液;取黑曲霉定量工作菌株,用1.1 mL 复溶液溶解后,制成1 000 ~10 000 cfu/mL 的菌悬液。以上5 种试验菌用于微生物计数。另取铜绿假单胞菌、大肠埃希菌、乙型副伤寒沙门菌制成50 ~100 cfu/mL 的菌悬液,用于控制菌检查。菌液制备后若在实验室温室下放置的,则应在2 h 内使用完成;若保存在2 ~8 ℃的冰箱,则可在24 h 内使用[8-9]。
2.2 供试液的制备
取供试品1 0 g,加入TSB 胰酪大豆胨培养基至100 mL,制成1:10的供试液。取1:10的供试液,加入TSB 胰酪大豆胨培养基制成1:50、1:80 的供试液[10]。
2.3 微生物计数方法适用性试验
2.3.1 平皿倾注法 ①试验组:取1:10的供试液9.9 mL,加入上述(金葡、铜绿、枯草、白念、黑曲霉)5 种试验菌液各0.1 mL,混匀,使其每1 mL 供试液里的加菌量不大于100 cfu。取1 mL 注平皿,每株试验菌每种培养基制备2 个平皿。②供试品对照组:取1:10的供试液9.9 mL,加入TSB 胰酪大豆胨培养基0.1 mL,混匀,取1 mL 注平皿,平行制备2 个平皿[11]。③菌液对照组:取TSB 胰酪大豆胨培养基9.9 mL,同法加入上述(金葡、铜绿、枯草、白念、黑曲霉)5 种试验菌液各0.1 mL,进行微生物回收试验。以上各组平皿按照《中国药典》2020年版四部要求注入15 ~20 mL 温度不超过45 ℃融化的胰酪大豆胨琼脂培养基(用于需氧菌培养)和沙氏葡萄糖琼脂培养基(用于霉菌和酵母菌培养),混匀,凝固,倒置培养。测定各平皿菌落数,计算各试验菌回收率,结果见表1 和表2。提示需氧菌总数计数采用平皿倾注法(1:10)实验,金葡菌和枯草杆菌的回收率结果低于50%,霉菌和酵母菌总数计数试验菌回收率均在50%~200%范围内。表明青翘感冒颗粒对金黄色葡萄球菌和枯草芽孢杆菌具有一定的抑菌活性[12],采用平皿倾注法(1:10)不能消除其抑菌活性,霉菌和酵母菌总数计数可采用平皿倾注法(1:10)。

表1 平皿倾注法需氧菌系统适用性结果
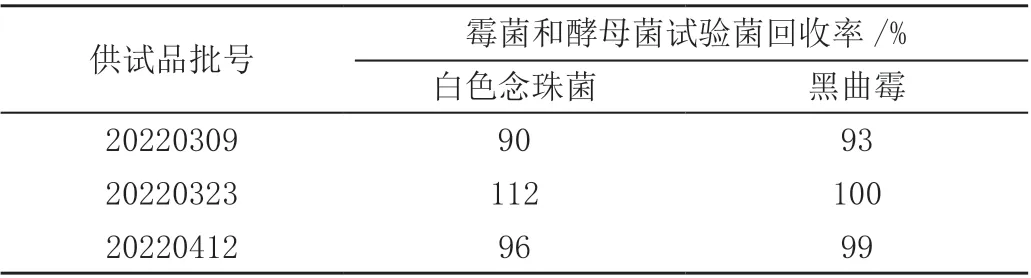
表2 平皿倾注法霉菌和酵母菌系统适用性结果
2.3.2 稀释法 ①试验组:取1:50、1:80 的供试液各9.9 mL,加入金葡球菌悬液(2.1)和枯草菌悬液(2.1)各0.1 mL,混匀,分别取1 mL 注皿,每株试验菌平行制备2 个平皿。并注入15 ~20 mL TSA(胰酪大豆胨琼脂)培养基,混匀,凝固,倒置培养24 h。测定各平皿菌落数,并计算金葡菌及枯草菌的回收率。②供试品对照组:取1:50、1:80 的供试液各9.9 mL,不加菌,以胰酪大豆胨液体培养基代替试验菌液,同试验组操作。③菌液对照组:取胰酪大豆胨液体培养基9.9 mL,加入试验组的2 种试验菌液各0.1 mL,其余操作同试验组。试验结果见表3。提示可知需氧菌总数计数采用稀释法,金黄色葡萄球菌和枯草芽孢杆菌回收率低于50%,表明采用稀释法不能去除其抑菌活性。
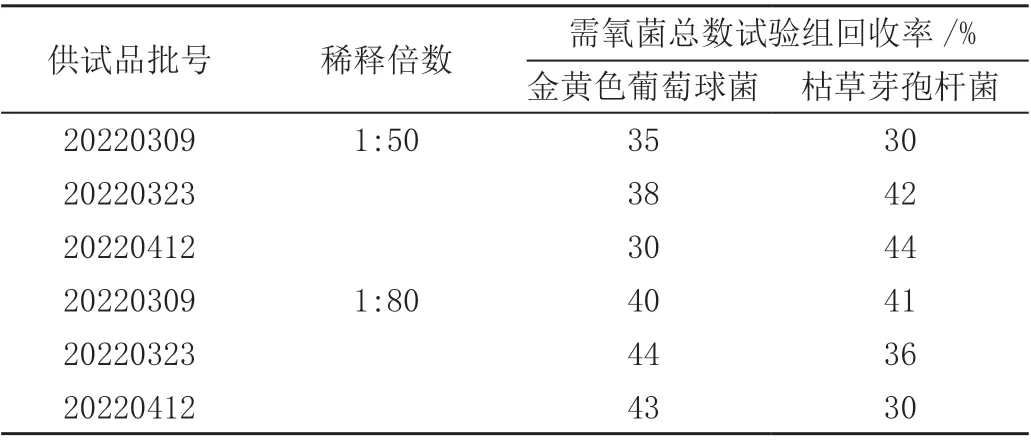
表3 稀释法需氧菌系统适用性结果
2.3.3 薄膜过滤法 ①试验组:取“2.2”项下1:10供试液1 mL 两组,分别加入置有100 mL 的pH7.0 无菌NaCl-蛋白缓冲液中,混匀,过滤。用pH7.0 无菌NaCl-蛋白缓冲液200 mL 进行滤膜冲洗两次,即100 mL/次,在第2 次1 0 0 mL 的冲洗液中分别加入≤100 cfu 的金葡球菌及枯草杆菌菌液,抽滤结束后,迅速将滤膜的菌面朝上放置于TSA 胰酪大豆胨培养基平板上。②供试品对照组:以稀释液代替试验菌液,其余同试验组制备。③菌液对照组:以稀释液代替供试液,其余同法按试验组制备。将上述试验组等各组平皿按照《中国药典》2020年版四部要求在规定条件下培养[13]。测定各组菌落,计算、即得各组回收率,结果金黄色葡萄球菌及枯草芽孢杆菌回收率均符合通则规定(50%~200%)的范围内,表明采用薄膜过滤法可去除青翘感冒颗粒的抑菌活性。取1:10 供试液和用于微生物计数的5 种试验菌液,按以上薄膜过滤法进行需氧菌总数计数方法适用性试验,见表4。
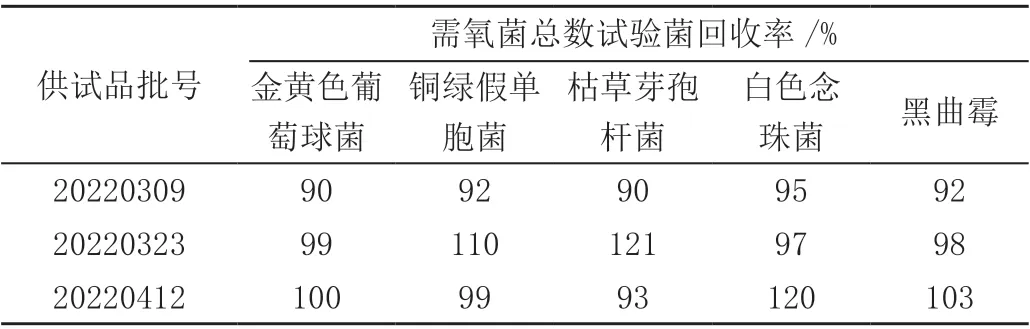
表4 薄膜过滤法需氧菌系统适用性结果
2.3.4 试验结果 由表4、表2 可知青翘感冒颗粒采用薄膜过滤法进行需氧菌总数计数方法适用性试验,采用平皿倾注法(1:10)进行霉菌和酵母菌总数计数方法适用性试验,各试验菌回收率均在50%~200%范围内,符合《中国药典》2020 年版规定,表明该方法有效、可行。
2.4 控制菌检查方法适用性试验(常规法)
(1)大肠埃希菌。取1:10 的供试液10 mL 和1.0 mL菌悬液(大肠埃希菌)(菌落数为50 ~100 cfu),加入到100 mL TSB(胰酪大豆胨培养基)中,混匀,于35 ℃的培养箱中培养24 h,即为试验组。取1:10 的供试液10 mL,以稀释液代替试验菌液,其余操作同试验组,作为供试品对照组。取TSB 代替供试液,其他同供试品对照组,作为阴性对照组。分别取上述TSB 培养物1.0 mL接种至100 mL MCB 麦康凯液体培养基中,置44 ℃培养箱中培养24 h。取上述MCB 培养物划线接种于MAC(麦康凯琼脂培养基平板)上,于35 ℃培养箱中培养18 h。(2)耐胆盐革兰阴性。取1:10 的供试液,25 ℃预培养2 h。分别取1 mL 的预培养物各2 份,1 份加入铜绿假单胞杆菌悬液(不大于100 cfu),1 份加入大肠埃希菌悬液(不大于100 cfu),接种至10 mL 肠道菌增菌液体培养基中,35 ℃培养48 h,作为试验组。取1 mL 预上述肠道菌增菌液接种至10 mL 肠道菌增菌液体培养基中,作为供试品对照组。取TSB 代替供试液,其他同供试品对照组,作为阴性对照组[14]。取上述EE 培养物接种划线在VRBGA(紫红胆盐葡萄糖琼脂培养基)平板上,于35 ℃培养箱中培养18 h。(3)沙门菌。①试验组:取供试品10.0 g,加入沙门1.0 mL 菌悬液(≤100 cfu),直接接种至100 mL TSB 胰酪大豆胨培养基中,混匀、培养箱35 ℃培养24 h。取上述培养物0.1 mL 接种至10 mLRV 沙门菌增菌液体培养基中,培养箱35 ℃培养24 h。取少量培养物(RV 沙门菌增菌液中)划线接种于木糖赖氨酸脱氧胆酸盐琼脂培养基(XLD)平板上,35 ℃培养48 h。②供试品对照组:取供试品10 g,直接接种至100 mL 胰酪大豆胨液体培养基中,其余操作同试验组。③阴性对照组:以TSB 代替供试液,其他同供试品对照组,作为阴性对照组。(4)试验结果。以上各组控制菌检查试验结果见表5。提示采用常规法进行控制菌检查方法适用性试验,试验组均能检出试验菌,阴性对照组均无菌落生长,表明该试验方法可行。

表5 控制菌检查方法适用性结果

表6 控制菌检查方法适用性结果
3.讨论
微生物是具繁殖力的活细胞,其在药品中会受到种种因素的影响处于不稳状态,导致检验结果的不准确,如药品储存条件、供试品的组合、原料来源、生产工艺的差别、检验方法的不同等都可造成结果的差异,影响因素中供试品的组合尤为重要。有些本身含有抑菌成分,如中药黄芩、冰片、青黛中都含有较强的杀菌成分,而在一定浓度下,对微生物仅起到抑菌作用,如抑菌成分消除或浓度降低,仍可生长、繁殖。采用常规法检验往往会显示假阴性的结果,还有些药品为保证质量,需在低温甚至冷冻环境中保存,可使细菌存活状态发生改变,呈休眠状态。因此微生物检验时应根据以上所述的种种情况采用不同的检验方法,使微生物处于稳定状态后,检验结果才能反映药品的真实污染状况[15]。
由于药品的抑菌活性会影响到微生物限度检查的准确性,为了消除其抑菌活性,本试验从常规法入手[16]。由微生物计数方法适用性试验结果可知青翘感冒颗粒中的成分对金黄色葡萄球菌、枯草芽孢杆菌有抑菌活性,采用常规的平皿倾注法不能进行需氧菌总数计数。本试验选择稀释法,制备1:50、1:80 的供试液对需氧菌总数计数进行方法适用性试验,结果表明,采用稀释法不能消除其抑菌活性。进一步选择薄膜过滤法,结果提示,各试验菌回收率均在50%~200%范围内,符合《中国药典》2020 年版有关规定,确定需氧菌总数计数采用薄膜过滤法;霉菌和酵母菌总数计数采用平皿倾注法(1:10);青翘感冒颗粒对控制菌无抑菌活性,可采用常规法进行控制菌检查。
