智能手机辅助铜纳米团簇比率荧光探针检测四环素
2023-01-03崔曦鹏李彦月张娟陈子繁罗洪陈辉何瑜
崔曦鹏,李彦月,张娟,陈子繁,罗洪,陈辉,何瑜
(1.湖北大学化学化工学院,湖北 武汉 430062;2.湖北省轻工业科学研究设计院有限公司,湖北 武汉 430052)
0 引言
四环素(Tc)是一种广谱抗生素,广泛用于革兰氏阳性和革兰氏阴性细菌胞内支原体、衣原体和立克次体引起的感染,对病原微生物具有很好的抑菌活性[1].四环素具有成本低、低毒等优点,已广泛应用于各领域[2-3].近年来,由于四环素在水产养殖、畜牧业和食品生产中的滥用使其残留造成了严重的环境污染[4].目前检测四环素的传统方法主要有高效液相色谱法[5],液体相色谱分析-质谱法[6],毛细管电泳法[7],电化学分析法[8],化学发光法[9],比色测定法[10]等.然而,这些方法的设备昂贵、操作复杂、耗时较长,不利于现场实时有效的检测四环素.因此,迫切需要建立一种快速、简便的方法来实现对四环素残留的实时检测.荧光分析法因具有成本低、操作简单、灵敏度高、检测限低、选择性好等优点,成为检测四环素的一种非常适用的方法.
镧系离子及其配合物因具有较大的斯托克斯位移,发光量子产率高和荧光寿命长等优点而受到人们的关注[11-12].值得注意的是,铕离子(Eu3+)可以特异性识别Tc,形成铕-四环素配合物(Eu-Tc),具有红色荧光发射,能有效降低背景干扰和散射荧光,并且基于天线效应(AEE),Tc将吸收的能量转移到Eu3+,使Eu3+的荧光增强[13].然而由于环境中配位水分子振动会导致荧光猝灭,Eu-Tc的荧光强度通常较弱[14],使得检测的灵敏度和稳定性较差,在实际应用中受到限制.比率型荧光探针由于其独特的抗干扰特性而在实际应用中成为一种更准确灵敏的方法.Cu NCs作为一种新型的环保型纳米材料,因其成本低,易制备,生物相容性好等优点而受到广泛关注.
本研究采用绿色环保的蛋清作保护剂制备的绿色荧光铜簇(EW-Cu NCs)作为内参比,结合Eu3+构建比率荧光纳米探针用于Tc的检测.在这种双发射传感器中,EW-Cu NCs作为能量供体增强Eu-Tc的发射,Eu3+作为特异性识别单元与Tc形成配合物,通过AEE使Eu3+产生红色荧光,同时由于EW-Cu NCs与Tc之间的内滤效应,使得EW-Cu NCs荧光被猝灭.因此,随着Tc的不断加入,Eu3+的荧光发射显著增强,而Cu NCs的荧光发射强度逐渐降低,且溶液伴随有明显的颜色变化(由绿色逐渐变为红色).此外,通过检测过程中荧光颜色的变化,可以利用智能手机采集颜色信号,通过颜色识别器软件将颜色信号转化为数据信号进行分析计算,从而实现定量检测.无需昂贵的仪器即可完成可视化比色传感,为Tc检测提供了一种新的策略.最后荧光法和智能手机比色法共同验证牛奶中四环素检测的可靠性,具有较高的灵敏度和出色的快速检测效果.
1 实验部分
1.1 实验材料与试剂氯化铕、四环素、土霉素、氯霉素、盐酸多西环素购自阿拉丁有限公司(上海),无水乙醇购自国药集团化学试剂有限公司(上海),氢氧化钠购自天津博迪化工公司(天津).
1.2 实验仪器Lambda 35型紫外光谱仪;LS55型荧光光谱仪(FL);Spectrum one型傅里叶红外光谱仪(FT-IR);Escalab 250Xi 型X线光电子能谱仪(XPS);Tecnai G20 F30型透射电子显微镜(TEM);JEM-2100 UHR型高分辨透射电子显微镜(HRTEM).
1.3 EW-Cu NCs的制备本实验中,柠檬酸(CA)作为还原剂,利用氯化铜(CuCl2)和鸡蛋清(EW)合成了具有绿色荧光发射的EW-Cu NCs.把鸡蛋清从整个新鲜鸡蛋中分离出来并用均质器均质化备用,再将3.0 mL CuCl2(0.01 mol/L)溶液和3.0 mL 蛋清(EW)溶液在反应试剂瓶中混合搅拌5 min使其均匀,加入1.0 mL CA(1 mol/L)溶液,在室温下搅拌反应2 h.反应结束后将所得溶液以6 000 r/min 离心10 min,取上清液于4 ℃下保存备用.
1.4 EW-Cu NCs/Eu3+荧光传感器检测四环素将50 μL EW-Cu NCs和100 μmol/L EuCl3以及80 μL NaOH(1 mol/L)充分混合,超纯水稀释至总体积为2 mL,形成荧光传感体系,室温下反应2 min至探针溶液荧光稳定,之后将不同浓度的四环素溶液加至反应体系中(混合溶液中四环素最终浓度为0.25~72.50 μmol/L),在最佳反应时间4 min时,用荧光分光光度计在激发波长为390 nm下记录反应混合体系526 nm和616 nm处的荧光强度变化.并用智能手机拍摄365 nm紫外灯照射下的不同浓度四环素存在下混合溶液的照片.
1.5 EW-Cu NCs/Eu3+作为荧光探针的选择性为了进一步研究这种EW-Cu NCs/Eu3+荧光探针的选择性,测试了该传感器对以下潜在干扰物质的荧光响应,包括常见的无机离子(K+,Mg2+,Ca2+,Na+,Al3+,Zn2+,Fe2+,Mn2+)和代表性氨基酸色氨酸(Trp),精氨酸(Arg),半胱氨酸(Cys),甘氨酸(Gly),组氨酸(His),以及谷胱甘肽(GSH),抗坏血酸(AA)和葡萄糖(Glucose),还有抗生素类物质土霉素(OTC),氯霉素(CHL),盐酸多西环素(DOX).与1.4所述的实验条件相同,用相同浓度的上述选择性物质代替Tc进行反应,激发波长390 nm下记录溶液在526 nm和616 nm处的荧光强度值变化.
1.6 EW-Cu NCs/Eu3+作为荧光探针对实际样品检测牛奶样品在超市中购买,为了去除牛奶中的蛋白质和脂质,根据文献的方法进行了一些操作.通常,将乙酸加入牛奶样品中,调至pH值为6,超声处理20 min,然后以10 000 r/min离心10 min.最后用0.22 μm滤膜过滤上清,去除沉淀.将不同浓度四环素溶液加标到制备的牛奶上清液中,以EW-Cu NCs/Eu3+探针溶液进一步检测,四环素最终加标浓度为5 μmol/L,10 μmol/L和20 μmol/L.将得到的溶液混合孵育4 min,记录其发射光谱(λex= 390 nm).
2 结果与讨论
2.1 EW-Cu NCs的表征分别用FL、TEM、XPS、和FT-IR等方法对EW-CuNCs进行了表征,并对其进行稳定性探究.如图1(a)所示,制备的EW-Cu NCs水溶性良好,且在紫外光下呈现出较强的绿色荧光,在最佳激发波长444 nm处出现了526 nm处的发光峰,如图1(a)插图所示,EW-CuNCs具有较强的绿色荧光,其量子产率为14.5%,荧光稳定性极佳.如图1(b)所示的TEM图谱,EW-Cu NCs的分散性良好,平均粒径为2.8 nm,HRTEM图像显示的EW-Cu NCs晶格条纹间距为0.315 nm.从图1(c)中Cu NCs的XPS光谱可以看出,在932.6 eV和952.3 eV处有两个明显的特征峰,分别归属于Cu(0)的2p3/2和2p1/2电子的结合能,表明Cu2+被成功还原为Cu NCs.从图1(d)可以看出,与EW的FT-IR光谱相比,O—H或N—H的特征吸收峰从3 300 cm-1位移到3 575 cm-1,C—H在2 959 cm-1处的伸缩振动位移到3 015 cm-1,表明EW-Cu NCs的形成.
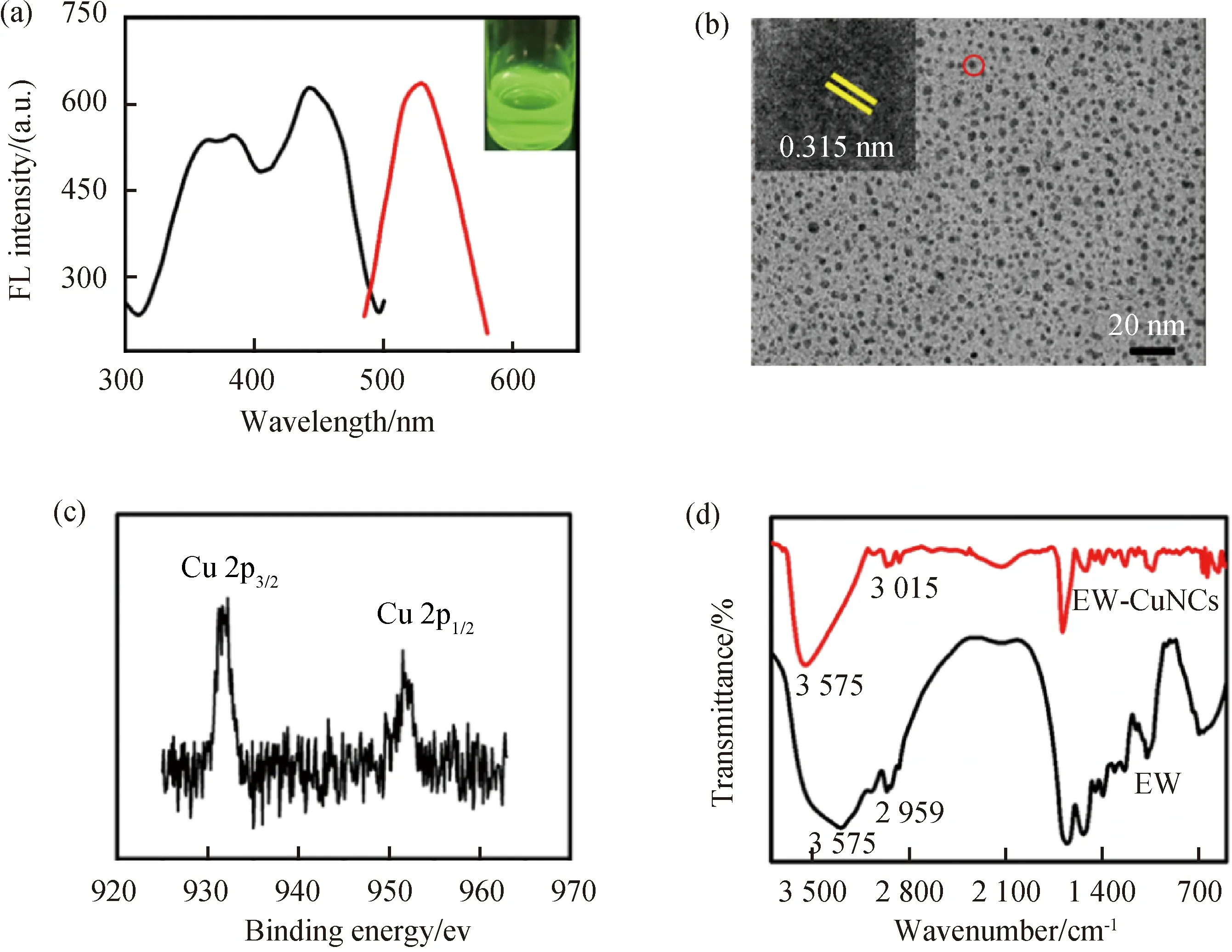
图1 EW-Cu NCs的(a)FL谱图、(b)TEM图,(c)Cu 2p 的XPS谱图和(d)EW的FT-IR谱图
2.2 EW-Cu NCs/Eu3+检测四环素的可行性在本实验中,所合成的EW-Cu NCs 在紫外灯下呈绿光.如图2,在激发波长390 nm的激发下,在526 nm处有最强荧光峰.由于配位水分子振动模式引起的猝灭效应使得Eu3+荧光较弱,EW-Cu NCs/Eu3+传感器在这一阶段表现出EW-Cu NCs的绿色荧光.然后,随着Tc的引入,由于对Tc与Eu3+的配位强度较高,Tc可以取代水分子与Eu3+配合,将吸收的能量转移到Eu3+,通过AEE使Eu3+产生红色荧光,强度逐渐增强,而EW-Cu NCs荧光逐渐被Tc猝灭.这是因为EW-Cu NCs的激发光谱与Tc的发射光谱之间高度重叠(图3(a)),表明两者之间存在内滤效应,由此两个发射峰强度各自发生变化.可以看到,加入 Tc后,Eu3+(616 nm)的荧光被激活,而EW-Cu NCs (526 nm)的荧光被猝灭(图3(b)).荧光颜色由绿色变为红色,荧光的颜色变化非常明显,可以通过肉眼轻松区分.因此,传感系统的荧光变化主要归因于Eu3+与Tc之间的相互作用,从而有可能进行Tc检测.

图2 EW-Cu NCs/Eu3+荧光探针基于天线效应检测Tc的示意图
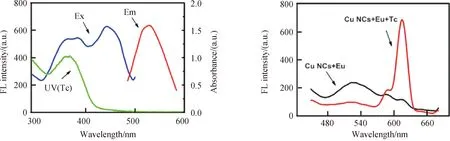
图3 (a)Cu NCs的荧光激发和发射光谱以及Tc的紫外吸收光谱和(b)激发波长为390 nm时,混合溶液EW-Cu NCs/Eu3+添加Tc前后的发射光谱图(Eu3+浓度为100 μmol/L,Tc浓度为72.50 μmol/L)
2.3 EW-Cu NCs/Eu3+作为荧光探针检测四环素为了使探针对Tc的响应效果达到最大,通过监测EW-Cu NCs/Eu3+在526 nm和616 nm处的发射强度变化,考察了Eu3+浓度、反应时间检测条件.如图4(a)所示,向反应体系中添加50 μmol/L Tc,当Eu3+浓度为100 μmol/L时,体系的荧光强度比值I616/I526最大.在此最佳Eu3+浓度条件下又研究了I616/I526随时间的响应变化,如图4(b)结果显示,I616/I526的比值在4 min内基本稳定,所以我们选择了4 min为反应时间进行后续的Tc检测.在优化条件下,EW-Cu NCs/Eu3+检测系统的两个荧光峰强度随着Tc加入浓度的变化趋势如图5(a)所示,从图5(b)可以看出,在0.25~72.50 μmol/L范围内,荧光强度比值I616/I526与Tc浓度呈良好的线性关系.通过拟合得到工作曲线为I616/I526=0.096CTc+0.73(R2=0.985),检测限为80 nmol/L.在本体系中,随着Tc浓度的增加,传感器的荧光经历了从绿色到橙色再到红色的变化(图6(a)).表1比较了本实验方法与其他Tc检测方法相类似的文献.
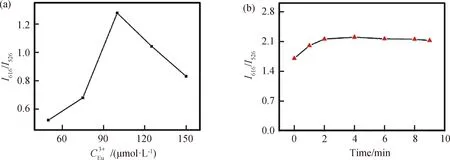
图4 (a)Eu3+浓度,(b)反应时间对EW-Cu NCs/Eu3+体系响应Tc程度的影响
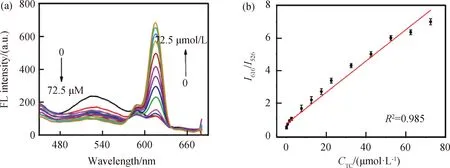
图5 (a)EW-Cu NCs/Eu3+探针随Tc浓度在0~72.50 μmol/L范围内的荧光光谱变化图,(b)0.25~72.50 μmol/L内,Tc浓度与荧光强度比I616/I526的线性关系
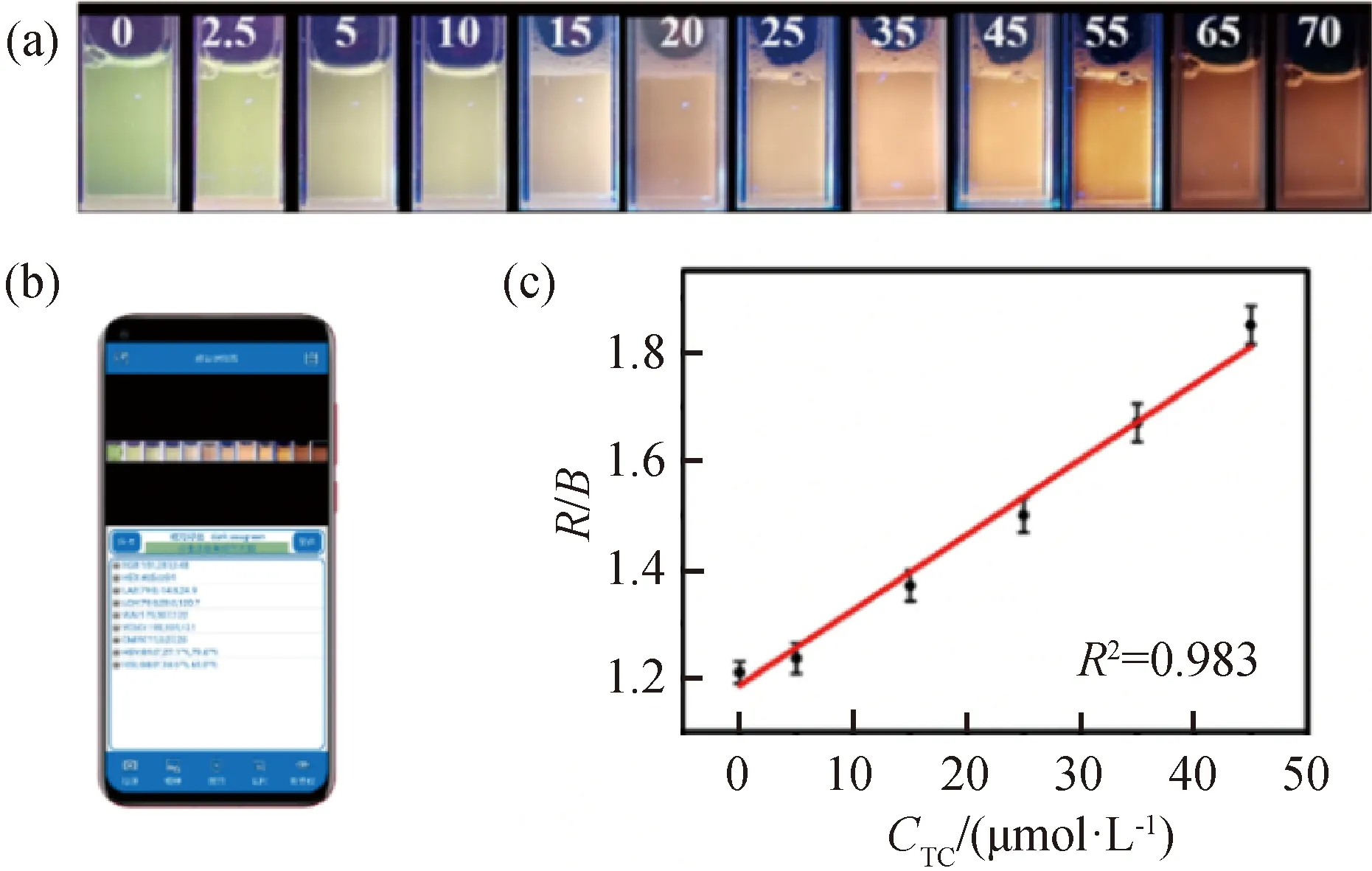
图6 (a)不同浓度Tc(0,2.5,5,10,15,20,25,35,45,55,65 和 70 μmol/L)存在下Cu NCs-Eu在365 nm紫外灯下的荧光照片,(b)安装颜色识别器软件的智能手机,(c)R/B值与2.5~45.0 μmol/L浓度范围Tc的线性关系
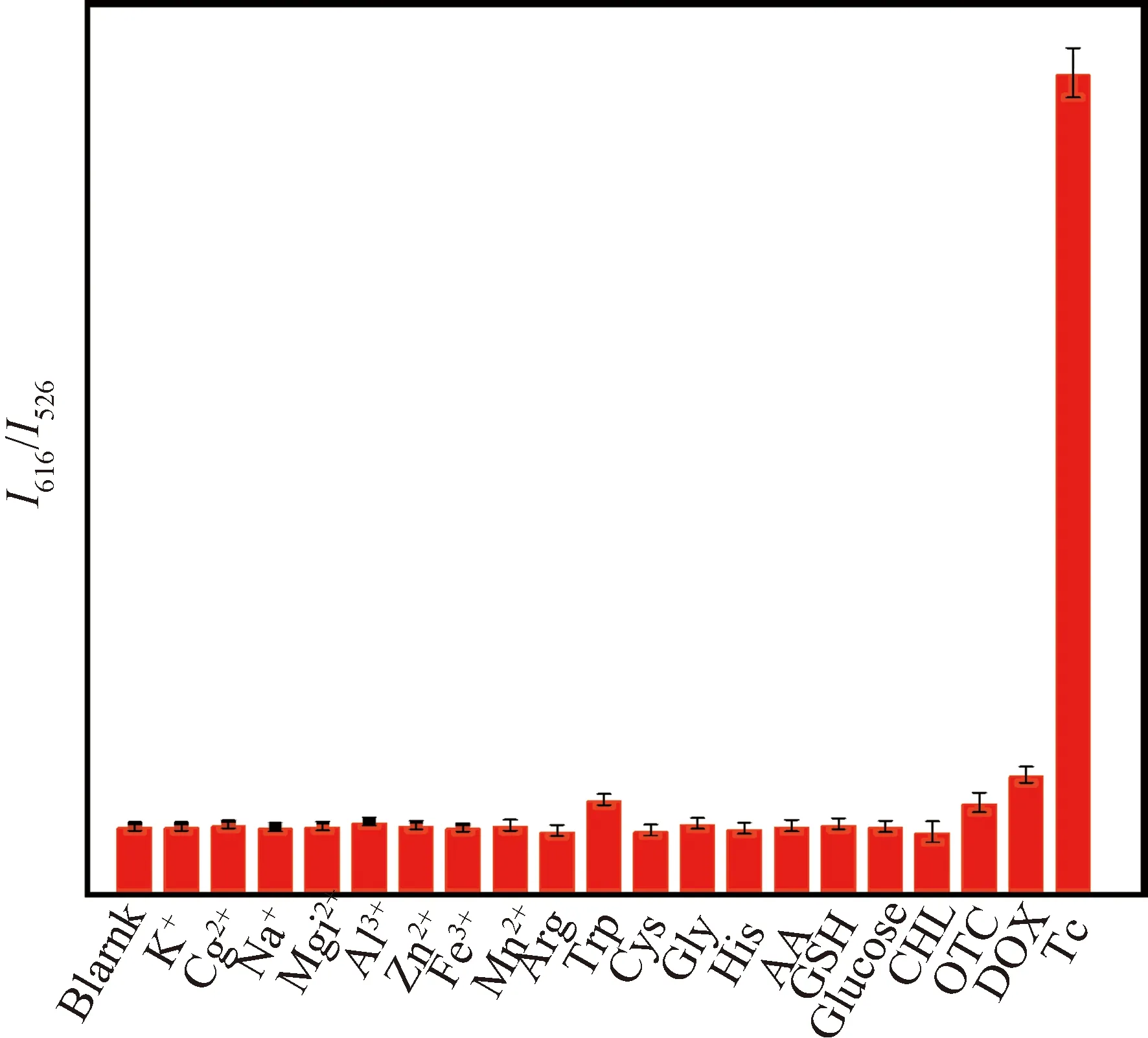
图7 EW-Cu NCs/Eu3+荧光探针对不同干扰物质的选择性测试
2.4 数字图像比色分析随着Tc的加入,检测体系溶液的荧光颜色由绿色逐渐转变为红色,为可视化传感检测提供了可能.在365 nm紫外灯激发下,用智能手机拍摄不同Tc浓度下混合物溶液颜色的变化(图6(a)).利用颜色识别器软件读取图片颜色,依次进行RGB值输出,最后对其进行数据处理(图6(b)).从图6(a)中选出的点做的图6(c)可以看出,R/B与2.5~45 μmol/L范围内Tc浓度呈良好的线性关系.通过拟合得到工作曲线为R/B=0.014CTc+1.19(R2=0.983),进而实现比色法定量分析.
2.5 EW-Cu NCs/Eu3+对四环素检测的选择性为验证本实验方案对四环素检测是否具有良好的选择性,我们选择常见的无机离子,氨基酸,GSH,AA,葡萄糖和一些四环素族抗生素氯霉素CHL,土霉素OTC,盐酸多西环素DOX(均为80 μmol/L)代替四环素进行探究,在相同的实验条件下测量探针荧光强度比值,实验结果如图7所示,与其他抗生素相比,EW-Cu NCs/Eu3+对Tc特异性响应,在Tc存在下I616/I526的比值发生了很大的变化,这是由于Tc与Eu3+形成配合物,从而激活了Eu3+的荧光发射.而其他潜在的干扰物质对EW-Cu NCs/Eu3+体系的影响较小,可以忽略不计,表明该探针对四环素的检测具有良好的选择性和特异性,证实了此比率探针在复杂环境中应用的可行性.

表1 不同荧光探针检测Tc的线性范围和检测限比较
2.6 EW-Cu NCs/Eu3+对实际样品中四环素的检测利用所开发的探针检测实际牛奶样中的四环素,验证了该传感器的潜在应用,检测结果呈现在表2中.结果表明,加标浓度与标准值比较接近,加标回收率为98%~105%,相对标准偏差1.7%~4.2%.这些结果表明,此荧光传感器在实际样品分析中具有一定的可靠性和良好的适用性.

表2 探针对实际样品牛奶中Tc的检测
3 结论
开发了EW-Cu NCs/Eu3+比率型荧光传感器用于四环素的定量检测.得到检测四环素的线性范围为0.25~72.50 μmol/L,最低检测浓度为80 nmol/L.根据检测过程中的溶液荧光颜色变化可以构建可视化传感器,并借助智能手机的颜色识别软件进行比色法定量分析,得到了2.5~45.0 μmol/L的线性检测范围.此外,EW-Cu NCs/Eu3+在Tc的检测应用中具有高选择性和特异性,最后对实际样品牛奶进行四环素加标检测,获得满意的回收率(98%~105%),表明此类探针在食品安全分析的应用中具有很好的应用前景.
