Co3O4负载rGO/g-C3N4臭氧光催化降解2,4-二氯苯氧乙酸活性研究
2023-01-03毛艳丽康海彦宋忠贤闫晓乐罗宏宇朱新锋
潘 龙,延 旭,毛艳丽,康海彦,宋忠贤,张 霞,闫晓乐,罗宏宇,朱新锋,胡 泊
(1.河南城建学院 市政与环境工程学院,河南 平顶山 467000; 2.辽源市食品质量安全检测中心, 吉林 辽源 136200)
在现代农业的发展进程中,化学除草剂的广泛应用,极大的推动了作物产量和品质的提升,生产效率的提高[1-3]。化学除草剂在使用过程中有少部分会进入环境当中,长期使用很容易引发生态及环境问题[4-6]。2,4-二氯苯氧乙酸(2,4-D)作为一种典型的化学除草剂,具有效率高,成本低的显著优势,但其化学性质稳定,难以自然降解。环境中痕量的2,4-D对眼睛和皮肤均具有刺激作用,会引发多种疾病的患病几率,具有一定的生物毒性和致癌性,严重威胁生态和饮水安全[7]。因此,探寻稳定高效、绿色节能的处理技术消除环境水体中痕量的2,4-D除草剂具有重要意义,也是水处理技术领域亟待解决的科学难题[8-9]。

本文采用多种技术制备了Co3O4/rGO/g-C3N4三元复合材料,以2,4-D为目标污染物深入考察光照、臭氧和各组分浓度对反应体系降解活性的影响,对Co3O4/rGO/g-C3N4臭氧光催化降解2,4-D的稳定性和臭氧-光催化反应机理进行了深入研究,为2,4-D处理技术的发展和催化体系的研究起到了积极作用。
1 实 验
1.1 实验试剂
本实验采用的尿素(CH4N2O)、乙酸钴(C4H6CoO4·4H2O)、乙醇(C2H5OH)、三氯甲烷(CHCl3)、乙二胺四乙酸二钠(EDTA-2Na)和叔丁醇(tBA)等化学试剂均为分析纯,氧化石墨烯采购于南京先丰纳米科技有限公司。
1.2 材料制备
1.2.1 g-C3N4制备
将10 g尿素放入到容积50 mL带盖的陶瓷坩埚中,用马弗炉以2.3 ℃/min的升温速率升温至550 ℃保持6 h后,待马弗炉自然冷却至室温后收集坩埚中得到的g-C3N4淡黄色粉末[26],记为GCN。
1.2.2 Co3O4/g-C3N4制备
称取50 mg GCN加入到50 mL乙醇中,持续搅拌、超声30 min,然后加入适量的乙酸钴,将以上混合液置于80 ℃下均匀搅拌,收集溶液蒸干后得到的暗黄色沉淀,在氩气氛围下以10 ℃/min的升温速率,在400 ℃下保持4 h,待反应结束自然冷却后收集得到灰色粉末。通过调节乙酸钴的用量(2.075、4.15、8.3、16.6和166 mg)得到Co3O4质量含量分别为0.25%、0.5%、1%和3%的样品,分别记为0.25Co3O4/GCN,0.5Co3O4/GCN,1Co3O4/GCN,3Co3O4/GCN。采用如上实验过程,不加入g-C3N4来制备纯Co3O4样品。
1.2.3 rGO/g-C3N4制备
在35 mL去离子水中加入适量氧化石墨烯(GO),超声搅拌分散均匀后加入200 mg的GCN样品继续超声搅拌2 h,然后将GO与GCN混合液移入50 mL的水热釜中,在180 ℃下反应6 h,待反应结束自然冷却后,收集反应釜中的沉淀,用乙醇和去离子水清洗数次,烘干备用。调节GO用量为GO和g-C3N4的质量比分别0.25,0.5,1和3来得到不同rGO/GCN样品,分别记为0.25rGO/GCN,0.5rGO/GCN,1rGO/GCN,3rGO/GCN。
1.2.4 Co3O4/rGO/g-C3N4制备
称取50 mg不同rGO/GCN样品加入到50 mL乙醇中,持续搅拌、超声30 min,然后加入适量的乙酸钴,将以上混合液置于80 ℃下均匀搅拌,收集溶液蒸干后得到灰色沉淀,在氩气氛围下以10 ℃/min的升温速率,在400 ℃下保持4 h,待反应结束自然冷却后收集得到灰色粉末,控制乙酸钴用量得到Co3O4质量含量分别为0.25%、0.5%、1%和3%的Co3O4/0.25rGO/g-C3N4样品,分别标记为0.25Co3O4/0.25rGO/GCN,0.5Co3O4/0.25rGO/GCN,1Co3O4/0.25rGO/GCN,3Co3O4/0.25rGO/GCN。
1.3 材料表征
利用X射线衍射(XRD)分析材料的晶体结构和组成;通过场发射扫描电子显微镜(SEM)、透射电子显微镜(TEM)观察材料的微观结构;利用傅里叶红外光谱(FT-IR)对材料中的化学键和化学基团进行分析检测;利用X射线光谱(XPS)分析样品的元素组成、化学态和电子态;采用紫外可见漫反射光谱(UV-Vis)表征所制备材料的光吸收特性(波长范围200~800 nm);采用电化学工作站CHI-660E和CHI-825C分别测试所制备样品的阻抗和瞬态光响应时间-电流性能;采用紫外-可见分光光度计在λmax=283 nm下测定降解过程中2,4-D的浓度变化情况。
1.4 实验过程
1.4.1 臭氧光催化实验
以氙灯为光源,在可见光(300 W,λ>420 nm)照射下,配制100 mL质量浓度为10 mg/L的2,4-D溶液,并加入到光催化反应器中。然后,加入50 mg制备好的催化剂,超声、搅拌分散均匀后在黑暗条件下持续搅拌30 min,以达到 2,4-D和催化剂之间的吸附-脱附平衡。然后,同时开启臭氧发生器(臭氧质量浓度为14.2 mg/L,流速为30 mL/min)和氙灯光源,每间隔10 min进行取样,经过充分离心后取上层清液测试2,4-D的浓度(λmax=283 nm),并计算降解率。
1.4.2 对照试验
仅使用氙灯可见光(300 W,λ>420 nm)照射进行反应或通入臭氧进行臭氧氧化实验来测试不同样品的光催化活性以及臭氧氧化活性,其他实验参数和实验步骤与臭氧光催化实验过程一致。
1.4.3 光电性能测试
采用三电极装置测得样品的瞬态光响应时间-电流和电化学阻抗谱(EIS)数据。测试过程中,采用Pt丝作为对电极,催化剂为工作电极,Ag/AgCl为参比电极,以0.5 mol/L的Na2SO4为电解液,在0.5 V偏压下用300 W,光强为45 mW/cm2的氙灯照射。以旋涂法将催化剂粉末涂覆在FTO导电玻璃上作为工作电极进行测试。
1.4.4 捕获实验
在臭氧光催化实验的暗反应前,分别加入1 mmol三氯甲烷(CHCl3)、乙二胺四乙酸二钠(EDTA-2Na)和叔丁醇(tBA),然后进行暗反应[19]。暗反应结束后开始光照,其他反应条件和步骤与臭氧光催化反应过程一致。
2 结果与讨论
2.1 XRD结果与分析
不同样品的相组成结果如图1所示,可以看出,氮化碳(CN)样品在13.2°和27.5°的衍射峰为石墨相氮化碳的特征峰,表明制备的样品为g-C3N4。经过水热反应与CN形成的rGO/GCN复合材料中并未观察到此特征峰,这是由于石墨烯浓度过低所引起,通过扫描电镜可以确定石墨烯的存在。此外,Co3O4的特征峰位于32°、37°、59°和66°,特征峰的位置和相对高度与Co3O4的XRD标准卡片(JCPDS No.43-1003)一致[27],表明成功制备了氧化钴样品,但是,与石墨烯和氮化碳进行复合生长后,特征峰消失,调节氮化碳、氧化钴和石墨烯的浓度比例结果仍然不变,这是由于样品中的氧化钴含量过低所引起。

图1 不同样品的XRD测试结果Fig.1 XRD patterns of different samples
2.2 SEM和TEM测试结果
为了研究所合成样品的微观结构和形貌特征,对不同样品进行SEM分析,结果如图2所示。可以看出,Co3O4由尺寸约为30~50 nm的颗粒堆积而成,如图2(a)所示。图2(b)为Co3O4与GCN的复合样品,可以看出GCN为层状结构,表面并未观察到Co3O4堆积情况出现,表明GCN的二维结构能显著提高Co3O4合成过程中Co2+离子的分散性,降低生成的纳米颗粒尺寸。在0.5Co3O4/0.25rGO/GCN样品中(图2(c))可看到rGO薄层,但是没有观察到Co3O4纳米颗粒,这是由于rGO和GCN比表面积比较大,合成过程中Co2+离子分散在rGO和GCN表面,经过反应得到的Co3O4纳米颗粒尺寸进一步减小,分散度进一步增加所引起的。图2(d)为0.5rGO/GCN样品的SEM测试结果,可以看出,rGO和GCN可以形成复合材料,负载高浓度的rGO也不会对GCN的形貌产生任何影响。对样品进行TEM测试(图2(e)、(f)),可以看出,Co3O4纳米颗粒的尺寸约为3~5 nm,这是由于石墨烯和GCN提高了氧化钴纳米颗粒的分散度所致。

图2 Co3O4(a),0.5Co3O4/GCN(b),0.5Co3O4/0.25rGO/GCN(c)和0.5rGO/GCN(d)的SEM图以及0.5Co3O4/0.25rGO/GCN的低倍TEM图像(e)和图(e)中箭头位置的局部放大图(f)Fig.2 SEM images of Co3O4(a), 0.5Co3O4/GCN (b), 0.5Co3O4/0.25rGO/GCN (c), and 0.5rGO/GCN (d); low-magnification TEM image of 0.5Co3O4/0.25rGO/GCN (e) and partial enlarged view of the arrow position in fig.(e)(f)
2.3 XPS结果与分析

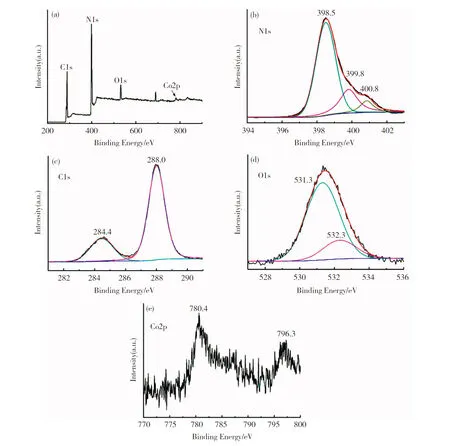
图3 0.5Co3O4/0.25rGO/GCN样品的XPS测试结果Fig.3 XPS spectra of 0.5Co3O4/0.25rGO/GCN sample:(a) full spectrum; (b) N1s; (c) C1s; (d) O1s; (e) Co2p
2.4 UV-vis结果与分析
图4为所制备的不同光催化剂样品在200~700 nm范围的紫外可见吸收光谱图。在所有样品中,GO和Co3O4在整个波长范围内都具有较高的吸收强度,这是由于GO自身的超强光吸收特性和Co3O4的窄带隙所致。GCN样品的光吸收边约位于425 nm处,当表面负载0.5wt.%的石墨烯或Co3O4后,光吸收边发生明显红移,在可见光和紫外区的光吸收性能得到提升。值得注意的是,当减少GO用量时,制备的0.25rGO/0.5Co3O4/GCN复合样品在可见光范围的吸收强度高于0.5rGO/GCN和0.5Co3O4/GCN样品,这是由于较低的GO浓度能增加光的透过性,提升了Co3O4的光吸收能力,整体吸光性能明显增强,也表明调节rGO、Co3O4和GCN三者的浓度比例来调节三元复合光催化剂吸光性能和光催化活性的重要性。利用下式来分析Co3O4半导体的禁带宽度[30]

图4 不同样品的紫外可见吸收光谱图及Co3O4样品的能带分析Fig.4 UV-vis DRS of different samples and band-gap analysis of Co3O4sample
αhν=A(hν-Eg)n/2
(1)
式中:α为吸收系数,cm-1;h为普朗克常量;Eg为禁带宽度;eV;ν是光的频率;A为吸收常数。
Co3O4为直接带隙半导体,n取1,通过计算得出相应的禁带宽度为1.4 eV。采用下式对Co3O4的价、导带位置进行分析[31]:
EVB=X-Ee+0.5Eg
(2)
ECB=EVB-Eg
(3)
式中:X为半导体内部各原子绝对电负性的几何平均值;Ee为标准氢电极下自由电子的能量,Ee=4.5 eV;EVB和ECB为价带和导带电位。通过计算可知,Co3O4的X值为5.903,进而求出EVB和ECB分别为2.1和0.7 eV。
2.5 红外光谱分析


图5 不同样品的FT-IR谱图Fig.5 FT-IR spectra of different samples
2.6 光电流性能测试
众所周知,光催化材料的光电流强度对光催化活性具有重要影响,我们对GCN,0.5Co3O4/GCN,0.5rGO/GCN和0.5Co3O4/0.25rGO /GCN样品的光电流-时间相应曲线进行了测定,如图6所示。在相同实验条件下,0.5Co3O4/0.25rGO/GCN样品具有最大的光电流强度,约为GCN样品的10倍,表明与rGO和Co3O4形成复合材料后能有效促进光生电子和空穴对的分离,并且经过多次测试后光电流强度没有明显降低。

图6 不同光催化剂样品的光电流性能曲线Fig.6 Transient photocurrent response of different photocatalyst samples
此外,0.5Co3O4/GCN和0.5rGO/GCN样品的光电流强度较GCN样品也有一定提升,但明显低于0.5Co3O4/0.25rGO/GCN样品,表明复合材料中各组分浓度比例对三元复合材料的光电流性能具有重要影响。
2.7 臭氧光催化活性分析
在可见光照射下,以2,4-D为目标污染物,研究不同样品的臭氧光催化活性,实验结果如图7所示。
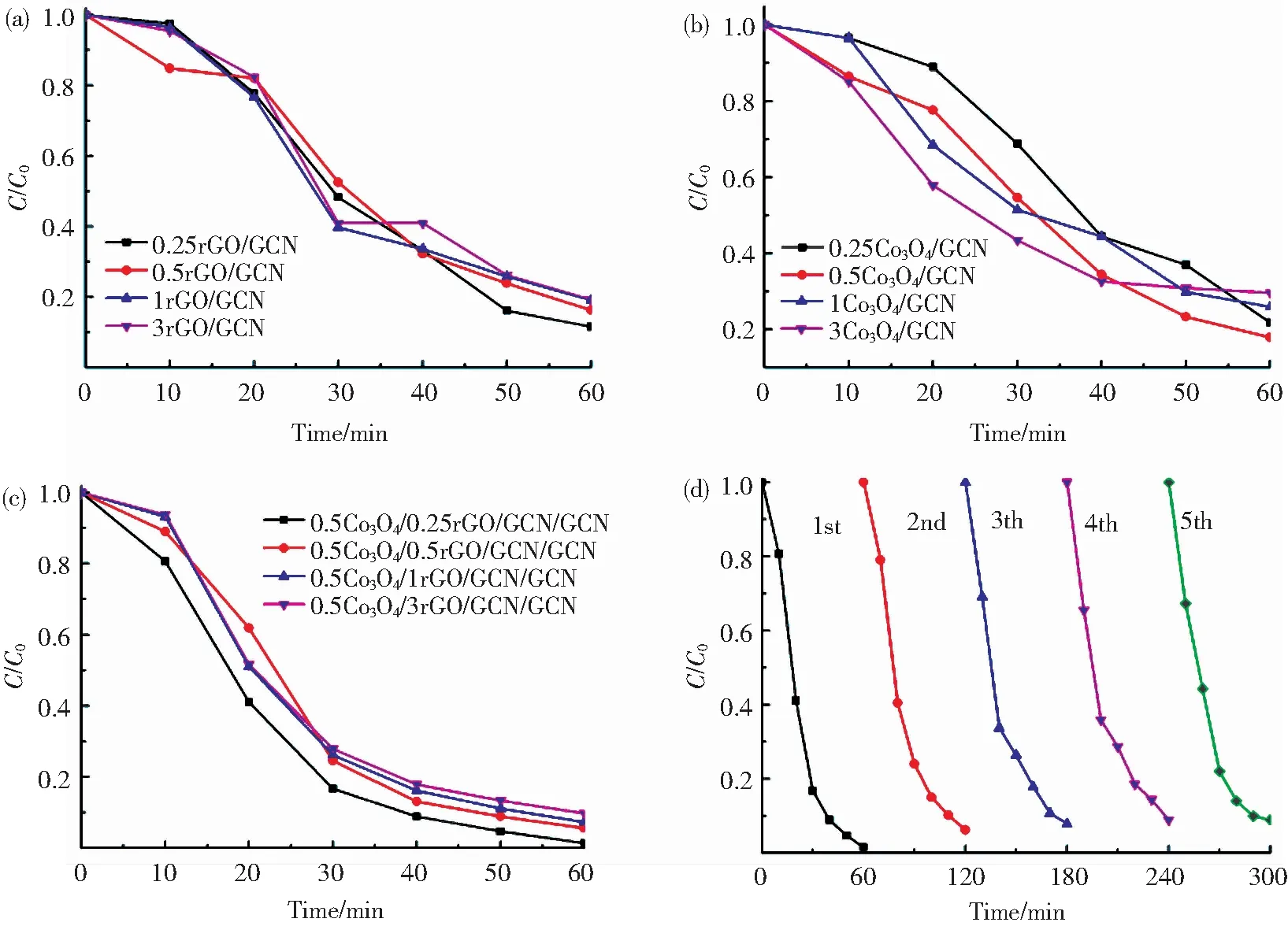
图7 不同rGO/GCN(a),Co3O4/GCN(b)和Co3O4/rGO/GCN(c)样品的2,4-D臭氧光催化降解实验和0.5Co3O4/0.25rGO/GCN样品5次循环实验结果(d)Fig.7 Photocatalytic ozonation experiments of different samples for 2,4-D degradation: rGO/GCN (a), Co3O4/GCN (b), and Co3O4/rGO/GCN (c); five cycles of experimentson 0.5Co3O4/0.25rGO/GCN sample (d)
图7(a)为不同rGO/GCN样品在相同实验条件下2,4-D臭氧光催化降解曲线,可以看出,随着rGO含量逐渐增高,2,4-D的降解率没有明显变化,当rGO的含量为0.25%时,光照1 h后降解率约为90%,达到最大降解活性。图7(b)为不同Co3O4/GCN对2,4-D臭氧光催化降解曲线,可以看出,0.5Co3O4/GCN样品对2,4-D具有最大的降解活性,光照1 h的降解率达到83%,表明Co3O4含量变化对臭氧光催化降解2,4-D活性有一定影响。当Co3O4、rGO和GCN三者形成Co3O4/rGO/GCN复合材料用于臭氧光催化降解实验时(图7(c)),对2,4-D的降解活性进一步增加,0.5Co3O4/0.25rGO/GCN样品在光照1 h后表现出最大的降解活性,最大降解率达到100%。此外,通过循环实验来研究Co3O4/rGO/GCN在臭氧条件下的稳定性和降解活性,用0.5Co3O4/0.25rGO/GCN样品经过5次循环实验测得的降解曲线结果(图7(d))表明,Co3O4/rGO/GCN复合光催化剂具有稳定的化学性质,经过多次循环实验后仍保有较强的降解活性。
2.8 光催化-臭氧氧化协同作用分析
为了深入研究光催化与臭氧氧化各自对2,4-D降解活性影响,对rGO/GCN、Co3O4/GCN和Co3O4/rGO/GCN材料仅在光催化、臭氧氧化作用下对2,4-D降解活性进行研究,降解曲线如图8所示。图8(a)为光催化氧化过程降解曲线,可以看出,经过60 min光照反应,GCN光催化降解2,4-D的降解率仅为5%,当GCN分别与0.5wt.%的Co3O4、rGO形成复合材料后降解活性也没有明显改善。然而,虽然0.5Co3O4/0.25rGO/GCN对2,4-D降解活性是所有样品中最高的,但也仅为7%,表明仅依靠光催化反应来降解2,4-D存在很大难度。图8(b)为相同实验条件下,仅通入臭氧的情况下加入不同光催化剂的2,4-D降解活性曲线,如图所示,几种样品对2,4-D的降解活性都显著增加,0.5rGO/GCN样品具有最好的降解活性,臭氧氧化1 h后的降解率达到67%,表明臭氧对2,4-D的具有较强的氧化性。通过对比可以看出,臭氧氧化过程的降解效率明显高于单独光催化反应过程,但远未达到臭氧-光催化协同降解效率,表明当臭氧和光催化反应条件同时具备更有利于2,4-D的高效、快速降解。以往研究表明,在臭氧光催化实验体系中,可以利用协同因子SF直观表达两项技术之间是否存在协同作用,SF=臭氧光催化反应速率常数/(光催化氧化速率常数+光臭氧反应速率常数)[34]。若该值>1,则表明两项技术之间具有协同作用;反之,则表明两项技术之间不具有协同作用。图8(c)表明0.5Co3O4/0.25rGO/GCN样品的光催化、光臭氧氧化和臭氧光催化反应速率分别为0.0008,0.0173和0.0709,进而求得协同因子SF值为3.91>1,表明臭氧氧化技术和光催化技术之间具有较好的协同作用。

图8 不同样品在光催化(a)和臭氧氧化(b)降解2,4-D活性实验以及0.5Co3O4/0.25rGO/GCN在不同反应条件下降解2,4-D的第一动力学速率分析(c)Fig.8 Photocatalytic (a)and ozonation (b)activity of different samples towards 2,4-D degradation and pseudo-first-order reaction kinetics (c) of 0.5Co3O4/0.25rGO/GCN for 2,4-D degradation under different reaction conditions
2.9 臭氧光催化反应原理


图9 可见光照射下0.5Co3O4/0.25rGO/GCN臭氧光催化降解2,4-D捕获实验结果(a)和臭氧光催化反应原理(b)Fig.9 Radical scavenger experiment results of photocatalytic ozonation degradation of 2,4-D by 0.5Co3O4/0.25rGO/GCN under visible light irradiation (a) and reaction mechanism of photocatalytic ozonation process (b)

3 结 论
1)本文通过简便的固相法和水热法制备了Co3O4负载rGO/氮化碳复合材料,为解决环境水体中除草剂残留问题,提高水环境质量和用水安全提供了一种可行方案。
2)在可见光照射下,利用臭氧光催化降解反应对2,4-D除草剂具有较好的降解活性,复合材料中各单元的组成与浓度对臭氧光催化降解2,4-D活性有重要影响。
3)循环实验结果表明这种复合材料在臭氧光催化反应过程中光化学稳定性良好。经过捕获实验研究发现·OH和h+是臭氧光催化反应过程中的主要活性物种,进而提出了可能的臭氧光催化反应机理。
