大鼠排泄物中ZCY-15排泄特征分析*
2023-01-02陆嘉君陈冰林城江
陆嘉君,陈冰,林城江
(上海交通大学医学院附属瑞金医院,上海 200025)
阿尔茨海默病(AD)是最常见的痴呆疾病,属进展缓慢的神经退行性疾病[1],主要病理特征为神经细胞外的β-淀粉样蛋白(Aβ)聚集和细胞内的tau聚集或神经纤维缠结(NFTs)的形成[2-3]。AD病例[4]最早于1907年报道,但其发病机制仍未明晰。AD患者的认知功能进行性丧失可能由脑功能紊乱或中毒、感染和循环系统异常等因素引起,导致大脑供氧减少、营养缺乏及肿瘤发生等[5-6]。目前,尚无治愈方法,现有方法仅可改善症状[7-8],治疗药物有乙酰胆碱酯酶抑制剂(AChEIs)[9](包括多奈哌齐[10]、加兰他明[11]和利凡他明[12])和应用于中重度AD的美金刚[13]。沈阳药科大学药化教研室参照美金刚及其酰胺类似物的结构设计并合成了系列芳香类美金刚类似物,同时,以AD模型大鼠为研究对象,通过Morris水迷宫试验、Y迷宫试验和新物体辨别等试验验证了ZCY-15[N-(3,5-二甲基金刚烷-1-基)-N-(3-甲基苯基)脲]具有显著的抗AD作用,改善学习和记忆能力的效果略优于美金刚,有成药潜力[14]。目前国内外未见ZCY-15在大鼠体内的排泄研究。本研究中建立了测定大鼠排泄物中ZCY-15浓度的超高效液相色谱串联质谱(UPLC-MS/MS)法,并分析了ZCY-15在大鼠体内的排泄特征。现报道如下。
1 仪器、试药与动物
1.1 仪器
I-CLASS型超高效液相色谱系统,Xevo TQ-S型三重四极杆质谱仪(美国Waters公司);5810R型全自动高速冷冻离心机,Mix-Mate型涡旋混匀器(德国Eppendorf公司);KS-250N型恒温超声仪(上海柯祁仪器设备有限公司);XP105DR型电子分析天平(瑞士Mettler Toledo公司,精度为0.1 mg);MD200-2型氮气吹干仪(上海那艾仪器有限公司);HX2001T型体重秤(慈溪市天东衡器厂)。
1.2 试药
ZCY-15(由沈阳药科大学药物化学教研室提供,含量≥98.0%);卡利拉嗪[内标(IS),中国食品药品检定研究院,含量≥99.9%];醋酸铵(天津市大茂化学试剂厂,含量≥99.9%);甲醇、乙酸乙酯均为色谱纯;乙腈、甲酸均为质谱纯;水为纯净水。
1.3 动物
SD大鼠60只,雌雄各半,7~9周,体质量(220±30)g,购自上海西普尔-必凯实验动物有限责任公司,实验动物生产许可证号为SCXK(沪)2018-0006,实验动物使用许可证号为SYXK(沪)2019-0027。将同性别SD大鼠每笼4只地安置于空调恒温室进行适应性饲养,室温20~24℃,相对湿度40%~70%,每日光照12 h,自由进食与饮水。
2 方法与结果
2.1 试验条件
2.1.1 色谱条件
色谱柱为AcquityUPLCBEHC18柱(100mm×2.1 mm,1.7μm);流动相为甲醇(A)-0.1%甲酸水溶液(B),梯度洗脱(0 min时70%A,1.0~2.5 min时95%A,2.6~4.0 min时70%A);流速为0.25 mL/min;柱温为50℃;进样量为5μL。
2.1.2 质谱条件
电喷雾离子源(ESI),离子源温度为150℃;雾化气温度为350℃;毛细管离子源电压为3 000 V;检测方式为正离子检测;扫描方式为多反应监测(MRM)模式;定量分析的离子反应m/z分别为ZCY-15 313.2→163.1,IS:427.2→382.0。
2.2 排泄样品预处理
分别精密量取大鼠空白胆汁、尿液样品各50μL,称量空白粪便样品50 mg,精密称定,分别加水200μL,涡旋振荡5 min,加乙酸乙酯300μL,混匀,涡旋振荡5 min,13 000 r/min离 心5 min,精密 量 取上清 液260μL,用氮气吹干,加70%甲醇100μL复溶,涡旋振荡5 min,13 000 r/min离心5 min,精密量取上清液20μL,置EP管中,加流动相180μL,涡旋15 s,转移至进样瓶。
2.3 溶液制备
取ZCY-15适量,精密称定,配制成质量浓度为1μg/mL的ZCY-15贮备液,用乙腈逐级稀释制成质量浓度分别为1,5,10,25,50,100,200 ng/mL的系列标准溶液和质量浓度分别为2,20,160 ng/mL的质量控制溶液。4℃保存待用。
取IS适量,精密称定,配制成质量浓度为10μg/mL的内标贮备液,用甲醇稀释并定容,反复摇匀,得质量浓度为50 ng/mL的IS工作液。4℃保存待用。
2.4 方法学考察
专属性试验:ZCY-15为外源性物质,故采用大鼠的空白胆汁、尿液及粪便作为标准曲线基质。取大鼠空白胆汁、尿液、粪便适量;以及分别加入5μL ZCY-15和IS工作液的50μL大鼠空白胆汁、尿液、粪便匀浆,按2.3项下方法操作,按2.1项下试验条件进样分析,记录质谱图。结果ZCY-15的保留时间为2.24 min,内标为0.95 min。大鼠的胆汁、尿液及粪便中的内源性成分不会干扰ZCY-15和内标的测定。详见图1。
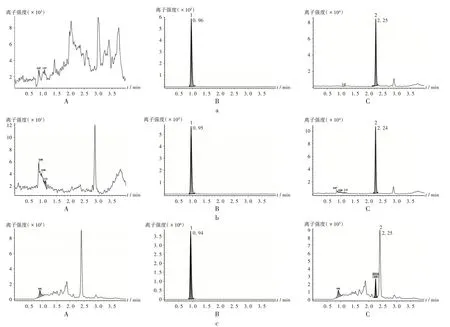
图1 大鼠空白排泄物中ZCY-15和IS超高效液相色谱串联质谱图1.Cariprazine 2.ZCY-15A.Blank sample B.Blank sample+IS C.Blank sample+ZCY-15a.Blank bile b.Blank urine c.Blank fecesFig.1 UPLC-MS/MS chromatograms of ZCY-15 and IS in the blank excreta of rats
线性关系考察:精密量取大鼠空白胆汁、尿液、粪便匀浆50μL,分别加入ZCY-15系列标准溶液5μL,制成质量浓度分别为1,5,10,25,50,100,200 ng/mL的模拟梯度胆汁、尿液、粪便匀浆样品,按2.3项下方法操作,按2.1项下试验条件进样分析,以ZCY-15质量浓度(X,μg/mL)为横坐标,峰面积(Y)为纵坐标进行线性回归,每个质量浓度平行3次,结果见表1。ZCY-15质量浓度在1~200 ng/mL范围内与峰面积线性关系良好。

表1 大鼠排泄物中ZCY-15的标准曲线(n=7)Tab.1 Standard curves of ZCY-15 in the excreta of rats(n=7)
准确度(RE)和精密度试验:取大鼠空白胆汁、尿液、粪便匀浆样品,按2.3项下方法操作,设定定量下限(LLQ)为1.00 ng/mL,低、中、高3种质量浓度(2,20,160 ng/mL),ZCY-15每个质量浓度平行6份,与“线性关系考察项”样本连续3 d同时进行测定。根据当日回归方程计算对应的质量浓度,与实际制备的样品质量浓度进行比较,计算得ZCY-15的LLQ和低、中、高质量浓度的准确度和精密度,详见表2。结果准确度和精密度均符合生物样品测定的规定要求。
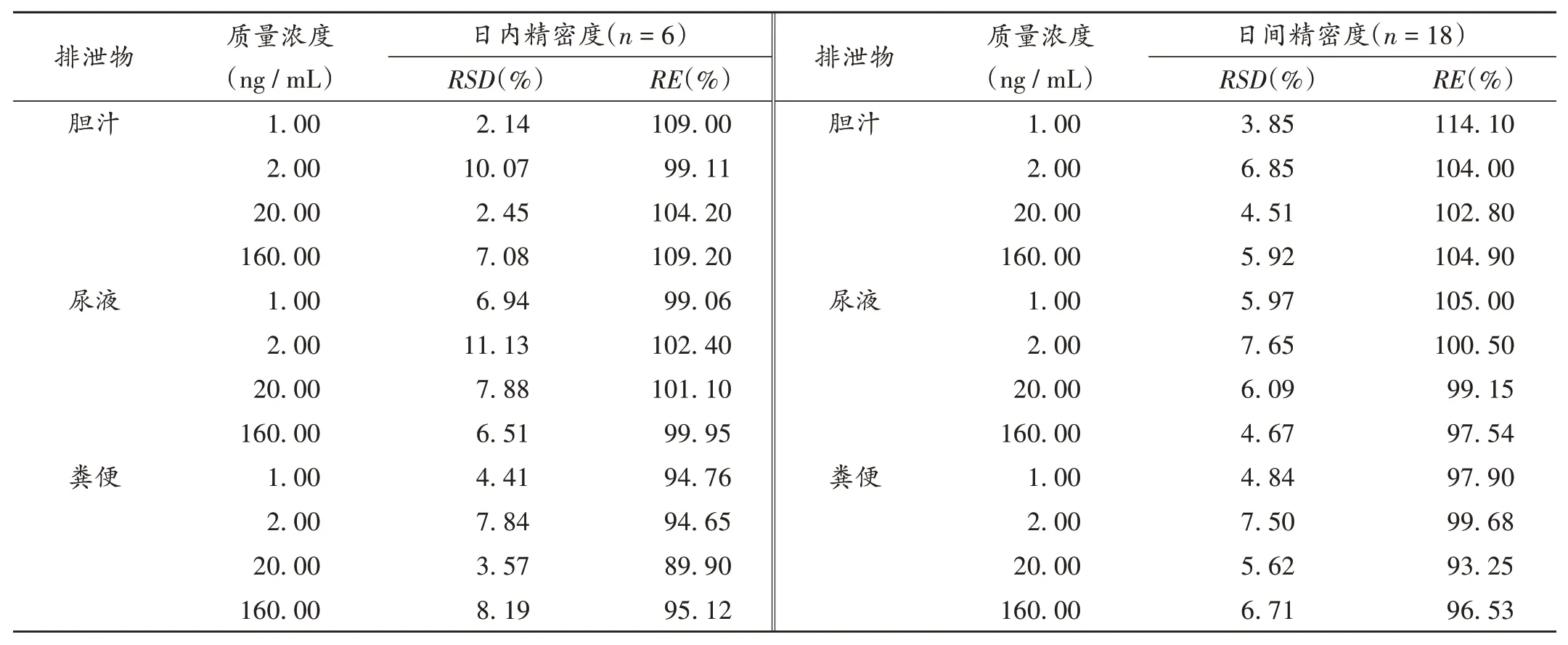
表2 大鼠排泄物中ZCY-15精密度试验结果Tab.2 Results of the precision test of ZCY-15 in the excreta of rats
提取回收率:取大鼠空白胆汁、尿液、粪便样品,分别加入2.2项下ZCY-15低、高质量浓度(2 ng/mL,160 ng/mL;下同)质控溶液和IS工作液各5μL,按2.3项下方法操作,每个质量浓度平行6份,按拟订试验条件进样分析,记录对应的色谱峰面积。同时,精密量取大鼠空白胆汁、尿液、粪便匀浆50μL,分别加入低、高质量浓度ZCY-15质控溶液和IS工作液各5μL,经处理,每个浓度平行6份,按拟订试验条件进样分析,记录对应的色谱峰面积,计算ZCY-15的提取回收率,结果见表3。可见,提取回收率符合生物样品测定的规定要求。
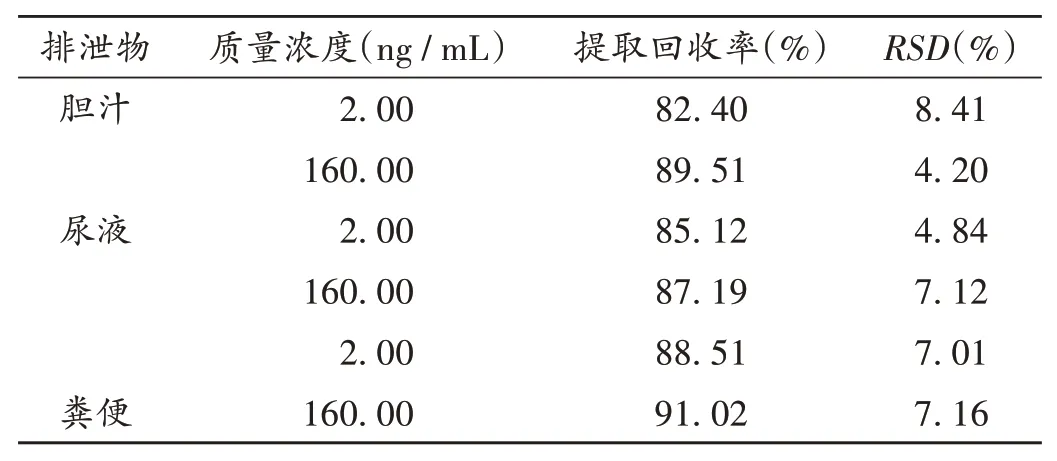
表3 大鼠排泄物中ZCY-15的提取回收试验结果(n=6)Tab.3 Results of the extraction recovery test of ZCY-15 in the excreta of rats(n=6)
基质效应:精密量取大鼠空白胆汁、尿液、粪便匀浆50μL,分别加入2.2项下低、高质量浓度ZCY-15质控溶液和IS工作液各5μL,涡旋10 s,按2.3项下方法操作,每个质量浓度平行6份进样分析,得色谱峰面积。用水代替匀浆,按2.3项下方法操作,每个质量浓度平行6份,按拟订试验条件进样分析,以基质存在下的色谱峰面积(由空白基质提取后加入ZCY-15和IS)与不含基质的色谱峰面积(ZCY-15和IS的纯溶液)比值,计算ZCY-15和IS的基质因子,进一步以ZCY-15基质因子与IS基质因子的比值,计算得内标归一化基质因子。ZCY-15和IS的基质效应见表4。结果表明,基质效应对排泄物匀浆样品的测定无明显影响,符合生物样品测定的规定要求。
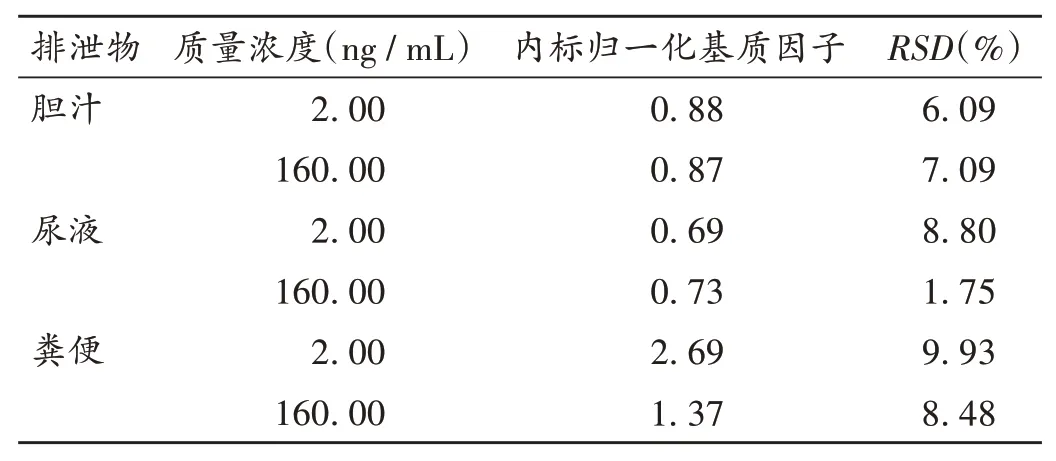
表4 大鼠排泄物中ZCY-15的基质效应(n=6)Tab.4 Matrix effects of ZCY-15 in the excreta of rats(n=6)
稳定性试验:取大鼠空白胆汁、尿液和粪便匀浆样品,分别加入2.2项下低、高质量浓度ZCY-15质控溶液和IS工作液各5μL,按2.3项下方法操作,每个质量浓度平行3份,按拟订试验条件进样分析,考察样品在室温下放置12 h、3次循环冻融、样品处理后在液相色谱仪自动进样器内放置24 h、-20℃冻存30 d的稳定性。结果含ZCY-15的排泄物匀浆样品具有良好的稳定性,符合生物样品测定的规定要求。结果见表5至表7。
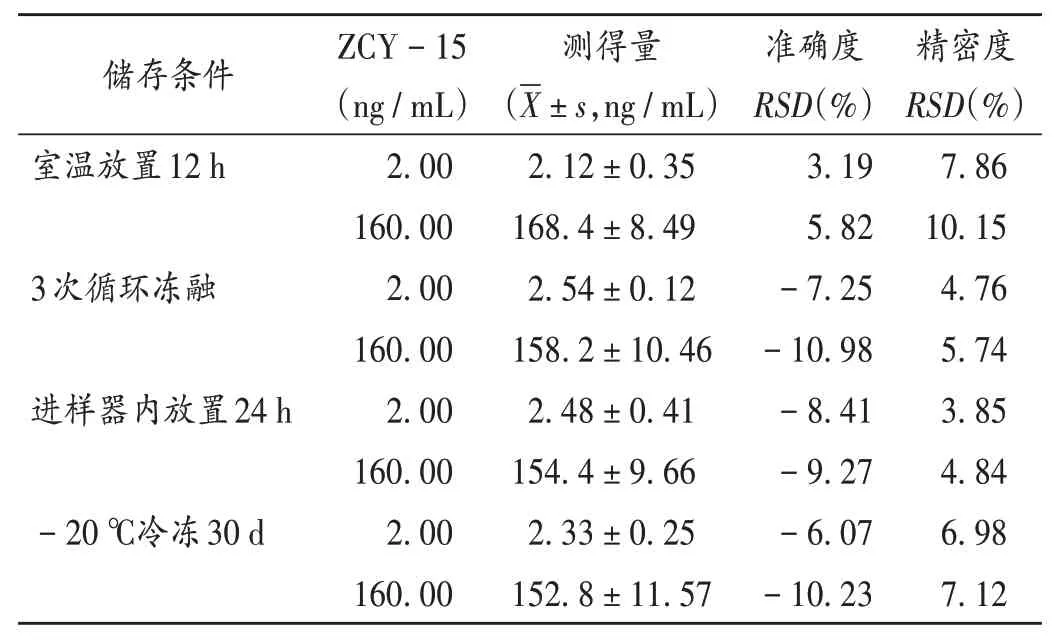
表5 大鼠胆汁匀浆样品中ZCY-15的稳定性试验结果(n=3)Tab.5 Results of the stability test of ZCY-15 in bile homogenate samples of rats(n=3)

表7 大鼠粪便匀浆样品中ZCY-15的稳定性试验结果(n=3)Tab.7 Results of the stability test of ZCY-15 in feces homogenate samples of rats(n=3)
稀释效应:取配制好的质量浓度为1 000 ng/mL ZCY-15的排泄物匀浆样品10μL,再加入90μL空白排泄物匀浆稀释,涡旋30 s,按2.3项下方法操作,每个质量浓度平行6份,按拟订试验条件进样分析,并与定量为100 ng/mL的实测值进行比较,得出稀释效应。当稀释倍数为10倍时,稀释的ZCY-15溶液的精密度的RSD为3.95%~6.48%,准确度为5.24%~10.86%。故超出定量上限的ZCY-15样品可用空白排泄物匀浆稀释后制样检测。
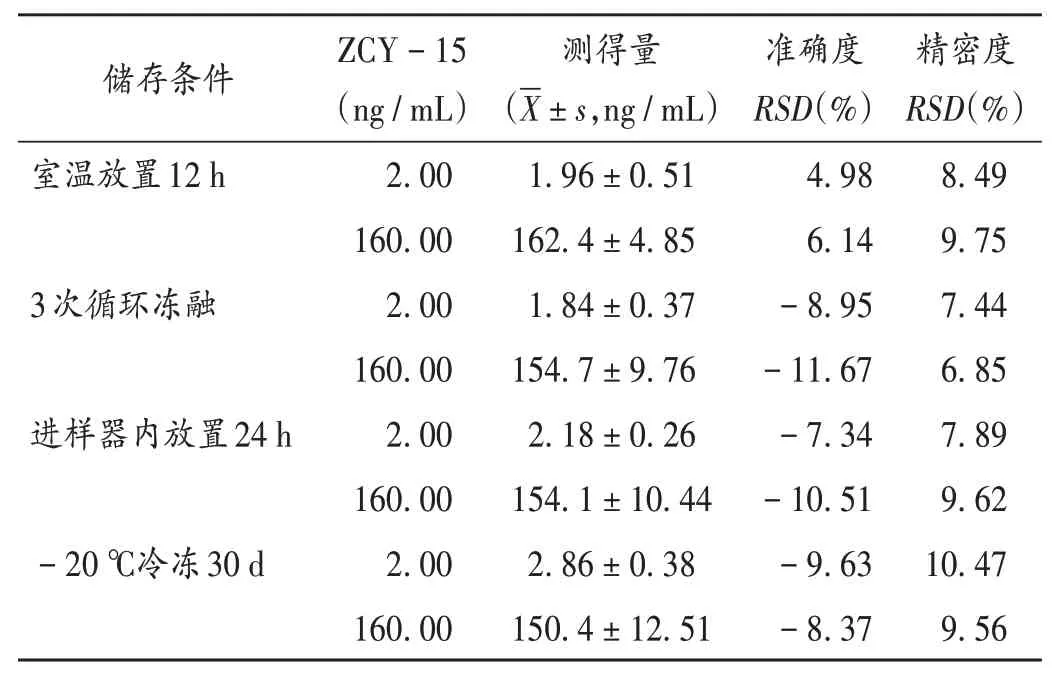
表6 大鼠尿液匀浆样品中ZCY-15的稳定性试验结果(n=3)Tab.6 Results of the stability test of ZCY-15 in urine homogenate samples of rats(n=3)
2.5 ZCY-15在大鼠胆汁、尿液和粪便中的排泄特征
分组与排泄样品采集:称量ZCY-154.50 mg,精密称定,置10 mL离心管中,加入100μL二甲基亚砜完全溶解,依次加入160μL吐温-80、1.4 mL丙二醇、1.6 mL聚氧乙烯蓖麻油-EL,37℃恒温超声(功率2 000 W,频率30kHz,下同)混匀5min,使化合物完全溶解,并转移至20 mL带塞玻璃试管中;精密加入16.74 mL生理盐水,37℃恒温超声处理5 min混匀,制成质量浓度为0.225 mg/mL的ZCY-15溶液。给药前,大鼠禁食12 h,可自由饮水。随机选取18只SD大鼠(雌雄各半),称定体质量、标记并计算给药量。随机分为胆汁组、尿液组和粪便组,各6只,雌雄各半。胆汁组大鼠以10%水合氯醛麻醉后迅速完成胆管插管,在大鼠清醒后缓慢灌胃ZCY-15(2.25 mg/kg),并于给药后0~2 h、2~4 h、4~6 h、6~8 h、8~12 h、12~24 h收集胆汁样本;尿液组和粪便组分别于灌胃ZCY-15后0~2 h、2~4 h、4~6 h、6~8 h、8~12 h、12~24 h、24~36 h、36~48 h、48~72 h,收集尿液及粪便样本。收集的样本密封处理,-20℃冻存待用。
实际排泄匀浆样本测定及数据处理:采集大鼠胆汁、尿液和粪便样本,按2.3项下方法操作,按2.1项下试验条件检测,计算ZCY-15的浓度,绘制药物累计排泄量-时间曲线。
灌胃给药后,分别采集不同时间点大鼠的胆汁、尿液和粪便,测定ZCY-15浓度并计算各时间段内不同排泄样本的平均药物累积排泄量。结果所有采集的尿液样本中ZCY-15的浓度均低于LLQ,未能检出;胆汁、粪便样本中ZCY-15的平均药物积累排泄量及占比见表8和表9;胆汁和粪便匀浆中ZCY-15的排泄率分别为(0.000 2±0.000 09)%和(0.99±0.57)%。胆汁、粪便匀浆中ZCY-15的平均药物累积排泄量-时间曲线见图2。
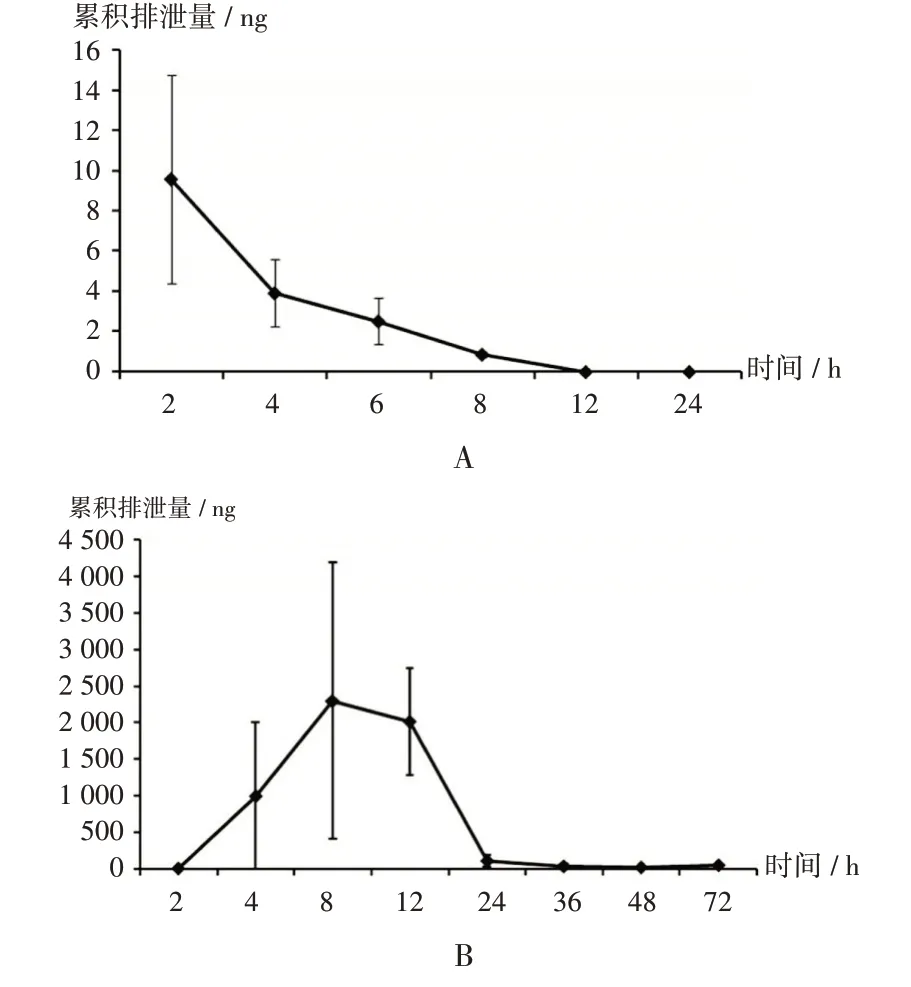
图2 灌胃给药ZCY-15(2.25 mg/kg)后大鼠胆汁、粪便中药物累积排泄量-时间曲线A.Bile B.FecesFig.2 Cumulative excretion-time curves in bile and feces of rats after the intragastric administration of ZCY-15(2.25 mg/kg)by gavage
表8 灌胃给药ZCY-15(2.25 mg/kg)后大鼠胆汁中平均药物累积排泄量及占比(±s,n=6)Tab.8 Average cumulative excretions and proportions in bile of rats after the intragastric administration of ZCY-15(2.25 mg/kg)(±s,n=6)
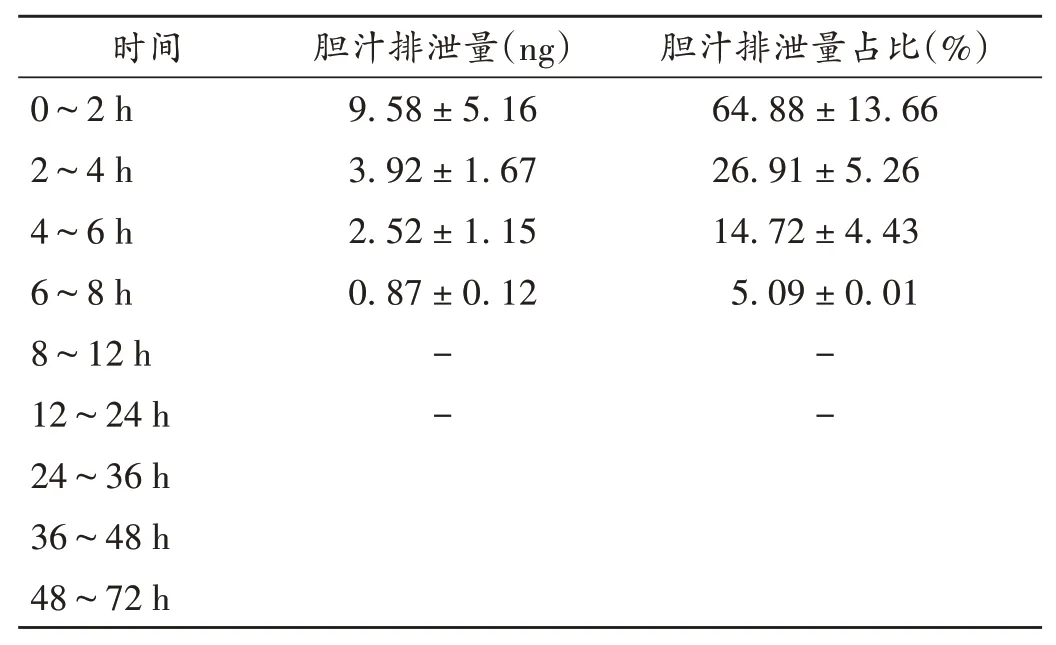
表8 灌胃给药ZCY-15(2.25 mg/kg)后大鼠胆汁中平均药物累积排泄量及占比(±s,n=6)Tab.8 Average cumulative excretions and proportions in bile of rats after the intragastric administration of ZCY-15(2.25 mg/kg)(±s,n=6)
注:-为ZCY-15浓度低于LLQ。表9同。Note:-indicates that the mass concentration of ZCY-15 is lower than the lower limit of quantification(for Tab.8-9).
时间0~2 h 2~4 h 4~6 h 6~8 h 8~12 h 12~24 h 24~36 h 36~48 h 48~72 h胆汁排泄量(ng)9.58±5.16 3.92±1.67 2.52±1.15 0.87±0.12--胆汁排泄量占比(%)64.88±13.66 26.91±5.26 14.72±4.43 5.09±0.01--
表9 灌胃给药ZCY-15(2.25 mg/kg)后大鼠粪便中平均药物累积排泄量及占比(±s,n=6)Tab.9 Average cumulative excretions and proportions in feces of rats after the intragastric administration of ZCY-15(2.25 mg/kg)(±s,n=6)
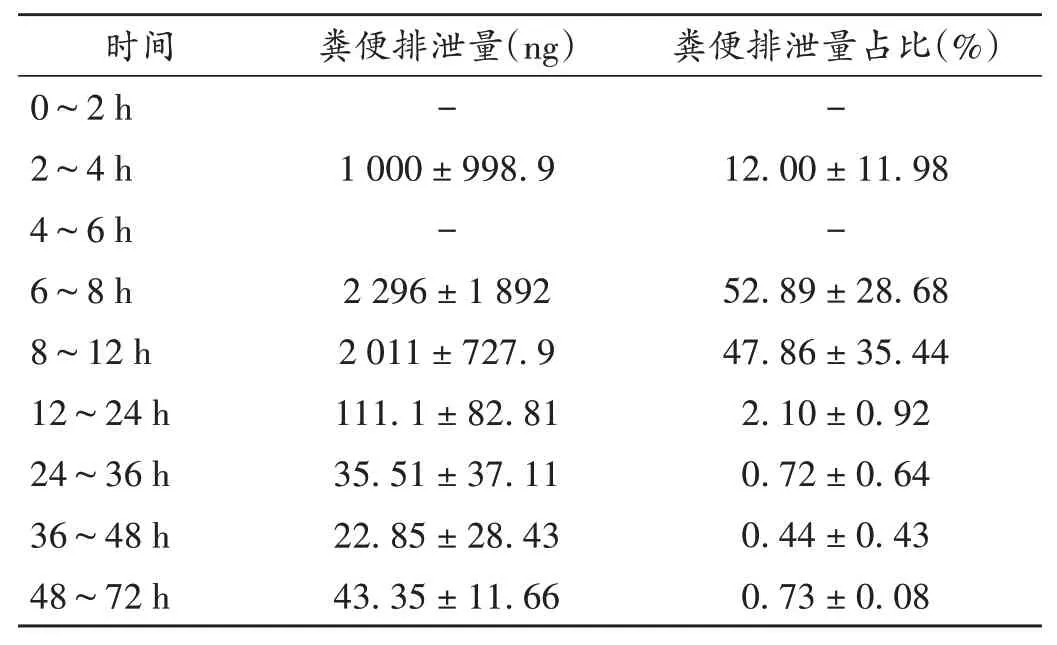
表9 灌胃给药ZCY-15(2.25 mg/kg)后大鼠粪便中平均药物累积排泄量及占比(±s,n=6)Tab.9 Average cumulative excretions and proportions in feces of rats after the intragastric administration of ZCY-15(2.25 mg/kg)(±s,n=6)
时间0~2 h 2~4 h 4~6 h 6~8 h 8~12 h 12~24 h 24~36 h 36~48 h 48~72 h粪便排泄量(ng)-1 000±998.9-2 296±1 892 2 011±727.9 111.1±82.81 35.51±37.11 22.85±28.43 43.35±11.66粪便排泄量占比(%)-12.00±11.98-52.89±28.68 47.86±35.44 2.10±0.92 0.72±0.64 0.44±0.43 0.73±0.08
3 讨论
大鼠灌胃给药ZCY-15后,经胆汁排泄的量极少,且呈现时间依赖性,即胆汁匀浆中ZCY-15质量浓度逐渐减少并在给药后约12 h基本排泄结束,排泄率仅为(0.000 2±0.000 09)%。由此推测,ZCY-15原形药物几乎不经胆汁代谢。收集大鼠口服ZCY-15后不同时间段的尿液样本,均未能检出ZCY-15,表明ZCY-15不能以原形经尿液排泄。根据以往ZCY-15药物代谢动力学研究结果可知,大鼠灌胃给药ZCY-15吸收量较低,生物利用度不高,故推测ZCY-15经粪便排泄量较大。给药后0~8 h,粪便中ZCY-15的排泄量逐渐升高,给药后6~8 h达排泄高峰;给药后8~24 h,排泄量逐步下降,给药后24 h排泄基本结束。但是经计算得ZCY-15经粪便排泄率仅为(0.99±0.57)%。可见,ZCY-15通过胆汁、尿液和粪便的整体排泄率较低,主要排泄时间为给药后0~24 h。
综上所述,本研究中建立的UPLC-MS/MS法能在4 min内准确测定大鼠胆汁、尿液和粪便中ZCY-15的质量浓度,仅少量ZCY-15以原形药物经粪便排泄,其余主要以代谢产物的形式排出体外。
