经食道超声引导经胸镶嵌手术治疗新生儿危重肺动脉瓣狭窄及闭锁
2022-12-30赵婉玉吴臣玉李维君钟德琳赵思玲
赵婉玉,吴臣玉,李维君,钟德琳,赵思玲,邱 红
(云南省阜外心血管病医院/昆明医科大学附属心血管病医院 超声科,云南 昆明 650102)
新生儿室间隔完整的危重肺动脉瓣狭窄(critical pulmonary stenosis,CPS)及危重肺动脉闭锁(critical pulmonary atresia,CPA)为动脉导管依赖的先天性心脏病,可发生严重的低氧血症及心功能不全。常规外科手术需心脏停跳及转体外循环,对于新生儿风险较大,
X线下经皮瓣膜球囊扩张成形术存在辐射及造影剂损伤风险[1]。近年来不断有研究探索外科杂交镶嵌技术治疗CPS/CPA[2-4],即经右室流出道插管行瓣膜球囊扩张术,已取得较好临床效果。本研究利用经食道超声心动图(transesophageal echocardiography,TEE)术中全程引导监测下,实施经胸球囊肺动脉瓣成形术(transthoracic balloon pulmonary valvuloplasty,TBPV),其中共实施CPS 2例、CPA3例,总结该技术的方法学,安全性、可行性,现报告如下。
1 资料与方法
1.1 资料
自2017年8月-2022年3月连续收集云南省阜外心血管病医院进行手术的5例CPS及CPA危重新生儿,其中男3例(60%),女2例(40%),年龄4~28(11.60±8.50)d,体重2.3~4.2(3.30±0.72)kg。5例CPS患儿均存在氧饱和度低,波动在40%~87%之间,其中2例诊断为CPS,3例诊断为CPA,5例新生儿的诊断、入院基本情况见表1。

表1 5例新生儿的诊断、入院基本情况
GPS及CPA纳入标准:(1)肺动脉瓣跨瓣压差(pressure gradient,PG)≥40 mm Hg或肺动脉闭锁;(2)告知家属知情同意并签署知情同意书。排除标准:(1)肺动脉瓣下漏斗部狭窄;(2)先天性瓣下或瓣下狭窄;(3)合并需要外科手术处理的疾病[5]。
1.2 仪器与方法
1.2.1 仪器
Philips7 PQC彩色多普勒超声诊断仪,配备新生儿食道超声探头S8-3t探头,频率1.7~10.0 mHz。
1.2.2 操作方法
常规麻醉、气管插管,胸骨正中切口,在右室流出道缝荷包,植入动脉鞘管后,分别在以下超声不同切面监测肺动脉瓣球囊扩张。
术前TEE检查:采用TEE40°大动脉短轴切面,评估肺动脉瓣叶增厚情况,瓣叶活动度及反流,测量肺动脉瓣环直径及其跨瓣压差,评估主肺动脉及左右肺动脉发育情况、右室流出道有无梗阻,评估三尖瓣反流程度,评估左、右室功能及右室发育情况。
术中TEE监测:采用TEE40°大动脉短轴切面,监测导丝进入肺动脉,沿导丝送入球囊,选择球囊直径一般为肺动脉瓣环的1.2~1.5倍,定位导管的位置,即球囊中部位于肺动脉瓣口,在TEE监测下充盈球囊,扩张肺动脉瓣,评估肺动脉瓣口血流变化情况及肺动脉压差变化,是否出现肺动脉瓣反流及三尖瓣反流,肺动脉瓣跨瓣压差低于30 mmHg认为扩张成功,如多次扩张,肺动脉瓣压差仍然保持在30~40 mmHg,观察是否存在右室流出道激惹、痉挛,操作方法见图1。
随访:出院后在门诊复查经胸超声心动图,评估肺动脉瓣跨瓣压差,瓣膜返流程度以及有无其它并发症。
1.3 统计学方法
采用 SPSS23.0统计学软件分析,计量资料用均数±标准差表示,计数资料以n(%)表示,组间比较采用配对t检验。P<0.05为差异有统计学意义。
2 结果
2.1 手术情况
3例患儿术前TEE显示肺动脉膜性闭锁,2例患儿术前TEE显示肺动脉瓣增厚,测量球囊扩张前肺动脉瓣峰值压差为81~108(94.5±13.5)mmHg,肺动脉瓣环内径7.0~9.0(8.40±0.80)mm,三尖瓣不同程度反流,右室发育正常,均无右室流出道明显梗阻,无肺动脉瓣反流,无主肺动脉及左右肺动脉发育不良。所有患儿均成功实施球囊扩张术,术中使用球囊直径8.0~10.0(9.60±0.80)mm,球瓣比均为1.1~1.2,术中TEE全程实时监测,术后即刻评价肺动脉跨瓣压差,扩张后下降至8~31(15.40±8.52)mmHg,差异有统计学意义(P<0.01)。术后肺动脉瓣反流均为少中量以内,三尖瓣反流明显减少。1例患儿因合并坏死性小肠结肠炎家属决定放弃治疗,其余均顺利出院,见表2。
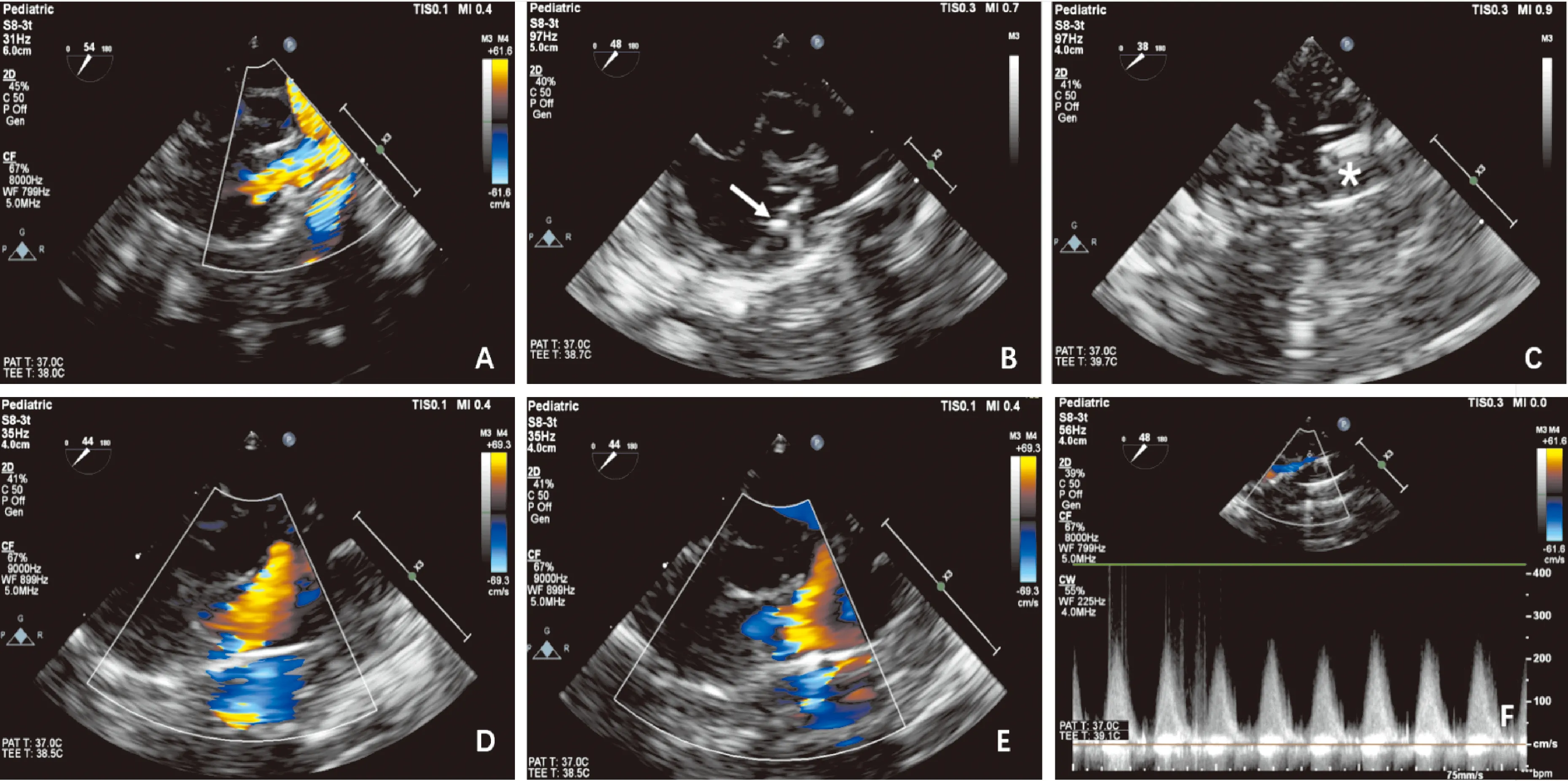
图1 术中经食管超声引导及评估CPS瓣膜球囊扩张
注:A:血流通过狭窄的肺动脉瓣口进入主肺动脉后呈五彩镶嵌色;B:球囊导管通过肺动脉瓣口;C:球囊充盈;D:球囊扩张术后肺动脉前向血流通畅;E:球囊扩张术后肺动脉瓣少量反流;F:肺动脉瓣前向血流速度减低,峰值压差减低(*球囊;→导丝)
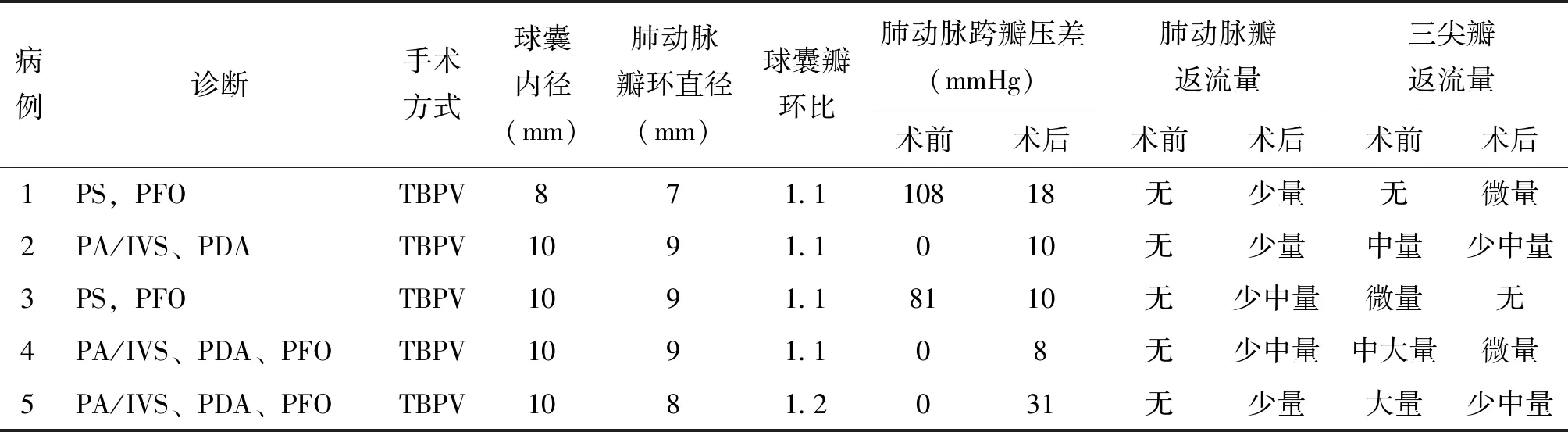
表2 5例新生儿的手术情况
2.2 随访情况
4例患儿均在门诊随访,1例失访,随访时间16~225(78.60±80.33)d,患儿均存活。肺动脉跨瓣压差9~16(9.09±5.14)mmHg,仍明显低于术前,接近术后即刻(与术前相比P<0.001,与术后即刻相比P>0.05),RV/LV横径由术前(0.56±0.11)增高至(0.63±0.04)(P<0.05),证明肺动脉瓣狭窄改善后促进右室发育,见表3。
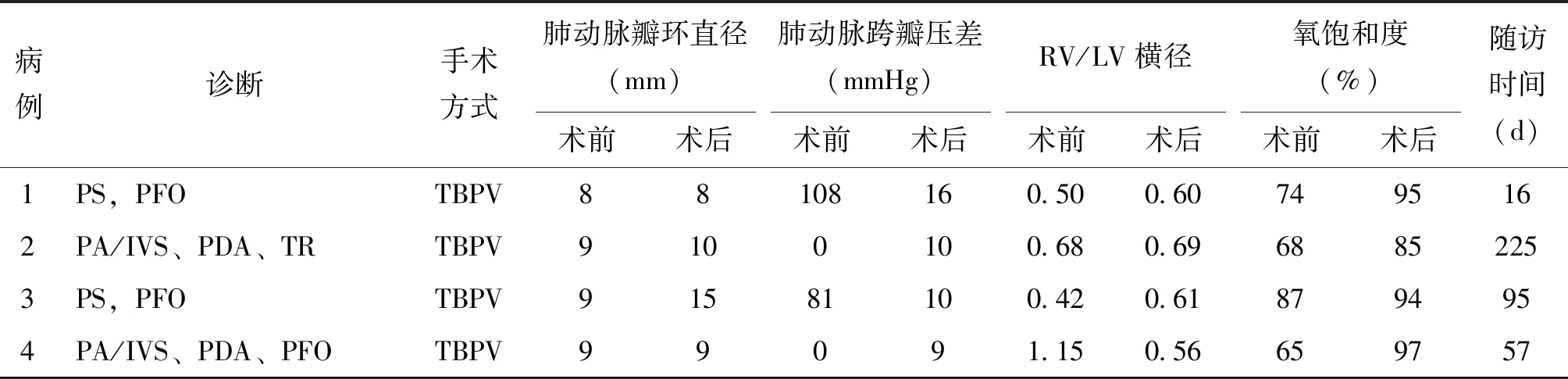
表3 4例新生儿的随访结果
3 讨论
介入和外科治疗相互镶嵌治疗模式开始应用在医学领域[6-9]。手术实施过程中完全超声引导监测,是一种相对安全的手术方式,尤其对新生儿更加适合。本研究完全TEE引导新生儿CPS/CPA的镶嵌手术有效降低了肺动脉瓣跨瓣压差,研究认为该手术是安全、有效的。
在TBPV操作中,术前TEE需评估肺动脉瓣增厚程度、瓣叶活动度及是否伴有反流。手术操作重点是多次详细评估肺动脉瓣环大小,测量跨瓣压差,评估右室流出道是否肥厚、梗阻,评估三尖瓣反流。其中球囊大小尺寸选择依据超声测量瓣环大小,多项研究认为球瓣比为1.2~1.4,此范围即可有效扩张瓣膜,有可预防瓣膜反流[10,11]。存在明显右室流出道肥厚及梗阻是手术的禁忌症,尤其术中容易导致右室流出道激惹或痉挛,超声引导中准确定位球囊中段位于瓣口中央亦是关键点,有文献认为对于新生儿球囊上2/3位于瓣口,扩张球囊尽量离开右室流出道可减少流出道撕裂风险。本研究中CPS选择的球瓣比均为1.1或1.2 手术压差下降明显。
手术实施过程中可实施多次球囊扩张,扩张次数以瓣口压差降低至30 mmHg为标准[12,13],当获得较好的压差减少即可减少三尖瓣的反流[14,15]。本研究患儿球囊扩张次数平均2~3次,均表现手术即刻三尖瓣反流明显减少。
超声心动图在经胸肺动脉瓣球囊扩张成形术治疗新生儿CPS、CPA中起着重要作用,参与了术前病例评估、术中实时全程引导监测和术后疗效评价。且围术期并发症发生率低,中期随访再狭窄发生率低,避免放射线危害。因此,纯超声引导下经胸肺动脉瓣球囊扩张成形术是治疗新生儿CPS、CPA安全有效的方法。
由于开展样本量少,经验尚不足,需要扩大样本进行进一步累计经验及其不足。虽然如此,超声引导杂交手术中肺动脉瓣球囊扩张对于危重新生儿具有明显优势,可作为瓣膜微创治疗技术应用于临床。
