超高效合相色谱法测定缬沙坦原料药中R-缬沙坦
2022-12-30丁建营刘发贵刘思光李铁健张贵民
丁建营,刘发贵,王 花,刘思光,李铁健,张贵民
(国家手性制药工程技术研究中心,山东 临沂 273400)
缬沙坦(valsartan)是一种口服有效的特异性血管紧张素Ⅱ(AT1)受体拮抗剂,临床用于治疗轻、中度原发性高血压[1-3]. 缬沙坦含有一个手性中心,存在一对对映异构体,其结构如图1所示. 由于R-缬沙坦药物活性远低于S-缬沙坦,为了减少用药所导致的不良反应率,故缬沙坦原料中需控制R-缬沙坦的含量. 目前已报道的测定R-缬沙坦的方法普遍为高效液相色谱法[4-7],其分析检测时间较长,流动相大多为易挥发和气味难闻的正己烷、异丙醇等溶剂,具有一定毒性,长期接触对人体具有一定危害.现行的2020年版《中华人民共和国药典》缬沙坦原料标准中R-缬沙坦的检测方法采用α-酸性蛋白柱(AGP)[8]. 该色谱柱对使用和保存均有较为严格的要求,例如需要冷藏,使用柱温要求20~30 ℃,碱性条件下色谱柱寿命下降明显,间接地提高了检测成本. 超高效合相色谱法(UPCC)作为一种新型色谱分离技术,使用二氧化碳为流动相,相比传统高效液相分析技术,具有速度快且有机溶剂使用量少、重现性好、绿色环保的优点[9-13],对手性化合物、热不稳定化合物、脂质、聚合物、高疏水性和/或强极性化合物的混合物具有很好的分离效果[14]. 本文采用UPCC建立了缬沙坦原料药中R-缬沙坦的检测方法,探讨UPCC法的主要影响因素. 该方法使用要求较为宽松的多糖键和型手性柱(IC-3)为色谱柱,避免较多AGP色谱柱的一些局限性,为缬沙坦质量标准研究提供进一步参考,也为UPCC在药品质量控制领域的应用提供借鉴.
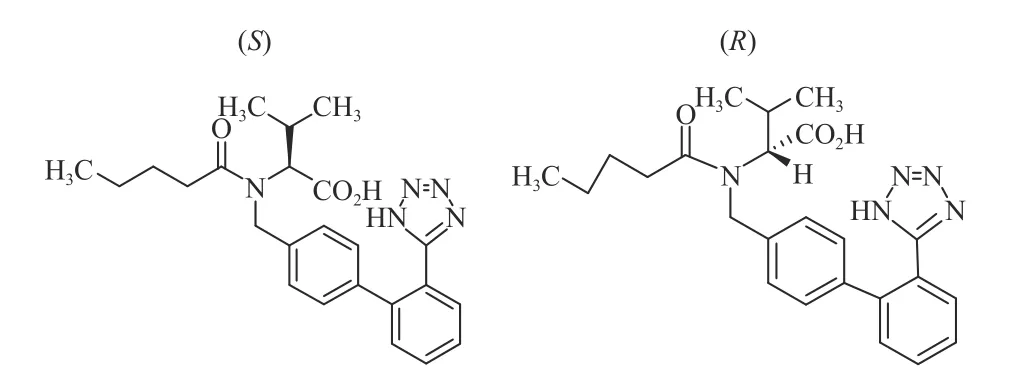
图1 S-缬沙坦和R-缬沙坦结构图Fig. 1 Chemical structure formulas of S-valsartan and Rvalsartan
1 试验部分
1. 1 仪器
Waters超高效合相色谱仪(美国沃特世公司),配备Empower 3化学工作站、合相管理器、柱温箱、PDA检测器;XPR10型百万分之一电子分析天平(Mettler Toledo公司);CHIRALPAK IC-3色 谱 柱(100 mm×3.0 mm,3 µm);CHIRALCEL OJ色谱柱(4.6 mm×250 mm,10 µm);CHIRALCEL IB色谱柱(4.6 mm×250 mm,5 µm).
1. 2 试剂
缬沙坦对照品(批号:100651-202006,纯度:100%,中国食品药品检定研究院),缬沙坦原料(批号:200501、220101、220201,山东新时代药业有限公司),R-缬沙坦对照品(批号:100836-201802,纯度:100%,中国食品药品检定研究院),乙醇胺(TCI,批号:PWAWN-MO),三氟乙酸(TCI,批号:7XK60),甲醇(Merck,色谱纯).
1. 3 色谱条件
色谱柱CHIRALPAK IC-3,流动相为甲醇(含0.5%乙醇胺)∶二氧化碳(体积比为20∶80);动态背压(ABPR)13.79 MPa;流速1.0 mL/min;检测器为电二极管阵列检测器(PDA),扫描范围:200~400 nm;柱温40 ℃;进样量:10 µL.
1. 4 溶液配制
对照储备液:称取R-缬沙坦对照品约5 mg,置于10 mL量瓶中,使用甲醇溶解并稀释至刻度,摇匀,即得. 对照溶液:精密量取对照品储备液1 mL,置于10 mL量瓶中,稀释至刻度,摇匀,即得.
供试品储备液:称取缬沙坦约100 mg,置于10 mL量瓶中,使用甲醇溶解并稀释至刻度,摇匀,即得. 供试品溶液:精密量取供试品储备液1 mL,置于2 mL量瓶中,稀释至刻度,摇匀,即得.
测试溶液:精密量取供试品储备液2.5 mL和对照储备液0.5 mL,置于5 mL量瓶中,使用甲醇溶解并稀释至刻度,摇匀,即得.
2 结果与讨论
2. 1 方法开发
2. 1. 1 色谱柱的筛选
参考S-缬沙坦和R-缬沙坦的化学性质,并结合UPCC仪器的特点,筛选了CHIRALCEL OJ、CHIRALCEL IB和CHIRALPAK IC-3色谱柱,试验发现前两款色谱柱无法将其分离,CHIRALPAK IC-3色谱柱有分离趋势. 后经调整流动相和柱温,S-缬沙坦和R-缬沙坦实现基线分离,结果如图2(a)~(e)所示.
2. 1. 2 ABPR和柱温的优化
ABPR是控制超临界CO2性能的重要参数,超临界流体的密度和粘度会随背压的增加而增加,对合相色谱来说,选择合适的背压对分离度、峰形均有较大的影响. 随着温度和压强的变化,密度为100%的CO2的质量浓度波动范围为0.2~1.1 g/mL,而待测成分的溶解性取决于CO2的密度,因此提高CO2的压强或者降低柱温能够增加待测成分在CO2中的溶解性. 考察了10.34、13.79、20.69 MPa背压下的测试结果,发现背压为10.34、20.69 MPa时,S-缬沙坦和R-缬沙坦峰形和分离度较差. 考察了色谱柱柱温为35、40 ℃时的测试结果,如图2(g)(h)所示. 由图2(g)(h)可见,降低柱温,缬沙坦及其对映异构体的保留时间提前. 升高柱温,保留时间延后且基线噪音减小. 经筛选,背压13.79 MPa、柱温为40 ℃时,缬沙坦与其异构体的峰形和分离度较好.

图2 方法开发色谱图(a)(b)CHIRALCEL OJ色谱柱(4.6 mm×250 mm,10 µm),(c)(d)CHIRALCEL IB色谱柱(4.6 mm×250 mm,5 µm),(e)CHIRALCEL IC-3色谱柱(100 mm×3.0 mm,3 µm),流动相:乙醇(内含0.2%三乙胺)溶液,(f)CHIRALCEL IC-3色谱柱(100 mm×3.0 mm,3 µm),流动相:乙醇(内含0.2%三氟乙酸)溶液,(g)CHIRALCEL IC-3色谱柱(100 mm×3.0 mm,3 µm),流动相:甲醇(内含0.5%乙醇胺)溶液,柱温 40 ℃,(h)CHIRALCEL IC-3色谱柱(100 mm×3.0 mm,3 µm),流动相:甲醇(内含0.5%乙醇胺)溶液,柱温 35 ℃Fig. 2 UPCC chromatograms of developmental method
2. 1. 3 流速的选择
合相色谱中,流速的变化会影响色谱保留时间和峰形,考察了流速0.9、1.0、1.5、2.0、3.0 mL/min,发现增大流速可使保留时间提前,峰形变窄,分离度降低,降低流速则反之. 试验结果表明,流速为1.0 mL/min时可获得较好的峰形和分离度.
2. 1. 4 流动相的选择
分离极性化合物时,温度和压强固然很重要,但是流动相的组成更为重要. UPCC流动相中的分子间相互作用力强烈依赖于流体密度,并且因其主要流动相为超临界CO2,极性过低,通常需加入有机溶剂作为改性剂改善峰形、保留时间和分离度. 常用的改性剂有甲醇、乙醇、异丙醇、乙腈、乙酸乙酯等[15]. 其次,向改性剂中加入酸性或碱性添加剂,这些添加剂能够附着于固定相的活性位点,用于增加固定相极性,增强极性溶剂的峰形[16]. 流动相经过筛选发现,改性剂为甲醇,添加剂为乙醇胺时,缬沙坦与其对映异构体的峰形和分离趋势较好,如图2(e)~(h)所示.
2. 2 方法学验证
2. 2. 1 专属性
按1. 3项下方法分别配制空白溶剂、对照溶液、供试品溶液和测试溶液,进样分析. 结果显示,空白溶剂对两者检测无干扰,测试溶液中S-缬沙坦和R-缬沙坦的分离度为2.038,如图3所示.
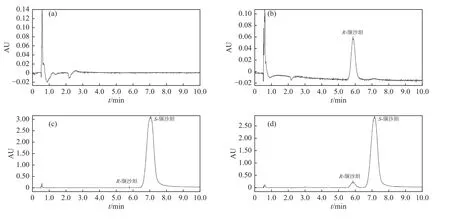
图3 专属性色谱图(a)空白溶剂,(b)对照溶剂,(c)供试品,(d)测试溶液Fig. 3 UPCC chromatograms of specificity
2. 2. 2 检测限和定量限
取1. 3项下S-缬沙坦和R-缬沙坦对照品储备液,使用甲醇逐步稀释,得到两者信噪比约为3的检测限溶液,信噪比约为10的定量限溶液. 结果表明,R-缬沙坦和S-缬沙坦的检测限分别为3.357、6.803 µg/mL,定量限分别为10.072、20.408 µg/mL.
2. 2. 3 溶液稳定性
按1. 3项下方法配制对照溶液、供试品溶液和测试溶液,每间隔1 h进样一次,连续考察12 h,对照溶液中R-缬沙坦峰面积相对标准偏差(RSD)为3.0%. 供试品溶液和测试溶液中S-缬沙坦峰面积RSD分别为7.1%和4.4%,R-缬沙坦峰面积RSD分别为8.0%和5.9%. 供试品溶液和测试溶液中无杂质个数的增加.
2. 2. 4 线性关系
取1. 3项下R-缬沙坦和S-缬沙坦对照储备液,采用甲醇配制成浓度梯度的混合线性溶液,依法测定. 峰面积(Y)为纵坐标,质量浓度(X)为横坐标,绘制线性回归曲线.R-缬沙坦在10.072~100.720 µg/mL质量浓度范围内,线性方程为Y=428.910 5X−1.059 8,r为0.998 0(n=7).S-缬 沙 坦 在20.408~102.040 µg/mL质量浓度 范 围 内,Y=443.936 8X−0.619 5,r为0.999 2(n=7).
2. 2. 5 回收率
按1. 3项下方法配制供试品储备液和R-缬沙坦的对照储备液,精密量取对照品储备液0.4、0.5、0.6 mL,分别加入供试品储备液2.5 mL,置于5 mL量瓶中加甲醇溶液定容即得80%、100%、120%的准确度溶液,每个浓度平行配制三份. 试验结果表明,R-缬沙坦回收率在99.40%~106.93%之间,平均回收率为104.35%,RSD为3.4%(n=9),结果如表1所列.

表1 R-缬沙坦回收率Table 1 Recoveries of R-valsartan
2. 2. 6 耐用性
分别考察标准条件,流速为(1.0±0.1) mL/min和背压为(13.79±0.69) MPa时,R-缬沙坦测定结果的变化,测试溶液含量的RSD为4.8%,表明此法耐用性良好.
2. 2. 7 样品检测
按1. 3项下方法制备供试品溶液,按1. 2项下条件测定,结果缬沙坦原料(200501、220101、220201)中R-缬沙坦的质量分数分别为0.36%、0.31%、0.35%.
3 结论
超高效合相色谱是不同于气相色谱、液相色谱的另外一种分离技术,是超高效液相色谱法与超临界流体色谱法的结合体,其流动相为液体和超临界气体的混合物. 对于液相色谱和气相色谱来说,合相色谱是一种可提供独特工作流程、应用和环境影响效益的补充性可靠色谱平台.
成功使用超高效合相色谱的关键是使化合物的性质与它的技术性质相匹配,以及改性剂和添加剂在优化分离中的重要作用.S-缬沙坦和R-缬沙坦要想得到良好分离,其极性需介于固定性和流动相之间,CO2作为流动相与正己烷的极性有点相似,在CO2中添加了甲醇为改性剂,其密度特性就随之变化,其变成取决于所用的共溶剂种类的二次保留机制. 其次,向改性剂中加入乙醇胺为添加剂,增加了固定相的极性. 之后通过柱温、流速等调整使其发生微妙的性质差异,从而得以分离. 本文首次建立了超高效合相色谱测定缬沙坦原料中R-缬沙坦的检测方法,经过系统验证,表明本方法简便、重复性高、准确度好,相比传统高效液相色谱法检测缬沙坦原料中R-缬沙坦的时间短,极大地提高了检测效率,并且有机试剂的使用少,不仅降低了成本,还减小了对实验人员的毒性危害.
