H-SAPO-34分子筛催化醇类转化的差异性研究
2022-12-28顾雅婷张雯娜韩晶峰楼才溢陈慧慧徐舒涛魏迎旭刘中民
顾雅婷,张雯娜,韩晶峰,楼才溢,陈慧慧,徐舒涛,魏迎旭#,刘中民*
1.低碳催化技术国家工程研究中心,中国科学院大连化学物理研究所,辽宁 大连 116023;2.中国科学院大学,北京 100049
引 言
低碳烯烃(乙烯、丙烯和丁烯)是重要的基础有机化工原料,在石油化工及精细化学品合成中起着不可或缺的作用.乙烯主要用于生产聚乙烯、聚苯乙烯、乙二醇和环氧乙烷等化工产品,丙烯主要用于生产聚丙烯、环氧丙烷、丙烯腈等有机化工原料,异丁烯主要用于生产汽油、润滑油添加剂、丁基橡胶、聚异丁烯,同时可以用来合成各种精细化工产品及中间体.近年来,低碳烯烃的需求量日益增大,化石类不可再生资源的消耗也在增加,因此开发环保、可持续生产低碳烯烃的路径迫在眉睫.
甲醇作为一种重要的平台化合物,可以由天然气、煤和生物质经气化得到的合成气进而制得.甲醇制烯烃(Methanol-To-Olefins,MTO)反应被认为是最具前景的采用非石油路线生产低碳烯烃的方法.该技术已经成功工业化,极大地缓解了石油资源短缺与匮乏的问题,对于低碳经济和国家能源战略安全具有重要意义.同时,丁醇作为重要的化工原料,是继乙醇之后一种新兴的生物质燃料,以生物法合成丁醇,并利用生物资源替代石油资源,能够实现环保、可持续发展,具有很大的应用潜力[1-3].相比传统的蒸汽裂解、催化裂化等工艺,由可再生资源生产丁烯及其它低碳烯烃的路线具有更加重要的意义[4-7].
用于醇类脱水制烯烃反应的催化剂种类繁多,包括研究者们已经报道的多种固体酸催化剂,例如无机酸、金属氧化物、沸石、酸性树脂等[8-11].其中,分子筛催化剂具有独特的孔道结构,且分子筛孔道/笼内具有多种酸性位点,通过酸性的调变和孔道结构的优化可以进一步提高其催化反应活性和控制产物选择性;同时,分子筛具有比表面积大、孔径分布均匀、水热稳定性好和择形催化等特点.因此,它已被广泛应用于化工生产过程[12-14],尤其是H-SAPO-34、H-ZSM-5 分子筛催化剂.其中,磷铝分子筛H-SAPO-34 在MTO 过程中表现出优异的催化性能和低碳烯烃选择性[15].得到广泛关注的分子筛催化C1分子甲醇是最为成功的分子筛催化醇类转化过程[16-19],并且近年来在第一个C-C 键的形成、反应高效转化期烯烃产物生成途径以及积碳失活方式等方面都取得了重要进展.但是由于MTO 反应机理极其复杂,仍然有许多问题(比如活性烃池物种的起源以及演变)值得进一步研究.1993年,BP 公司在叔丁醇脱水制异丁烯的过程中采用了Theta-1 分子筛催化剂[20].Madeira等[21,22]证实相比其它沸石,乙醇在H-ZSM-5 沸石催化剂上转化为C5-C11碳氢化合物的稳定性和活性更高,且有报道[23,24]认为单分子乙醇脱水机理与双分子乙醇脱水机理在乙醇脱水制乙烯的过程中共同存在.Mentzel 等[25]报道了在醇类制烯烃反应中,H-ZSM-5 沸石可以选择性地催化异丙醇制C4-C12烯烃.Zhang 等[26,27]通过研究具有中孔(10 元环孔)结构的沸石上正丁醇转化为异丁烯的反应过程,发现了ZSM-23 分子筛对生成异丁烯具有较高的选择性.醇类转化反应与醇分子本身链长和支链结构密切相关[28],与其它醇类相比,正丁醇转化过程中,中间体结构的不同、空间位阻效应、反应物的扩散以及水分子的影响都会导致脱水过程及反应机理有所不同.
本文旨在研究甲醇和丁醇在具有CHA 拓扑结构的H-SAPO-34 分子筛上的反应过程,采用气相色谱-质谱联用(Gas Chromatography-Mass Spectrum,GC-MS)技术、反应后催化剂溶解-萃取-存留物种分析技术,以及13C 交叉极化魔角旋转核磁共振(Cross Polarization Magic Angle Spinning Nuclear Magnetic Resonance,CP MAS NMR)技术进一步探讨两种醇类转化产物分布和反应中间物种的相似性与差异性.
1 实验部分
1.1 试剂和催化剂
12C-甲醇(CH3OH,纯度>99.9%)购于天津市科密欧化学试剂有限公司,12C-丁醇(C4H9OH,纯度>99.4%)购于阿法埃莎(天津)化学有限公司.13C-甲醇和13C-丁醇(纯度>99%)都来源于Cambridge Isotope Laboratories,Inc.二氯甲烷(CH2Cl2,纯度>99.5%)购于西陇科学股份有限公司.氢氟酸(40wt%)购于天津市科密欧化学试剂有限公司.高纯He 气(纯度为99.9%)购于大连特种气体有限公司.
H-SAPO-34 分子筛的合成方法参考文献[29]:以三乙胺(NEt3)为模板剂,硅溶胶(31wt%)、磷酸(85wt%)和拟薄水铝石(68.6wt%)分别作为硅源、磷源和铝源,采用水热合成法合成H-SAPO-34.合成的H-SAPO-34 分子筛具有良好的结晶度,分子筛晶粒呈现出规整的立方体形貌且分布均匀,晶粒大小约为3 μm,硅含量为0.09(Si/(Si+P+Al)=0.09).其相关表征,包括X-射线衍射(X-ray Diffraction,XRD)、X-射线荧光(X-ray Fluorescence,XRF)、扫描电子显微镜(Scanning Electron Microscope,SEM)、氨气程序升温脱附(NH3-temperature Programmed Desorption,NH3-TPD)实验等,已在文献[30]中进行了详细描述.
1.2 醇类转化性能评价与催化剂存留物种分析
1.2.1 醇类转化性能评价
12C 和13C 的甲醇、12C 和13C 的丁醇转化反应在固定床反应器中进行,采用内径为4 mm 的石英管微反应器.焙烧后的分子筛催化剂通过压片,并筛分成40~60 目的颗粒.饱和管内的甲醇或丁醇由载气(He)携带进入装有分子筛催化剂的反应器中进行反应,热电偶插入微反应器催化剂床层中间位置,以精确测量催化剂的床层温度.催化剂装填量为50 mg,甲醇质量空速(Weight Hourly Space Velocity,WHSV)为1 h−1;为了保持甲醇和丁醇以CH2为基准的进料空速一致,丁醇的实际WHSV 为0.58 h−1.典型的反应过程描述如下:取50 mg 40~60 目的分子筛颗粒装入石英管反应器,在650 ℃下通入空气活化0.5 h,再引入He 气活化0.5 h,待反应器温度降至预设反应温度350 ℃后,切换至原料甲醇或丁醇进料进行反应.使用Agilent GC 7890A 气相色谱仪连续采样并对气相产物进行在线分析.色谱仪使用HP-PLOT Q 色谱柱和氢火焰离子化检测器(Flame Ionization Detector,FID).对柱箱进行程序升温,温度由80 ℃升至220 ℃并保持10 min,升温速率为20 ℃/min.甲醇/丁醇转化率和选择性计算以CH2为基准.
1.2.2 反应后催化剂存留物种分析
在反应进行至22 min 时迅速取出催化剂,在液氮中速冷,根据Guisnet 等[31]报道的方法对反应后的催化剂进行存留物种分析.典型的操作过程描述如下:称取25 mg 反应后的催化剂样品于聚四氟乙烯瓶中,然后向瓶内加入约0.5 mL 20wt%的氢氟酸水溶液,震荡摇匀后静置30 min,等待催化剂样品完全溶解.向溶解后的溶液中加入0.5 mL 二氯甲烷(含有10 ppmv/v六氯乙烷为内标)震荡摇匀并静置30 min 以充分萃取有机存留物种,收集下层有机相液体,采用Agilent 7890A/5975C GC/MSD 联用系统进行分析.采用色谱柱为HP-5,柱箱起始温度为60 ℃,升温速率为5 ℃/min,升至280 ℃并保持20 min.根据NIST10 数据库定性.
1.3 13C CP MAS NMR 检测醇类转化后催化剂上的中间物种
采用13C CP MAS NMR 对H-SAPO-34 分子筛催化13C-甲醇和13C-丁醇反应催化剂表面物种进行检测.首先,在350 ℃下将13C-甲醇、13C-丁醇分别通入H-SAPO-34 分子筛催化剂床层反应22 min,然后将反应后的催化剂样品用液氮速冷,迅速转移至Ar 气氛手套箱内并装入NMR 转子中,密封后进行13C CP MAS NMR 测试.13C CP MAS NMR 谱图测试在配备3.2 mm HFXY 四共振探头的Bruker Avance NEO 500(11.75 Tesla)谱仪上进行,13C 核共振频率为125.75 MHz,使用CP 脉冲序列.13C-甲醇采样转速为12 kHz 和10 kHz,采样次数分别为1 960 次和1 696 次;13C-丁醇采样转速为12 kHz 和20 kHz,采样次数分别为26 116 次和3 664 次.脉冲时间间隔为2 s,接触时间为2 ms,化学位移参考金刚烷的高场次甲基峰(δC29.5).
2 结果与讨论
2.1 H-SAPO-34 上甲醇转化反应产物分布
在反应温度为350 ℃、甲醇WHSV 为1 h−1的条件下,对甲醇转化之后的气相流出物进行检测和跟踪.甲醇转化产物分布随时间的改变如图1所示.从图中可以看出,整个甲醇转化过程大致可分为三个阶段:反应诱导期、反应高效转化期、反应失活期.低碳烯烃(乙烯、丙烯和丁烯)是主要的反应产物,这说明八元环孔口的H-SAPO-34 具有优异的低碳烯烃选择性.在反应开始的最初2 min,甲醇并未完全转化,转化率为95%.气相产物中有微量的甲烷,主要产物乙烯、丙烯及丁烯,选择性分别为17%、41%、18%;随着反应的进行,甲醇转化率增加,当反应进行至22 min,甲醇达到完全转化,反应进入高效转化期.值得注意的是,在反应诱导期中,烃池物种大量生成且积累到较高水平,使得甲醇转化进入高效转化阶段.在随后的反应历程中,甲醇转化率均维持100%,乙烯、丙烯选择性上升,且丙烯的选择性高于乙烯的选择性,丁烯、戊烯、己烯等高碳链烯烃选择性下降.反应产物中丙烷的选择性较低约为7%,说明氢转移反应比较微弱.182 min 后反应进入失活期,当反应时间为282 min 时,对应的甲醇转化率降至77%,随着积碳物种的生成,H-SAPO-34分子筛床层限制甲醇分子的晶内扩散,使得反应物料难以进入分子筛内表面,因而甲醇转化率下降,导致催化剂快速失活.此前我们的工作[32]采用自建的扩散原位表征方法首次呈现催化剂扩散性质随MTO 反应的演变过程,解释了H-SAPO-34 上八元环孔口的限制作用引导其催化MTO 反应以生产低碳烯烃为主的产物特点,揭示了由扩散性能改变导致产物分布的变化.

图1 350 ℃下甲醇在H-SAPO-34 分子筛上反应的转化率和产物选择性随时间(TOS)的变化Fig.1 The conversion and selectivity of products of the methanol conversion on H-SAPO-34 with time on stream (TOS) at 350 ℃
此外,除了扩散性能引起产物分布差异,分子筛催化甲醇反应过程中活性烃池物种的变化、反应途径的选择以及反应条件的差异将直接影响产物分布.在早期甲醇转化反应机理研究[33-35]中,由烯烃物种、环戊烯基物种以及芳烃物种主导的烯烃循环、环戊二烯循环、芳烃循环引导了H-SAPO-34分子筛中烯烃产物的生成.随着甲醇反应的进行,乙烯和丙烯的选择性升高,C4烯烃选择性降低,这可能是由于在反应高效转化期,三种循环共同作用生成烯烃,其中由于H-SAPO-34 笼的限域作用,较大的环戊烯基物种和芳烃物种是主要的活性物种,随着反应的失活,受到扩散限制和反应活性物种的改变,烯烃作为烃池物种引导低碳烯烃的生成.因此,酸性分子筛上烯烃循环与芳烃循环的比例、苯基碳正离子甲基取代基的个数等对烯烃产物的生成均产生较大影响[36,37],而烃池物种的生成也受到分子筛结构、酸性、扩散性能等多方面的影响.因此,分子筛催化甲醇转化时,不同阶段的反应活性物种、反应途径的选择以及扩散限制等共同决定了甲醇转化产物分布.
2.2 H-SAPO-34 上丁醇转化反应产物分布
我们进一步考察了350 ℃下H-SAPO-34 分子筛催化丁醇转化为烯烃(Butanol-To-Olefins)反应性能.图2展示了350 ℃下H-SAPO-34 分子筛上丁醇转化的气相产物分布随时间的变化.在近21 h 反应过程中,丁醇的转化率一直保持在100%,丁醇转化反应的主要产物是丁烯,说明丁醇转化主要发生丁醇脱水反应.产物丁烯的选择性随反应时间的延长由50%逐渐增加到82%.此外,丙烯、戊烯等其它产物的选择性在初始时较高,随反应时间延长而逐渐降低,其中丙烯产物初始选择性为39%.丁醇反应21 h(1 262 min)后仍未失活,依然保持很高的反应活性,且以丁烯为主要产物,因此可以推测在350 ℃,空速为0.58 h−1的反应条件下,丁醇脱水生成丁烯为主要反应,特别是在反应后期.对于H-SAPO-34 分子筛催化丁醇反应,各种烯烃的生成以及它们可能涉及的反应中间体、反应途径还有待进一步探究.
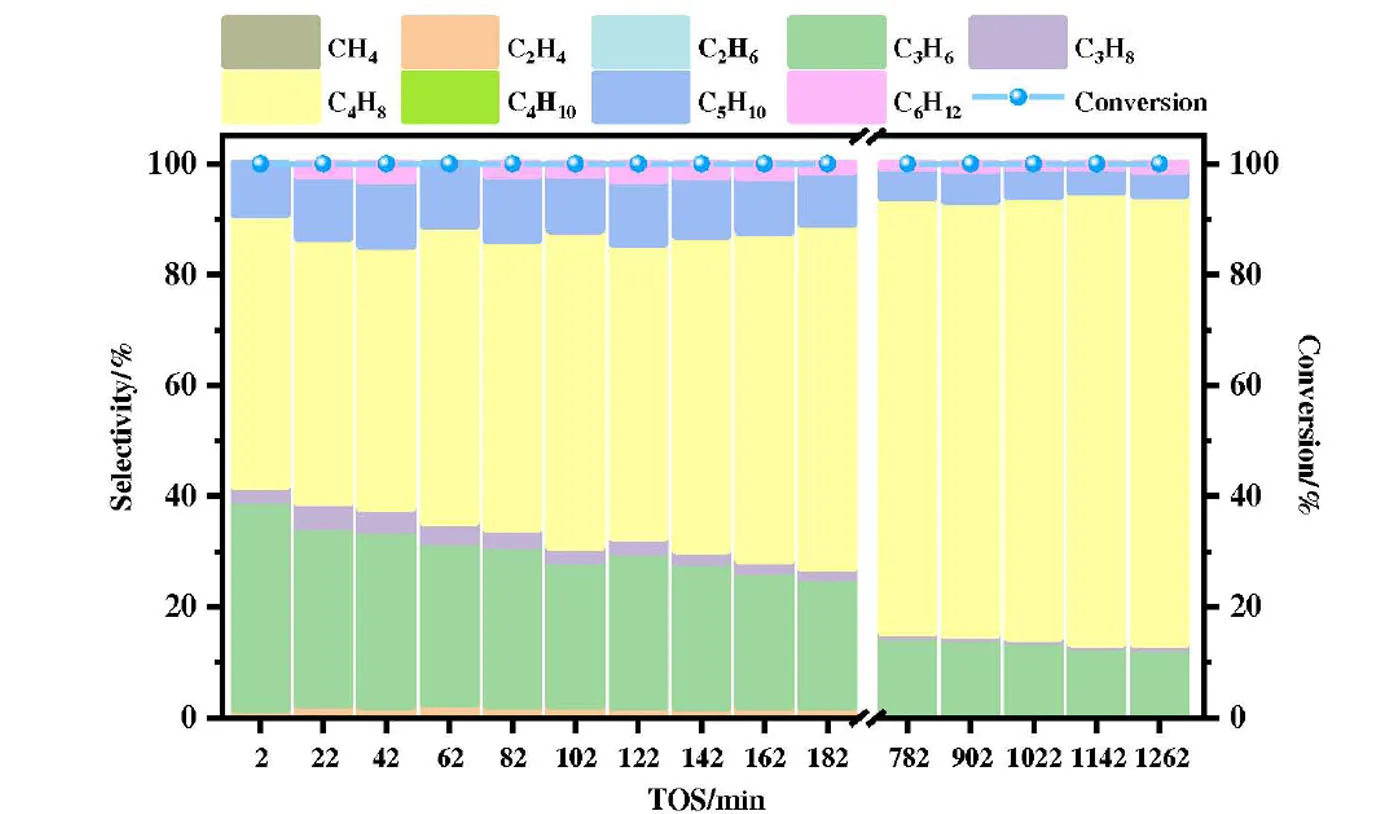
图2 350 ℃下丁醇在H-SAPO-34 分子筛上反应的转化率和产物选择性随时间(TOS)的变化Fig.2 The conversion and selectivity of products of the butanol conversion on H-SAPO-34 with time on stream (TOS) at 350 ℃
2.3 H-SAPO-34 催化甲醇转化反应后催化剂存留物种组成
为了确定H-SAPO-34 分子筛笼内存留有机物种,当甲醇转化22 min 时,切断甲醇进料,用液氮速冷方式,得到22 min 反应后的催化剂,用氢氟酸溶解反应后的H-SAPO-34 分子筛催化剂,并用CH2Cl2萃取其中的有机物种,采用GC-MS 分析存留有机物种组成,结果如图3所示.由图3可以看出,该反应条件下,H-SAPO-34 分子筛上有机物种主要包括环烷烃、多甲基苯、金刚烷、萘四类物种.在22 min 时,甲醇100%转化,反应处于高效转化期,此时存留物种主要为多甲基苯物种,包括保留时间为17.0 min 的三甲基苯、20.5 min 的四甲基苯、25.1 min 的五甲基苯,这些物种可能作为重要的芳烃物种参与芳烃循环引导低碳烯烃生成,促使甲醇高效转化.与此同时,存留物种分析中检测到环烷烃(如环戊烷、环己烷),这可能是由于高碳链的烯烃受到H-SAPO-34 孔口限制不易扩散出来,发生环化反应所致.除此之外,还观察到少量的甲基茚,对应的保留时间为20.3 min,其作为积碳前驱体引导多甲基萘的生成已经被报道[38].值得注意的是,在350 ℃反应条件下有少量金刚烷类化合物的生成,但这并不是主要的积碳物种.一般而言,金刚烷类在低温(250~300 ℃)反应条件容易生成[39],是H-SAPO-34 催化剂上低温失活的主要物种.此时存留物种中观察到萘基物种,它可能是350 ℃反应条件下主要的失活物种.由此可见,在350 ℃反应条件下,主要的存留物种由环烷烃、多甲基苯类以及萘基物种组成,这些物种与反应过程中烯烃物种的生成以及烯烃物种的转化密切相关.

图3 H-SAPO-34 分子筛催化甲醇转化22 min 后催化剂中存留物种的气相色谱图Fig.3 Gas chromatograms of retained organic species in the H-SAPO-34 after methanol conversion for 22 min
2.4 H-SAPO-34 上丁醇转化反应后催化剂存留物种组成
H-SAPO-34 催化甲醇转化过程中催化剂上主要的存留有机物种是多甲基苯类、环烷烃以及萘基物种,同时这些存留有机物种可能在烃池物种生成以及积碳物种演变过程中发挥关键性的作用,此前已经报道了甲醇转化过程中由环戊烯基物种、芳烃物种以及烯烃物种参与三循环机理可以共同引导烯烃的生成[33-35].而对于丁醇转化反应,其表现出与甲醇不同的产物分布,为了揭示两者之间的异同点,我们选取丁醇转化22 min 后H-SAPO-34 分子筛催化剂中存留的有机物种进行GC-MS 分析.如图4所示,350 ℃丁醇转化,H-SAPO-34 分子筛笼内有机物种主要为甲苯、二甲苯、三甲苯(保留分别为时间为11.5 min、13.7 min、17.0 min),其可能是由低碳烯烃物种通过聚合、环化、氢转移以及芳构化过程产生.同时发现存留有机物种中含有较多带侧链的芳烃(保留时间为19.8 min),这些物种可能是由多甲基苯物种和丁基发生侧链烷基化而来.此外,还有少量金刚烷类物种、萘基物种、四氢萘和甲基茚物种的出现,这些与H-SAPO-34 上甲醇转化的失活物种类似,同时该反应中萘基物种也有可能由带有侧链的烷基苯物种经过环化生成茚等物种演变生成[38].值得注意的是,存留物种中发现了环状烷烃、环状烯烃(如环戊烷、环己烷、环戊二烯、环己烯等)的存在,这些物种可能是由长链烯烃物种逐步环化、氢转移反应而来.对比分析甲醇和丁醇转化过程中存留有机物种可以发现,多甲基苯物种均是主要的存留有机物种,可见多甲基苯物种均可能作为醇类转化生成烯烃的重要中间物种.然而,尽管多甲基苯是两种醇类转化重要的中间物种,而在甲醇转化中主要以多甲基数目的甲基苯为主,在丁醇转化中主要是含有少甲基数目的甲基苯.这主要源于在甲醇转化过程中,当烃池物种多甲基苯积累形成,反应进入高效转化期,此时这些多甲基苯参与芳烃循环,不断与甲醇发生甲基化反应,促进了多甲基数目的甲基苯的形成,同时之前机理研究发现在H-SAPO-34 催化甲醇转化过程中,含有甲基数目较多的六甲基苯以及七甲基苯基碳正离子是主要的活性烃池物种,这些物种在限域的H-SAPO-34 空间内具有较好的稳定性[40].而在丁醇转化过程中,却以甲基数目较少的甲基苯为主,这主要是由于丁醇转化过程中生成的长链烯烃物种直接发生聚合、环化、氢转移等二次反应生成少甲基数取代的甲基苯.同时在整个甲醇和丁醇转化过程中均观察到各种环状有机物种的生成,说明在醇类转化过程中,环状有机物种可能由反应过程中的烯烃物种演变而来.
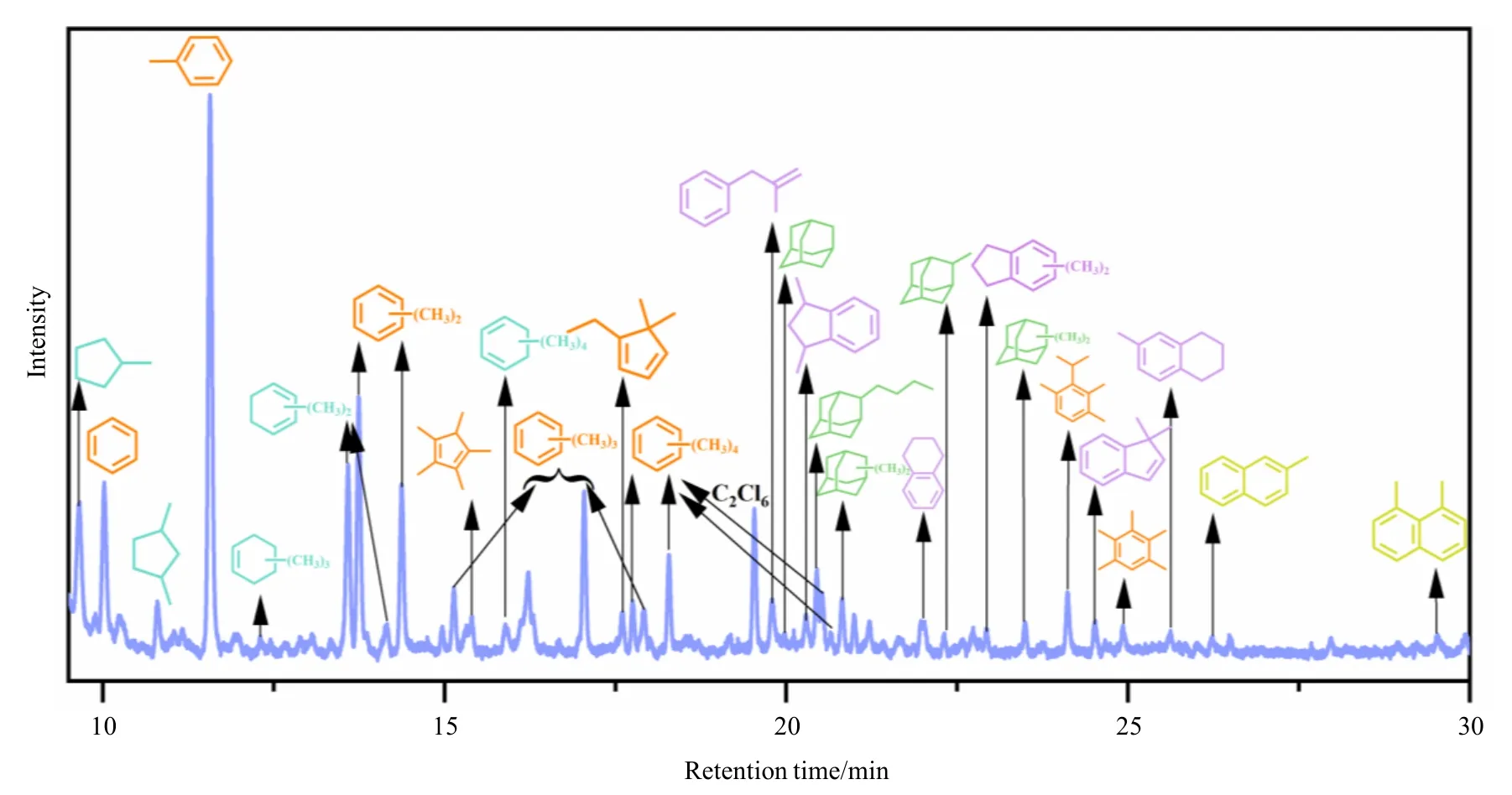
图4 H-SAPO-34 分子筛催化丁醇转化22 min 后催化剂中存留有机物种的气相色谱图Fig.4 Gas chromatograms of retained organic species in the H-SAPO-34 after butanol conversion for 22 min
2.5 H-SAPO-34 分子筛催化甲醇和丁醇反应表面物种的固体NMR 研究
为了深入研究H-SAPO-34 分子筛催化甲醇和丁醇反应过程中反应活性中间物种,我们进行了13C CP MAS NMR 测试,谱图如图5(a)所示.从图中可以看出,δC20 处出现一个较强的信号峰,主要来自多甲基苯的甲基信号[41].据报道,δC30~40 的信号可归属为饱和烷烃物种的亚甲基信号,饱和烷烃物种包括烷基金刚烷、饱和环烷烃以及链状的烷烃物种等[41].此外,催化剂表面δC51.5 的信号可归属为吸附态的甲醇.在13C CP MAS NMR 谱图中,明显可以看到位于δC126~135 的多甲基苯物种芳环碳的信号[42],这些芳烃物种来自于烯烃聚合、环化和氢转移等反应过程,与存留物种GC-MS 分析相一致.值得注意的是,δC116.5 处出现一个显著的信号峰,可能来自于聚合的烯烃碳的信号[43].除此之外,在δC155.2 有共振峰的出现,但δC250.0 处由于旋转边带的影响并不能确定,因此,将转速由12 kHz 变为10 kHz,如图5(c)所示,可以观察到δC250.0 处有微弱的信号,说明有环戊烯基碳正离子的生成.这两类不饱和物种在高效转化期大量积累说明多甲基苯、环戊烯基碳正离子是甲醇转化生成的关键中间物种[40,44],两者之间可以相互转化,共同引导低碳烯烃的生成.并且13C CP MAS NMR 成功观测了催化剂表面生成的碳正离子物种,这些结果对应了2.3 节存留物种分析中芳烃和环戊烯基物种的生成.
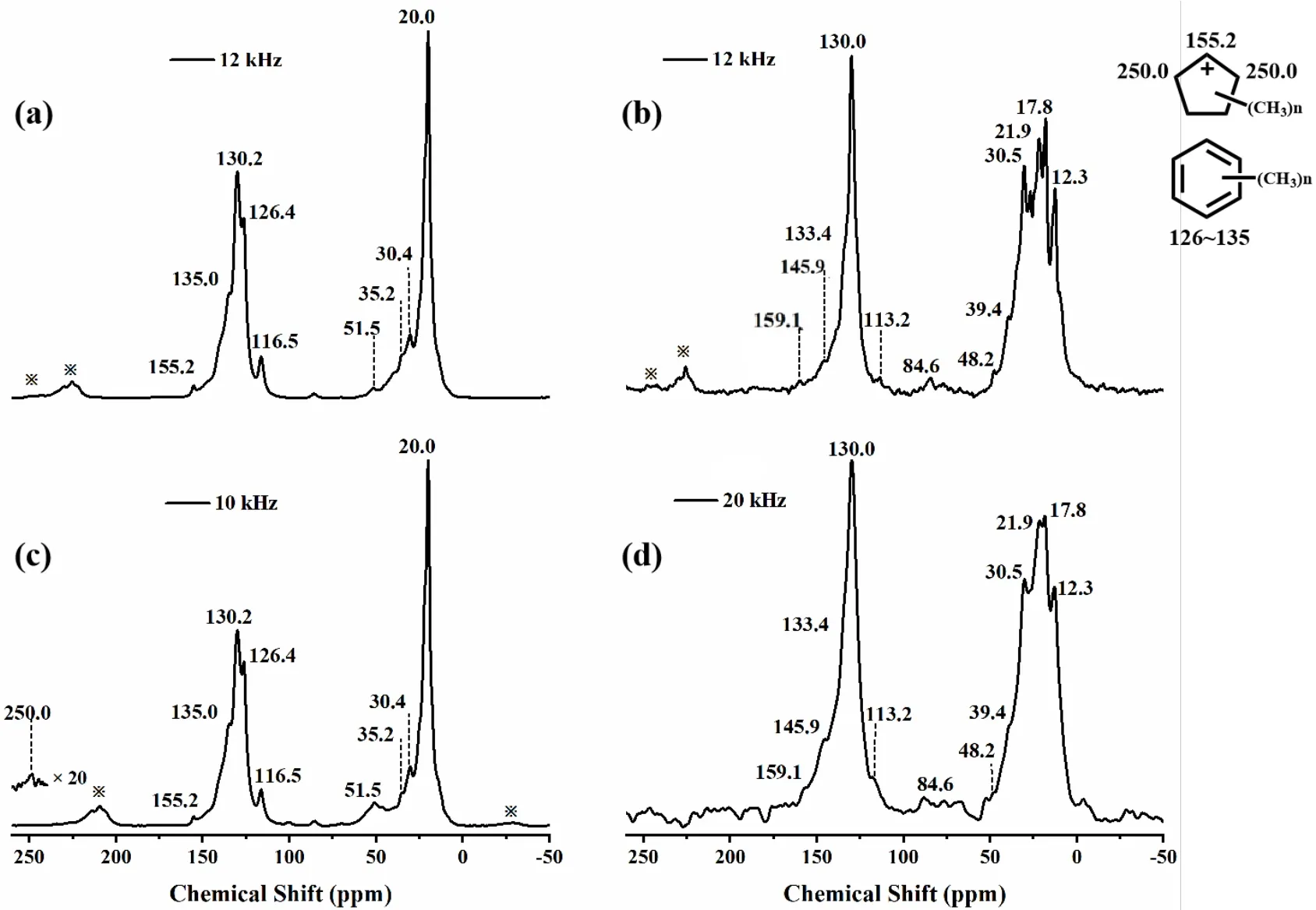
图5 13C-甲醇(a, c)和13C-丁醇(b, d)分别在H-SAPO-34 催化剂上反应的13C CP MAS NMR 谱图,反应时间为22 min.※表示旋转边带Fig.5 13C CP MAS NMR spectra of H-SAPO-34 catalyst after 13C-methanol conversion (a, c) and 13C-butanol conversion(b, d), respectively.The reaction time was 22 min.※indicates the spinning sidebands
丁醇转化气相产物分析发现丁烯为主要产物,推测丁醇在分子筛表面进行吸附、脱水、转化等一系列反应并最终生成丁烯.进一步采用13C CP MAS NMR 技术对13C-丁醇转化22 min 后H-SAPO-34分子筛表面物种的生成与作用进行详细研究.图5(b)显示与甲醇转化不同,δC10~50 区域内观测到更为显著且复杂的化学位移信号(δC12.3、17.8、21.9、30.5、39.4、48.2),其中δC12.3 可归属于链状烷烃中甲基(-CH3)碳的信号峰[45],δC17.8、21.9 处的信号可归属于环烷烃或链状烷烃中亚甲基(-CH2-)碳或者甲基苯中甲基碳的信号峰[46],而δC30 ~ 50 处信号被认为是烯烃低聚或者二次反应生成的烃类物种(如环烷烃、金刚烷类化合物)中具有sp3杂化的亚甲基(-CH2-)碳的信号峰[43],这意味着丁醇通入分子筛生成烯烃后,二次反应生成结构更为复杂的烃类物种,这些烃类物种可能正是存留物种中观察到的环状有机物种如环烷烃以及金刚烷物种,复杂的烃类物种将进一步促进丁醇转化.值得注意的是,δC84.6 处出现一个较弱的信号峰,可能来自于丁氧基或者丁基醚类[45].δC113.2 处的信号峰可类似甲醇转化中位于δC116.5 处的聚合烯烃碳的信号[43].此外,δC130~140同样出现了芳烃物种的信号峰,且其信号峰较强,说明丁醇转化生成的长链烯烃物种容易发生聚合、环化、氢转移反应生成大量芳烃.然而与甲醇转化不同的是,在丁醇转化过程中,即使改变转速后,在350 ℃反应条件下仍未观测环戊烯碳正离子特征信号出现,说明在丁醇转化过程中,芳烃物种是主要的中间物种.
13C CP MAS NMR 实验清楚地揭示了在350 ℃反应条件下,甲醇和丁醇在H-SAPO-34 分子筛上转化的过程,两种醇类转化均捕获到了芳烃物种,说明芳烃物种是甲醇转化和丁醇转化的分子筛催化剂上共同的存留物种,可以作为中间物种引导反应发生,也可能作为共同的积碳物种引导失活的发生.在甲醇转化中,这些中间物种来自于烯烃聚合、环化和氢转移等反应过程;而在丁醇转化过程中,丁醇首先脱水生成丁烯,进而丁烯通过裂解、聚合、环化、芳构化等二次反应生成低碳烯烃以及C4+以上产物,同时小分子烯烃和丁烯又可以通过环化、芳构化进一步生成环状有机物种.
3 结论
本文针对分子筛催化醇类转化,采用GC-MS、13C CP MAS NMR 技术详细研究了甲醇和丁醇在H-SAPO-34 分子筛上的转化过程.在甲醇转化过程中,C1物种甲醇通过MTO 反应生成具有C-C键的烯烃产物,并以乙烯、丙烯和丁烯作为主要产物;而丁醇反应以脱水为主,在反应初期也会发生催化裂解反应,以丙烯和丁烯作为主要产物.研究发现,甲醇和丁醇在H-SAPO-34 催化剂上转化都以多甲基苯物种、环状烷烃物种以及少量的萘基物种作为存留有机物种.而丁醇转化除了多甲基苯物种,还有少量含有丁基侧链的芳烃物种生成,这些可能是积碳失活物种的前驱体.重要的是,芳烃物种是H-SAPO-34 分子筛催化醇类转化共同的存留物种,在不同反应阶段作为反应的中间物种和积碳失活物种作用于醇类转化反应.
致谢
感谢国家自然科学基金(22002157、21991092、21991090、22022202)的资助.
利益冲突
无
