取食施硅水稻对褐飞虱成虫体内保护酶和解毒酶活性的影响
2022-12-28韩永强李丹丹邓权权侯茂林
韩永强, 李丹丹, 邓权权, 侯茂林
(1. 宜春学院生命科学与资源环境学院, 江西省作物生长发育调控重点实验室, 江西 宜春 336000; 2. 中国农业科学院植物保护研究所, 植物病虫害生物学国家重点实验室, 北京 100193)
褐飞虱Nilaparvatalugens是我国水稻上重要的害虫之一,不仅刺吸稻株汁液造成直接危害,也可传播病毒造成间接危害,严重威胁水稻生产安全(Chengetal., 2013)。目前褐飞虱防治主要依赖化学杀虫剂,但长期过量使用杀虫剂,不仅会增强褐飞虱抗药性,导致杀虫剂防效下降;同时会杀死害虫天敌,破坏稻田生态平衡,造成害虫再猖獗(Tanakaetal., 2000)。应用抗虫品种是防治褐飞虱经济有效的措施之一,然而褐飞虱致害性的变异加剧了抗虫品种的选育难度(吕仲贤等, 2002)。采用栽培管理措施提高植物自身抗虫性成为害虫防治可供选择的方法之一。
硅通常不被认为是植物生长所必需的元素,但由于它在植物营养方面的重要作用,被认为是一种“有益物质”或“准必需物质”(Ma, 2004)。研究表明,褐飞虱取食施硅水稻时存活率、羽化率、栖息率、取食量、产卵量和卵孵化率降低,而且若虫期延长、成虫寿命缩短、种群增长率降低(Heetal., 2015; Yangetal., 2017b; Linetal., 2022),说明施硅能够增强水稻对褐飞虱的抗生性、降低褐飞虱对水稻的选择性。此外,施硅也可调控褐飞虱诱导的水稻防御反应,包括激活水杨酸信号通路、增强多种防御酶活性、促进植物次生代谢物积累(Alagaretal., 2010; Yangetal., 2017a; Linetal., 2022)和诱导胼胝质沉积(Yangetal., 2018)。
与植物防御策略相对应,昆虫也进化出多种生理机制以适应植物防御,其中保护酶系和解毒酶系就是主要的适应方式之一(刘建业等, 2014)。超氧化物歧化酶(superoxide dismutase, SOD), 过氧化物酶(peroxidase, POD)和过氧化氢酶(catalase, CAT)是昆虫体内重要的保护酶系,在维持昆虫内环境活性氧平衡及生理代谢平衡方面具有重要作用(Lozinskayaetal., 2004)。此外,谷胱甘肽S-转移酶(glutathione-S-transferase, GST), 羧酸酯酶(carboxylesterase, CarE)和多功能氧化酶(mixed-functional oxidase, MFO)是昆虫体内重要的解毒酶系,能够代谢外源和内源有毒物质,是昆虫适应逆境胁迫及植物防御的重要方式(Tiwarietal., 2011)。
施硅对褐飞虱寄主选择性、取食行为、生长发育、存活、繁殖和种群增长的影响已有报道(Heetal., 2015; Yangetal., 2017b; Linetal., 2022)。前人研究证实,寄主植物、水稻品种能诱导褐飞虱、白背飞虱Sogatellafurcifera和灰飞虱Laodelphaxstriatellus体内酶活性发生变化(吴刚等, 1993; 赵士熙等, 1993; 吕仲贤等, 1997; 朱麟等, 2000; 陈建明等, 2002; Yaoetal., 2002; 周亦红等, 2003; 刘玉坤等, 2011; 丁杰, 2020),施硅可引起水稻组织和理化性状的变化(Yangetal., 2017a; 贾路瑶等, 2020; Linetal., 2022),褐飞虱取食施硅水稻后其体内酶活性也可能发生改变。为此,本研究采用水培实验,测定和分析水稻施硅对褐飞虱成虫保护酶和解毒酶活性的影响,以期阐明取食施硅水稻后褐飞虱体内酶活性的变化与施硅增强水稻抗虫性之间的关系,为硅肥用于褐飞虱种群调控奠定理论基础。
1 材料与方法
1.1 供试水稻及施硅处理
供试水稻品种为台中1号(Taichung Native 1, TN1)(感虫品种)。水稻种子用10% H2O2消毒并用去离子水清洗3次后,置于人工气候室催芽至露白,以放有石英砂的塑料育秧盒(长×宽×高=40 cm×30 cm×15 cm)作苗床播种,10 d后幼苗移栽到装有30 L木村B营养液(Yoshidaetal., 1976)的塑料盒(长×宽×高=71 cm×45 cm×18 cm)中。每塑料盒移栽48株稻苗,营养液每7 d更换1次,每天调节pH值至5.0~6.0之间。
采用营养液添加Na2SiO3·9H2O的方法设置施硅与不施硅处理。施硅处理(Si+)与不施硅处理(Si-)的硅添加浓度分别为112与0 mg Si/L。为避免雨水的影响和自然发生害虫的为害,水培稻苗置于温室内。
1.2 供试虫源
褐飞虱初始种群采自宜春学院实习农场,用盆栽不施硅TN1稻苗在温室纱网笼罩中饲养2代后,取褐飞虱长翅型雌成虫用于实验。
1.3 试虫处理
取移栽后30日Si+和Si-水培稻苗,稻苗茎基部用海绵塞(直径4 cm,高3 cm)固定后插入到装有150 mL施硅或不施硅营养液的玻璃管(直径4 cm,高25 cm)中,玻璃管管口以海绵塞封口,上下海绵塞相距8 cm,在两个海绵塞中间接入10头褐飞虱长翅型雌成虫,接虫稻苗置于人工气候室(温度26±1℃,相对湿度85%±5%,光周期14L∶10D)。待取食时间达24, 48, 72和96 h时,随机采集接虫稻苗上的褐飞虱成虫,每处理每时段采集180头(每60头为1次重复,重复取样3次),液氮速冻后-80℃保存,用于酶活性测定。
1.4 酶液制备及酶活性测定
1.4.1酶液制备:取1.3节冷冻保存的褐飞虱成虫60头,称重后,按重量(g)∶体积(mL)=1∶9的比例加入无菌0.9%生理盐水,冰浴匀浆,匀浆液于4℃ 2 500 r/min条件下离心10 min,取上清液为保护酶和解毒酶待测液。
1.4.2酶活性测定:采用南京建成生物工程研究所生产的CAT, POD, SOD, GST, CarE和MFO活性检测试剂盒测定1.3节不同处理褐飞虱成虫体内酶活性。测定方法按照各酶活性试剂盒说明书进行,酶液蛋白质含量采用考马斯亮蓝法(Bradford, 1976)测定。酶活性单位用U/mg表示。每处理每时段的保护酶和解毒酶活性采用不同样品重复测定3次。
1.5 数据分析
试验所得数据采用SPSS16.0统计软件进行分析。用双因素方差分析(two-way ANOVA)检验施硅处理、取食时间及两者交互作用对褐飞虱成虫保护酶和解毒酶活性影响的显著性。用独立样本t检验比较同一取食时间Si+和Si-处理组间酶活性的差异显著性(P=0.05)。
2 结果
2.1 取食施硅水稻对褐飞虱成虫体内保护酶活性的影响
2.1.1CAT活性:双因素方差分析结果表明,施硅处理对褐飞虱成虫CAT活性影响不显著(F=0.236,df=1,23,P=0.634),而取食时间有显著影响(F=14.813,df=3,23,P<0.001),两者之间存在的交互作用也有显著影响(F=8.747,df=3,23,P=0.001)(图1: A)。褐飞虱成虫取食水稻植株24, 48和96 h时,CAT活性在Si+与Si-处理组间差异不显著(|t|≤2.022,df=4,P≥0.113);取食Si+植株72 h时CAT活性最大,比取食Si-植株的显著增加16.5%(|t|=4.087,df=4,P=0.015)(图1: A)。
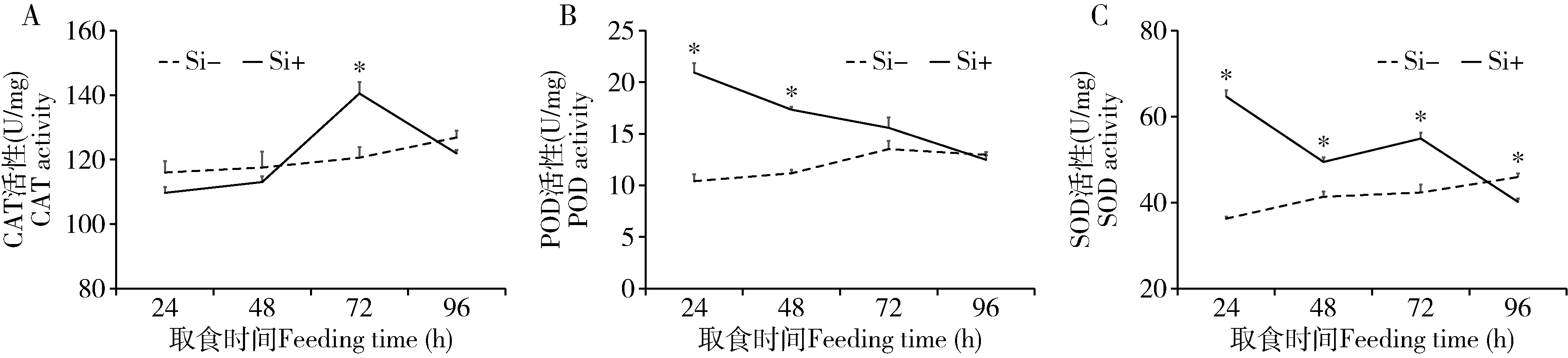
图1 褐飞虱成虫取食施硅(Si+)或不施硅(Si-)水稻植株后体内保护酶过氧化氢酶(CAT)(A)、过氧化物酶(POD)(B)和超氧化物歧化酶(SOD)(C)活性的变化Fig. 1 Changes in the activities of protective enzymes, catalase (CAT)(A), peroxidase (POD)(B) and superoxide (SOD)(C), in Nilaparvata lugens adults feeding on rice plants applied with silicon (Si+) or not applied with silicon (Si-) Si+: 施硅(112 mg Si/L)水稻植株Rice plants grown in nutrient solution added with 112 mg Si/L; Si-: 不施硅水稻植株Rice plants grown in nutrient solution without addition of silicon. 图中数值为平均数±标准误;星号表示同一时间点Si+和Si-处理组间差异显著(P<0.05, t检验)。图2同。Data in the figure are mean ±SE. The asterisk indicates significant difference between Si+ and Si- treatment groups at the same time point (P<0.05, t-test). The same for Fig. 2.
2.1.2POD活性:施硅处理(F=97.309,df=1,23,P<0.001)、取食时间(F=6.868,df=3,23,P=0.003)及其交互作用(F=27.170,df=3,23,P<0.001)均显著影响褐飞虱成虫POD活性(图1: B)。褐飞虱成虫取食水稻植株24和48 h时,Si+处理组POD活性显著高于Si-处理组(|t|≥9.299,df=4,P≤0.001),分别增加101.2%和55.2%;取食水稻植株72和96 h时,POD活性在Si+和Si-处理组间没有显著差异(|t|≤1.585,df=4,P≥0.188)(图1: B)。
2.1.3SOD活性:与POD活性一样,施硅处理(F=163.636,df=1,23,P<0.001)、取食时间(F=15.232,df=3,23,P=0.001)及其交互作用(F=69.227,df=3,23,P<0.001)对褐飞虱成虫SOD活性均有显著影响(图1: C)。褐飞虱成虫取食Si+植株24, 48和72 h时,其SOD活性分别比取食Si-植株的显著增加78.2%, 19.6%和29.7%(|t|≥5.166,df=4,P≤0.007);取食96 h时,SOD活性反而显著降低12.6%(|t|=5.008,df=4,P=0.007)(图1: C)。
2.2 取食施硅水稻对褐飞虱成虫体内解毒酶活性的影响
2.2.1GST活性:施硅处理(F=327.578,df=1,23,P<0.001)、取食时间(F=58.650,df=3,23,P<0.001)对褐飞虱成虫GST活性有显著影响,两者间的交互作用也有显著影响(F=48.460,df=3,23,P<0.001)(图2: A)。褐飞虱成虫取食Si+植株24, 48, 72和96 h时,其GST活性分别比取食Si-植株的显著增加57.2%, 200.7%, 84.7%和45.9%(|t|≥4.711,df=4,P≤0.009)。

图2 褐飞虱成虫取食施硅(Si+)或不施硅(Si-)水稻植株后体内解毒酶谷胱甘肽S-转移酶(GST)(A),羧酸酯酶(CarE)(B)和多功能氧化酶(MFO)(C)活性的变化Fig. 2 Changes in the activities of detoxification enzymes, glutathione-S-transferase (GST)(A), carboxylesterase (CarE)(B) and mixed-functional oxidase (MFO)(C), in Nilaparvata lugens adults feeding on rice plants applied with silicon (Si+) or not applied with silicon (Si-)
2.2.2CarE活性:施硅处理对褐飞虱成虫CarE活性有显著影响(F=69.680,df=1,23,P<0.001),取食时间对褐飞虱成虫CarE活性没有显著影响(F=2.813,df=3,23,P=0.073),两者的交互作用对褐飞虱成虫CarE活性有显著影响(F=13.242,df=3,23,P<0.001)(图2: B)。褐飞虱成虫取食水稻植株24和48 h时,CarE活性在Si+与Si-处理组间差异不显著(|t|≤1.975,df=4,P≥0.119);取食72和96 h时,Si+处理组显著低于Si-处理组(|t|≥5.203,df=4,P≤0.007),分别降低38.1%和32.0%。
2.2.3MFO活性:施硅处理(F=20.098,df=1,23,P<0.001)、取食时间(F=17.380,df=3,23,P<0.001)对褐飞虱成虫MFO活性有显著影响,两者之间的交互作用对MFO活性有显著影响(F=15.541,df=3,23,P<0.001)(图2: C)。褐飞虱成虫取食水稻植株24和48 h时,其MFO活性在Si+和Si-处理组间没有显著差异(|t|≤1.268,df=4,P≥0.273);取食72和96 h时,Si+处理组显著高于Si-处理组(|t|≥2.988,df=4,P≤0.040),分别增加70.2%和28.3%。
3 讨论
研究表明,杀虫剂、温度、干旱、CO2浓度、寄主植物能诱导昆虫体内保护酶活性发生变化,以适应外界不利环境。如褐飞虱被黄绿绿僵菌侵染后,体内SOD和CAT含量显著上升(张珏锋等, 2018);高温、干旱、CO2浓度升高能使褐飞虱体内SOD和CAT活性显著升高(冯从经等, 2001; 罗定, 2012; 曾芸芸等, 2012);褐飞虱和白背飞虱取食感染水稻黑条矮缩病或南方水稻黑条矮缩病的稻株后,体内SOD, POD和CAT活性显著增加(Xuetal., 2014; 陈晨等, 2016)。
本研究发现,褐飞虱成虫取食Si+水稻植株24和48 h时,SOD和POD活性显著高于取食Si-植株;取食Si+植株72 h时,SOD和CAT活性显著高于取食Si-植株(图1)。推测取食Si+植株可能会增加褐飞虱体内自由基含量,进而诱导SOD, POD和CAT活性上升,以清除过量自由基。说明取食Si+水稻前期(24-48 h)和中期(48-72 h),褐飞虱通过增大体内保护酶活性的方式来保护和维持机体的正常功能。这与吕仲贤等(1997)、陈建明等(2002)和刘玉坤等(2011)的研究结果相类似,他们的结果表明,褐飞虱、白背飞虱和灰飞虱取食耐虫性或抗生性水稻品种,体内SOD, POD和CAT活性显著高于取食感虫品种的。
褐飞虱成虫取食Si+植株72-96 h内,CAT, POD和SOD活性均有不同程度的降低,并在96 h时低于Si-处理组,其中SOD活性的降低达到显著水平(图1)。可见取食Si+水稻后期(72-96 h),由于保护酶活性不能长时间维持应激水平,导致体内活性氧物质不断积累,自由基代谢失衡,从而对虫体造成氧化损伤。在稻纵卷叶螟Cnaphalocrocismedinalis上也报道了类似结果,稻纵卷叶螟幼虫取食施硅水稻前期,体内SOD, POD和CAT活性呈上升趋势;取食后期,SOD, POD和CAT活性下降(韩永强等, 2016)。推测褐飞虱体内保护酶活性的变化可能与施硅提高了水稻对褐飞虱的抗生性有关(Heetal., 2015; Yangetal., 2017b; Linetal., 2022)。
昆虫在长期进化过程中形成了解毒、避毒、藏毒等适应性策略来应对植物防御。比如,通过改变解毒酶活性,对摄入体内的外源或内源有毒物质(如杀虫剂、植物次生代谢物等)进行解毒和排毒(陈澄宇等, 2015)。其中,GST能催化有毒物质的亲电子基团与还原型谷胱甘肽(GSH)的巯基偶联,增加其疏水性使其易于排出体外(尤燕春等, 2013);CarE能水解酯类化合物的酯键,或与亲脂类有毒化合物结合,通过降低其有效浓度来降低毒性(张丽阳和刘承兰, 2016);MFO可通过过氧烷基、羟基化环氧化和硫醚氢化等方式参与杀虫剂和毒素的代谢(余源婵等, 2022)。
本研究中,褐飞虱成虫取食Si+植株24-96 h时,GST活性均显著高于Si-处理组(图2: A)。原因可能是昆虫取食胁迫诱导植物激活体内的防御反应,施硅处理可能在一定程度上放大了植物的这种诱导防御反应(Yangetal., 2017a; Linetal., 2022),通过增加植物次生代谢物的合成和积累,从而引起褐飞虱GST活性上升。GST活性升高是植食性昆虫对干旱(罗定, 2012)、CO2浓度升高(刘建业等, 2014)、寄主植物(刘玉坤等, 2011; Xuetal., 2014; 陈晨等, 2016; 丁杰, 2020)、抗虫品种(Yaoetal., 2002; 周亦红等, 2003; 凌炎, 2007)、杀虫剂(凌炎, 2007; 肖彩云等, 2020; 张凯伦等, 2020)的应激反应。因此,本研究中褐飞虱GST活性上升可能是对施硅水稻中次生化合物含量增大的反应。
前人研究表明,褐飞虱和白背飞虱取食感染南方水稻黑条矮缩病或经杀虫剂处理的水稻后,体内CarE活性显著降低(张珏锋等, 2018; 杨洪等, 2019; 肖彩云等, 2020);取食耐虫性或抗生性水稻品种的褐飞虱、白背飞虱和灰飞虱体内的CarE活性被显著抑制(吴刚等, 1993; 赵士熙等, 1993; 朱麟等, 2000; 刘玉坤等, 2011)。此外,褐飞虱、白背飞虱和灰飞虱在施硅或抗虫水稻上的生长发育延迟,存活率降低、寿命缩短(吴刚等, 1993; 赵士熙等, 1993; 刘玉坤等, 2011; Heetal., 2015; Yangetal., 2017b; Linetal., 2022)。本研究发现,褐飞虱成虫取食Si+水稻植株24-96 h时,CarE活性低于Si-处理组,并在72和96 h时差异达到显著水平(图2: B)。由此推测,CarE活性被抑制可能会干扰昆虫正常的生长发育,最终导致昆虫死亡,这可能是施硅增大水稻对褐飞虱抗生性的结果。
在本研究中,褐飞虱成虫取食水稻植株72和96 h时,Si+处理组MFO活性显著高于Si-处理组(图2: C)。已有研究证实,水稻品种、杀虫剂、CO2浓度、寄主植物能诱导昆虫体内MFO活性上升。如褐飞虱、白背飞虱和灰飞虱取食耐虫性或抗生性水稻品种时体内MFO活性升高(刘玉坤等, 2011);杀虫剂或高CO2浓度处理能使褐飞虱、灰飞虱、西花蓟马Frankliniellaoccidentalis和花蓟马F.intonsa体内MFO活性显著升高(凌炎, 2007; 刘建业等, 2014; 张凯伦等, 2020);草地贪夜蛾Spodopterafrugiperda幼虫取食次生代谢物含量高的寄主植物后,体内MFO活性上升(鲁智慧等, 2020)。因此,褐飞虱可能通过增大体内MFO活性的方式以维持其正常的生理代谢。
根据本研究结果,水稻施硅引起褐飞虱成虫体内保护酶活性先上升后下降,解毒酶GST和MFO活性升高、CarE活性降低。这些变化是因为水稻施硅改变了叶鞘组织结构特征的直接结果,还是施硅影响植物生理代谢过程、诱导植物增加次生代谢物合成和积累的间接结果,抑或是施硅的直接和间接影响的综合结果,还有待深入研究。本研究结果为探究褐飞虱体内酶活性的变化与施硅增强水稻抗虫性之间的关系提供了理论依据,也为合理利用硅肥调控褐飞虱种群奠定了理论基础。
