逍遥散加减方治疗慢性乙型肝炎临床疗效及安全性Meta分析
2022-12-28余璐妮王梓怡字晨霞梅志刚
余璐妮,王梓怡,字晨霞,梅志刚, 2*
逍遥散加减方治疗慢性乙型肝炎临床疗效及安全性Meta分析
余璐妮1,王梓怡1,字晨霞1,梅志刚1, 2*
1. 湖南中医药大学,湖南 长沙 410208 2. 三峡大学医学院 国家中医药管理局中药药理科研三级实验室,湖北 宜昌 443002
评价逍遥散加减治疗慢性乙型肝炎(chronic hepatitis B,CHB)的临床疗效和安全性。电子检索中国知网(CNKI)、维普数据库(VIP)、万方数据库(Wanfang)、中国生物医学文献数据库(CBM)、中华医学期刊网、Web of Science、PubMed等数据库中逍遥散加减方治疗CHB的中英文文献,时间从建库至2022年5月26日。由2名研究者独立筛选文献、提取数据和评价纳入研究偏倚风险后,对资料进行系统性评价和Meta分析。共纳入30项研究,研究对象2705例。逍遥散加减方治疗CHB在改善总有效率[RR=0.78,95%CI(0.76,0.83),<0.000 01]、乙肝病毒(hepatitis B virus,HBV)-DNA转阴率[RR=0.85,95%CI(0.80,0.91),<0.000 01]、乙型肝炎e抗原(hepatitis Be antigen,HBeAg)转阴率[RR=0.65,95%CI(0.56,0.76),<0.000 01]、总胆红素(total bilirubin,TBIL)[SMD=−0.97,95%CI(−1.34,−0.60),<0.000 01]、天冬氨酸氨基转移酶(aspartate transaminase,AST)[SMD=−0.73,95%CI(−1.08,−0.50),<0.000 01]和丙氨酸氨基转移酶(alanine aminotransferase,ALT)[SMD=−1.03,95%CI(−1.42,−0.64),<0.000 01] 等方面效果显著优于对照组。目前临床证据表明,逍遥散加减方单用或联合临床常规药物,治疗CHB安全有效,但该研究结论仍需更多高质量的临床试验予以验证。
逍遥散;慢性乙型肝炎;Meta分析;乙肝病毒;总胆红素;天冬氨酸氨基转移酶;丙氨酸氨基转移酶
慢性乙型肝炎(chronic hepatitis B,CHB)是由乙型肝炎病毒(hepatitis B virus,HBV)持续感染而致的肝脏慢性疾病,发展严重可导致肝硬化、肝癌等,严重威胁患者的生命安全[1-2]。我国是一个乙肝大国,CHB病程长、传染性强、治愈率低,因此CHB长期以来都是我国面临的重大公共卫生问题[3]。目前CHB治疗的总体目标是最大限度地抑制或消除HBV[3]。尽管核苷酸类似物或干扰素可以有效抑制HBV复制,但这些都不是治愈性治疗[4]。这些药物普遍存在着临床治愈率低、停药复发率高、患者需终身服药等问题,导致极高的卫生经济支出及民生负担[5],故寻找有效治疗CHB的临床替代疗法非常重要。
中医认为CHB常由湿热疫毒之邪内侵,当人体正气不足无力抗邪时发病,或因外感、情志、饮食、劳倦而诱发。本病的病位主要在肝,常多涉及脾、肾2脏及胆、胃、三焦等腑[6]。逍遥散为《太平惠民和剂局方》中的经典方,具有调达肝气、柔肝缓急、疏肝解郁、养血健脾之效,可解两胁作痛、头痛目眩、神疲食少之证[7],临床多见于治疗肝郁脾虚型的CHB,然而其疗效和安全性目前尚缺乏循证证据。本研究拟对逍遥散加减方治疗CHB的临床随机对照试验进行Meta分析,旨在系统评价逍遥散加减方治疗CHB的疗效和安全性,以期为临床合理采用中医药防治本病提供依据。
1 方法
1.1 纳入标准
(1)研究对象:符合CHB相关诊断标准。即通过血清学标志物进行HBV感染的诊断。乙型肝炎e抗原(hepatitis Be Antigen,HBeAg)的存在可诊断为感染,如果存在时间超过6个月,则提示慢性感染[8]。
(2)干预措施:试验组干预措施为逍遥散加减方或逍遥散加减方联合临床常规用药,对照组干预措施为临床常规用药,如有基础干预措施要求试验组与对照组基础干预措施相同。
(3)结局指标:治疗总有效率及肝功能指标丙氨酸氨基转移酶(alanine aminotransferase,ALT)、总胆红素(total bilirubin,TBIL)、天冬氨酸氨基转移酶(aspartate transaminase,AST)、HBeAg转阴率、乙肝病毒(hepatitis B virus,HBV)-DNA转阴率。其中,治疗总有效率的评定标准为显效:患者疾病症状消失,疼痛降低,肝功能检查正常;有效:患者疾病症状降低,肝功能检查改善;无效:上述效果未达到。
总有效率=(显效例数+有效例数)/总例数
(4)研究类型:随机对照试验(randomized controlled trial,RCT),且接受治疗4周以上。
1.2 排除标准
①重复发表的文献;②无法获取完整资料的文献;③合并其他疾病或已发展为肝硬化、肝癌、肝衰竭等重症肝病者。
1.3 检索策略
检索中国知网(CNKI)、维普数据库(VIP)、万方数据库(Wanfang)、中国生物医学文献数据库(CBM)、中华医学期刊网、Web of Science、PubMed等数据库中逍遥散加减方治疗CHB的中英文文献,时间为建库至2022年5月26日。中文检索词包括逍遥散、加味逍遥散、逍遥散加减、逍遥丸、逍遥丸加味、慢性乙型肝炎、慢乙肝、乙肝等,英文检索词包括Xiaoyao Powder、Xiaoyao San、Rambling Powder、Xiaoyao pill、CHB、chronic viral hepatitis B和HBV等。中英文文献检索策略见表1。

表1 中英文文献检索策略
1.4 文献筛选
由2名研究者独立筛选文献,意见不同时通过讨论达成一致。首先通过阅读标题与摘要排除明显不符合纳入标准的文献,其次对初筛后的文献进行全文阅读以确定是否纳入研究,并剔除信息不完整或无法全文阅读的文献。
1.5 数据提取
根据预先制定的数据提取表,由2名研究者独立提取数据,最后进行核对,存在分歧时讨论决定。数据提取的内容包括:①研究基本信息(研究题目、第1作者、研究时间);②研究设计及风险偏倚评估所需信息;③研究对象特征(性别、疾病情况、年龄等);④分组情况:试验组和对照组的样本量、干预措施、疗程等;⑤结局指标。
1.6 偏倚风险评估
由2名研究者独立评价,最后交叉核对。采用Cochrane手册5.1.0风险偏倚评估工具,评价内容包括:①随机分配方法;②分配方案隐藏;③对研究对象、治疗方案实施者是否采用盲法;④研究结局评价盲法;⑤结局数据的不完整性;⑥选择性报告;⑦其他可能的偏倚风险,对这7个方面做出“低风险(low risk)”“高风险(high risk)”“不清楚(unclear risk)”的判断。
1.7 资料分析
采用RevMan 5.4.1进行数据分析,二分类变量采用相对危险度(relative risk,RR)表示,连续性变量采用标准化均数差(SMD)表示。对研究结果进行异质性检验,若存在明显异质性(≤0.10或2≥50%),则采用随机效应模型进行合并分析,反之则采用固定效应模型进行Meta分析,<0.05为差异有统计学意义。若不宜进行Meta分析则只进行定性分析。通过绘制漏斗图进行发表偏倚分析。
2 结果
2.1 文献筛选结果及纳入研究的基本特征
检索共得到586篇相关文献,中文文献584篇,英文文献2篇。经过筛选最终纳入30篇[9-38]文献,全部为中文文献,共包含2705例研究对象。文献的筛选流程见图1。纳入研究的基本特征见表2。
2.2 纳入研究的偏倚风险评估结果
30项研究中所有文献均提及了随机分组,其中16项研究[10,12,16-19,22-23,25-29,35-37]采用随机数字表法(可判断为低风险),1项研究[30]采用信封分组法(可判断为低风险),5项研究[13-14,20-21,38]采用就诊顺序进行分组,属于伪随机范畴(判断为高风险),其余8项未描述随机方法(判断为不清楚);有1项研究[30]提及分配隐藏(可判断为低风险),其余29研究均未提及分配隐藏(判断为不清楚);所有研究均未提及对受试者和研究者及结局评价者施盲(判断为不清楚);有2项研究[26,28]在治疗过程中出现病例脱落情况(可判断为高风险),其余28项研究均有明确结局指标且数据完整(可判断为低风险);所有研究均未发现有重复发表和已发表偏倚(可判断为低风险);其他偏倚未知(可判断为不清楚)。纳入研究的偏倚风险评估结果见图2。
2.3 Meta分析结果
2.3.1 总有效率 25篇[9-15,17-19,21-26,28-32,34,36-38]文献有提及,共纳入2300例,试验组1172例,对照组1128例。合并分析各研究间无异质性(=0.97,2=0),采用固定效应模型分析。结果显示差异有统计学意义[RR=0.78,95%CI(0.76,0.83),<0.000 01],表明逍遥散加减治疗CHB总有效率更高。按照干预措施不同分为逍遥散方剂单用组和逍遥散方剂联合临床常用药组,进行亚组分析,各亚组分析结果与总体一致,逍遥散方剂单用或联合临床常用药均能显著提高临床总有效率,见图3。
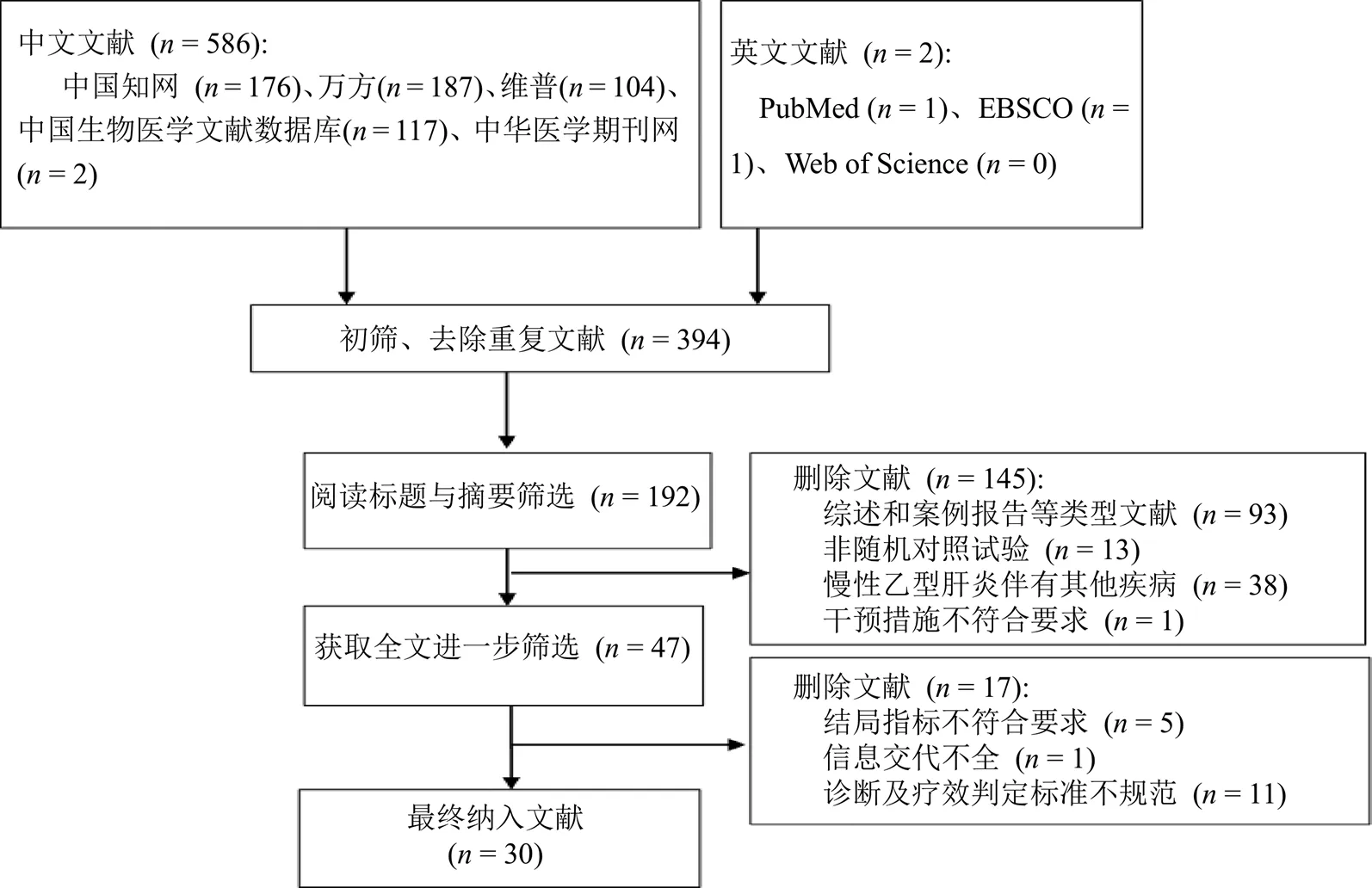
图1 文献筛选流程

表2 纳入文献基本特征
T-试验组 C-对照组 ①总有效率 ②HBV-DNA转阴率 ③HBeAg转阴率 ④TBIL ⑤AST ⑥ALT ⑦生活质量 ⑧不良反应
T-test group C-control group ①total effective rate ②HBV-DNA negative conversion rate ③HBeAg negative conversion rate ④TBIL ⑤AST ⑥ALT ⑦quality of life ⑧adverse reactions
对两组的总有效率进行潜在性发表偏倚分析,结果显示,漏斗图不完全对称,提示可能存在发表偏倚,见图4。
2.3.2 HBV-DNA转阴率 17篇[9-11,13,15-16,18,20,22,25-28,31,33,35,38]文献提及HBV-DNA转阴率,纳入1511例,试验组817例、对照组694例。合并分析各研究间异质性小(=0.01,2=49%),采用固定效应模型分析,结果显示差异有统计学意义[RR=0.85,95%CI(0.80,0.91),<0.000 01],表明逍遥散加减治疗CHB对提高患者HBV-DNA转阴率更优。按照干预措施不同分为逍遥散方剂单用组和逍遥散方剂联合临床常用药组,进行亚组分析,各亚组分析结果与总体一致,逍遥散方剂单用或联合临床常用药均能提高HBV-DNA转阴率,见图5。

图2 纳入研究的偏倚风险评估

图3 总有效率的Meta分析森林图
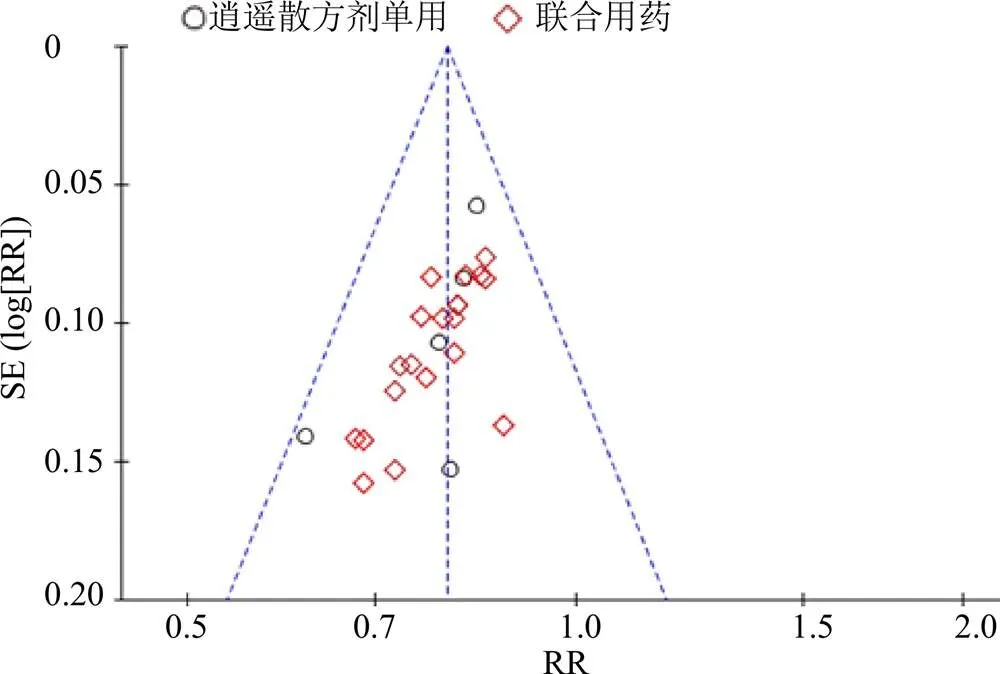
图4 总有效率偏倚分析漏斗图
对两组的HBV-DNA转阴率进行潜在性发表偏倚分析,结果显示,漏斗图不完全对称,提示可能存在发表偏倚,见图6。
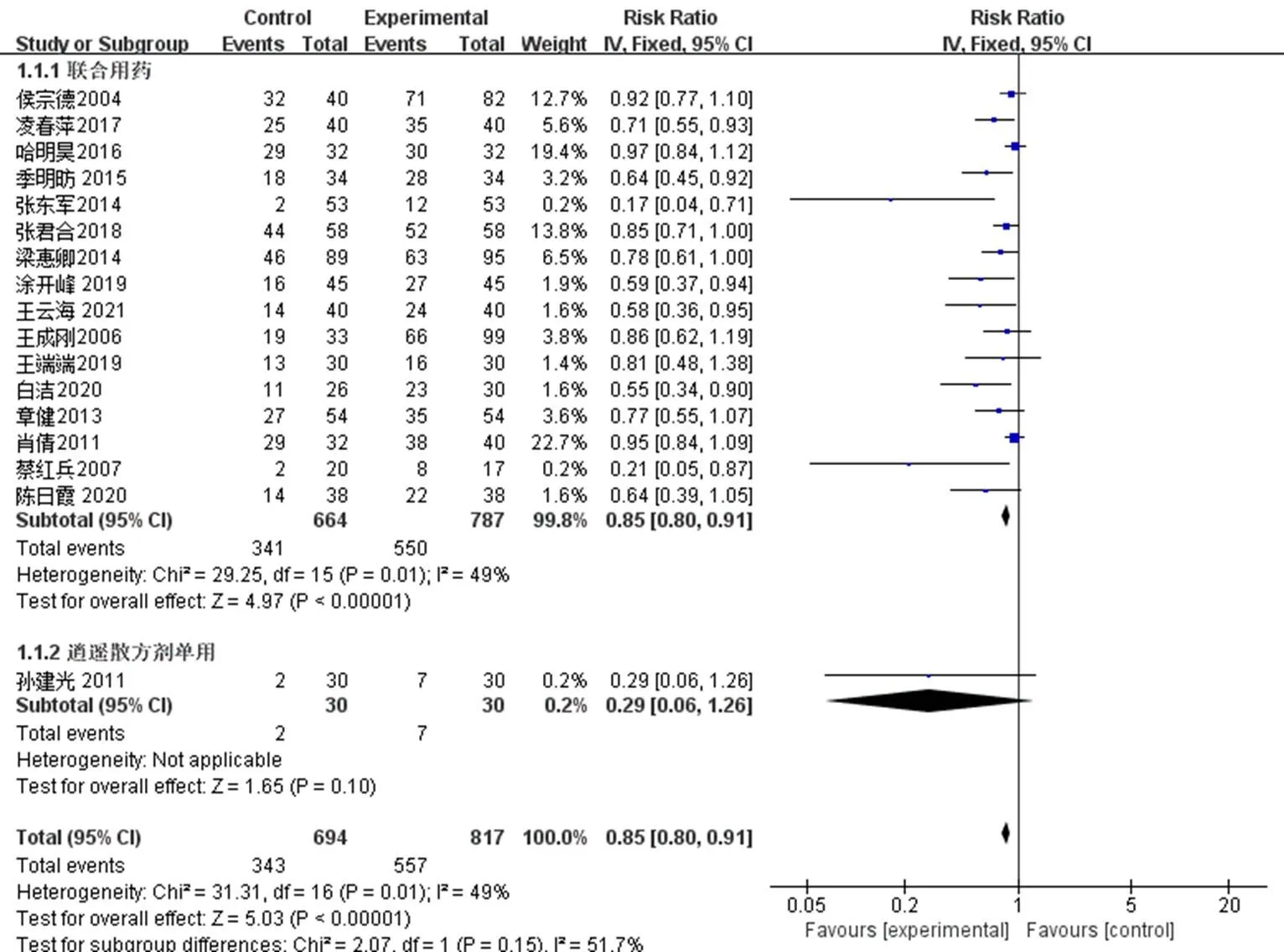
图5 HBV-DNA转阴率的Meta森林图

图6 HBV-DNA转阴率偏倚分析漏斗图
2.3.3 HBeAg转阴率 14篇[11,13,15,18,22,25-28,31,33-35,38]文献提及HBeAg转阴率,纳入1273例,试验组662例、对照组611例。各研究间异质性小(=0.28,2=16%),采用固定效应模型分析,结果显示差异有统计学意义[RR=0.65,95%CI(0.56,0.76),<0.000 01],表明逍遥散加减治疗CHB对提高患者HBeAg转阴率更优。按照干预措施不同分为逍遥散方剂单用组和逍遥散方剂联合临床常用药组,进行亚组分析,其中,联合用药亚组分析结果与总体一致,而逍遥散方剂单用亚组的结果显示试验组的HBeAg转阴率更高。然而由于逍遥散方剂单用亚组仅纳入1项研究且该研究的样本量较小,因此还需要更多的高质量研究来证明逍遥散方剂单用对HBeAg转阴率的影响。见图7。
并对两组的HBeAg转阴率进行潜在性发表偏倚分析,结果显示,漏斗图不完全对称,提示可能存在发表偏倚,见图8。
2.3.4 TBIL 16篇[9-10,13-15,17,20-22,24,27-28,32,36-38]文献提及TBIL,纳入1452例,试验组760例、对照组692例。由于各研究间异质性过大(<0.000 01,2=90%),采用随机效应模型分析。结果显示差异有统计学意义[SMD=−0.97,95%CI(−1.34,−0.60),<0.000 01],表明逍遥散加减治疗CHB能显著降低TBIL。按照干预措施不同分为逍遥散方剂单用组和逍遥散方剂联合临床常用药组,进行亚组分析,各亚组分析结果与总体一致,逍遥散方剂单用或联合临床常用药均能显著降低TBIL,见图9。

图7 HBeAg转阴率的Meta分析森林图
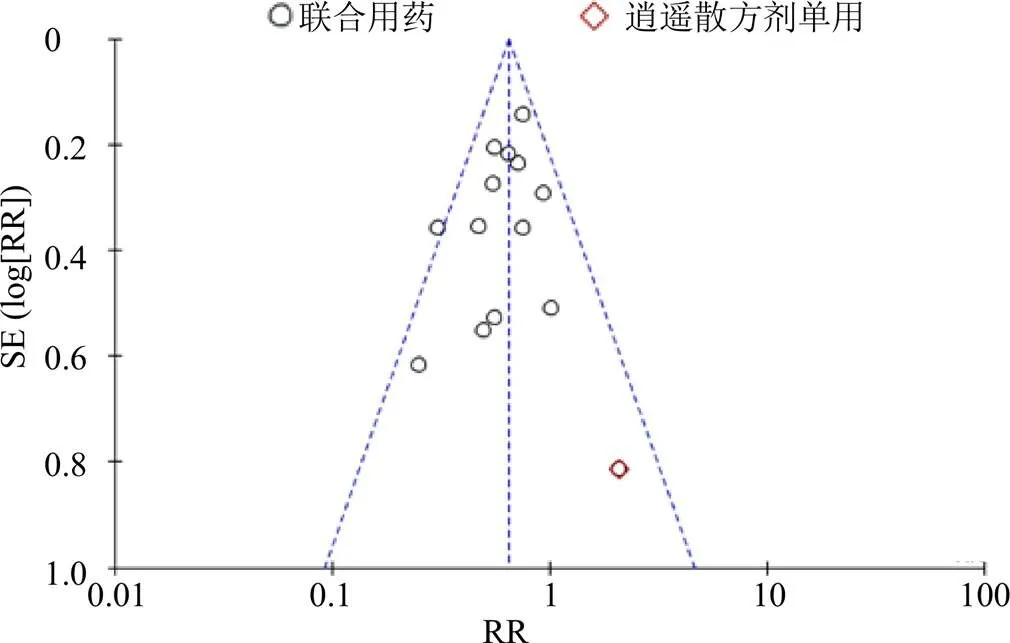
图8 HBeAg转阴率偏倚分析漏斗图
由于2个亚组异质性仍较大,在亚组基础上采用逐一剔除单个研究的方式进行敏感性分析来寻找异质性来源。分别针对2个亚组的敏感性分析显示,在剔除任一研究后异质性无明显下降,考虑还存在其他异质性来源,患者病程、指标测量时间等因素可能造成了研究见潜在的异质性。
对两组的TBIL进行潜在性发表偏倚分析,结果显示,漏斗图不完全对称,提示可能存在发表偏倚,见图10。
2.3.5 AST 17篇[13-15,17-18,20-22,24-25,27-29,32,36-38]文献提及AST,纳入1558例,试验组834例、对照组724例。由于各研究间异质性过大(<0.000 01,2=83%),采用随机效应模型分析。结果显示差异有统计学意义[SMD=−0.73,95%CI(−1.08,−0.50),<0.000 01],表明逍遥散加减治疗CHB能显著降低AST。按照干预措施不同分为逍遥散方剂单用组和逍遥散方剂联合临床常用药组,进行亚组分析,各亚组分析结果与总体一致,逍遥散方剂单用或联合临床常用药均能显著降低AST,见图11。
由于逍遥散方剂联合临床常用药亚组异质性仍较大,在亚组基础上采用逐一剔除单个研究的方式进行敏感性分析来寻找异质性来源。针对联合用药亚组的敏感性分析显示,在剔除任一研究后异质性无明显下降,考虑还存在其他异质性来源,患者病程、所用临床常用药、指标测量时间等因素可能造成了研究潜在的异质性。

图9 TBIL的Meta分析森林图

图10 TBIL偏倚分析漏斗图
对两组的AST进行潜在性发表偏倚分析,结果显示漏斗图不完全对称,提示可能存在发表偏倚,见图12。
2.3.6 ALT 22篇[9-11,13-22,25,27-30,32,36-38]文献提及ALT,纳入2062例,试验组1089例、对照组973例。由于各研究间异质性过大(<0.000 01,2=94%),采用随机效应模型。结果显示差异有统计学意义[SMD=−1.03,95%CI(−1.42,−0.64),<0.000 01],表明逍遥散加减治疗CHB能显著降低ALT。按照干预措施不同分为逍遥散方剂单用组和逍遥散方即联合临床常用药组,进行亚组分析,各亚组分析结果与总体一致,逍遥散方剂单用或联合临床常用药均能显著降低ALT,见图13。
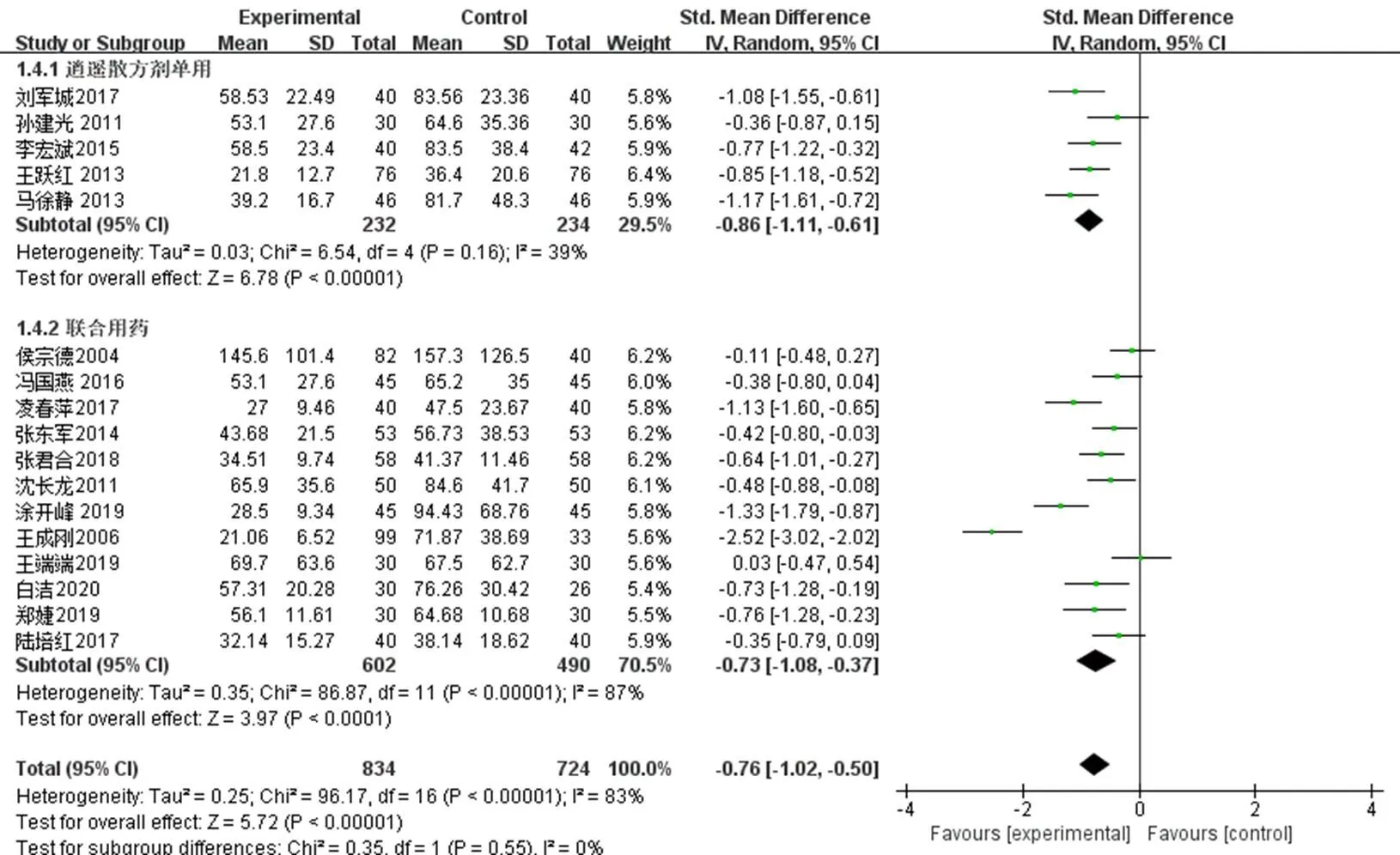
图11 AST的Meta分析森林图

图12 AST偏倚分析漏斗图
由于2个亚组异质性仍较大,在亚组基础上采用逐一剔除单个研究的方式进行敏感性分析来寻找异质性来源。敏感性分析显示,逍遥散方剂单用亚组在剔除王跃红[32]的研究后异质性下降(=0.57,2=0),但合并结果未发生明显改变,对比各项研究发现,王跃红研究与其他研究的主要差异在于对照组用药不同以及疗程较短,怀疑此为造成异质性的主要原因。而联合用药亚组的敏感性分析显示,在剔除任一研究后异质性无明显下降,考虑还存在其他异质性来源,患者病程、所用临床常用药、指标测量时间等因素可能造成了研究的潜在异质性。
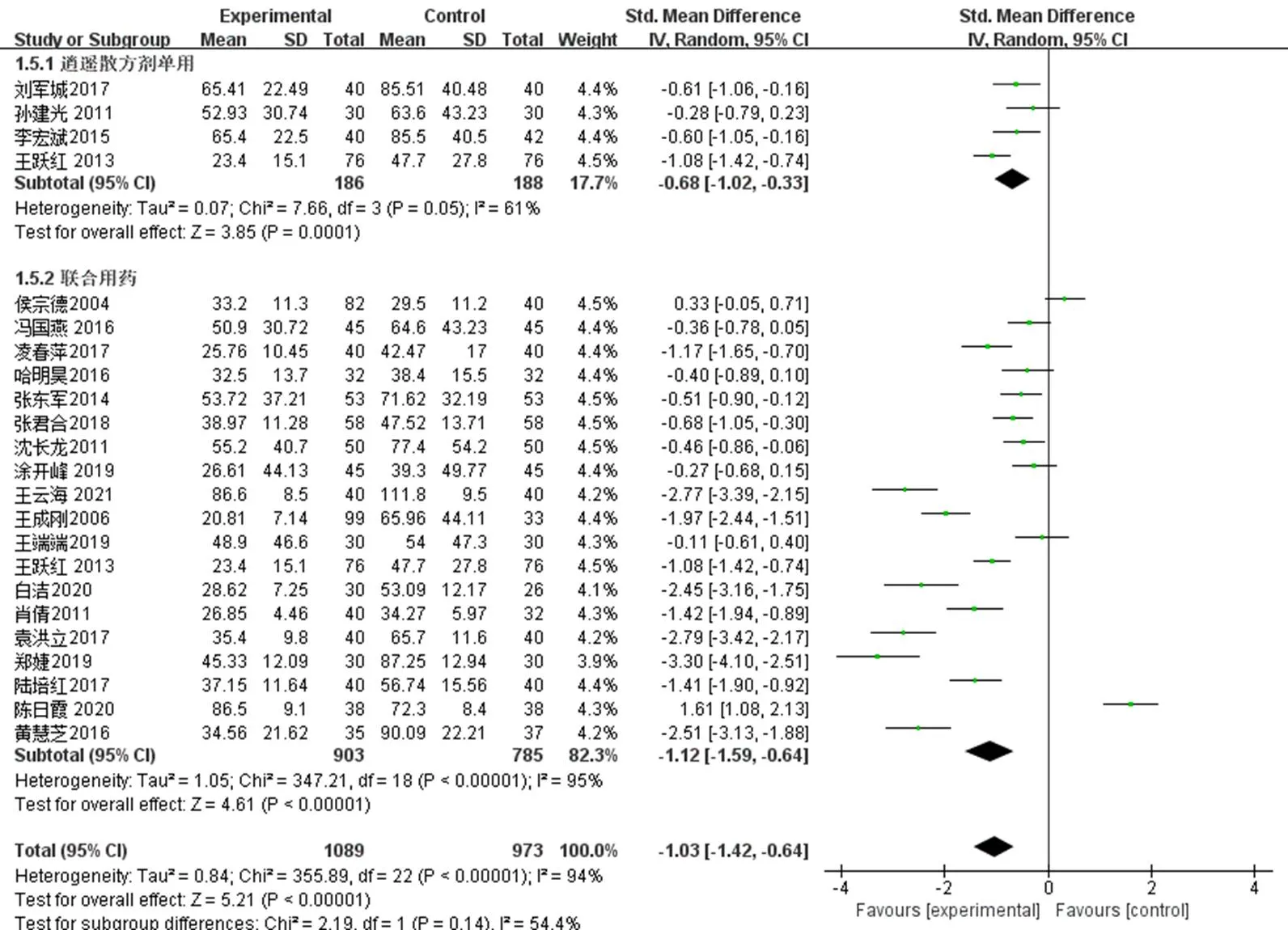
图13 ALT的Meta分析森林图
对两组的ALT进行潜在性发表偏倚分析,结果显示漏斗图较为对称,提示不存在发表偏倚或存在其他偏倚,见图14。
2.3.7 生活质量 4篇[10,12,23,26]文献提及生活质量。有1项研究[10]通过比较试验组和对照组治疗前后的中医证候积分、抑郁自评量表(self-rating depression scale,SDS)和舒适状况量表(general comfort questionnaire,GCQ)等评分的变化来研究两组生活质量的变化,得出试验组的改善程度更显著(<0.05),差异有统计学意义。有2项研究[12,23]通过比较试验组和对照组治疗前后躯体功能、心理功能、社会功能、物质生活4个维度的评分来研究两组生活质量的变化,2项研究均得出试验组4个维度的评分显著高于对照组(<0.05),差异有统计学意义。有1项研究[26]通过比较试验组和对照组治疗前后慢性肝病量表(chronic liver disease questionnaire,CLDQ)评分的变化来研究两组生活质量的变化,得出试验组生活质量改善情况优于对照组(<0.01),差异有统计学意义。
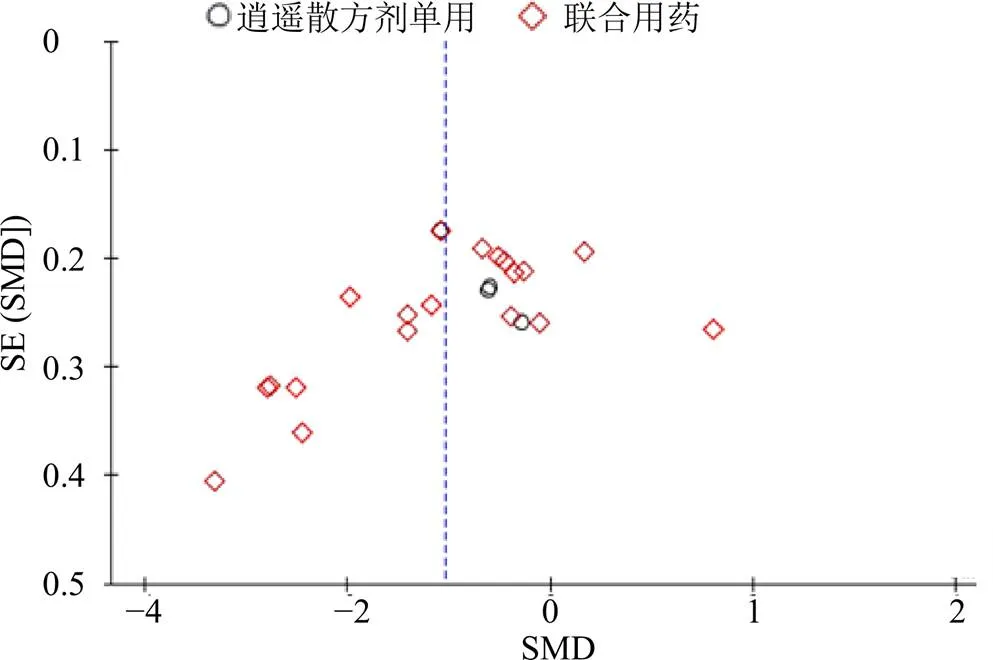
图14 ALT偏倚分析漏斗图
2.3.8 不良反应 12篇[10,12,15,19,21-22,25-26,28-29,36-37]文献涉及不良反应,且这些研究的试验组均为逍遥散加减联合常规化学药治疗。其中有7项研究[12,19,21-22,25,36-37]在研究过程中未出现明显的不良反应;1项研究[10]未报告不良反应例数,仅提及两组均出现数例消化道、皮疹、头晕乏力等轻度药物不良反应,且组间比较无显著差异(>0.05);1项研究[15]报告仅有对照组出现3例耐药反应;1项研究[29]报告试验组出现1例头痛,对照组出现1例嗜睡和1例恶心,两组间差异无显著性(=0.411)。2项研究[26,28]报告数例不良反应,其中1项研究[26]报告试验组出现1例乏力、1例腹胀、2例厌食、4例焦虑和2例失眠,对照组出现18例乏力、7例腹胀、8例厌食、14例焦虑和10失眠,另一项研究[28]报告试验组出现6例发烧、7例乏力、3例焦虑、3例抑郁和5例失眠,对照组出现12例发烧、14例乏力、9例焦虑、8例抑郁和11例失眠,两项研究均显示试验组不良反应发生率显著低于对照组(<0.05)。
3 讨论
根据纳入和排除标准筛选随机对照试验,纳入了30项研究。该Meta分析的结果表明,逍遥散加减方能显著提高治疗总有效率,表明逍遥散加减方治疗CHB患者临床总体疗效更优。HBV-DNA转阴率、HBeAg转阴率、ALT、AST和TBIL是CHB严重程度的临床试验指标[39]。这些结局指标的结果表明,逍遥散加减方的治疗可以显著缓解肝损伤,改善临床症状。本研究筛选出4项研究有生活质量的报道,研究表明逍遥散加减方更能显著提高患者生活质量。本研究筛选出10项研究有不良反应的报道,主要是对药物的轻度不良反应及耐药反应,不良反应发生率分析显示逍遥散加减方对不良反应的发生率无增加风险,提示其在临床使用的安全性。
本研究的对照组用药主要为核苷酸类似物。长期给予具有高耐药屏障的强效核苷酸类似物如恩替卡韦等,是CHB首选的治疗方法[40]。但这些药物在治疗CHB时,会存在一些不良反应,如在长期阿德福韦治疗中,范可尼综合征病例的报道越来越多;拉米夫定和替比夫定的使用与大多数线粒体毒性病例有关,通常表现为肌病、神经病变或乳酸性酸中毒[41]。
CHB中医证型以肝郁脾虚证为主[42]。逍遥散为治疗肝郁脾虚型CHB的代表方,由柴胡、白术、当归、茯苓、白芍、炙甘草、薄荷及煨生姜组成,方中柴胡疏肝解郁,使肝气得以条达;当归甘辛苦温,养血和血;白芍酸苦微寒,养血敛阴、柔肝缓急;白术、茯苓、甘草健脾益气;薄荷疏散郁遏之气,透达肝经郁热;煨生姜温运和中,且能辛散达郁[43]。现代药理研究证明,逍遥散具有保肝降酶、抗炎等作用[44]。刘杨等[45]研究表明,逍遥散组能明显降低大鼠肝郁脾虚证证侯积分,显著升高-木糖排泄率和脑组织内5-羟色胺(5-hydroxy tryptamine,5-HT)、去甲肾上腺素(norepinephrine,NE)的含量,明显减轻肝细胞脂肪变性程度及炎细胞浸润程度,明显降低Toll样受体-4(Toll-like receptor 4 polypeptide,)和β干扰素TIR结构域衔接蛋白(β-interferon TIR domain adaptor protein,)mRNA和蛋白表达,因此逍遥散可通过参与调节TLR-4/TRIF炎症信号通路的活性,以发挥疏肝健脾的功效,参与肝郁脾虚证的治疗。王晓强等[46]研究提示,逍遥散具有清除自由基作用,能减少体内自由基浓度,降低自由基的氧化作用,使体内超氧化物歧化酶(superoxide dismutase,SOD)消耗减少,失活速度减慢,有利于升高SOD活性,促进机体抗氧化防御体系的提高或恢复功能,加速红细胞的代谢,避免自由基及其产物在细胞内积聚从而达到保肝作用。陈丹丹等[47]通过实验推测逍遥散可能是通过改善细胞膜通透性,促进肝细胞再生、合成蛋白及加快肝细胞修复来治疗肝郁脾虚型肝病。苗祥东[48]通过研究发现当归对化学致毒物所致的动物肝损伤有明显的保护作用,可降低血清中的谷丙转氨酶(serum glutamate pyruvate transaminase,SGPT)值,恢复肝细胞正常功能,促进肝细胞再生及肝细胞RNA合成,刺激人体产生干扰素,并且能有效抑制HBV-DNA。王卫京等[49]利用分子对接技术分析柴胡中抗HBV的有效成分,结果显示,柴胡中含有多种抑制HBV的组分,能够较好地与HBV核蛋白结合,且由于是多种组分对HBV核蛋白具有抑制作用,故HBV很难对柴胡产生耐药性。戴俐明等[50]研究表明,白芍中的白芍总苷可明显对抗CCl4所致的SGPT升高,血清总蛋白和肝糖原含量的降低,并在镜下可见肝小叶内点片状坏死灶明显减少,肝细胞的浊肿及嗜酸变明显减轻,汇管区炎症细胞浸润减少,表明白芍总苷可使肝变性、坏死显著减轻。段会平等[51]研究表明,茯苓中的羧甲基茯苓多糖在HBV-DNA克隆转染HepG2/2.2.15细胞株培养中对HBeAg分泌有较好的抑制作用。
然而,本研究尚存在一些局限性:①纳入文献全部为中文文献,检索到的英文文献较少且数据缺失或不符合纳入标准。纳入研究大部分未提及盲法、分配隐瞒,不能排除研究对象的选择性偏倚。②单独使用逍遥散来治疗CHB的研究较少。在许多研究中,中医药仍然作为化学药的辅助手段进行治疗[52]。对于单独使用逍遥散治疗CHB的疗效尚不能明确。③纳入的研究疗程由4周到5个月不等,且有部分研究未对患者进行中医辨证,逍遥散治疗肝郁脾虚型CHB,对于其他证型的CHB可能无法达到预期的疗效,这些潜在的异质性影响了证据的质量。④漏斗图对称性不加,可能存在发表偏倚,影响了加味逍遥散的疗效评判。
综上所述,逍遥散治疗CHB虽然有着悠久的历史,但其抗病毒作用的疗效及其潜在作用机制尚待深入研究。目前临床研究多为单中心、小样本研究,缺乏多中心、大样本、双盲随机对照研究,导致其循证医学证据级别不高,不利于西医同行对逍遥散防治CHB疗效的认可[44]。此外,逍遥散作为潜在治疗CHB的中药复方,其主要的药效物质基础以及抗炎、抗纤维化作用机制有待系统挖掘。
利益冲突 所有作者均声明不存在利益冲突
[1] 刘影, 徐汉辰, 王磊. 中医药对慢性乙型肝炎免疫调节作用概述 [J]. 上海中医药杂志, 2022, 56(5): 93-97.
[2] 连志丽. 替诺福韦联合苄星青霉素阻断乙肝合并梅毒感染患者母婴传播的效果分析 [J]. 医学理论与实践, 2022, 35(11): 1900-1902.
[3] 史媛媛. 长效干扰素与常规干扰素治疗慢性乙肝60例临床对比观察 [J]. 基层医学论坛, 2015, 19(5): 640-642.
[4] Lok A S, Zoulim F, Dusheiko G,. Hepatitis B cure: From discovery to regulatory approval [J]., 2017, 66(4): 1296-1313.
[5] 叶永安. 中西医结合治疗慢性乙型肝炎的机遇与挑战 [J]. 中西医结合肝病杂志, 2019, 29(3): 197-200.
[6] 中华中医药学会肝胆病专业委员会, 中国民族医药学会肝病专业委员会. 慢性乙型肝炎中医诊疗指南(2018年版) [J]. 中西医结合肝病杂志, 2019, 29(1): 97-102.
[7] 田水林, 施琳, 施卫兵. 逍遥散联合恩替卡韦治疗肝郁脾虚型慢性乙型肝炎疗效研究 [J]. 陕西中医, 2020, 41(6): 754-757.
[8] Manne V, Gochanour E, Kowdley K V. Current perspectives into the evaluation and management of hepatitis B: A review [J]., 2019, 8(4): 361-369.
[9] 王云海. 丹栀逍遥散加减治疗慢性乙型肝炎的效果评价 [J]. 中国医药指南, 2021, 19(7): 116-117.
[10] 陈日霞. 丹栀逍遥散加减治疗慢性乙型肝炎肝郁气滞证临床研究 [J]. 现代中医药, 2020, 40(5): 59-61.
[11] 哈明昊, 黄钟鸣, 唐东旭, 等. 恩替卡韦联合逍遥散治疗肝郁脾虚型慢性乙型肝炎疗效观察 [J]. 中西医结合肝病杂志, 2016, 26(4): 222-223.
[12] 徐红帅. 甘草酸二铵联合逍遥散加味治疗慢性乙型肝炎疗效观察 [J]. 现代中西医结合杂志, 2016, 25(6): 624-626.
[13] 孙建光. 加减逍遥散治疗肝郁脾虚证慢性乙型肝炎疗效观察 [J]. 中国药物警戒, 2011, 8(5): 269-271.
[14] 刘军城, 庄慧雁. 加减逍遥散治疗肝郁气滞型乙型肝炎的临床观察 [J]. 云南中医中药杂志, 2017, 38(12): 43-44.
[15] 涂开峰. 加味逍遥散对慢性乙肝患者辅助疗效的研究 [J]. 黄冈职业技术学院学报, 2019, 21(3): 86-87.
[16] 肖倩. 加味逍遥散合阿德福韦酯治疗e抗原阴性肝郁脾虚型慢性乙型肝炎的疗效及对外周血T淋巴细胞水平的影响 [J]. 辽宁中医杂志, 2011, 38(12): 2332-2333.
[17] 陆培红, 杨伟莲. 加味逍遥散联合多烯磷脂酰胆碱胶囊治疗慢性乙型病毒性肝炎临床疗效观察 [J]. 新中医, 2017, 49(5): 41-43.
[18] 侯宗德, 杜玉英. 加味逍遥散联合拉米夫定治疗82例慢性乙型肝炎的临床观察 [J]. 实用肝脏病杂志, 2004, 7(4): 234-235.
[19] 黄慧芝, 彭莉莉. 加味逍遥散联合重组人干扰素α-2b治疗肝郁脾虚型慢性乙肝35例 [J]. 江西中医药, 2016, 47(4): 45-46.
[20] 王成刚, 石中顺, 程为玉. 加味逍遥丸联合拉米夫定治疗HBeAg阴性慢性乙型肝炎99例 [J]. 中国中西医结合杂志, 2006, 26(4): 369-370.
[21] 冯国燕, 张永峰, 冯立清. 加味逍遥散治疗慢性乙型肝炎疗效观察 [J]. 甘肃医药, 2016, 35(3): 175-178.
[22] 张君合, 刘俊玲, 刘家义, 等. 加味逍遥丸联合替诺福韦酯治疗肝郁脾虚型慢性乙肝的临床研究 [J]. 现代药物与临床, 2018, 33(10): 2629-2633.
[23] 许树深, 陈志强, 黄志昂. 逍遥散加味辅助甘草酸二铵治疗慢性乙型肝炎的效果评价 [J]. 内蒙古中医药, 2017, 36(S1): 102-103.
[24] 马徐静. 逍遥散加味治疗慢性乙型肝炎46例 [J]. 中国医药科学, 2013, 3(9): 99-100.
[25] 凌春萍, 毛德文, 陈月桥, 等. 逍遥散加味治疗慢性乙型肝炎肝郁脾虚兼血瘀证的临床研究 [J]. 辽宁中医杂志, 2017, 44(6): 1216-1219.
[26] 梁惠卿, 唐金模, 吴春城, 等. 逍遥散联合α干扰素治疗HBeAg阳性慢性乙型肝炎的临床观察 [J]. 中国中西医结合杂志, 2014, 34(6): 666-670.
[27] 白洁. 逍遥散联合恩替卡韦对慢性乙型病毒性肝炎患者乙肝病毒的脱氧核糖核酸阴转率、乙型肝炎e抗原阴转率的影响 [J]. 中国药物经济学, 2020, 15(8): 113-115.
[28] 王端端, 陈月桥, 毛德文, 等. 逍遥散联合重组人干扰素α-2b治疗慢性乙型肝炎的研究 [J]. 中西医结合肝病杂志, 2018, 28(4): 197-199.
[29] 郑婕. 逍遥散配合复方甘草酸苷治疗慢性乙型肝炎发生的作用探讨 [J]. 中国医药指南, 2019, 17(3): 170-171.
[30] 袁洪立, 袁平波, 陈倩儿, 等. 逍遥散汤剂辅助恩替卡韦治疗肝郁脾虚型慢性乙型肝炎效果评价 [J]. 华夏医学, 2017, 30(3): 50-52.
[31] 季明昉. 逍遥散治疗慢性乙型肝炎68例 [J]. 河南中医, 2015, 35(11): 2669-2670.
[32] 王跃红. 逍遥散治疗慢性乙型肝炎的临床疗效与安全性 [J]. 中国医药指南, 2013, 11(32): 189-190.
[33] 蔡红兵, 徐舒, 李洪, 等. 逍遥丸联合阿德福韦治疗肝郁脾虚型慢性乙型肝炎疗效观察 [J]. 湖南中医杂志, 2007, 23(5): 1-2.
[34] 李娟, 李芳霞, 马羽萍. 逍遥丸为主治疗慢性乙型肝炎60例临床分析 [J]. 海南医学, 2009, 20(S6): 236-237.
[35] 章健. 逍遥丸辅助阿德福韦酯对慢性乙型肝炎患者的临床疗效评价 [J]. 实用药物与临床, 2013, 16(3): 215-217.
[36] 李宏斌, 孟伟民. 逍遥散治疗肝郁气滞症候乙型肝炎的近远期疗效研究 [J]. 国际病毒学杂志, 2015(3): 161-164.
[37] 沈长龙, 戴征强, 谌业江, 等. 逍遥散配合复方甘草酸苷治疗慢性乙型肝炎的疗效观察 [J]. 国际中医中药杂志, 2011, 33(12): 1124-1125.
[38] 张东军, 林翼金, 李斌义, 等. 益肝逍遥散联合拉米夫定治疗慢性乙型肝炎肝郁脾虚证临床观察 [J]. 辽宁中医药大学学报, 2014, 16(11): 7-10.
[39] Terrault N A, Lok A S F, McMahon B J,. Update on prevention, diagnosis, and treatment of chronic hepatitis B: AASLD 2018 hepatitis B guidance [J]., 2018, 67(4): 1560-1599.
[40] European Association for the Study of the Liver Electronic address: easloffice@easloffice eu, European Association for the Study of the Liver. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection [J]., 2017, 67(2): 370-398.
[41] Kayaaslan B, Guner R. Adverse effects of oral antiviral therapy in chronic hepatitis B [J]., 2017, 9(5): 227-241.
[42] 毛果, 蔡光先, 陈斌. 基于中医证候疗效评价的慢性乙型肝炎肝郁脾虚证最佳方药的探究 [J]. 湖南中医杂志, 2014, 30(8): 12-15.
[43] 陈柏尧, 王建超, 徐艺倪, 等. 慢性乙型肝炎从肝郁脾虚论治研究进展 [J]. 辽宁中医杂志, 2021, 48(2): 203-206.
[44] 殷琼慧, 马卫闽. 逍遥散治疗慢性乙型肝炎的研究进展 [J]. 北方药学, 2015, 12(12): 93-94.
[45] 刘杨, 李明磊, 贾飞, 等. 逍遥散对非酒精性脂肪性肝炎肝郁脾虚证大鼠TLR-4/TRIF信号转导通路的影响 [J]. 中国实验方剂学杂志, 2018, 24(17): 108-113.
[46] 王晓强, 高权国. 逍遥散的药理研究进展 [J]. 中医药信息, 2007, 24(1): 40-42.
[47] 陈丹丹, 杨祎楠, 耿放, 等. 逍遥散对“肝郁脾虚证-肝病”的干预作用研究 [J]. 中成药, 2013, 35(9): 2010-2013.
[48] 苗祥东. 当归愈肝散治疗慢乙肝的临床观察 [J]. 辽宁中医杂志, 2003, 30(1): 32-33.
[49] 王卫京, 詹世平, 丁仕强. 用分子对接技术研究柴胡抗乙肝病毒的有效成分 [J]. 大连大学学报, 2019, 40(3): 51-55.
[50] 戴俐明, 陈学广, 徐叔云. 白芍总甙对实验性肝炎的保护作用 [J]. 中国药理学通报, 1993, 9(6): 449-453.
[51] 段会平, 侯安继, 陆付耳, 黄久乐. 羧甲基茯苓多糖对HBV转染细胞表达功能影响的实验研究 [J]. 中华实验和临床病毒学杂志, 2005, 19(3): 290-292.
[52] 覃婕, 黄万金, 王钿, 等. 中医药治疗慢性乙型肝炎及相关疾病的研究进展与思考 [J]. 河北中医, 2021, 43(12): 2090-2093.
Efficacy and safety of modified Xiaoyao Powder against chronic hepatitis B: A Meta-analysis
YU Lu-ni1, WANG Zi-yi1, ZI Chen-xia1, MEI Zhi-gang1, 2
1. Hunan University of Chinese Medicine, Changsha 410208, China 2. Third-Grade Pharmacological Laboratory on Chinese Medicine Approved by National Administration Traditional Chinese Medicine, College of Medicine, China Three Gorges University, Yichang 443002, China
To systematically evaluate the efficacy and safety of modified Xiaoyao Powder (逍遥散) in the treatment of chronic hepatitis B (CHB).Chinese and English literature on the treatment of CHB by Xiaoyao Powder in CNKI, VIP, Wanfang, CBM, Chinese Medical Journey, Web of Science, and PubMed were searched electronically. The retrieval time was from database establishment to May 26, 2022. Two researchers independently screened extracted data and evaluated the risk of bias, and then conducted a systematic review and Meta-analysis.A total of 30 studies involving 2705 patients were included. In the treatment of CHB, Xiaoyao Powder was significantly better than the control group in the improvement of the overall effective rate [RR = 0.78, 95%CI (0.76, 0.83),<0.000 01], hepatitis B virus (HBV)-DNA negative conversion rate [RR = 0.85, 95%CI (0.80, 0.91),<0.000 01], hepatitis Be antigen (HBeAg) negative conversion rate [RR = 0.65, 95%CI (0.56, 0.76),<0.000 01], total bilirubin (TBIL) [SMD = −0.97, 95%CI (−1.34, −0.60),<0.000 01], aspartate transaminase (AST) [SMD = −0.73, 95%CI (−1.08, −0.50),<0.000 01], alanine aminotransferase (ALT) [SMD = −1.03, 95%CI (−1.42, −0.64),<0.000 01].Current evidence shows that modified Xiaoyao Powder used alone or combined with conventional clinical drugs have a certain efficacy and safety in the treatment of CHB, and more high-quality clinical trials need to be carried out to verify the conclusion.
Xiaoyao Powder; chronic hepatitis B; Meta-analysis; hepatitis B virus; total bilirubin; AST; ALT
R285.64
A
0253 - 2670(2022)24 - 7831 - 12
10.7501/j.issn.0253-2670.2022.24.020
2022-08-10
湖南中医药大学中西医结合一流学科重点项目(2021ZXYJH01);湖北省医学青年拔尖人才项目(EWT2019-48)
余璐妮(2000—),女,2020级八年制中医学本硕连读学生。E-mail: yyyln123@163.com
梅志刚,男,教授,博士生导师,主要从事中药药理研究。E-mail: meizhigang@hnucm.edu.cn
[责任编辑 潘明佳]
