中硼硅管制瓶内表面离子迁移特性研究
2022-12-27田英良温玉琳王焕一赵志永孙诗兵
田英良,温玉琳,王 帆,王 华,王焕一,赵志永,孙诗兵
(1.北京工业大学材料与制造学部,北京 100124;2.江苏潮华玻璃制品有限公司,镇江 212321;3.沧州四星玻璃股份有限公司,沧州 061739)
0 引 言
药品包装是药品不可分割的部分,直接关系药品质量和人民安全健康[1-2]。药用玻璃是全球公认最佳的药品包装材料,其中中硼硅药用玻璃因具有良好的化学稳定性、耐热稳定性和气密透明性,被广泛应用于疫苗及生物制品、血液制品、冻干制剂用品等[3]。在药液长期储存过程中,玻璃瓶内表面阳离子会向药液迁移,这将影响药液的药效,且存在较大安全隐患[4]。
《化学药品注射剂与药用玻璃包装容器相容性研究技术指导原则(试行)》文件中提到,玻璃中的某些金属离子迁移入药品,会对药物稳定性、安全性产生影响,比如Na+的迁入会影响药液pH值,一些有害离子的迁入会影响药物安全性。为保证药物质量,应结合玻璃容器组分及添加物质,对涉及到的所有阳离子进行迁移试验及安全性评估,根据Si、B、Al等元素的迁移量及变化趋势预测玻璃容器受侵蚀产生脱片或玻璃屑的可能性[5]。
国内外对玻璃容器内表面离子迁移做过很多相关研究。但是国外大多采用模拟液或缓冲溶液来研究离子迁移规律,这并不能直接反映盛装药液的实际情况,而且研究的离子种类大多集中在Si4+、B+、Al3+,缺乏对玻璃中其他离子的迁移研究[6-10]。国内研究大多关注离子迁移方法的验证或Pb、Cd、As、Sb等重金属元素迁移量的测定,缺乏药瓶本身和药液本身对离子迁移影响的研究[11-13]。
本文用中硼硅药用玻璃管制瓶盛装真实药液,探究药液储存时间、药液pH值、药液浓度、玻璃瓶规格等因素对玻璃瓶内表面阳离子迁移的影响,观察玻璃瓶内表面受侵蚀情况。
1 实 验
1.1 原材料
试验所用药品为冻干粉状,中硼硅管制瓶为同一厂家、同一批次,多元素标准溶液、硅元素标准溶液均来自国家有色金属及电子材料分析测试中心,钠元素标准溶液来自中国计量科学研究院,标准值均为100 μg/mL,柠檬酸、柠檬酸三钠为化学分析纯试剂,均来自北京化工厂。
1.2 药液制备
试验所用药品为冻干粉状,溶剂为去离子水,分别制备质量浓度为0.002 5 g/mL、0.005 0 g/mL、0.010 0 g/mL、0.020 0 g/mL的药液,并将药液储存到聚四氟乙烯瓶内。
1.3 测量与表征
1.3.1 药液离子浓度测量
本试验采用电感耦合等离子体发射光谱仪(ICP-AES)对药液中的离子浓度进行测量。在使用该仪器测量样品之前,需使用标准溶液进行校准,Na、K、Ca、Si、B、Al元素谱线选择分别为589.592 nm、766.400 nm、317.933 nm、251.611 nm、249.773 nm、396.152 nm。建立标准曲线,每个元素校准拟合相关系数不低于0.995。测试过程中射频功率为1 150 W,泵速为50 r/min,辅助气体流量为0.5 L/min,雾化器气体流量为0.6 L/min,冷却气体流量为12 L/min。测量3次取平均值。
1.3.2 表面微观形貌表征
本试验采用扫描电子显微镜对玻璃内表面进行微观形貌观察。将切好的玻璃片放入酒精中,使用超声波清洗机清洗30 min以清除表面污物,再放入烘箱中烘干。因为玻璃表面不导电,因此需要喷涂一层金膜,然后再用扫描电子显微镜观察。使用扫描电子显微镜观察玻璃瓶内表面的侵蚀情况,使用X射线能量色散光谱仪(EDS)进行面扫描进一步确认玻璃瓶内表面是否产生脱片。
2 结果与讨论
2.1 储存时间对离子迁移影响
将配制的质量浓度为0.020 0 g/mL的药液盛放到4个20 mL玻璃瓶中,分别于1 d、7 d、14 d、28 d后将药液取出混匀,测量3次药液中Al3+、B3+、Ca2+、K+、Na+、Si4+的浓度,取平均值。其中Ca2+、K+、Na+含量较多,超出仪器测试范围,需将药液稀释1 000倍后,再进行测量,相应测量结果乘以1 000即Ca2+、K+、Na+浓度。另外,以聚四氟乙烯瓶盛装并储存了相应时间的0.020 0 g/mL的药液作为空白对照,将测量数据减去空白药液的离子浓度,得到药液储存时间对离子迁移浓度的影响(见图1)。
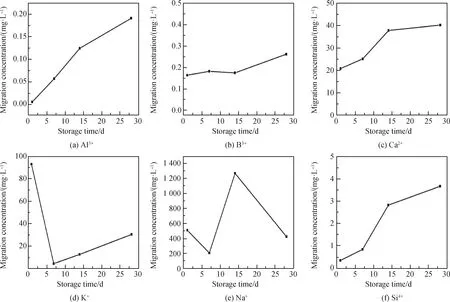
图1 药液储存时间对离子迁移浓度的影响
图1显示随着储存时间的延长,Al3+、B3+、Ca2+、Si4+迁移浓度增加。这是因为药液中的去离子水会侵蚀玻璃瓶,H+与玻璃网络中的K+和Na+发生了交换。随着交换的进行,药液中OH-含量不断增多,对玻璃网络的侵蚀不断增加,造成玻璃中Si4+迁移。硅的损失使玻璃网络被破坏,从而导致Al3+、B3+、Ca2+、Si4+迁移浓度增大。
药液储存1~7 d时K+迁移浓度下降,随着储存时间进一步延长,迁移浓度略有上升。药液中Na+迁移浓度在储存时间为1~7 d时下降,7~14 d时上升,14~28 d时下降。用EDS测定玻璃瓶表面元素含量,结果表明,储存7 d时玻璃表面K+和Na+含量高于储存1 d时的元素含量。这说明药液中K+和Na+迁移浓度在1~7 d下降是玻璃表面吸附作用造成的。随着储存时间进一步延长,Si4+的持续损失会造成玻璃网络被破坏,K+和Na+迁移浓度在7~14 d上升。进一步延长储存时间后K+迁移浓度继续上升,而Na+迁移浓度呈下降趋势,这是因为Na+与氧的结合能力比K+高,Na+会与Si—O键反应[14-16]。
用SEM测试储存药液1 d、7 d、14 d、28 d后玻璃瓶内表面的微观形貌,测试结果如图2所示。由图2可以观察到,未盛装药液的玻璃瓶内表面较为平滑,无凹坑和划痕。储存时间为1 d时,玻璃瓶内表面有凸起部位,当储存时间进一步延长到7 d时,玻璃瓶内表面出现凹坑,储存到14 d时,玻璃瓶内表面凹坑变多且变得明显,28 d时玻璃瓶内表面出现划痕。

图2 不同药液储存时间下玻璃瓶内表面的SEM照片
玻璃瓶内表面的凸起可能是玻璃在加热期间形成的气体夹杂物或者气泡[17]。凸起部位主要成分为硼酸钠,而下层是富硅层[18]。这些凸起是水溶性的,在清洗过程中会被冲走,一旦被冲走玻璃瓶内表面就会留下凹坑。
储存28 d时,玻璃瓶内存在划痕和一些透明絮状物(见图3)。经EDS-mapping面扫描分析可知,絮状物主要由Al、Si、Ca、Na、O、B等元素构成。这些元素是玻璃的主要成分,在药液中含量较少,表明这些絮状物是从玻璃表面脱落下来的,称为脱片。

图3 玻璃瓶中产生的絮状物
2.2 玻璃瓶规格对离子迁移的影响
2 mL、5 mL、10 mL、20 mL四种规格玻璃瓶的相关尺寸如表1所示。从表1中可以看出,随着玻璃瓶规格增大,玻璃瓶与药液接触的相对表面积会减小。

表1 玻璃瓶规格
将0.020 0 g/mL的药液分别盛装到2 mL、5 mL、10 mL、20 mL的玻璃瓶中,于28 d后将药液取出混匀,测量3次药液中Al3+、B3+、Ca2+、K+、Na+、Si4+的浓度,取平均值。其中Ca2+、K+、Na+同样需要稀释1 000倍之后进行测量。6种离子的迁移浓度随玻璃瓶规格变化的结果如图4所示。
从图4中可以看出,随着玻璃瓶规格增大,药液中Al3+、B3+、Ca2+、K+、Na+、Si4+迁移浓度降低,这是因为玻璃瓶规格的增大使得瓶与药液接触的相对表面积减小。相对表面积越小,说明单位体积药液中药液与玻璃瓶接触面积越小,药液与玻璃瓶发生离子交换的可能性越小,所以药液中的离子迁移浓度降低。
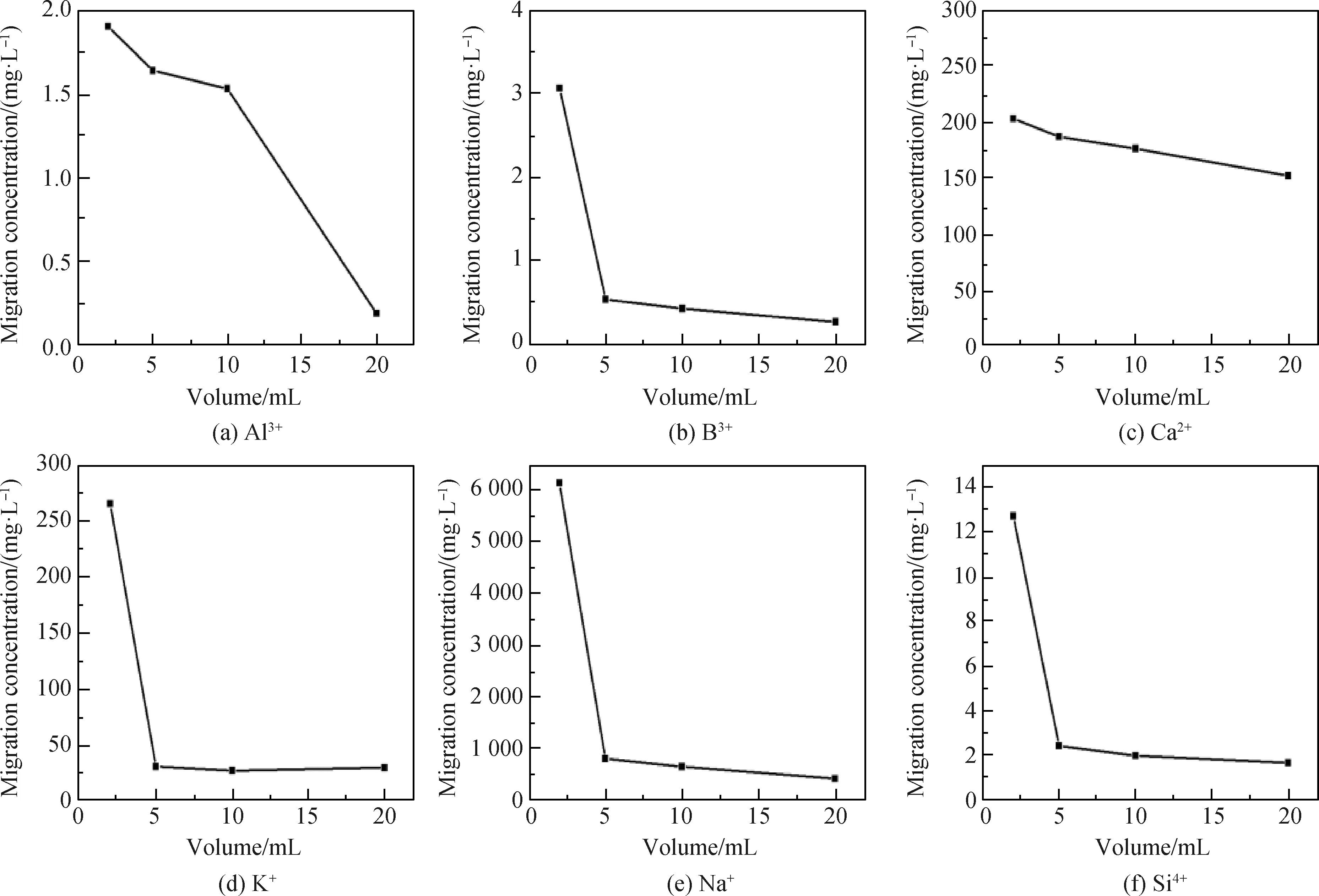
图4 不同玻璃瓶规格对离子迁移浓度的影响
不同规格玻璃瓶储存0.020 0 g/mL药液28 d后,玻璃瓶瓶底内表面的SEM照片如图5所示。从图5中可以看出,2 mL玻璃瓶内表面的坑洞个数最多,侵蚀最严重,5 mL玻璃瓶内表面除了凸起部位,还有两个较明显的坑,10 mL玻璃瓶内表面除了凸起部位外还有少量的小坑,20 mL玻璃瓶内表面几乎没有坑洞。这说明玻璃瓶规格越小,玻璃瓶内表面受侵蚀越严重。

图5 盛装药液的不同规格玻璃瓶内表面的SEM照片
2.3 药液浓度对离子迁移的影响
将4种质量浓度(0.002 5 g/mL、0.005 0 g/mL、0.010 0 g/mL、0.020 0 g/mL)药液分别盛装到2 mL玻璃瓶中储存28 d,离子迁移浓度随药液浓度的变化如图6所示。
从图6中分析可知,随着药液浓度升高,Al3+、B3+、Ca2+、K+、Na+、Si4+的总体浓度均呈上升趋势。在药液质量浓度为0.020 0 g/mL时,各个离子的迁移浓度均达到了最大值。这是因为药液浓度越高,药液中水含量越少,水分子可以与玻璃骨架直接发生反应生成一层硅胶保护膜Si(OH)4。这层硅胶保护膜不仅会阻碍药液中有效成分对玻璃的侵蚀,而且还可以阻碍Na+和H+扩散。随着水含量越来越少,生成的硅胶保护膜越来越少,玻璃被侵蚀的可能性越来越高。所以随着药液浓度升高,药液中Al3+、B3+、Ca2+、K+、Na+、Si4+迁移浓度呈上升趋势。

图6 药液浓度对离子迁移浓度的影响
图7为盛装不同浓度药液的2 mL玻璃瓶内表面的SEM照片。从SEM照片中可以看出:当盛装质量浓度为0.020 0 g/mL的药液时,玻璃瓶内表面有大量坑洞;当盛装药液质量浓度降低到0.010 0 g/mL时,玻璃瓶内表面坑洞减少,仅有一两个明显坑洞;当药液质量浓度下降到0.005 0 g/mL时,玻璃瓶内表面凸起减少,有轻微划痕;当药液质量浓度为0.002 5 g/mL时,玻璃内表面划痕不明显。
2.4 模拟液pH值对离子迁移的影响
采用pH值为2(质量分数为3%的柠檬酸),pH值为7.1(去离子水)和pH值为8(质量分数为3%的柠檬酸三钠)的三种模拟液,研究了酸性药液、中性药液和碱性药液对玻璃瓶内表面阳离子迁移的影响。空白浓度为储存到聚四氟瓶中7 d的三种模拟液各离子浓度。将上述三种模拟液储存到20 mL玻璃瓶中,于第7天后取出,将每种模拟液混匀,进行离子浓度测试,每种离子的测试浓度减去空白浓度即实际迁移浓度。
图8为不同pH值模拟液对离子迁移浓度的影响。从图8中可以明显看出,每种离子的迁移浓度在中性条件下最低。其中Al3+、B3+、Ca2+在酸性模拟液下的迁移浓度高于在碱性模拟液下的迁移浓度,K+、Na+、Si4+在碱性模拟液下的迁移浓度高于在酸性模拟液下的迁移浓度。
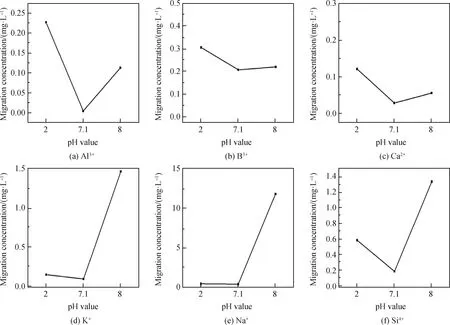
图8 不同pH值模拟液对离子迁移浓度的影响
碱性溶液对玻璃的侵蚀是通过OH-侵蚀玻璃,破坏玻璃网络实现的,而酸性溶液对玻璃的侵蚀是通过离子交换反应实现的。
水是弱电解质,会电离出少量的OH-和H+。由于水中OH-含量较低,所以水对玻璃网络的侵蚀能力比碱性溶液差。同样,水中的H+含量比酸性溶液中的H+含量低,与玻璃中Na+的交换频率比酸性溶液小,所以对玻璃的侵蚀比酸性溶液差。因此,在中性条件下,药液中离子迁移浓度最小。
碱性条件下,玻璃被侵蚀后生成的硅酸离子与Ca2+在玻璃表面生成溶解度较小的硅酸钙,阻碍网络进一步破坏,所以Ca2+迁移浓度较小。Al3+与Ca2+类似,硅酸铝在碱性溶液中的溶解度较小,阻碍了对玻璃的进一步侵蚀。在酸性条件下,由于柠檬酸溶液对Al3+和Ca2+有很强的螯合作用,对玻璃中Al3+和Ca2+的夺取能力较强,所以Al3+和Ca2+迁移浓度较高[19]。OH-可以直接破坏玻璃网络,非桥氧数量增多,有利于形成[BO4]四面体立体结构,所以B3+在高pH值下的迁移量较小。在酸性条件下,非桥氧数量相对较少,有利于形成[BO3]三角体结构,[BO3]是平面结构,相对[BO4]来说不稳定,所以在低pH值下,B3+的迁移量较大。
OH-是亲核试剂,玻璃中的Si原子较容易受到亲核攻击[20]。所以,药液中OH-含量越多,玻璃中迁移出来的Si元素越多。碱性溶液中的OH-会破坏玻璃的基本骨架,使玻璃网络中与氧连接较弱的氧化物脱离玻璃主体,Na+和K+在玻璃网络中由于单键能较低,与O的连接能力较弱,一旦玻璃网络受OH-侵蚀,Na+和K+很容易从玻璃网络中脱离出来。所以在碱性条件下,Na+和K+的迁移量比酸性条件下多。
不同pH值模拟液下玻璃瓶内表面形貌如图9所示。SEM照片显示,当盛装碱性模拟液时,玻璃瓶内表面损坏比较严重,并且有两道明显的划痕,没有发现坑洞。当盛装酸性模拟液时,玻璃瓶内表面出现破坏,有三处坑洞。当盛装去离子水时,玻璃瓶内表面只有少量的凸起,受侵蚀程度最小。

图9 盛装不同pH值模拟液的玻璃瓶内表面的SEM照片
3 结 论
(1)延长药液储存时间会促进玻璃瓶内表面离子向药液迁移,使内表面受侵蚀程度增大,甚至会出现脱片现象。
(2)离子迁移浓度随玻璃瓶规格增大而减小,规格越大,相对表面积越小,离子迁移浓度越小。
(3)药液浓度越高,离子迁移量越大,玻璃瓶内表面受侵蚀程度越大。
(4)在不同pH值条件下,各离子迁移浓度不同,Al3+、B3+、Ca2+迁移浓度大小为酸性>碱性>中性;K+、Na+、Si4+迁移浓度大小为碱性>酸性>中性;中性药液对离子迁移浓度影响最小,对玻璃瓶的侵蚀也最小。
