盐酸万古霉素口服液中万古霉素效价含量方法学验证
2022-12-26章瑛杨毅生张春华姚闽
章瑛,杨毅生,张春华,姚闽
江西省药品检验检测研究院,国家药品监督管理局中成药质量评价重点实验室,江西省药品与医疗器械质量工程技术研究中心,江西 南昌 330029
大多数抗生素是微生物的次级代谢产物,同时抗生素本身结构复杂,每种抗生素大多是几种相似组分的混合物,加之抗生素的不稳定,产品中混杂着分解产物、异构物等。所以给抗生素药品分析检定工作带来很大困难。而微生物检定法是以抗菌活性为指标来衡量抗生素中有效成分的效力的一种方法。
本研究以管碟法建立盐酸万古霉素口服液中盐酸万古霉素的效价含量测定方法[1-4],并按《中国药典》2020 年版四部通则1200 生物活性测定方法、《抗生素微生物检定法及其标准操作》及《药品微生物检验手册》对建立的方法予以验证[5-6]。
1 仪器与药材
1.1 仪器
ZY-300 Ⅳ抑菌圈测定仪、MS205DU 电子天平、ZY-300G 牛津放量器、PYX-DHS600×600×750 隔水式恒温培养箱、MLS-3781L-PC 高压蒸汽灭菌器。
1.2 试药与菌种
万古霉素标准品(中国食品药品检定研究院,批号:130360-201302,含量:每毫克相当于1 066 万古霉素单位);盐酸万古霉素口服液(批号:IP013-2008002、IP013-2009001、IP013-2009002,规格:50 mg/mL);抗生素检定培养基Ⅷ号(北京三药科技开发公司,批号:200418;北京陆桥技术股份有限公司,批号:210220;北京奥博星生物技术有限责任公司,批号:20210811,青岛高科园海博生物技术有限公司,批号:20201205);菌种:枯草芽孢杆菌[CMCC(B)63501],来源于中国食品药品检定研究院。
2 试验方法与结果
2.1 菌悬液、缓冲液及双碟制备
2.1.1 菌悬液制备取枯草芽孢杆菌的营养琼脂斜面培养物,接种于盛有营养琼脂培养基的培养瓶中(36 ℃培养7 d),用革兰染色法涂片镜检,有芽孢在85%以上。用灭菌水将芽孢洗下,在65 ℃加热30 min,备用。
2.1.2 缓冲液的制备磷酸缓冲液(pH6.0):取磷酸氢二钾2 g 与磷酸二氢钾8 g,加水适量溶解,用水稀释至1 000 mL,摇匀,在115 ℃灭菌30 min,即得。
2.1.3 双碟制备取直径约90 mm,高16~17 mm 的平底双碟,分别注入加热融化的培养基(编号:Ⅷ)20 mL,使在碟底内均匀摊布,放置水平台面上使凝固,作为底层。另取培养基适量加热融化后,放冷至60 ℃,加入试验菌悬液适量,摇匀,在每一双碟中分别加入5 mL,使在底层上均匀摊布,作为菌层,放置水平台面上冷却凝固。在每一双碟中以等距离均匀放置牛津杯4个,用陶瓦圆盖覆盖,备用。
2.2 标准品和供试品溶液的制备
2.2.1 标准品储备溶液的制备精密称取万古霉素标准品用灭菌水制成每1 mL 含1 000 万古霉素单位的溶液,作为标准品储备溶液。精密量取储备溶液适量,用磷酸缓冲液(pH6.0)稀释制成100 U/mL 溶液。再将100 U/mL 的标准溶液,用磷酸缓冲液(pH6.0)稀释制成高低剂量溶液,浓度分别为10 U/mL(S1)、5 U/mL(S2)的溶液。
2.2.2 供试品储备溶液的制备取一份盐酸万古霉素口服溶液样品(1 瓶盐酸万古霉素粉剂+1 瓶稀释剂),先握住盐酸万古霉素粉剂瓶的颈部,在硬表面上拍打底部边缘以松开粉末,然后从瓶子上取下瓶盖,轻敲密封垫衬套的顶部,以松开可能黏附在衬套上的所有粉末,再缓慢地剥离内衬密封垫,取一瓶稀释剂,摇动几秒,打开稀释瓶,将倒入约一半的溶液到盐酸万古霉素粉剂瓶中,盖上盖子并垂直摇动大约45 s,然后将剩余的稀释剂加入盐酸万古霉素粉剂瓶中,盖上盖子并摇动大约30 s,即得50 mg/mL的溶液。精密量取2 mL,置100 mL 量瓶中,加水稀释至刻度,摇匀,即得1 000 U/mL 的供试品储备溶液。精密量取储备溶液适量,用磷酸缓冲液(pH6.0)稀释制成100 U/mL 溶液。再将100 U/mL 的标准溶液,用磷酸缓冲液(pH6.0)稀释制成高低剂量溶液,浓度分别为10 U/mL(T1)、5 U/mL(T2)的溶液。
2.3 专属性
用样品中的稀释剂代抗生素进行试验,未出现抑菌圈。结果见图1。

图1 盐酸万古霉素专属性图
2.4 线性
用上述100 U/mL 的标准品溶液,以5 U/mL 为中心浓度(Co),剂距为1∶0.8,用磷酸缓冲液(pH6.0)稀释成浓度为2.00、2.56、3.20、4.00、6.25、7.81、9.76、12.20、15.25 U/mL 的系列溶液,按照抗生素生物检定法第一法管碟法(一剂量法)进行线性测定,每一个浓度为一组,每组4 个双碟,在每一双碟的加菌培养基上置6 枚牛津杯,间隔的3 枚内加入标准品的某一特定浓度Ck,另3 枚内加入标准品的中心浓度Co。经培养16 h 后,使用抑菌圈测定仪测定各个抑菌圈的直径。分别求得每组3 个双碟中心浓度Co所致的抑菌圈直径平均值及C1-C9所致抑菌圈直径的平均值(Ck=1-9)。令fk=-,分别计算fk值,则8 组双碟可得出f1-9 的9 个反应参数。以fk值为纵坐标,以相应的标准品浓度对数为横坐标,得出回归直线方程式y=6.614 1x-4.560 1,r=0.999 6,在2.00~15.25 U/mL 的万古霉素浓度范围内,fk(mm)与浓度对数lgC 线性关系良好。
2.5 精密度
取盐酸万古霉素口服液(批号:IP013-2009001)样品测定6 次。标准品溶液和供试品溶液高低浓度剂量同“2.2.2 供试品溶液制备”,分别为10 U/mL、5 U/mL。结果平均含量为标示量的104.0%,相对标准偏差(RSD)为2.49%。见表1。

表1 重复性试验
2.6 准确度(回收率%)
制备9 份1 000 U/mL 的供试品溶液,从标准品储备溶液和供试品溶液中精密量取4 mL、5 mL、6 mL,分别置100 mL 量瓶中,加磷酸缓冲液(pH6.0)稀释至刻度,摇匀,即得80 U/mL、100 U/mL、120 U/mL 的溶液各三份。按《中国药典》2020 年版四部生物检定法第一法管碟法(二剂量法)测定相应的含量。分别测定3 次。结果回收率均在90.0%~110.0%范围内,平均回收率为99.5%。见表2。
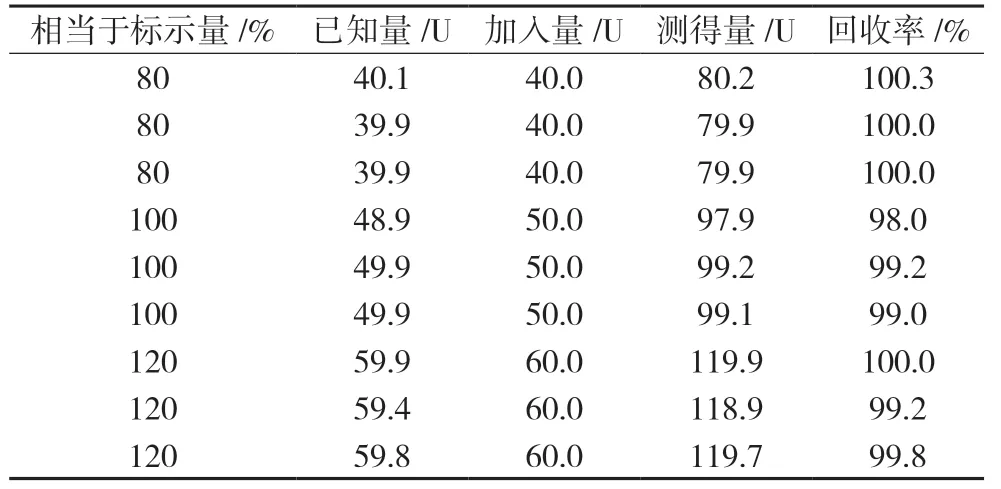
表2 回收率试验结果
2.7 适用性
因本品种对培养基和缓冲液的pH 值较稳定,方法较成熟,故只对不同来源培养基及溶液稳定性进行验证。采用4 个厂家的培养基进行验证,结果RSD为0.75%,不同品牌培养基对结果影响较小。见表3。选一批样品处理后,冰箱冷藏放置1 d、4 d、14 d,分别测定结果,偏差为0.72%,溶液稳定性良好。见表4。
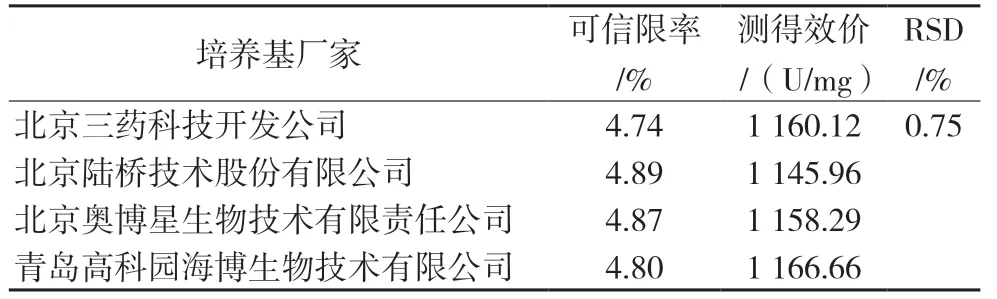
表3 不同厂家培养基测定结果

表4 溶液稳定性试验结果
3 讨论
抗生素微生物检定法分为稀释法和浊度法两种方法。其中,管碟法为国际通用方法,国内外药典均收载了此法。此法是根据抗生素在一定浓度范围内,对数剂量与抑菌圈直径(面积)呈直线关系,通过比较标准品与供试品产生抑菌圈的大小,计算出供试品的效价。但由于操作步骤及影响因素较多,需要从每个环节严格控制实验条件,才能使结果准确可靠[7-11]。在此次试验中总结了如下影响因素。
3.1 前期因素
(1)试验实验室应注意防止抗生素及微生物的污染,其由样品处理的试验间和制备双碟的半无菌间两部分组成。半无菌间需用紫外线灯达到空气消毒,时间30 min 以上为宜。(2)双碟和牛津杯的选择尽量使用同一生产企业且同一批次。碟子大小不均,底部不平,会造成培养基厚薄不一,导致抑菌圈不圆,大小差异大,直接影响实验结果的准确性。牛津杯内径不一和重量差异大,形成的抑菌圈大小差异较大,在培养基平面上下陷的深度不一致,也可使溶液扩散不均匀。双碟和钢管使用前应先用专用洗液进行浸泡以后再用水冲洗,沥干,置150~160 ℃干热灭菌2 h 备用。(3)培养箱选择隔水式恒温培养箱为宜,隔板上备有带孔的玻璃板并垫平。最主要使用之前要测定水平度,使双碟放入培养时不会由于平面不平而钢管里液体流出导致破圈或不成圈现象。(4)抑菌圈测定仪的技术指标应符合抑菌圈测量仪检定规程的要求,尤其是抑菌圈测定的准确度及精密度的要求,检验合格方能确保试验结果的准确可靠。
3.2 试验过程中的因素
(1)盐酸万古霉素具有吸湿性,在称取万古霉素标准品的时候容易吸湿,故天平室的湿度要控制好并且称取时要快速,否则数据不准确而导致实验得出的效价值有偏差。(2)试验菌的敏感度,特别要防止染菌,制备菌层时含菌浓度要适宜。在双碟倒入底层和铺菌层时一定要铺平,尤其是菌层,否则影响培养基的厚度H。H 与管中心到抑菌圈边缘距离r 相互影响:H 增大,r 缩小;H 减小,r 增大。还有在制备菌层时,培养基温度不宜过高或者温度正常但受热时间太长,可能会使试验菌部分被杀死或全部被杀死,从而使抑菌圈破裂或甚至无圈。故最好培养基加热融化后,置恒温水箱内一段时间使培养基均匀降温平衡后,加入试验菌。本试验使用的实验菌株为枯草芽孢杆菌,芽孢悬液对温度抵抗力强,可提高培养基温度到65 ℃,更利于摊布双碟,如温度过低,极易凝固,而导致菌层不平。(3)滴加溶液时候容易溅出落在琼脂培养基表面上或者钢管内有气泡。故滴加溶液时距离管口不要太高,适当调节,如有溶液溅出可以预先备好消毒小滤纸片轻轻吸去,这样培养后不会影响破圈。另外还需注意滴加溶液的顺序和时间,溶液的高低浓度按照SH-TH-SL-TL 的顺序进行滴加,每个双碟用时控制在1 min 内,避免抗生素在培养基内的扩散产生差异,降低碟间和剂间的差异,引起可信限率偏大,误差增大。(4)双碟叠放不宜超过3 个,保证双碟的温度一致,使试验菌生产速度一致,避免造成抑菌圈变小或者不圆整,减小试验误差。
本实验中可能还有未涉及的因素,但各因素往往不是孤立的而是相互联系、相互作用和相互影响的。所以在操作过程中,严格按照操作规范,谨慎小心操作,减少外界与人为因素引起的误差,使测定结果与真实值更为接近,提高实验的准确性。
4 结论
盐酸万古霉素口服液中万古霉素的效价含量测定用的管碟法(二剂量法),该方法抑菌圈直径与万古霉素浓度的对数值呈良好的线性关系,专属性、精密度、准确度和适用性均满足实验要求,适合用于盐酸万古霉素口服液中万古霉素的效价含量测定。
