重组人血管内皮抑制素注射液同步放化疗治疗局部晚期非小细胞肺癌的临床效果
2022-12-21瞿玲凤赵景胜罗家顺
瞿玲凤 赵景胜 罗家顺
1.吉首大学医学院,湖南湘西 416000;2.吉首大学一附属医院肿瘤科,湖南湘西 416000
肺癌新发和死亡病例居我国癌症榜首[1],非小细胞肺癌(non-small cell lung cancer,NSCLC)占新发肺癌病例的85%左右,是最常见的亚型,首次诊断时约30%的NSCLC 为Ⅲ期[2]。局部晚期非小细胞肺癌(locally advanced non-small cell lung cancer,LANSCLC)包括无法切除的ⅢA-N2、ⅢB 和ⅢC期[3],大约占所有肺癌的15%[4]。同步放化疗(concurrent chemoradiotherapy,cCRT)在世界范围内已被广泛用于Ⅲ期不可切除的NSCLC 患者的综合治疗,基于PACIFICⅢ期临床研究结果,PACIFIC 方案(cCRT 后12 个月的Durvalumab 免疫巩固)在2018 年成为新的标准治疗策略[5],但Durvalumab 药物价格昂贵,超出了大部分患者的经济承受能力[6],相当部分患者因经济困难不能承受免疫治疗费用,因此限制了免疫治疗的使用。提高cCRT 疗效,可能进一步提高PACIFIC 方案的疗效。因此,这就需要在cCRT 的基础上提高LANSCLC的疗效。本研究对予重组人血管内皮抑制素注射液同步放化疗治疗的LANSCLC 患者的临床疗效及不良反应进行回顾性分析。
1 资料与方法
1.1 一般资料
回顾性分析2017 年11 月至2020 年12 月吉首大学第一附属医院肿瘤科49 例LANSCLC 住院患者的临床资料,根据放化疗期间是否予重组人血管内皮抑制素注射液同步治疗将其分为研究组(23 例)和对照组(26 例),研究组予重组人血管内皮抑制素注射液同步放化疗治疗,对照组予cCRT 治疗。本研究通过医院医学伦理委员会审批[伦审批号:2018 年伦审(1)号]。研究组中,男21 例,女2 例;年龄40~73 岁,平均(59.87±9.13)岁;肺癌类型:鳞癌16 例,腺癌6例,鳞腺癌1 例;TNM 分期:Ⅲa 期8 例,Ⅲb 期12例,Ⅲc 期3 例。对照组中,男24 例,女2 例;年龄37~77岁,平均(58.62±9.41)岁;肺癌类型:鳞癌22 例,腺癌2 例,鳞腺癌2例;TNM 分期:Ⅲa 期8 例,Ⅲb 期13 例,Ⅲc 期5例。两组患者的一般资料比较,差异无统计学意义(P>0.05),具有可比性。纳入标准:①具有可测量或可评价的肿瘤病灶,经病理确诊为NSCLC,且根据美国癌症联合会(American Joint Committee on Cancer,AJCC)第8 版肺癌临床分期标准[7]分为Ⅲ期者;②无放化疗禁忌证,接受cCRT 治疗模式;③卡氏功能状态(Karnofsky performance status,KPS)评分[8]>60 分,可配合完成治疗者。排除标准:①有其他恶性疾病肿瘤病史者;②无复查影像学资料,无法评估疗效者;③合并严重心、肺、脑等疾病,影响预期生存者。
1.2 方法
1.2.1 对照组 ①化疗方案:紫杉醇脂质体(南京绿叶制药有限公司,国药准字H20030357,生产批号:117050209、117100109、117120809、118071009、119050 609、119121009、120010221、218060209、218110509、219 040309、219101009、220020121、220050109)135 mg/m2,d1;顺铂(齐鲁制药有限公司,国药准字H20023460,生产批号:8A002A89、8A004A89、8K034A89、8L036A89、8L039A89)75 mg/m2,分3 d 使用(d1~3),21 d 为1 个周期,执行2 个周期,调强放疗期间同步执行,同时给予护心、护胃、营养支持治疗及对症止呕治疗。
②放疗方法:调强适形放疗,所有患者都采用个体化体模及体罩固定,进行螺旋CT 定位扫描,扫描范围从下颌下缘至肝下缘。层厚5 mm,层距为0。共扫描5 组。自然呼吸平扫1 组,自然吸气未增强扫描2 组,自然呼气未增强扫描2 组。扫描完成后,图像传输到瓦里安Eclipse 计划系统制作放疗计划,在每组图像上勾画靶区,包括肺部原发灶肿瘤区(gross tumor volume,GTV)、临床靶区(clinical target volume,CTV)(GTV 外放0.5 cm)、计划靶区(planning target volume,PTV)(CTV 外放0.5 cm)、累及淋巴结区域(gross tumor volume of lymph nodes,GTVnd)、计划累及淋巴结靶区(planning gross tumor volume of lymph nodes,PGTVnd)(GTVnd 外放0.5 cm),PTV 与PGTVnd 融合后为最终靶区PTV1。靶区剂量50.0~72.6Gy/25~36次,中位剂量60 Gy/30 次,2.0~2.3 Gy/次,5 次/周。
1.2.2 研究组 在化疗阶段增加重组人血管内皮抑制素注射液(商品名:恩度,山东先声生物制药有限公司,国药准字S20050088,生产批号:201707034、201712072、201806038、201809063、201812079、201904 013、201909042、201912072、202003017、2020004026),具体方法为:重组人血管内皮抑制素注射液:30 mg/d,持续静脉泵入,连续给药7 d,21 d 为1 个周期,与化疗同步,其余同步放化疗方案同对照组。
1.3 观察指标及评价标准
观察两组患者的临床表现、复查的影像学资料、生存情况,比较两组患者的客观有效率(objective responserate,ORR)、中位无进展生存时间(progression-free survival,PFS),1 年生存率、2 年生存率、中位生存时间(overall survival,OS)及不良反应发生情况。
①放化疗结束后4 周内根据复查胸部CT 等影像学资料评估近期疗效,使用RECIST 实体瘤客观疗效评定标准[9],主要分为完全缓解(complete response,CR)、部分缓解(partialresponse,PR)、稳定(stabledisease,SD)、进 展(progression disease,PD),ORR=CR+PR。CR:全部肿瘤病灶消失,维持4 周;PR:缩小30%以上,维持4 周;SD:介于PR 和PD 之间;PD:病灶增加20%,或出现新病灶。②远期疗效评价中位PFS、1 年生存率、2 年生存率、中位生存时间。PFS:自放化疗开始至肿瘤出现任何进展(转移或局部进展)的时间;OS:自放疗开始至死亡或最后随访的时间。③不良反应评定按美国国家癌症研究所不良事件通用毒性标准(National Cancer Institute Common Terminology Criteria for Adverse Events 4.0,NCI-CTCAE 4.0)[10]分为0~Ⅳ度。
1.4 统计学方法
采用SPSS 26.0 统计学软件进行数据分析,符合正态分布的计量资料用均数±标准差()表示,组间比较使用t 检验;计数资料用率表示,两组间比较采用χ2检验;等级资料采用秩和检验。生存分析采用Kaplan-Meier 法计算,差异性检验采用log-rank法。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者近期疗效的比较
49 例患者均可评价疗效,两组患者的近期疗效比较,差异无统计学意义(P>0.05);两组患者的ORR比较,差异无统计学意义(P>0.05)(表1)。
2.2 两组患者远期疗效的比较
随访截至2022 年3 月1 日,中位随访时间36.07 个月,生存状态随访率100%。两组的中位PFS比较,差异无统计学意义(P>0.05);两组的1 年生存率、2 年生存率、中位生存时间比较,差异无统计学意义(P>0.05)(表2、图1~2)。
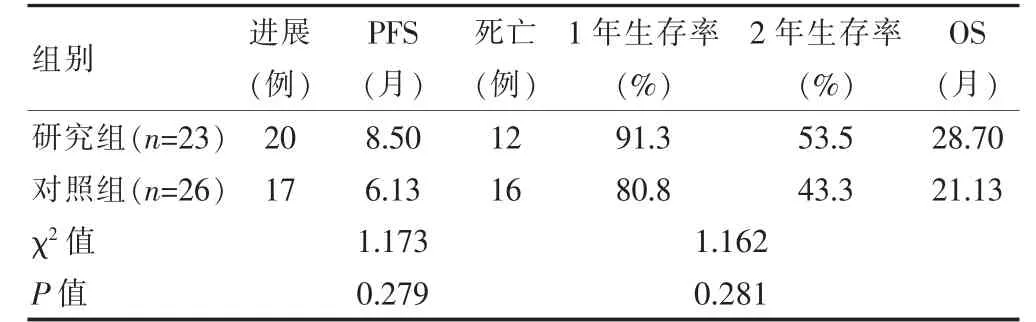
表2 两组患者远期疗效的比较
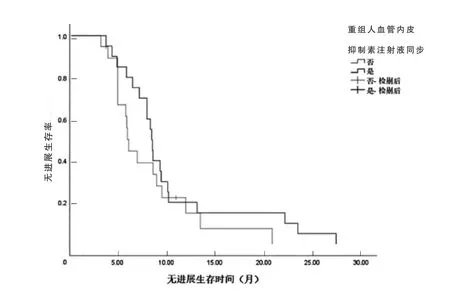
图1 两组无进展生存率的比较

图2 两组总生存率的比较
2.3 两组患者不良反应的比较
两组患者在整个治疗过程中均能耐受相关不良反应。两组的不良反应主要包括骨髓抑制、消化道反应、放射性肺炎及食管炎。多为Ⅰ、Ⅱ级反应。骨髓抑制主要为白细胞减少,仅观察组中1 例因血小板减少所致的Ⅲ度骨髓抑制,消化道反应主要为恶心、呕吐,仅对照组1 例腹泻所致Ⅱ级消化道反应。两组的放射性肺炎、放射性食管炎、骨髓抑制、消化道反应的不良反应发生情况比较,差异均无统计学意义(P>0.05)(表3)。
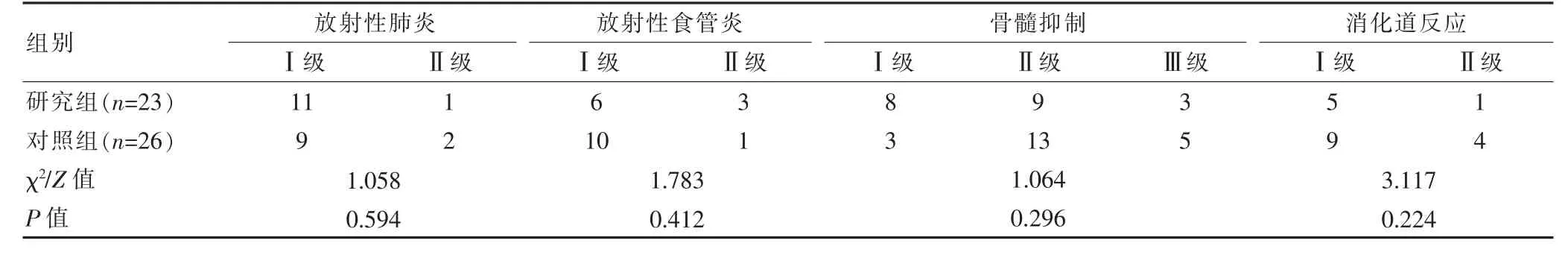
表3 两组患者不良反应的比较(例)
3 讨论
对于LANSCLC,目前,cCRT 在世界范围内已被广泛用于Ⅲ期不可切除的NSCLC 患者的综合治疗。在我国,以铂类为基础的双药化疗与放疗同步或序贯是治疗Ⅲ期不可切除的NSCLC 的标准治疗方案。然而,尽管优化了治疗方案,接受这种治疗的NSCLC 患者的中位PFS 仍较短,达8~10 个月,5 年生存率约为15%[4]。因此,需要寻求新的治疗方案,进一步提升疗效。相关PACIFIC Ⅲ期临床研究显示:Ⅲ期不可切除的NSCLC 患者放化疗后使用PD-L1 抑制剂Durvalumab 免疫治疗与安慰剂比较,显著提高了OS(中位OS 未达到vs.28.7 个月,P=0.002 51,数据截至2018 年3 月22 日)和PFS(中位PFS 16.8 个月vs.5.6 个月,P<0.000 1,数据截至2017 年2 月13日),基于这些结果,PACIFIC 方案(cCRT 后12 个月的Durvalumab 免疫巩固)在2018 年成为新的标准治疗策略[5]。然而,免疫巩固治疗因不良事件停药率较高、有一定的致死率[11]。且在部分经济落后地区,相当部分患者因经济困难不能承受免疫治疗费用,便限制了免疫治疗的使用,这就需要在cCRT 阶段提高LANSCLC 的疗效。cCRT 阶段疗效的提高,有望最终提高PACIFIC 方案的疗效。
PACIFIC 之外,曾有多项研究以试图提高Ⅲ期NSCLC 的疗效,但为阴性结果。有研究显示通过诱导化疗后对不可切除LANSCLC 行手术治疗并不能改善其OS[12]。对于LANSCLC 最佳的同步化疗方案尚未确定,常用方案包括顺铂-依托泊苷和每周低剂量卡铂-紫杉醇[13-14]。Ⅲ期研究(PROCLAIM 和RTOG0617)显示,在含铂同步放化疗中加入多靶点抗叶酸药物培美曲塞和抗EGFR 抗体西妥昔单抗均未提高ⅢA 及ⅢB 期患者生存率[15-16],同样,将放射剂量从标准的60 Gy 增加到74 Gy 同步化疗,患者仍无生存获益,并且可能具有潜在危害。由此可见,60 Gy 是目前比较适合的放疗剂量,疗效更好(28.7 个月vs.20.3 个月,P=0.004)[16]。研究发现,诱导化疗虽然在一定程度上可降低肿瘤复发及远处转移的风险,但同时也会增加局部晚期患者的不良反应,且不会延长患者的OS[17]。在巩固化疗方面,也有研究证实cCRT 后给予巩固化疗并不能提高局部晚期患者生存率[18]。目前不推荐在标准剂量cCRT 之后巩固化疗[13]。
血管生成抑制剂可使肿瘤血管短暂地“正常化”,改善肿瘤乏氧状态,利于有效地进行氧气和药物输送,从而提高常规疗法的疗效[19]。血管正常化理论表明,抗血管生成治疗与其他治疗相结合具有潜在的协同作用,且有临床数据显示,抗血管生成药物与其他NSCLC 系统治疗方式(包括化疗、小分子靶向治疗、免疫治疗、放疗)联合使用可发挥更好的抗肿瘤作用,延缓耐药,且不良反应可管理[19-20]。Zhai等[21]采用重组人血管内皮抑制素注射液联合EP 方案同步放化疗治疗67 例不能手术的Ⅲ期NSCLC 患者,其中位PFS 13.3 个月,中位OS 34.7 个月,2 年总生存率59.9%。Ma等[22]报道的5 年生存率分析示,重组人血管内皮抑制素注射液联合cCRT 治疗LANSCLC 中位OS 为29.7 个月(95%CI:22.8~36.6 个月),显著优于单用cCRT 治疗组21.3 个月(95%CI:15.9~26.7 个月)。尽管多数结果证实重组人血管内皮抑制素注射液联合cCRT 可提高NSCLC 患者的临床疗效,但目前并无Ⅰ级证据证实重组人血管内皮抑制素注射液联合cCRT 可提高NSCLC 患者的临床疗效,且亦有临床数据显示是否联合重组人血管内皮抑制素注射液疗效差异无统计学意义。陈淅涓等[23]报道NP 方案同步放疗联合重组人血管内皮抑制素注射液(21 例)与NP方案同步放疗(21 例)治疗LANSCLC 患者的ORR 分别为43.00%、52.38%,中位PFS 分别为16.8 个月、15.3 个月,1 年生存率分别为66.67%和61.90%,两组的近期疗效、远期疗效及不良反应发生率比较,差异无统计学意义(P>0.05)。
本研究中,研究组2 年生存率与Zhai等[21]的数据(59.9%)相近,中位OS 也与Ma[22]等的数据(29.7 个月vs.21.3 个月)相仿,研究组中位PFS 较对照组延长了约2 个月,提示重组人血管内皮抑制素注射液联合放化疗可能可延长LANSCLC 患者生存期、延缓病情进展,在临床上可考虑使用。本研究结果差异无统计学意义,可能与病例数少、联合的化疗方案不同及纳入了部分放疗剂量低于60 Gy 的患者相关。除此之外,本研究认为可能还与重组人血管内皮抑制素注射液的剂量及给药时间相关。Zhai等[21]及Ma等[22]重组人血管内皮抑制素注射液的剂量均为7.5 mg/(m2·d),且在放疗前5~7 d 连续给药,放疗期间每2 周予1 次,共4 个周期。本研究资料的重组人血管内皮抑制素注射液用法:重组人血管内皮抑制素注射液30 mg/d,持续静脉泵入7 d,间歇14 d 重复给药,与化疗同步,执行2 周期。这提示血管靶向药重组人血管内皮抑制素注射液的剂量及介入的时机可能对临床疗效有影响,在放化疗前5~7 d 予重组人血管内皮抑制素注射液抗血管生成治疗可能效果会更好,这可能与5~7 d 连续给药后肿瘤血管正常化,缺氧环境得到改善,联合放化疗治疗可达到较好的肿瘤抑制效果相关。对于重组人血管内皮抑制素注射液联合cCRT 治疗LANSCLC,重组人血管内皮抑制素注射液的最佳使用方案尚未确定,联合哪种化疗方案更能提高疗效也需进一步研究。
本研究是一项样本量小的回顾性研究,需前瞻性临床随机对照试验,以进一步探索重组人血管内皮抑制素注射液联合cCRT 治疗LANSCLC 的疗效和安全性,使用重组人血管内皮抑制素注射液的时机、最佳剂量、频率和疗程、联合的化疗方案都值得进一步探索。
