子宫动脉栓塞术联合B超引导下清宫术治疗剖宫产瘢痕妊娠患者的临床效果
2022-12-12吴定权曹春峰通信作者李捷
吴定权,曹春峰(通信作者),李捷
1 镇江市第四人民医院 (江苏镇江 212003);2 镇江瑞康医院 (江苏镇江 212000)
剖宫产瘢痕妊娠(cesarean scar pregnancy,CSP)主要是指受精卵、滋养叶细胞在子宫术后瘢痕区种植。CSP初期患者无典型临床症状,故识别及诊断难度较大,易延误最佳治疗时机,严重时甚至会造成子宫破裂[1]。单纯采用药物治疗CSP所需时间较长,难以取得预期效果,仅适用于病情发展初期、症状稳定,且未见子宫破裂的患者,由于CSP发生在有剖宫产史的女性中,其瘢痕区子宫肌壁往往较为薄弱,但新生滋养血管及纤维重构组织较丰富,故妊娠期子宫破裂、大出血等并发症发生率高,严重威胁患者生命安全[2-3]。目前,临床针对Ⅰ、Ⅱ型(国内分型)CSP患者常采取清宫手术治疗,但手术过程中若无影像引导,患者可发生难以控制的大出血[4]。近年来,越来越多的研究发现,因瘢痕区妊娠组织的血供主要来自子宫动脉下行支,故采取子宫动脉栓塞术(uterine artery embolization,UAE)可引发妊娠组织缺血坏死[5]。基于此,本研究探讨UAE联合B超引导下清宫术治疗CSP患者的临床效果,现报道如下。
1 资料与方法
1.1 一般资料
选择2012年1月至2020年12月镇江市第四人民医院收治的100例CSP患者为研究对象,按照手术方式的不同将其分为对照组与试验组,各50例。对照组年龄22~47岁,平均(34.68±3.18)岁;孕次2~4次,平均(2.45±0.40)次。试验组年龄22~47岁,平均(34.36±3.11)岁;孕次2~4次,平均(2.41±0.30)次。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会审核批准,患者及其家属对本研究内容知情同意。
纳入标准:符合CSP诊断标准;术前行彩色多普勒超声检查显示子宫增大,子宫前壁下段肌层可见孕囊及不均质包块;CSP分型(国内分型)为Ⅰ~Ⅱ型;伴有腹痛、阴道不规则流血及停经等临床症状。排除标准:CSP分型(国内分型)为Ⅲ型;伴有其他部位异位妊娠;伴有妊娠高血压及糖尿病;伴有心脑血管疾病;患有精神疾病。
1.2 方法
对照组采用B超(SonoScape S8 Exp便携式超声诊断仪,探头频率3~5 MHz,粤械注册20142230246)引导下清宫术治疗:患者于术前连续口服3 d米非司酮(武汉九珑人福药业有限公司,国药准字H20033551,规格:25 mg/片),25 mg/次,2次/d,同时单次肌内注射注射用甲氨蝶呤(江苏恒瑞医药股份有限公司,国药准字H32026443,规格:100 mg/瓶),剂量为50 mg/m2;第4天进行手术,患者取膀胱截石位,行常规消毒、铺巾后,在B超引导下扩张宫颈,选择6~7号刮头对瘢痕妊娠组织进行吸刮,待超声显示孕囊被吸出后完成手术操作;术后密切监测患者阴道出血量。
试验组采用UAE联合B超引导下清宫术治疗:术前经患者子宫动脉注射注射用甲氨蝶呤,剂量为100 mg(左、右侧动脉各注射50 mg),然后选用艾力康560~710 μm型明胶海绵颗粒[杭州艾力康医药科技有限公司生产,国食药监械(准)字2006第3770360号]作为栓塞剂,使用GE Optima CL323i型DSA机经右股动脉行双侧UAE,即患者取平卧位,行局部麻醉后,用5F邦特子宫动脉导管或Cordis Cobra C2导管成袢后超选择至双侧子宫动脉,各灌注注射用甲氨蝶呤50 mg,然后用艾力康560~710 μm型明胶海绵颗粒将双侧子宫动脉栓塞至残干样改变,保留部分主干,部分患者术前行上腹下丛神经阻滞,经后入路L5/S1左旁穿刺至L5/S1前区,注射造影剂,确认上腹下丛区域后,注入镇痛药(1%罗哌卡因3 ml+0.9%氯化钠注射液17 ml,共20 ml)用以减轻患者术中及术后疼痛,对于术后视觉模拟评分法(visual analogue scale,VAS)评分≥4分的患者,采用止痛药进行止痛;进行介入术后24~28 h,对患者行B超引导下清宫术,方法同对照组。
1.3 评价指标
(1)检测并记录两组术前及术后第1、2天人绒毛膜促性腺激素(human choionic gonadotophin,HCG)水平(血清酶免化学发光法),同时观察两组术后第2天子宫内膜厚度。(2)统计两组术中出血量、术后HCG降低至正常水平用时、住院时间及术后12 h疼痛程度(采用VAS进行评估,分值为0~10分,评分越高表示患者疼痛程度越严重)。(3)统计两组术后异位栓塞、低热及下腹痛、闭经、感染等并发症发生情况。(4)统计两组术后妊娠组织残留、大出血、子宫切除及转行宫腔镜手术占比。
1.4 统计学处理
2 结果
2.1 两组手术前后HCG水平及术后子宫内膜厚度比较
术前,两组HCG水平比较,差异无统计学意义(P>0.05);术后第1天,试验组HCG水平高于对照组,差异有统计学意义(P<0.05);术后第2天,试验组HCG水平低于对照组,子宫内膜厚度大于对照组,差异有统计学意义(P<0.05),见表1。

表1 两组手术前后HCG水平及术后子宫内膜厚度比较
2.2 两组手术相关指标及术后疼痛程度比较
试验组术中出血量少于对照组,术后HCG降低至正常水平用时及住院时间均短于对照组,术后12 h VAS评分低于对照组,差异有统计学意义(P<0.05),见表2。

表2 两组手术相关指标及术后疼痛程度比较
2.3 两组术后并发症发生情况比较
两组术后并发症发生率比较,差异无统计学意义(χ2=1.7778,P=0.1824),见表3。
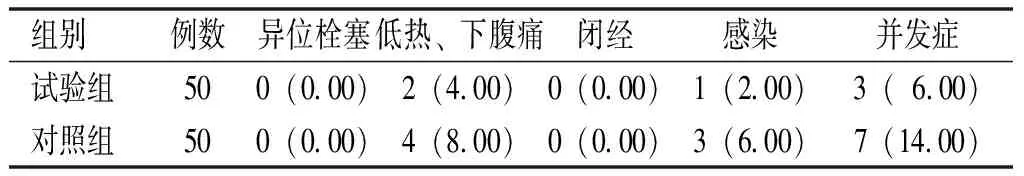
表3 两组术后并发症发生率比较[例(%)]
2.4 两组手术结局比较
试验组术后妊娠组织残留、大出血、子宫切除及转行宫腔镜手术患者占比均低于对照组,差异有统计学意义(P<0.05),见表4。
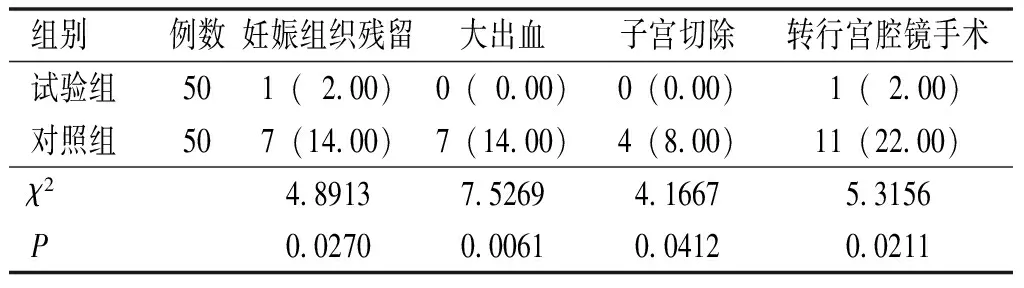
表4 两组手术结局比较[例(%)]
3 讨论
CSP属于异位妊娠的一种,具有较高的临床发病率,主要是由剖宫产导致子宫内膜损伤后形成瘢痕,孕囊着床于瘢痕处所致。该病临床表现缺乏特异性,具有较高的误诊率,可能诱发子宫大出血,严重时需进行子宫切除手术,且术中患者易发生并发症,威胁生命安全[6-7]。目前,临床关于CSP的发病原因及机制并无统一结论,可能与患者产后子宫切口愈合不良、缝合不当存在密切关联;随着患者病情发展,孕囊逐步增大、血供不断增加,继发子宫大出血的风险较高[8]。近年来,越来越多的研究表明,我国CSP发病率逐渐增高,尽早诊治对于降低患者大出血发生率与子宫切除率、保留患者生育能力具有积极的意义[9]。现阶段,临床仍无针对CSP的统一治疗方案,在保证患者手术安全的前提下,尽早将孕囊排出,保留患者子宫及生育功能是治疗CSP患者的预期目标。针对CSP患者的治疗措施主要包括局部化疗后清宫术、甲氨蝶呤全身用药、超声引导下孕囊内注射等,可抑制滋养细胞生长,促使胚胎组织坏死脱落;然而,不同治疗措施存在不同的弊端,且有其适应证[9-10]。CSP分型为国内Ⅲ型、国外Ⅱ型均为清宫手术禁忌证,即使先行UAE再行清宫术,患者仍有较大可能发生子宫破裂、大出血,危及生命;对于此类患者,临床多直接行开腹或腔镜下病灶清除手术、瘢痕修补手术治疗[10]。
本研究结果显示,两组术前HCG水平比较,差异无统计学意义(P>0.05);术后第1天,试验组HCG水平高于对照组(P<0.05);术后第2天,试验组HCG水平低于对照组,子宫内膜厚度大于对照组(P<0.05);试验组术中出血量少于对照组,HCG降低至正常水平用时及住院时间均短于对照组,术后12 h VAS评分低于对照组(P<0.05);两组术后并发症发生率比较,差异无统计学意义(P>0.05);试验组术后妊娠组织残留、大出血、子宫切除及转行宫腔镜手术患者占比均低于对照组(P<0.05)。由此可知,采用UAE联合B超引导下清宫术治疗CSP患者的效果显著。采用药物保守治疗CSP耗时较长、瘢痕病灶消退效果不明显,患者HCG水平下降速度也较缓慢,故保守治疗期间患者若出现阴道大量出血的情况,需转行开腹手术,必要时需切除子宫。清宫术在CSP治疗中也较常用,但传统清宫术具有较高的大出血风险,近年来临床逐渐应用B超引导下清宫术治疗CSP患者,该手术借助B超可更加清晰地显示妊娠部位及周围血管分布情况,避免对微血管造成损伤,提高手术操作精确率,进一步降低患者大出血发生风险。进行UAE的过程中,在栓塞子宫动脉前,向患者孕囊局部灌注高浓度甲氨蝶呤,可促使胚胎组织迅速坏死,用明胶海绵颗粒栓塞子宫动脉致主干呈残干样改变,可起到降低术中出血量的目的,有效预防大出血,其中,明胶海绵颗粒是一种中期栓塞剂,术后2~12周即可被机体自行吸收[11],有利于保留患者子宫供血及生育能力;另外,UAE可阻断子宫血供,导致胚胎因缺血及缺氧死亡,而使用合适的栓塞材料栓塞动脉末梢,可保证毛细血管不受损害,通过其他交通支路供血,避免周围组织缺血坏死,故该手术还可作为清宫术后大出血的挽救措施,对促进患者术后恢复具有积极意义。
综上所述,UAE联合B超引导下清宫术治疗CSP患者的效果显著,具有创伤小、术后并发症发生率低、疼痛程度轻等优势,可最大限度保留患者子宫,促进患者康复。
