低浓度失效含铑均相催化剂回收铑的工艺研究
2022-12-10张金池姜东解雪刘贵清张帆
张金池,姜东,解雪,刘贵清,张帆
(江苏北矿金属循环利用科技有限公司,江苏 徐州 221121)
铑具有高熔点、高硬度、卓越的催化活性和优异的化学稳定性,广泛应用于电镀、玻璃纤维、汽车尾气净化、化工催化和航天等领域[1-3]。然而,我国铑资源十分稀少,铑产量仅约为铂钯的5%,且价格昂贵,从含铑二次资源中循环利用和再生回收铑成为冶金和化工领域的重要课题。铑催化剂在催化氢化、羰基合成、氢甲酰化等[4]有机反应中起到关键催化作用,尤其在羰基合成乙酸和乙酸酐领域应用最为广泛。但在催化剂使用过程中,各种高沸点的有机副产物和原料中的杂质在反应系统中不断积累,加之反应体系中O、S、Cl 等元素与铑直接配位,导致催化剂失去活性。失活的废铑催化剂中铑含量较高,其成为重要的铑二次资源[5]。目前,失效均相铑催化剂富集回收铑的方法有焚烧法、熔炼法、消解法、萃取法和吸附法等[6-9],但存在环境污染、回收率低、设备要求高等问题。因此,本文针对乙酸酐生产中使用的失效铑催化剂,提出氧化络合-硫化沉淀工艺,实现铑的高效富集回收,该工艺具有良好的工业应用前景。
1 试验方法
试验所用含铑废催化剂由国内某企业提供,为深棕色黏稠液体,有强烈的刺激臭味,铑含量为110 g/t,密度为1.16 g/cm3。首先将废催化剂在水浴条件下用HCl+H2O2氧化一段时间,然后加入HCOOH+C2H2O4混合溶液,保温反应一段时间,反应结束后真空抽滤进行固液分离,络合沉淀渣用王水溶解,溶液定容后通过电感耦合等离子光谱发生仪(ICP)检测铑含量,考察了H2O2加入量、HCOOH+C2H2O4加入量(HCOOH与C2H2O4体积比为1 ∶1)、反应温度和时间对铑回收率的影响。向络合沉淀后液中添加一定量Na2S,硫化沉淀用王水溶解后定容,采用ICP 检测铑含量,考察了溶液初始pH、Na2S 用量、反应温度和时间对铑沉淀率的影响。试验所用氧化络合-硫化沉淀工艺流程如图1 所示。

图1 氧化络合-硫化沉淀工艺流程
试验所用设备包括数显恒温水浴锅、数显强力搅拌器、循环水式多用真空泵、电热恒温真空干燥箱和电子天平。
2 结果与讨论
2.1 氧化络合回收铑试验
氧化络合回收铑试验考察了不同因素对铑回收率的影响。一是H2O2用量,二是HCOOH+C2H2O4用量,三是反应温度,四是络合沉淀时间。
2.1.1 H2O2用量对铑回收率的影响
控制反应温度80 ℃、HCOOH+C2H2O4混合液用量40 mL、氧化反应时间60 min、沉淀时间120 min,考察H2O2用量对铑回收率的影响,结果如图2 所示。
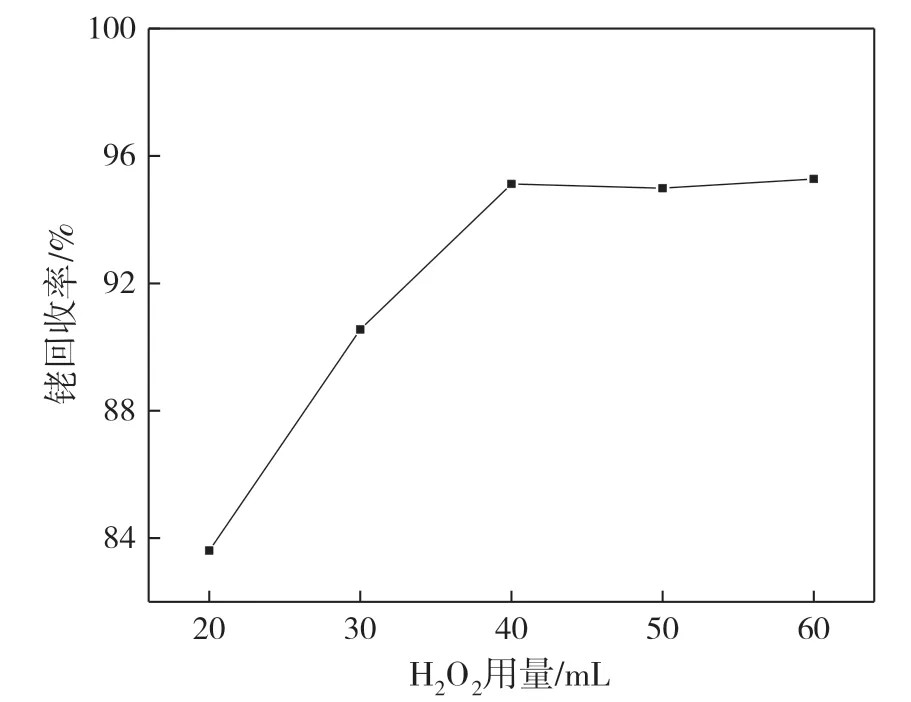
图2 H2O2 用量对铑回收率的影响
由图2 可知,随着H2O2用量的增加,铑回收率逐渐上升。当H2O2用量由20 mL 增加至40 mL时,铑回收率由83.61%增加到95.12%。随着氧化剂用量的增加,失效催化剂中“搭桥”后形成的铑簇团配合物被分散,铑膦配合物被分解,抑制剂被逐渐破坏,使得铑回收率不断增加。当H2O2用量大于40 mL时,铑回收率基本保持不变,氧化剂量达到一定程度后,铑簇团离子和抑制剂大部分已被氧化破坏,故铑回收率不再显著变化。因此,H2O2用量选择40 mL。
2.1.2 HCOOH+C2H2O4用量对铑回收率的影响
控制反应温度80 ℃、H2O2用量40 mL、氧化反应时间60 min、沉淀时间120 min,考察HCOOH+C2H2O4混合液用量对铑回收率的影响,结果如图3 所示。

图3 HCOOH+C2H2O4 用量对铑回收率的影响
由图3 可得,铑回收率随着HCOOH+C2H2O4混合液用量的增加而逐渐上升。当HCOOH+C2H2O4用量由20 mL 增加至40 mL时,铑回收率由86.77%增加到95.12%,主要原因是失效催化剂中铑膦配合物能和HCOOH+C2H2O4形成络合物沉淀。当HCOOH+C2H2O4混合液用量大于40 mL时,铑回收率稳定在95%。所以,HCOOH+C2H2O4混合液用量选取40 mL。
2.1.3 反应温度对铑回收率的影响
控制HCOOH+C2H2O4混合液用量40 mL、H2O2用量40 mL、氧化反应时间60 min、沉淀时间120 min,考察反应温度对铑回收率的影响,结果如图4 所示。
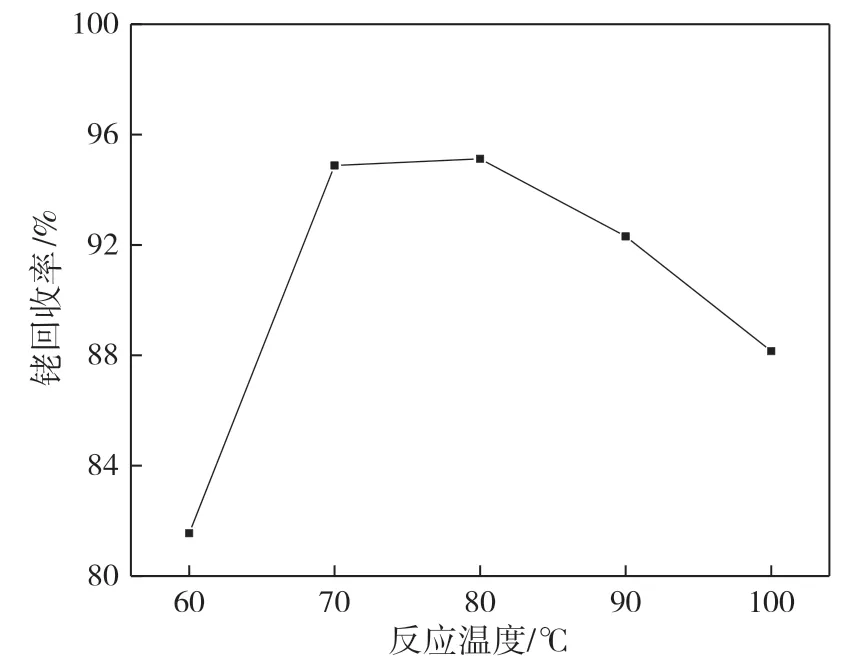
图4 反应温度对铑回收率的影响
由图4 可知,随着反应温度的升高,铑回收率先增加后降低。当反应温度由60 ℃升高至70 ℃时,铑回收率由81.55%增加到94.88%;继续升高温度至100 ℃,铑回收率由94.88%降低至88.15%,原因是反应温度的升高造成HCOOH 挥发量增加,不利于铑的回收。虽然80 ℃温度下,铑回收率达95.12%,但反应温度的升高会增加试剂消耗和能耗。因此,最佳反应温度为70 ℃。
2.1.4 络合沉淀时间对铑回收率的影响
控制反应温度80 ℃、H2O2用量40 mL、HCOOH+C2H2O4混合液用量40 mL、氧化反应时间60 min,考察络合沉淀时间对铑回收率的影响,结果如图5 所示。
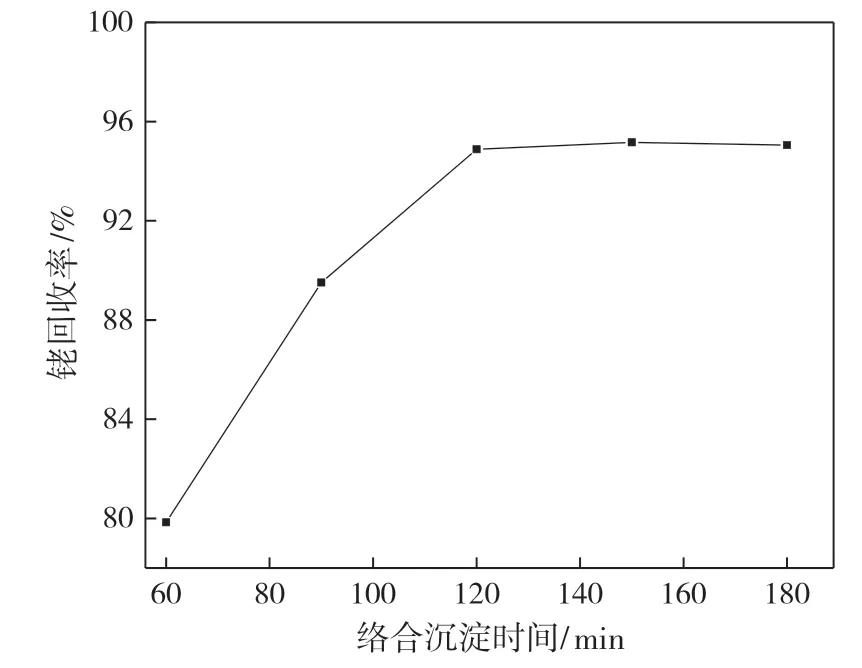
图5 络合沉淀时间对铑回收率的影响
由图5 可得,铑回收率随着反应时间的延长而逐渐增加。当反应时间由60 min 延长到120 min时,铑回收率由79.84%增加到94.88%;继续延长反应时间至180 min,铑回收率仅由94.88%增加到95.05%,铑回收率基本不变,说明络合沉淀反应基本达到平衡。因此,120 min 为最佳络合沉淀时间。
综上,失效均相铑催化剂氧化络合沉淀试验的最佳工艺参数为:H2O2用量40 mL,HCOOH+C2H2O4用量40 mL,反应温度70 ℃,络合沉淀时间120 min。该条件下,铑回收率达94.88%。
2.2 络合沉淀后液硫化沉淀富集铑试验
络合沉淀后液硫化沉淀富集铑试验研究了不同因素对铑沉淀率的影响。一是溶液初始pH,二是反应温度,三是Na2S 用量,四是反应时间。
2.2.1 溶液初始pH 对铑沉淀率的影响
控制反应温度70 ℃、Na2S 用量10 g、反应时间120 min,考察络合沉淀后液初始pH 对铑沉淀率的影响,结果如图6 所示。

图6 溶液初始pH 对铑沉淀率的影响
由图6 可知,随着溶液初始pH 的增加,铑沉淀率先增加后缓慢降低。当溶液初始pH 由0.3 增大至1时,铑沉淀率由44.72%增加到68.48%,这是由于溶液酸度过高时,Na2S 与H+反应生成H2S 气体逸出,使得溶液中S2-浓度降低,既污染环境,又不利于铑的沉淀。溶液初始pH 由1 继续增大至8时,铑沉淀率由68.48%缓慢降低至65.38%,原因是溶液中OH-浓度过高时,H3RhS3、Rh(HS)3会和OH-结合而反溶,导致铑沉淀率降低。因此,络合沉淀后液的初始pH选择1 为宜。
2.2.2 反应温度对铑沉淀率的影响
调节络合沉淀后液初始pH 为1,控制Na2S 用量10 g、反应时间120 min,考察反应温度对铑沉淀率的影响,结果如图7 所示。

图7 反应温度对铑沉淀率的影响
由图7 可得,随着反应温度的增加,铑沉淀率先增加后降低。当反应温度由50 ℃升高至70 ℃时,铑沉淀率由44.15%增加到68.48%,这是由于温度升高,使活化分子数目增多,加快了沉淀反应速率,有利于沉淀反应向正方向进行。当反应温度继续升高至90 ℃,铑沉淀率由68.48%降低至59.84%,原因是反应温度升高造成沉淀产物H3RhS3、Rh(HS)3溶解度增加,不利于铑的沉淀。因此,最佳反应温度为70 ℃。
2.2.3 Na2S 用量对铑沉淀率的影响
调节络合沉淀后液初始pH 为1,控制反应温度70 ℃、反应时间120 min,考察Na2S 用量对铑沉淀率的影响,结果如图8 所示。
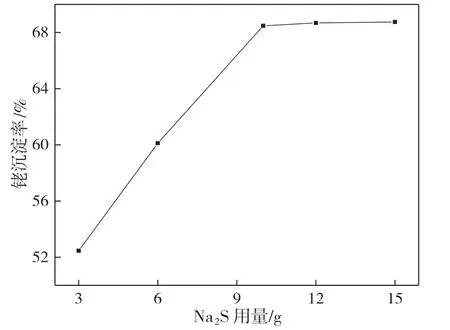
图8 Na2S 用量对铑沉淀率的影响
由图8 可知,铑沉淀率随着Na2S 用量的增加而上升。当Na2S 用量由3 g 增加至10 g时,铑沉淀率由52.46%增加到68.48%。随着Na2S 用量由10 g进一步增加至15 g,铑沉淀率由68.48%缓慢增加至68.75%,铑沉淀率基本保持不变,说明沉淀反应已达到动态平衡。因此,Na2S 用量选择10 g 较为适宜。
2.2.4 反应时间对铑沉淀率的影响
调节络合沉淀后液初始pH 为1,控制Na2S 用量10 g、反应温度70 ℃,考察反应时间对铑沉淀率的影响,结果如图9 所示。
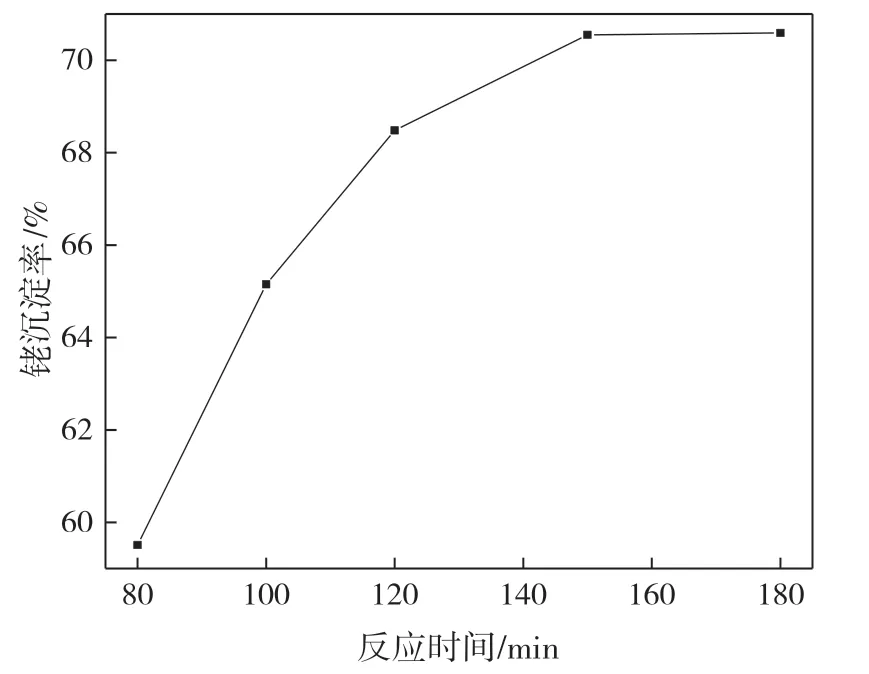
图9 反应时间对铑沉淀率的影响
由图9 可知,铑沉淀率随反应时间延长而不断增加。当反应时间由80 min 延长至150 min时,铑沉淀率由59.51%增加到70.55%。随着反应时间继续延长至180 min,铑沉淀率仅由70.55%增加至70.59%,铑沉淀率几乎不变,说明沉淀反应几乎达到最大限度。因此,最佳反应时间为150 min。
综上,失效均相铑催化剂络合沉淀后液硫化沉淀富集铑的优化参数为:溶液初始pH=1,反应温度70 ℃,Na2S 用量10 g,反应时间150 min。优化条件下,铑沉淀率达70.55%。经两步工艺处理,铑的综合回收率高达96.39%。
3 结论
本文提出了一种低浓度失效含铑均相催化剂的绿色铑回收工艺,通过氧化络合-硫化沉淀工序,实现铑的高效富集回收。失效均相铑催化剂氧化络合试验的最佳工艺参数为:H2O2用量40 mL,HCOOH+C2H2O4用量40 mL,反应温度70 ℃,络合沉淀时间120 min。最佳条件下,铑回收率达94.88%。失效均相铑催化剂络合沉淀后液硫化沉淀富集铑的优化参数为:溶液初始pH=1,反应温度70 ℃,Na2S 用量10 g,反应时间150 min。优化条件下,铑沉淀率达70.55%。经两步工艺处理,铑的综合回收率高达96.39%。
