不锈钢表面超疏水Ni/TiO2复合镀层的制备及力学性能研究
2022-12-07胡传波尹华伟
姚 鑫,胡传波,尹华伟,崔 政,吕 丹
(1. 重庆三峡学院环境与化学工程学院 三峡库区水环境演变与污染防治重庆市重点实验室,重庆 404000;2. 西华大学能源与动力工程学院,四川 成都 610039;3. 香港浸会大学理学院化学系,香港 999077;4. 材料腐蚀与防护四川省重点实验室,四川 自贡 643000)
0 前 言
不锈钢由于具有优良的力学性能被大量用于日常生活和生产制造中。然而,由于不锈钢的表面能高、吸附能力强等原因,在大气环境下受潮湿空气和腐蚀性污染物的影响,容易引起其耐腐蚀性能下降,从而导致产品性能退化,甚至缩减产品使用寿命,最终造成经济损失。因而,采取相应措施对不锈钢表面进行保护是十分必要的。
近年来,超疏水表面因具有优良的自清洁[1]、防腐[2]以及减阻减摩[3]等性能而引起了广泛关注。特别是在金属防护领域,在基体上构建超疏水表面也逐渐成为提高金属耐腐蚀性的一种重要手段[4]。超疏水技术实际上来源于自然界中的超疏水现象,诸如荷叶上自由滚动的水珠、在水面上行走的水黾等。有研究[5]发现,荷叶表面的超疏水性是由于其表面微纳米结构乳突的存在和生物蜡质所共同引起的;水黾能在水面上行走则是由于空气可以吸附在其腿部上特殊的微纳米结构缝隙中,并在表面形成一层稳定的气膜,阻碍了水滴的浸润[6]。受此启发,研究人员通常在疏水表面构建粗糙结构或者使用低表面能物质修饰粗糙表面,来获取超疏水性能,以实现水滴与基材高效分离,从而降低基材的腐蚀风险。目前为止,已开发例如激光刻蚀法[7]、溶胶 - 凝胶法[8]以及电化学沉积法[9]等多种制备超疏水表面的技术。
在金属表面通常采用化学刻蚀法、喷涂法等制备超疏水表面。一般来说,化学刻蚀法虽然操作步骤少、制备时间短,但存在对微观形貌控制不精确、粗糙程度不均匀等缺点;喷涂法不受基体材料尺寸、形状等因素限制,但涂层与基体结合力差、表面耐久性低。相比而言,电化学沉积法对设备要求不高,原理简单、易操作,具有表面形貌与粗糙度可控等优点。然而,有关电沉积技术在不锈钢基体上构建超疏水表面的报道较少,研究尚不充分。Liang等[10]采用电沉积技术并通过改变电流密度来调控镀层形貌,发现当电流密度为7 A/dm2时,可在不锈钢上获得片状镍薄膜,经氟化改性后其接触角高达166°。蒋斌等[11]采用两步电沉积技术在不锈钢基体上构建超疏水表面,初次沉积时获得金字塔尖锥体结构,二次沉积后便出现花瓣状微纳结构,此时不锈钢表面则表现出超疏水性能,接触角为153.74°;进一步研究表明,该结构可降低海水点蚀的风险。为了实现某些特定功能,一些纳米颗粒通常也被添加到镀层结构中。例如SiO2纳米微粒能增强超疏水表面的耐磨、耐蚀与耐温性能[12];Al2O3的添加可提高镀层表面硬度,使其有效抵抗机械变形[13]。Huang等[14]采用电沉积技术将Ni与TiO2共同沉积在316L不锈钢表面,经改性后获得接触角为174.9°的超疏水表面,证实纳米颗粒TiO2的加入能提高镀层的表面粗糙度。然而,文献[14]并未对TiO2添加前后镀层的性能进行比对分析,尤其是缺乏机械稳定性方面的分析。考虑到不锈钢的实际使用情况,需加强不锈钢超疏水复合镀层在机械稳定性方面的研究。
本工作采用电沉积技术结合氟化改性技术在不锈钢表面制备超疏水Ni/TiO2复合镀层。通过考察电流密度对Ni镀层表面形貌的影响,确定了最佳电流密度。在此基础上,采用Ni与TiO2共沉积的方式制得Ni/TiO2复合镀层。经氟化改性后,获得超疏水复合镀层。相关测试对比结果表明,该超疏水复合镀层具有较高的接触角、稳定的力学性能、较好的耐蚀性以及良好的自清洁性,能有效增强基体的防污耐蚀能力。
1 实 验
1.1 实验材料
实验试剂主要包括磷酸钠(Na3PO4· 12H2O,98%,质量分数,下同)、氢氧化钠(NaOH,96%)、硼酸(H3BO3,99.5%)、无水乙醇(CH3CH2OH,99.7%)、无水碳酸钠(Na2CO3,99.8%)、氯化钾(KCl,99%)、六水氯化镍(NiCl2· 6H2O,98.5%)、十二烷基苯磺酸钠(C18H29NaO3S,SDBS,90%)、盐酸(HCl,36~38%)、1H,1H,2H,2H - 全氟癸基三甲氧基硅烷(FAS)、纳米二氧化钛(TiO2,锐钛矿型40 nm),所有化学药品均为分析纯。整个实验过程中均使用去离子超纯水(电导率为18.2 MΩ·cm)。
1.2 Ni镀层的制备
电镀前,需将不锈钢片(20 mm×20 mm×1 mm)依次用不同目数的金相砂纸打磨至表面光亮无明显划痕。然后,将其放入80 ℃碱溶液(pH = 9)中静置约10 min,便于清除油渍。碱溶液主要由NaOH(25 g/L)、Na2CO3(35 g/L)与Na3PO4·12H2O(35 g/L)组成。随后将不锈钢片浸没于HCl溶液[125 mL/L,pH=(1.5±0.1)]中约2 min以去除氧化膜,再放置于HCl溶液[30 mL/L,pH=(1.5±0.1)]中活化约30 s。每一步操作后均需用去离子水冲洗,之后吹干备用。
电镀采用两电极体系,以镍片为阳极,不锈钢片为阴极,且两极间距为3 cm,阴阳两极面积比为1∶2。电镀液为200 g/L NiCl2· 6H2O溶液(50 ℃),并使用130 g/L H3BO3溶液将镀液pH值调至4.5。同时,添加30.0 g/L KCl和0.1 g/L SDBS分别作为阳极活化剂与表面活性剂。电镀过程中考察了电镀时间为10 min时不同电流密度(J=3,5,7,9,11 A/dm2)对Ni镀层形貌与结构的影响,以确定最佳电流密度,获得表面形貌最优的Ni镀层。待电镀后,用去离子水冲洗镀层2 min并风干。
1.3 Ni/TiO2复合镀层的制备
复合电镀液由200 g/L NiCl2· 6H2O、30 g/L KCl、6 g/L TiO2以及0.6 g/L SDBS组成。为使纳米TiO2颗粒在镀液中均匀分散,电镀前需在室温下对加入纳米TiO2颗粒的镀液体系磁力搅拌6 h,搅拌速度为350 r/min。电镀采用上述确定的最佳电流密度,电镀间距、阴阳极面积比以及温度与电镀镍保持一致。根据复合镀层沉积理论,在磁力搅拌下,纳米TiO2在镀液中形成均匀且稳定的悬浮分散系,同时吸附Ni2+、H+而带正电,并在静电引力与机械碰撞下被吸附到阴极表面,与Ni2+共同沉积,形成Ni/TiO2复合镀层。此时,H+也因吸附电子生成氢气。电镀后,仍需对样品进行冲洗并风干。
1.4 镀层改性
将1 g FAS加入到20 mL乙醇中,充分磁力搅拌后得到改性液。将所得电镀样品首先浸泡在改性液中室温改性10 min,之后自然干燥10 min,随后放入100 ℃烘箱中烘干20 min取出,即可得到FAS改性样品。相同条件下,对裸不锈钢片也进行改性处理以便对比分析。为便于叙述,用CS表示裸不锈钢,SCS表示改性不锈钢,Ni表示镍镀层,SNi表示改性镍镀层,NT表示Ni/TiO2复合镀层,SNT 表示改性Ni/TiO2复合镀层。图1展示了在不锈钢基体上制备超疏水Ni/TiO2复合镀层的原理图。改性期间,FAS分子所含的硅氧烷基团(Si-OCH3)在溶液中水解为Si-OH,这些Si-OH可以与金属镀层或TiO2表面的-OH发生脱水缩合形成Si-O-R键(R指Ni或TiO2)从而完成改性。
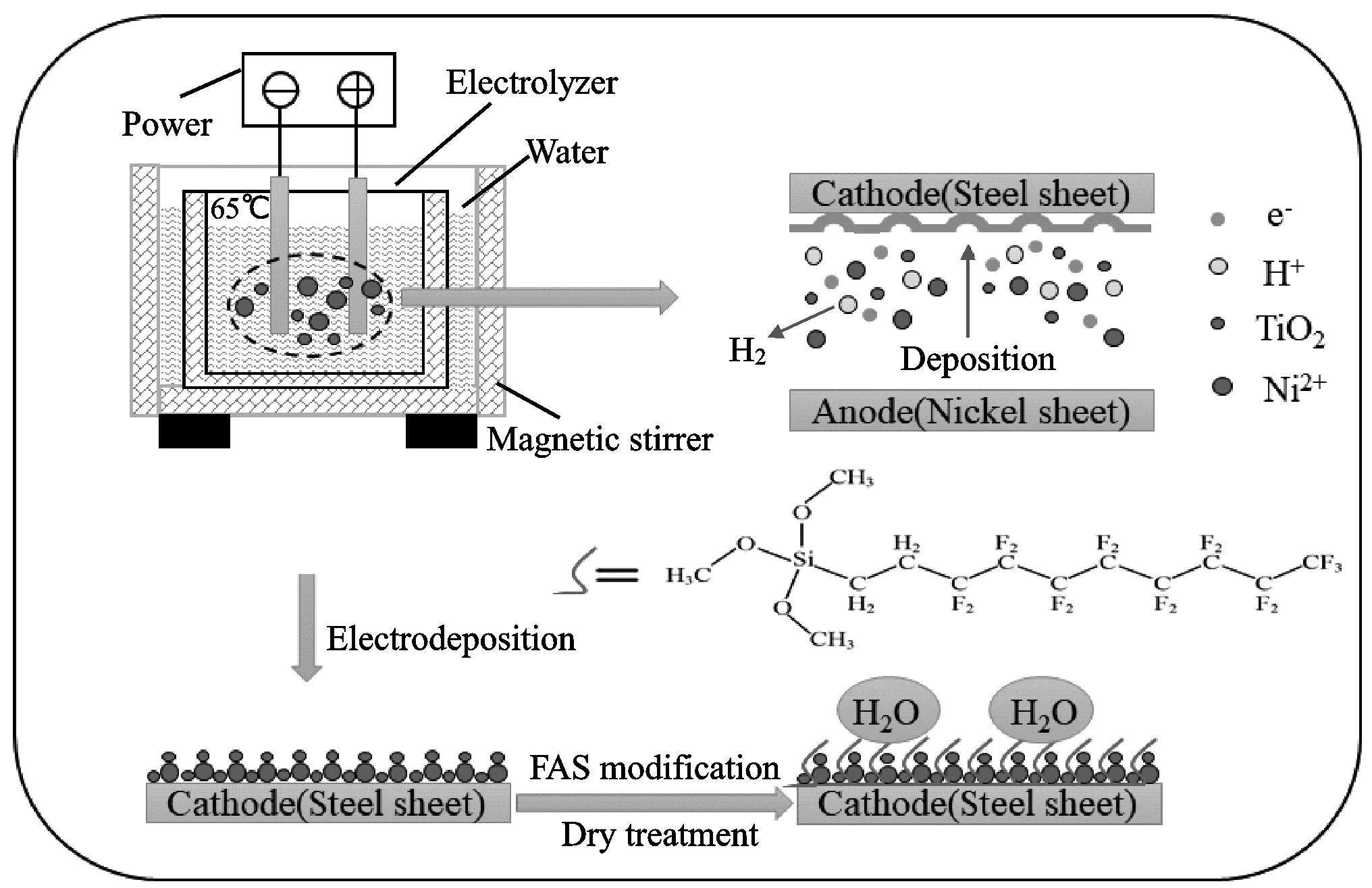
图1 超疏水Ni/TiO2复合镀层电沉积原理图
1.5 性能表征
采用Ultra Plus型场发射扫描电子显微镜(FESEM)观察样品表面形貌,并用配套能谱仪(EDS)进行元素微区分析。使用Ultima Ⅳ型X射线衍射仪(XRD)对镀层进行物相分析,XRD功率为3 kW,2θ范围为10°~80°,扫描速率4 (°)/min。采用Dataphysics - OCA20型接触角测量仪,室温下使用体积为3 μL的去离子水测量样品(样品测试面尺寸为20 mm×20 mm)上5个不同的点的静态接触角(CA)与滚动角(SA),其值取5次测量的平均值。为测试改性样品表面的稳定性,进行了胶带剥离实验和磨损实验。胶带剥离实验的过程如下:首先将样品平整放置于实验台,使用透明胶带将其固定并压实,然后迅速撕下胶带,这样反复操作10次,完成剥离实验。磨损实验过程如下:将待测样品疏水面朝下放置于1 000目金相砂纸上,并在其上放置重量为100 g的砝码,以2 cm/s的速度推动样品沿直线移动10 cm,以评价样品的耐磨性能。使用CHI660E型电化学工作站对样品的Tafel极化曲线进行分析,测试电压范围为-0.25 V ~ 0.05 V,扫描速率为10 mV/s,测试在室温下进行。测试过程采用三电极体系,其中待测样品为工作电极,铂电极为对电极,饱和甘汞电极(SCE)为参比电极。实验前将样品浸泡在3.5% NaCl溶液中静置30 min,使开路电位达到稳定。
2 结果与讨论
2.1 电流密度对Ni镀层表面形貌的影响
图2为不同电流密度下Ni镀层FESEM形貌及J=9 A/dm2时Ni镀层的EDS谱,其中图2a~2e中的插入图为对应电流密度下形貌的放大图。可以发现,随着电流密度逐步增大,镀层表面形貌结构也发生动态变化。

图2 不同电流密度下Ni镀层FESEM形貌及J=9 A/dm2时Ni镀层的EDS谱
当电流密度为3 A/dm2时,镀层表面可见均匀分布的不规则锥形颗粒,其单个尺寸约为200 nm。当电流密度升至5 A/dm2时,部分锥形颗粒生长明显,其单个尺寸约为400 nm。这主要是因为低电流密度下阴极极化的影响较小,颗粒的生长速度大于沉积速度,因而颗粒表现出长大的趋势[15]。当电流密度为7 A/dm2时,镀层表面的Ni颗粒明显增多但尺寸有所降低,其外观呈针状结构,这是阴极极化作用加强的结果。当电流密度增至9 A/dm2时,镀层表面形貌发生显著变化,镀层表面有片状沉积物层叠堆积,并呈现出花瓣状结构,这是扩散过电位与析氢反应共同作用造成的[16]。其中,瓣状结构的厚度约在20 nm左右,表明在电流密度为9 A/dm2时能够获得粗糙的微纳米级结构。当电流密度达到11 A/dm2时,镀层结构类似于电流度为9 A/dm2时的, 也呈现出花瓣状结构。然而, 由于电流密度的过度增加,使得氢气在阴极大量析出,造成瓣状结构表面出现圈状纹路,同时也引起整个镀层产生鼓泡、脱皮等现象,难以获得高质量的镀层结构。J=9 A/dm2时Ni镀层的EDS谱如图2f所示。可以看出,所得镀层中只有Ni元素存在,且含量达到100%,说明Ni镀层已经均匀地沉积在不锈钢基体表面。结合以上分析,认为电流密度为9 A/dm2时可获得具有稳定粗糙结构的纯Ni镀层。
2.2 复合镀层表面结构与成分分析
图3为NT复合镀层的FESEM形貌、XRD谱以及EDS谱。图3a为最佳电流密度下(9 A/dm2)电沉积10 min所得NT复合镀层表面形貌。观察发现,镀层表面分散分布着TiO2颗粒,部分区域甚至有纳米颗粒的堆积。相比Ni镀层,NT复合镀层的花瓣状结构更加明显,并与团聚在周围的TiO2纳米颗粒构成了更加粗糙的微纳米结构。可见,TiO2的加入不仅影响了Ni的成核,而且增加了镀层的表面粗糙度。图3b为复合镀层的XRD谱。显然,经过电沉积后,复合镀层表面有结晶态的镍存在,其特征衍射峰对应于(111)、(200)和(220)晶面,衍射角分别对应44.8°、53.2°以及78.2°[17]。然而,在复合镀层的XRD谱中并未出现TiO2特征峰,这应该是因为TiO2含量较低,未达到引起衍射反应的含量。为验证TiO2的存在,对样品进行了EDS化学成分检测,结果如图3c所示。可以看出,复合镀层中除Ni元素以外,还检测到O、Ti元素的存在,但含量很少,表明TiO2纳米颗粒的确已经共同沉积到镀层表面。

图3 NT复合镀层的FESEM形貌、XRD谱以及EDS谱
2.3 改性镀层表面形貌与成分分析
图4为不同样品的表面形貌与部分改性镀层的EDS谱,图4a~4d中的插入图是对应样品的放大图。由图4a可见,CS样品表面较平整、光滑,仅可观察到细微打磨划痕。由图4b可知,经FAS改性后,可以观察到SCS样品表面形貌无明显变化,但由于改性液的渗透,干燥之后划痕中留下了可见的溶剂蒸发痕迹。与图2d相比,图4c中SNi镀层经改性液修饰后,其表面形貌并未发生明显变化,仍然保持着粗糙的花瓣状结构。图4d显示SNT镀层表面形貌为团簇状的花瓣结构,与图3a相比并无显著区别。观察到在团簇结构间隙之间填充了数量较多的纳米球,这与前述分析结果一致。这种结构的形成更利于捕获空气,从而提高镀层的超疏水性能。为了确定FAS已经成功组装在镀层表面,对改性后的镀层进行了EDS分析,结果见图4e、4f。结果表明,SNi镀层与SNT复合镀层中除了Ni元素外均包含C、F、O、Si 4种元素,显然这些元素来自于FAS。
2.4 润湿性能分析
图5为不同样品水接触角与滚动角。测试发现水滴在CS表面逐渐汇集,表现为明显的亲水性;经FAS改性后,水滴呈微凸状铺于SCS样品表面,说明基体表面经低表面能材料FAS改性后能够表现出一定的疏水性能;水滴在SNi镀层表面呈球状,与CS表面相比,其接触角增加,滚动角降低,达到超疏水状态。这主要是由于粗糙微纳米结构的建立可捕获大量空气,使水滴与镀层表面的接触状态由固 - 液转变为固 - 气 - 液,减少了液滴与镀层之间的接触面积,并在FAS协同作用下,获得超疏水表面;水滴以球状立于SNT复合镀层表面,在受到微小的扰动时,水滴便会从表面滚落。经测量,在CS、SCS、SNi、SNT 4种样品中,SNT复合镀层的接触角最高,滚动角最低,超疏水性能佳。研究表明,材料的表面形貌以及粗糙度对其润湿性起着非常重要的作用[18]。由此可得出,TiO2纳米颗粒的加入更利于粗糙微纳米结构的建立,可以使SNT复合镀层的超疏水性能得到进一步提高。
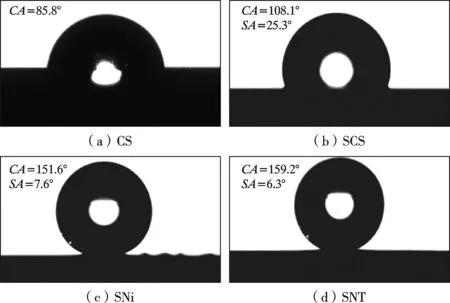
图5 不同样品表面的水接触角与滚动角
2.5 机械性能分析
机械稳定性在超疏水表面实际应用中起到重要作用。图6为胶带剥离后不同改性样品表面的水接触角。在剥离实验中,胶带从各样品表面剥离后,SCS表面水滴的微凸状已基本消失,疏水性能降低,其接触角下降。这说明FAS与不锈钢基体之间的黏附力较弱,很容易将其剥离;对于SNi镀层,虽然有部分镀层脱落,但水滴仍以球形立于表面,其镀层表面接触角下降,但尚能基本维持超疏水性能;SNT复合镀层几乎未受胶带剥离的影响,其表面结构仍然完整,接触角依旧高达158.5°,具备较佳的耐胶带剥离能力。究其原因,这是由于TiO2颗粒的加入可以使镀层形成稳固的微纳米粗糙结构,从而提高镀层的机械稳定性,有效保证了复合镀层表面的超疏水性能。

图6 胶带剥离实验后不同改性样品表面的水接触角
图7为磨损实验后不同改性样品表面的水接触角。各样品经磨损实验后,可见SCS样品表面移动区间内有白色痕迹,这是样品表面FAS膜在机械力作用下摩擦脱落所致;SNi镀层经磨损实验后,砂纸表面残留有少量的颗粒,同时镀层表面也有明显划痕存在,其接触角减小到149.1°,丧失了超疏水性能;类似的现象也发生在SNT复合镀层表面,经过磨损实验后,虽然其接触角也有所降低,却仍能保持超疏水性能。这主要归因于FAS分子与粗糙Ni/TiO2镀层之间较高的结合强度,可以显著提高镀层的耐磨性。

图7 磨损实验后不同改性样品表面的水接触角
2.6 耐蚀性能分析
材料的耐腐蚀性是其实现工业应用的一个极为重要的指标。本工作利用Tafel极化曲线评价所获样品的耐蚀性,不同样品在3.5%NaCl溶液中的Tafel极化曲线如图8所示。同时,采用曲线外推法计算出各样品的自腐蚀电位(Ecorr)和自腐蚀电流密度(Jcorr),结果如表1。表1中,缓蚀效率计算公式如下[19]:

表1 不同样品的Tafel极化曲线拟合结果
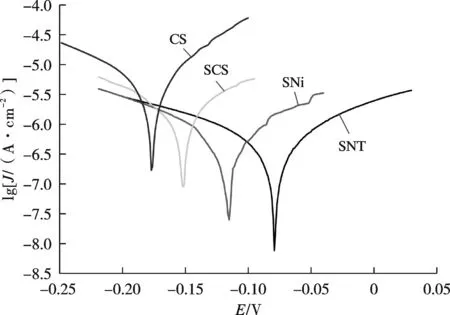
图8 不同样品在3.5%NaCl溶液中的Tafel极化曲线
η=(Jcorr, bare-Jcorr, coated/Jcorr, bare×100%
(1)
式中:η为缓蚀效率,Jcorr,bare为不锈钢(CS)的自腐蚀电流密度,Jcorr,coated分别为SCS、SNi和SNT的自腐蚀电流密度。
结合图8与表1可知,经FAS改性后,CS样品的Ecorr发生明显正移,同时Jcorr下降。对于SNi与SNT样品,其Ecorr均发生了正移(SNi的Ecorr正移62 mV,SNT的Ecorr正移99 mV),Jcorr均发生了下降。一般来说,自腐蚀电流密度越小,其耐腐蚀性能越好[20]。SNi与SNT的腐蚀电流密度与CS样品相比分别低1~2个数量级,缓蚀效率也分别达到93.6%和98.4%,表明SNi和SNT能起到优异的耐腐蚀作用。特别对于SNT复合镀层,由于TiO2与Ni2+共沉积可获得更为粗糙的微纳米结构,有利于截留气体,使腐蚀性溶液难以达到材料表面,故其耐腐蚀性能最佳。
2.7 自清洁性能分析
图9展示了各改性样品表面灰尘自清洁过程。采用粉笔灰模拟灰尘污染。由图9a可见,当液滴开始滴落在SCS表面时,几乎没有滑落,遇到了较大阻力;随着液滴不断滴落,受到重力的作用,液滴开始缓慢滑落。然而,由于SCS表面的自清洁性能较差,仍有部分灰尘黏附在其表面,未被彻底清除。对于SNi和SNT而言,如图9b与9c所示,滴落在超疏水表面的水滴会立即滚落,且能够完全带走镀层表面上的灰尘,从而对滚落路径实现清洁。可见,具备粗糙结构与低表面能物质的镀层,才使得灰尘与镀层表面之间的附着力显著减小,并在滚落水滴的作用下使灰尘极易从超疏水表面滚落,展现出优异的自清洁性能。

图9 不同样品表面灰尘自清洁过程
3 结 论
本工作采用电沉积和氟化改性相结合的方法在不锈钢表面成功制备了超疏水Ni/TiO2复合镀层。考察了电流密度对Ni镀层表面形貌的影响,并在电流密度为9 A/dm2时,获得粗糙纳米花瓣状结构的Ni镀层。在最佳电流密度(J=9 A/dm2)条件下,采用TiO2与Ni2+共沉积的方法,制取具有微纳米结构的Ni/TiO2复合镀层,经FAS改性后,便可获得超疏水Ni/TiO2复合镀层,其接触角高达159.2°。究其原因,这应该是微纳米粗糙结构的构建与低表面能物质的协同作用。经过10次胶带剥离实验,超疏水Ni/TiO2复合镀层表面结构仍然完整。磨损实验表明该表面可以抵抗一定的摩擦损伤,经过磨损后仍能保持超疏水性能,体现了良好的机械稳定性。相比不锈钢,超疏水Ni/TiO2复合镀层的自腐蚀电位正移了99 mV,电流密度降低了2个数量级,具有更好的耐腐蚀性。同时,自清洁实验也证实,超疏水Ni/TiO2复合镀层具有良好的自清洁性能。因此,超疏水Ni/TiO2复合镀层能显著提高不锈钢材料的性能,可推广到实际领域应用。
