生乳汤回流提取工艺优化
2022-12-05李兰兰虎亚光贾新烨谭建伟
李兰兰, 虎亚光, 贾新烨, 张 睿, 谭建伟
(甘肃省妇幼保健院药学部,甘肃 兰州 730050)
母乳喂养对母婴健康都有重要意义,我国《中国儿童发展纲要(2011—2020年)》和《国民营养计划(2017—2030)》[1-2]都明确提出,到2020年0~6个月婴儿纯母乳喂养率达到50%以上目标。但《中国母乳喂养影响因素调查报告(2019年)》显示,我国6个月内婴儿纯母乳喂养率仅为29.2%,远低于43%的世界平均水平[3]。
泌乳量不足是导致纯母乳喂养失败的主要原因之一[4],发病率约为20%~30%[5-6]。中医认为,气血郁闭和气血亏虚是产后缺乳的主要病因病机[5,7]。生乳汤以传统验方为基础,根据中医对产后缺乳的主要分型、治疗产后缺乳的基本用药配伍规律组方,由当归、川芎、芍药等药材组成,在临床应用中呈现出较好的催乳效果。本实验采用Box-Behnken响应面法优化生乳汤回流提取工艺,以期为该方进一步开发提供依据。
1 材料
1.1 仪器 UltiMate 3000高效液相色谱仪[赛默飞世尔科技(中国)有限公司];SQP型电子分析天平[十万分之一,赛多利斯科学仪器(北京)有限公司];TWCL-T型调温磁力搅拌器(海科雳仪器设备有限公司)。
1.2 试剂与药物 当归(甘肃和润医药集团有限公司,批号201101A);川芎(兰州安泰堂中药饮片有限公司,批号20072101);炒白芍(甘肃康乐药业有限责任公司,批号200310);柴胡(甘肃和润医药集团有限公司,批号200903),经专家鉴定为正品。阿魏酸(批号D1804017,纯度≥99.5%)、芍药苷(批号D1728076,纯度≥98%)对照品均购于阿拉丁试剂(上海)有限公司。乙腈为色谱纯(德国Merck公司);其余试剂均为分析纯。
2 方法与结果
2.1 阿魏酸、芍药苷含量测定
2.1.1 色谱条件 Accucore aQ C18色谱柱(150 mm×4.6 mm,2.6 μm);流动相乙腈-0.05 mol/L磷酸(16∶84);体积流量1.0 mL/min;柱温30 ℃;检测波长232 nm;进样量10 μL。
2.1.2 溶液制备
2.1.2.1 对照品溶液 精密称取阿魏酸、芍药苷对照品适量,甲醇溶解,即得(两者质量浓度分别为136.67、640 μg/mL)。
2.1.2.2 供试品溶液 按照处方比例称取药材,加10倍量80%乙醇浸泡30 min,回流提取1 h,提取液冷却至室温,取200 μL,水浴挥干,加1 mL甲醇溶解残渣,过0.22 μm微孔滤膜,取续滤液,即得。
2.1.2.3 阴性样品溶液 按处方量称取缺当归和川芎、缺炒白芍的药材,制成阴性样品,按“2.1.2.2”项下方法制备,即得。
2.1.3 专属性试验 取对照品、供试品、阴性样品溶液适量,在“2.1.1”项色谱条件下进样测定,结果见图1。由此可知,该方法专属性良好,阴性无干扰。
2.1.4 线性关系考察 取“2.1.2”项下对照品溶液,稀释成阿魏酸(芍药苷)质量浓度分别为91.11(426.67)、45.55(213.33)、22.78(106.67)、12.42(58.18)、4.14(19.39)、1.77(8.31)μg/mL,在“2.1.1”项色谱条件下进样测定。以对照品质量浓度为横坐标(X),峰面积积分值为纵坐标(Y)进行回归,得阿魏酸、芍药苷方程分别为Y=0.511X+0.478(R2=0.999 3)、Y=0.220 3X+1.824 1(R2=0.999 0),分别在91.11~1.77、426.67~8.31 μg/mL范围内线性关系良好。
2.1.5 精密度试验 取“2.1.2”项下对照品溶液适量,在“2.1.1”项色谱条件下进样测定6次,测得阿魏酸、芍药苷峰面积RSD分别为0.36%、0.19%,表明仪器精密度良好。
2.1.6 重复性试验 取同一批提取液6份,按“2.1.2.2”项下方法制备供试品溶液,在“2.1.1”项色谱条件下进样测定,测得阿魏酸、芍药苷含量RSD分别为2.18%、3.78%,表明该方法重复性较好。
2.1.7 稳定性试验 取同一份供试品溶液,于0、2、4、8 h在“2.1.1”项色谱条件下进样测定,测得阿魏酸、芍药苷峰面积RSD分别为0.36%、0.87%,表明溶液在8 h内稳定性良好。
2.1.8 加样回收率试验 取同一份各成分含量已知的提取液6份(阿魏酸10.791 μg/mL、芍药苷169.83 μg/mL),分别加入80%、100%、120%水平对照品溶液,按“2.1.2.2”项下方法制备供试品溶液,在“2.1.1”项色谱条件下进样测定,计算回收率。结果,阿魏酸、芍药苷平均加样回收率分别为97.34%、98.01%,RSD分别4.07%、2.58%。
2.2 浸膏得率测定 在恒重器皿中加入提取液40 mL,置于95 ℃烘箱中烘干,移至干燥器中冷却至室温,立即称定质量,计算浸膏得率,公式为得率=[(提取液中浸膏量×提取液总体积)/(处方药材总量×40)]×100%。
2.3 单因素试验
2.3.1 料液比 按处方比例称取药材5份,80%乙醇分别按1∶6、1∶8、1∶10、1∶12、1∶14料液比回流提取60 min,按“2.1.2”项下方法制备供试品溶液,在“2.1.1”项色谱条件下进样测定。结果,料液比为1∶14时阿魏酸含量最高,故选择1∶12~1∶20作进一步优化。
2.3.2 乙醇体积分数 按处方比例称取药材5份,分别用50%、60%、70%、80%、90%乙醇按1∶10料液比回流提取60 min,按“2.1.2”项下方法制备供试品溶液,在“2.1.1”项色谱条件下进样测定。结果,乙醇体积分数为70%时阿魏酸含量最高,故选择50%~90%作进一步优化。
2.3.3 提取时间 按处方比例称取药材5份,80%乙醇按1∶10料液比分别回流提取30、60、90、120、150 min,按“2.1.2”项下方法制备供试品溶液,在“2.1.1”项色谱条件下进样测定。结果,提取时间为60 min时阿魏酸含量最高,故选择30~90 min作进一步优化。
2.3.4 提取次数 按处方比例称取药材3份,80%乙醇按1∶10料液比分别回流提取1、2、3次,每次60 min,按“2.1.2”项下方法制备供试品溶液,在“2.1.1”项色谱条件下进样测定。结果,提取次数为2次时阿魏酸含量最高,故选择2次,并不再进行优化。
2.4 Box-behnken响应面法 在单因素试验基础上,选择乙醇体积分数(A)、料液比(B)、提取时间(C)作为影响因素,固定提取次数为2次,阿魏酸(Y1)、芍药苷(Y2)含量及浸膏得率(Y3)作为评价指标,设计三因素三水平试验,因素水平见表1,结果见表2。

表1 因素水平
采用Design-Expert 11.0软件对表2数据进行多元二次回归拟合,得方程分别为Y1=-27.292 44+0.904 35A+1.102 62B+0.390 425C-0.008 356A2-0.043 734B2-0.002 014C2(R2=0.948 9,信噪比19.260 9)、Y2=-1 036.293 1+22.049 06A+41.845 94B+4.949 29C-0.168 875AB-0.145 266A2-0.932 422B2-0.021 415C2(R2=0.962 5,信噪比18.309 7)、Y3=-27.254 06+0.942 125A+1.905 31B+0.349C-0.008 997A2-0.046 797B2-0.001 979C2(R2=0.960 6,信噪比20.914 4),方差分析分别见表3~5,可知模型具有高度显著性,数据无异常点。

表2 试验设计与结果

表3 阿魏酸含量方差分析

表4 芍药苷含量方差分析
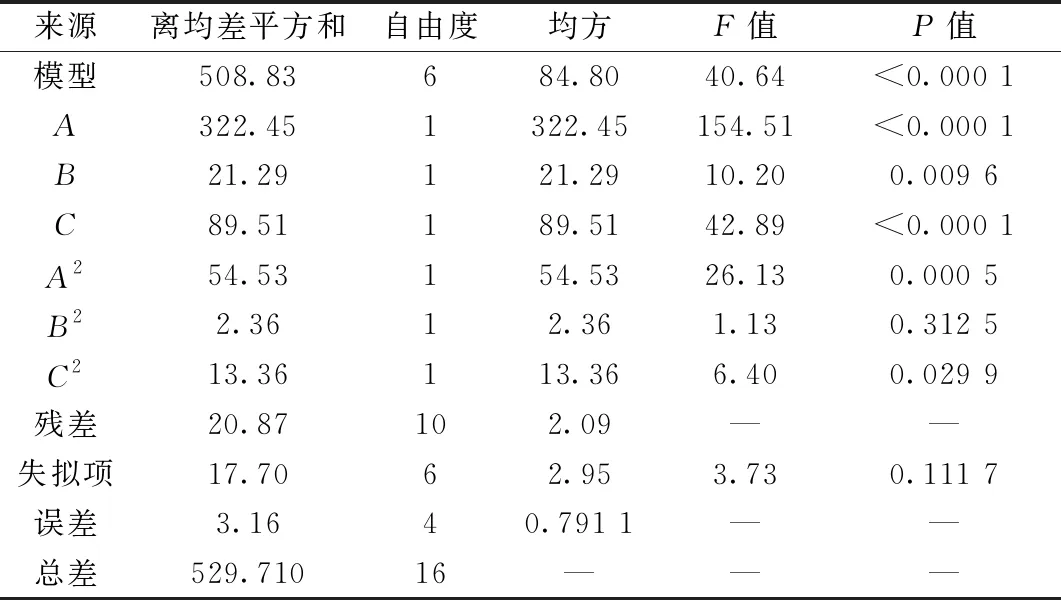
表5 浸膏得率方差分析
响应面分析见图2,可知固定提取时间时,阿魏酸含量随着乙醇体积分数、料液比增加逐渐降低,芍药苷含量随乙醇体积分数、料液比增加先升后降,浸膏得率随着乙醇体积分数、料液比增加逐渐降低。
2.5 验证试验 最优工艺为乙醇体积分数57.79%,料液比1∶14.248,提取次数2次,每次90 min,阿魏酸、芍药苷含量及浸膏得率分别为22.725 mg、292.64 mg、30.17%,考虑到实际操作可行性,将其修正为乙醇体积分数58%,料液比1∶14,提取次数2次,每次90 min。按照上述优化工艺进行3批验证试验,测得阿魏酸、芍药苷含量及浸膏得率分别为22.31 mg、291.69 mg、30.54%,RSD分别为1.89%,1.25%、1.13%,与预测值22.725 mg、292.64 mg、30.17%接近(偏差分别为1.31%、0.22%、0.86%),表明该模型合理,工艺稳定。
3 讨论
3.1 色谱条件优化 阿魏酸在217、235、322 nm波长处有紫外吸收峰[8],其中322 nm处吸收最强,而芍药苷在192、232 nm波长处有紫外吸收峰[9],为了保证能同时测定2种成分含量,故选择232 nm作为检测波长。再考察流动相甲醇-水、乙腈-水的分离效果,发现后者洗脱时分离度较好,但色谱峰有拖尾现象,由于阿魏酸是有机酸,易电离[10],故加入磷酸以改善峰形,发现乙腈-0.05 mol/L磷酸盐缓冲液(16∶84)分离情况理想。
3.2 评价指标确定 当归、川芎中均含有阿魏酸,是从当归中最早分离出的有机酸[11-13],也是2015年版《中国药典》[14]2种药材质量控制的指标成分;白芍具有养血、抗炎、镇痛等药理作用,单萜糖苷类化合物白芍总苷是该药材主要活性物质,其中芍药苷含量最高,约达3%[15-16],故本实验选择阿魏酸、芍药苷作为指标。另外,浸膏得率是评价提取工艺的重要指标之一,与后期制剂的生产成本和疗效密切相关,故本实验也选择其作为指标。
4 结论
本实验采用Box-behnken响应面法优化生乳汤回流提取工艺,该方法稳定可靠,可用于该方后续剂型的研究。
