知母皂苷对葛根素在正常、糖尿病大鼠体内药动学的影响
2022-12-05黄海兰刘奕明林爱华
黄海兰, 王 浩, 刘奕明,2, 林爱华
(1.广州中医药大学第二附属医院I期临床研究室,广东 广州 510120;2.广州中医药大学第二附属医院,广东省中医证候临床研究重点实验室,广东 广州 510120;3.广州中医药大学第二附属医院珠海医院,广东 珠海 519000)
葛根为豆科植物野葛或甘葛藤的干燥根,被用于治疗糖尿病及其并发症[1],葛根素为其主要有效成分,可通过抑制胰岛细胞凋亡、上调胰岛素分泌[2]来降低血糖,同时具有保护心脑血管、抗炎等药理活性[3],但它为P-糖蛋白(P-gp)底物[4],水溶性、脂溶性均较低,大部分以原型从粪便排泄,绝对口服生物利用度仅约为7%[5],限制了口服给药的临床应用,而注射液又易导致溶血和过敏反应[6]。因此,有必要探索更方便有效的方法来增加葛根素口服吸收。
葛根-知母为经典的治疗糖尿病药对,两药配伍兼具清热生津、滋阴润燥之功效[7]。知母皂苷为知母主要药理活性物质,可通过抑制TNF-α释放、上调细胞中IRS-1蛋白表达来改善高血糖[8],对芒果苷在大鼠体内的吸收有明显促进作用[9],但对葛根素是否有类似影响目前尚不明确。因此,本实验考察知母皂苷对葛根素在正常、糖尿病大鼠体内药动学的影响,评价该成分促吸收作用,以期为葛根-知母药对临床应用提供依据。
1 材料
1.1 仪器 TRIPLE QUADTM5500 型液相色谱-质谱联用仪(LC-MS/MS),配置Turbo Ionspray离子源(ESI)、LC-30AD高效液相色谱仪(日本岛津公司)、Analyst 1.7数据处理系统(美国AB公司);5418R高速冷冻离心机(德国Eppendorf公司);VX-Ⅱ多管涡旋振荡器(北京踏锦科技有限公司);MS105DU电子天平[十万分一,梅特勒-托利多仪器(上海)有限公司)];N-EVAP24进口氮吹仪(美国Organomation公司)。
1.2 试剂与药物 葛根素对照品(批号MUST-21010610,纯度>98%),购自成都曼思特生物科技有限公司;芦丁对照品(批号O0714AS,纯度>98%),购自大连美仑生物技术有限公司;知母皂苷冻干粉,实验室自制。肝素钠,购自上海如吉生物科技有限公司;链脲佐菌素(批号111607-200301,纯度≥98%),购自美国Sigma公司。AB-8大孔吸附树脂,购自广州松洲国熙有限公司。知母(批号170408241,产地河北),购自广东康美药业股份有限公司,经专家鉴定为正品。高糖高脂饲料(基础饲料52.2%,蔗糖20%,猪油15%,酪蛋白10%,胆固醇1.2%,磷酸氢钙0.6%,石粉0.4%,预混料0.4%)。甲醇、乙腈均为色谱纯,购自美国默克公司;甲酸为分析纯,购自上海麦克林生化科技有限公司;水为超纯水,经Milli-Q系统设备制备。
1.3 动物 SPF级SD大鼠,雄性,购自南方医科大学,体质量180~220 g,合格证号44002100028394,动物生产许可证号SCXK(粤)2016-0041。
2 方法
2.1 对照品、内标溶液制备
2.1.1 对照品溶液 精密称取葛根素对照品2.00 mg,甲醇溶解并定容,制成0.2 mg/mL贮备液,在-30 ℃下保存,用时甲醇依次稀释至0.05、0.1、0.5、1、5、10、20、50 μg/mL,分别精密吸取10 μL,90 μL空白血浆制成质量浓度为5、10、50、100、500、1 000、2 000、5 000 ng/mL的溶液,即得。
2.1.2 内标溶液 精密称取芦丁对照品2.20 mg,甲醇溶解并定容,制成0.22 mg/mL贮备液,在-30 ℃下保存,用甲醇稀释至2.2 μg/mL,即得。
2.2 药液制备
2.2.1 知母皂苷 参考文献[9-10],取适量知母根茎粉碎,过60目筛,75%乙醇分别按料液比1∶8、1∶6各提取1次,每次1 h,趁热过滤,滤液浓缩至无醇味,离心后将上清液用AB-8大孔吸附树脂进行纯化,洗脱体积流量为3 mL/min,分别以3倍柱体积纯水、6倍柱体积NaOH洗脱后,纯水洗脱至中性,20%、80%乙醇继续洗脱,收集80%乙醇洗脱液,浓缩至无醇味后冻干成粉末,醋酐-浓硫酸反应呈蓝绿色,表明所纯化有效部位为甾体皂苷,外标法[11]测得知母皂苷B2含量为87.7%,0.5%CMC-Na稀释至所需质量浓度,即得。
2.2.2 葛根素 精密称取葛根素对照品适量,0.5%CMC-Na稀释至10 mg/mL,即得。
2.3 糖尿病大鼠模型建立 12只正常大鼠适应性喂养普通饲料3 d后,再采用高糖高脂饲料喂养28 d。于第28天禁食不禁水12 h后,大鼠腹腔注射30 mg/kg链脲佐菌素,于给药后第3、7天检测空腹血糖(FBG),以FBG≥16.7 mmol/L为合格。
2.4 分组、给药与采血 24只正常大鼠随机分为4组,每组6只,给药前禁食不禁水12 h,分别灌胃给予葛根素(100 mg/kg)及葛根素-低、中、高剂量知母皂苷(50、100、200 mg/kg)混合药液;12只糖尿病大鼠随机分为2组,每组6只,分别灌胃给予葛根素及葛根素-知母皂苷(100 mg/kg)混合药液,于给药前和给药后0.083、0.167、0.33、0.5、1、2、3、4、6、8、10、12、24 h眼眶采血各500 μL,置于含肝素钠的EP管中,4 ℃、3 000 r/min离心15 min,取上层血浆,置于-80 ℃冰箱中保存待测。
2.5 LC-MS/MS条件
2.5.1 色谱 Inertsil ODS-3色谱柱(2.1 mm×100 mm,3 μm);流动相0.1%甲酸(A)-乙腈(B),梯度洗脱(0~1 min,5%B;1~2 min,5%~30%B;2~4 min,30%~70%B;4~5 min,70%~5%B;5~7 min,5%B);体积流量0.3 mL/min;柱温40 ℃;进样量5 μL。
2.5.2 质谱 电喷雾离子源(ESI);雾化温度450 ℃;喷雾电压(IS)-4 500 V;气帘气(CUR)20;碰撞气(CAD)7;氮气1(GS1)40;氮气2(GS2)50;负离子多反应检测模式(MRM);定量离子对葛根素m/z415.1~295.1,芦丁m/z609.3~271.0。
2.6 血浆处理 血浆在室温下融化后取100 μL至EP管中,加入20 μL内标溶液,振荡10 s,再加入400 μL乙腈沉淀蛋白,振荡3 min,4 ℃、13 000 r/min离心15 min,取360 μL上清液,氮气吹干,吹干物用200 μL乙腈-水(30∶70)复溶,振荡3 min,微孔滤膜过滤,测定时进样5 μL作LC-MS/MS分析。
(3)桩孔必须挖一节、浇筑一节护壁,护壁高度一般为1m,严禁不及时浇筑护壁的冒险作业。对软弱地层、涌水涌沙地层,护壁节段高度可减少 0.3~0.5m。
2.7 数据处理与统计学分析 采用DAS 2.0软件中的非房室模型计算AUC、Cmax、Tmax、t1/2等主要药动学参数,其中Cmax,Tmax为实测值,AUC以梯形法测定。再通过SPSS 25.0软件进行统计学处理,多组间比较采用单因素方差分析,2组间比较采用t检验。P<0.05表示差异具有统计学意义。
3 结果
3.1 方法学考察
3.1.1 专属性试验 取空白血浆、空白血浆+对照品(5 ng/mL)+内标、给药24 h后血浆适量,按“2.6”项下方法处理,在“2.5”项条件下进样测定,结果见图1。由此可知,葛根素测定不受内源性物质影响,表明该方法专属性良好。
3.1.2 线性关系考察 取含药血浆适量,按“2.6”项下方法处理,在“2.5”项条件下进样测定。以对照品、内标峰面积比值(Y)对血药浓度(X)进行回归,得方程为Y=0.011 5X+0.011 4(r=0.997 4),在5~5 000 ng/mL范围内线性关系良好,定量下限为5 ng/mL。
3.1.3 精密度、准确度试验 分别配制含定量下限及低、中、高(10、200、4 000 ng/mL)质量浓度葛根素的质控血浆,按“2.6”项下方法处理,同一天内在“2.5”项条件下进样测定6次,考察日内精密度;同法每天测定1次,连续3 d,考察日间精密度,测得两者RSD分别不大于6.98%、7.47%。再以实测、真实质量浓度比值考察准确度,测得其数值在96.97%~103.21%范围内,均符合生物样品分析要求。
3.1.4 提取回收率、基质效应试验 配制含“3.1.3”项下3个质量浓度葛根素的质控血浆各6份,按“2.6”项下方法处理,在“2.5”项条件下进样测定,计算峰面积A1;取空白血浆适量,按“2.6”项下方法处理,其残留物用含5、100、2 000 ng/mL葛根素的乙腈-水(30∶70)复溶,在“2.5”项条件下进样测定,计算峰面积A2;将5、100、2 000 ng/mL对照品溶液溶于乙腈-水(30∶70)中,在“2.5”项条件下进样测定,计算峰面积A3,以A1/A2为提取回收率,A2/A3为基质效应,测得两者分别在88.94%~91.85%、96.32%~109.13%范围内,均符合生物样品分析要求。
3.1.5 稳定性试验 配制含“3.1.3”项下3个质量浓度葛根素的质控血浆,室温放置4 h,考察其室温稳定性;在-80 ℃下反复冻融3次,考察其冻融稳定性;在4 ℃进样器中放置24 h,考察其待测液稳定性;在-80 ℃冰箱中放置30 d,考察其长期稳定性,以当天标准曲线衡量的质量浓度并计算其准确度,测得其数值均在89.27%~110.00%范围内,表明葛根素在不同条件下稳定性良好。
3.2.1 正常大鼠 图2、表1显示,葛根素单一给药后Tmax较短,各时间点血药浓度较低;合用各剂量知母皂苷后葛根素Cmax、AUC0-∞升高(P<0.05),CLZ/F下降(P<0.05),提示知母皂苷可增加葛根素在正常大鼠体内的暴露水平,并降低后者消除速率。
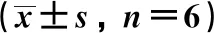
表1 正常大鼠中葛根素主要药动学参数
3.2.2 糖尿病大鼠 图3、表2显示,与表1比较,葛根素Cmax、AUC0~t、AUC0~∞降低(P<0.05),与文献[12]报道一致;合用知母皂苷后,葛根素Cmax、AUC0~t、AUC0~∞升高(P<0.01),Tmax延长(P<0.05),CLZ/F、VZ/F降低(P<0.01),提示知母皂苷可增加葛根素体内暴露水平,并延迟后者吸收,降低后者消除速率。

表2 糖尿病大鼠中葛根素主要药动学参数
4 讨论与结论
在样品前处理过程中发现,乙酸乙酯萃取时提取回收率低,固相萃取时价格昂贵,而乙腈萃取时蛋白信号强。因此,选择乙腈作为提取溶剂。
研究表明,胡椒碱[13]、维拉帕米[14]可抑制CYP450酶、P-gp活性,减少葛根素代谢和外排,增加其体内血药浓度;知母皂苷BⅡ抑制药物代谢酶的作用较弱[15],对P-gp活性的影响尚不明确。本实验发现,葛根素在糖尿病大鼠中的血药浓度降低,可能与糖尿病状态下Ⅱ相代谢酶UGT1a1、UGT1a7活性上升[12,16],与葛根素代谢加快有关;知母皂苷对葛根素的吸收促进作用更强,可能与该成分在正常、病理状态下对葛根素吸收、代谢等过程的影响程度不同有关。
本实验中葛根素给药剂量参考文献[17],并根据玉液汤[18]、芪参玉液胶囊[19]中知母与葛根1∶1的比例,探讨在该比例下知母皂苷对葛根素药动学的影响,并对两者以0.5∶1、2∶1比例配伍时进行相关考察,发现各剂量组无显著差异。前期报道,葛根素能延缓糖尿病并发症的发展[20],提示知母皂苷增加该成分体内暴露量时,有利于它发挥上述作用,并且其剂量过高时的吸收存在自身浓度抑制现象[21],故通过配伍等方式增加其吸收尤为重要。
综上所述,本实验研究知母皂苷对葛根素在大鼠体内药动学的影响,可为葛根-知母药对临床应用提供依据。另外,知母皂苷B2能促进芒果苷吸收[22],而本实验所用的知母皂苷也主要为该类型,同样可促进葛根素吸收,提示它有望成为促吸收中药的成分,其机制有待进一步研究。
